体质量指数对中枢性性早熟女童GnRH激发试验结果的影响
2020-05-13沈春荣
王 静,沈春荣
(台州市立医院儿内科,浙江 台州 318000)
中枢性性早熟(central precocious puberty,CPP)是指男孩9岁前、女孩8岁前由于下丘脑-垂体-性腺轴功能提前启动出现的生殖器官迅速发育并呈现第二性征的内分泌疾病[1]。近年来全球儿童肥胖的发病率呈逐年增高趋势,与此同时女童青春期启动时间显著提前,促性腺激素释放激素(gonadotropin-releasing hormone,GnRH)激发试验是临床上常用的诊断中枢性性早熟的金标准,通过判断下丘脑-垂体-性腺轴功能的启动情况鉴别诊断中枢性性早熟及周围性性早熟。有学者指出,体质量指数(body mass index,BMI)会影响GnRH激发试验结果促黄体生成素(luteinizing hormone,LH)峰值,国外研究发现,性早熟儿童LH激发峰值与体质量指数呈负相关[2],但国内关于体质量指数对GnRH激发试验促卵泡生成素(follicle-stimulating hormone,FSH)、LH基础值和峰值影响的研究较少,本次研究欲通过探究BMI对GnRH激发试验诊断中枢性性早熟女童LH峰值的影响,旨在为临床上准确诊断中枢性性早熟女童LH峰值提供科学依据。
1资料与方法
1.1病例收集
选取2018年1月至2019年8月于台州市立医院诊断为特发性中枢性性早熟(idiopathic central precocious puberty,ICPP)的96例女童为研究对象。ICPP诊断标准参照中枢性性早熟诊断与治疗共识(2015版)[1],并按照BMI将被研究儿童分为肥胖组、超重组和正常体重组,BMI=体质量(kg)/身高2(m2),BMI的Z分值≥2为肥胖,1~2为超重,<1为正常体质量[3]。纳入标准:①年龄<18岁;②未服用过对肥胖有影响的药物;③无遗传代谢性疾病;④无严重心肝肾等器质性疾病;⑤患儿家属均知情并同意参与本次研究。
1.2资料收集
由经过培训的调查员采用标准技术方法测量受试儿童的身高、体重(清晨空腹体重),分别精确至0.1kg、0.1cm,按照BMI计算结果对患儿进行分组。第二性征评估采用Tanner分期标准,由统一培训的儿科内分泌医师进行评估。骨龄通过拍摄左手正位X线片(包括腕骨及桡尺骨下端),统一由医院内分泌专科医师按G-P图谱法测算骨龄。卵巢及子宫容积通过超声检查计算(0.523×长×宽×厚度)[4],下丘脑-垂体磁共振成像检查排除颅内占位病变。
1.3 GnRH激发试验
患儿入院后第二天清晨空腹进行GnRH激发试验,空腹肘静脉注射戈那瑞林(国药准字:H10960064),剂量为2.5ug/kg,最大量不超过100μg/kg,于注射时的0min、30min、60min、90min抽取5mL静脉血置于胶促凝管中备用。在Access2全自动化学发光免疫分析仪中(武汉明德生物科技股份有限公司)用酶促化学发光检测法检测LH水平和FSH水平,操作严格按照说明书步骤进行。
1.4统计学方法
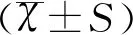
2结果
2.1儿童一般情况
共有96例女童完成本研究,其中正常组37例,超重组33例,肥胖组26例。各组BMI比较差异均有统计学意义(χ2=6.16~12.88,P<0.05),而年龄、骨龄、子宫容积、卵巢容积(t=0.05~1.04,P>0.05)、乳房分期(χ2=0.68~0.99,P>0.05)在三组儿童间比较差异均无统计学意义,见表1。

表1 三组患儿临床特征Table 1 Clinical characteristics of children with ICPP in the three groups
2.2三组患儿LH及FSH基础值、LH及FSH峰值和峰值LH/FSH比较
正常组、超重组和肥胖组儿童LH基础值和FSH基础值逐渐下降,组间两两比较,差异均具有统计学意义(t=5.30~12.80,P<0.05),LH峰值和峰值LH/FSH在超重组和肥胖组患儿均低于正常体重组(t=2.99~8.10,P<0.05),而超重组和肥胖组差异无统计学意义(t=0.59~1.89,P>0.05);FSH峰值在各组间差异均无统计学意义(P>0.05),见表2。

表2 各组性早熟患儿血清激素水平Table 2 Serum hormone levels of children with OCPP in the three groups
注:*指与正常组比较,差异有统计学意义;#指与超重组比较,差异有统计学意义。
3.讨论
3.1儿童肥胖是性早熟的危险因素
近年来,儿童肥胖已经成为世界范围内的公共健康问题,严重威胁儿童的健康发育。研究显示儿童肥胖不仅和高脂血症、高血糖、高胰岛素血症等有关[5],还是性早熟的危险因素。肥胖对女性激素水平的影响贯穿青春前期、青春期及成年期,肥胖可使女童性发育提前,但对其机制的研究由于混杂因素众多目前尚没有完全清楚[6]。因此探究BMI对GnRH激发试验诊断中枢性性早熟女童LH及FSH基础值、LH及FSH峰值水平的影响,对性早熟的诊断和进一步研究提供理论依据。
3.2 BMI与女童性激素水平的关联性及关联机制探讨
本研究结果提示超重组和肥胖组儿童LH及FSH基础值、LH峰值和峰值LH/FSH均低于正常体重组,提示青春期肥胖女童LH分泌减弱,与文献报道的正常体质量者血清LH基础值及LH峰值显著高于超重及肥胖组结果一致[4,7]。具体机制尚未明确,较多的研究提示肥胖在一定程度上抑制了下丘脑-垂体-性腺轴的功能,可能与雌二醇、胰岛素水平、瘦素等调节有关。有研究发现中枢性性早熟患儿中,肥胖组患儿雌二醇、胰岛素水平和瘦素水平均高于正常体重组,且肥胖组患儿伴有较强的胰岛素抵抗[4]。对人类和动物的研究表明雌激素在下丘脑起负反馈作用,可能与肥胖患儿低LH峰值相关。Sliwowska等[8]研究发现肥胖组ICPP患儿中存在高胰岛素,并认为胰岛素可能作用于下丘脑中特定的候选神经元,参与生殖功能的调节。Al-Safi等[9]的研究发现肥胖妇女的胰岛素升高与低内源性LH分泌有关。BMI对LH分泌的影响也可能与瘦素调节有关。瘦素是控制食物摄入和能量平衡关键信号之一,通过中央和外围受体参与多种生理功能。最近的研究发现外源脂肪因子(包括瘦素)通过与瘦素受体结合而改变下丘脑GnRH脉冲释放,在一般人群中的研究发现高水平瘦素使GnRH脉冲释放频率增加并可促进青春期开始[10]。但是,在大多数肥胖个体中的研究发现,肥胖ICPP患儿血清瘦素浓度升高与体内瘦素抵抗有关,且肥胖ICPP患儿中瘦素信号传导的神经生物学反应呈现出中枢瘦素作用不足,提示肥胖患儿存在瘦素抵抗与低LH峰值相关。
GnRH激发试验是诊断中枢性性早熟诊断的金标准,能够对促性腺激素轴活化水平进行准确检测,而肥胖对青春期启动激素水平有影响,可能对下丘脑促性腺激素释放激素(GnRH)的分泌产生影响,因此对于肥胖患儿诊断中枢性性早熟LH峰值切点值得商榷[4]。
综上所述,BMI与GnRH激发试验女童性激素水平密切相关,体质量指数越高,LH基础值、LH峰值、峰值LH/FSH比值越低,临床上应该加以重视。
