Cd(II)有机骨架化合物的合成及其荧光性能
2020-05-13朱文庆朱玉梦
朱文庆, 朱玉梦, 李 扬, 樊 盼, 张 瑾
(西安工程大学 环境与化学工程学院,陕西 西安 710048)
金属离子与有机配体之间通过配位键自组装形成的金属-有机骨架化合物(MOFs)是一类新兴的结晶性固态多孔材料[1-2]。MOFs具有空间结构可设计性和多样性,在非均相催化、气体吸附与分离、水体污染物处理、单分子磁性、光致发光性能及药物传递与释放等领域表现出良好的应用前景[3-10]。
镉配合物是一类重要的有机材料,配体结构和组成对其性能有较大影响[11-12]。2,5-二羟基对苯二甲酸(H4-DHBDC)具有良好的对称性,且苯环上的两个羧酸配位能力强、易于形成稳定的高维骨架材料[13-15],当羧基脱去质子后可以与金属离子进行良好配位,其配位模式的多样性使得H4-DHBDC可构筑结构新颖且功能多样的MOFs材料[16-17],与此同时,其羧基邻位的两个羟基功能团,在未参与配位时会裸露在MOFs的孔道/空腔内,可使整个MOFs相当于一个三维结构的路易斯酸,这对某些化学反应具有潜在的催化效果。此外,研究表明,当芳香类多齿含氮配体的引入并参与配位,还可以进一步增强骨架中有机单元之间的π-π*堆积和π-π*共轭效应,进而提高MOFs的光致发光性能[18]。而1,4-双咪唑苯(BIB)是重要的芳香类多齿含氮配体。因此,基于H4-DHBDC和BIB配体的结构特点,如何通过反应条件的有效控制,构筑具有羟基功能化的Cd(Ⅱ)配合物,无疑对拓展其结构、性能和应用研究具有重要的科学意义。
本文以2,5-二羟基对苯二甲酸为主配体,1,4-双咪唑苯(BIB)为辅助配体,Cd(NO3)2·4H2O为金属盐,采用溶剂热法,在105 ℃下反应48 h,构筑了一例化学式为[Cd2(H2-DHBDC)2(BIB)2]n的金属有机骨架化合物,并利用单晶X-射线衍射仪(SCXRD)、粉末衍射仪(PXRD)、元素分析仪(EA)、红外光谱仪(FT-IR)、热重分析仪(TGA)和荧光分光光度计(FS)对该化合物的结构和性能进行了表征。
1 实验部分
1.1 仪器与试剂
EQUINX55型傅里叶变换红外光谱仪(KBr压片);Vario ELⅢ型元素分析仪;Bruker Aper II CCD型X射线单晶衍射仪;TGA/SDTA851型热重分析测试仪;RF-5301型荧光分光光度计;Bruker D8 Venture型粉末X-射线衍射仪。
二次蒸馏水为实验室自制;其余所用试剂均为分析纯。
1.2 合成
将H4-DHBDC 19.8 mg(0.1 mmol)和BIB 20.7 mg(0.1 mmol)溶于2 mL DMF中,Cd(NO3)2·4H2O 61.68 mg(0.2 mmol )溶于4 mL去离子水中,搅拌10 min,待其充分溶解;将两种溶液移入20 mL反应瓶中,封口后超声振荡10 min。将反应瓶放入105 ℃烘箱中,恒温加热48 h。冷却至室温,过滤,用DMF和去离子水交替洗涤产物,自然晾干。通过元素分析仪测定化合物中碳元素实验值为46.61%(理论值46.31%),氢元素实验值为2.76%(理论值2.72%),氮元素实验值为9.94%(理论值10.80%)。

表1 化合物的晶体学数据Table 1 Crystal data of the complex
1.3 晶体结构测定
晶体尺寸为0.27 mm×0.21 mm×0.18 mm的晶体,于室温使用经石墨单色化的MoKα射线(λ=0.071073 Å),并运用φ-ω扫描方式收集数据,在1.75°≤θ≤25.60°, -10≤h≤8, -11≤k≤11, -15≤l≤15收集衍射点5350个,其中独立衍射点3633个,用于直接解结构的衍射点3095个(Rint=0.0315)。用SHELX-97程序完成晶体结构的解析和精修,晶体结构的解析由直接法解出[19],全矩阵最小二乘法进行精修。采用理论加氢法确定氢原子,全部非氢原子坐标及其各向异性热参数由全矩阵最小二乘法修正。化合物的相关晶体学数据见表1。
2 结果与讨论
2.1 晶体结构
化合物的配位结构图如图1所示。由图1(a)可见,配合物的最小结构单元由两个配位环境相同的Cd2+,两个H2-DHBDC2-和两个1,4-双咪唑苯分子构成。其中Cd2+分别与来自3个不同H2-DHBDC2-配体中的3个羧基上的5个氧原子(O1, O2, O2#, O4, O5)和来自两个不同1,4-双咪唑苯配体中的两个咪唑环上的氮原子(N1, N3),配位构成了一个七配位的扭曲五角双锥构型。Cd—O键长为2.229(8)~2.611(8) Å, O—Cd—O键角为52.2(3)~173.0(3)°。化合物的主要键长键角见表2和表3。

(a)

(b)

(c)图1 配合物的配位结构(a)和配位模式(b)、 (c)Figure 1 Coordination environment of complex and coordination pattern of the H4-DHBDC

图2 配合物的一维链状结构图Figure 2 1D of chain structure of the complex
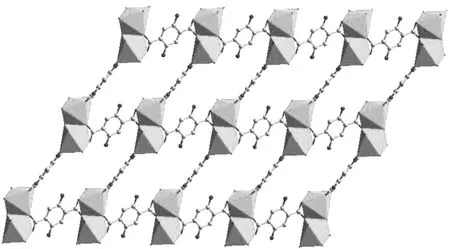
图3 配合物的二维层状结构图Figure 3 The 2D layer in complex

图4 配合物的三维结构图Figure 4 The 3D framework of complex

表2 配合物的主要键长
在化合物中,配体H4-DHBDC表现出两种不同的配位模式:一种是配体中的两个羧基氧均采用双齿螯合的配位模式连接了两个Cd2+;另一种是两个羧基氧螯合一个Cd2+后,其中一个氧桥联另一个Cd2+,以螯合-桥式三齿的配位模式与Cd2+配位,如图1(b)、 (c)所示。其中心对称的双核次级结构单元由H2-DHBDC2-配体采取第二种配位模式在沿a轴方向上无限延伸连接成了一条一维链状直线(图2)。链与链之间被采取第一种配位模式的H2-DHBDC2-连接成了二维网状结构(图3)。这个二维结构进一步被两个不同1,4-双咪唑苯上的氮原子连接成了三维网状结构,其中化合物被H2-DHBDC2-斜插贯穿整个孔道,导致有效孔径减少(图4)。

表3 配合物的主要键角Table 3 Selected bond angles of the complex

ν/cm-1

ν/cm-1
2.2 表征
(1) FT-IR
图5为配合物的FT-IR谱图。由图5可见,配体在3250 cm-1~3000 cm-1的特征吸收峰消失,说明配体与Cd2+进行了配位。此外,配体H4-DHBDC中C=O的伸缩振动吸收峰在形成配合物后由1648 cm-1前移至1667 cm-1;C—O键吸收峰由1496 cm-1处前移至1526 cm-1,两组峰的强度明显降低,这进一步说明了配体中的C=O和C—O与Cd2+产生了配位。
(2) PXRD
图6为配合物的PXRD曲线。由图6可知,在25 ℃下,样品中主要衍射峰的位置和强度与标准样品的衍射峰基本吻合,说明样品为纯相,结晶度高。

2δ/(°)
(3) TGA
图7为配合物的TGA曲线。由图7可见,当温度为364~386 ℃时,配合物急速失重,失重率为37.64%,对应失去的是两个H2-DHBDC2-,理论值为37.78%;当温度升高至386~686 ℃,配合物发生第二次失重,失重率为37.58%。最后剩余的产物为CdO,实际值为24.78%,理论值为24.75%。TGA分析结果表明,配合物具有良好的热稳定性。

Temperature/℃

λ/nm
(4) FL
图8为配合物的固体荧光发射谱图。由图8可见,用波长为376 nm的光源激发H4-DHBDC配体和配合物时,H4-DHBDC配体在472 nm处出现最大发射峰,配合物在500 nm处出现最大发射峰,其发射峰位置相对于H4-DHBDC配体而言发生了较大幅度的红移。配合物与H4-DHBDC配体的发射峰形状相似,但前者发光强度远大于配体。其可能原因为:(1)Cd2+的4d轨道是全满结构,很难被还原或氧化,不能发生d-d跃迁。因此配合物的荧光发射既不是由配体到金属中心的电荷跃迁(LMCT),也不是从金属中心到配体的电荷跃迁(MLCT),而很可能是在Cd2+作用下,其配体的内部电子转换所致,即荧光增强的一部分原因是配体内部的π-π*电荷跃迁,双核镉簇在整个过程中只是起到了电子传导的作用;(2)双核Cd—O体系中,相邻的Cd2+之间形成了平行四边形结构,增强了整个配位聚合物的刚性和共平面性,更有利于电子传导;(3)在三维网状结构中,芳香性的有机配体之间相互靠近,有利于配体间的共轭作用产生和电荷转移,即配体与配体间的电荷转移(LLCT)[20]。
采用溶剂热法合成了一种具有三维网状结构的Cd(Ⅱ)有机骨架化合物[Cd2(H2-DHBDC)2(BIB)2]n。配合物具有较好的热稳定性,其骨架的初始分解温度为364 ℃。用波长为376 nm的光源激发配合物时,在500 nm处出现最大发射峰。该配合物有在荧光传感器、荧光离子设别等方面有潜在应用价值。
