氟代二苯乙烯氨基酸的合成及性能
2020-05-13郑林波赵孔娥朱芳芳胡晓松
郑林波, 赵孔娥, 朱芳芳, 胡晓松
(武汉理工大学 化学化工与生命科学学院,湖北 武汉 430070)
伴随着蛋白质科学研究的快速发展,天然氨基酸因其携带的功能基团有限,无法满足化学、生物学研究对蛋白质结构和功能日益增长的特定要求。非天然氨基酸可以通过结构设计赋予它们多样性功能基团,从而具备如荧光性能、光敏特性、氧化还原活性。非天然氨基酸已经在酶活性测试、蛋白质结构和蛋白质相互作用分析等方面发挥了一定作用[1-5]。例如,Peter等[6]实现了非天然氨基酸以基因编码形式定点插入到蛋白质中,制得具备某些特性的非天然氨基酸的设想。此外,非天然氨基酸也可以通过化学合成法、体外生物合成法等方式掺入蛋白质结构内[7]。
荧光探针已经成为研究复杂生物学过程的有力工具之一,具有良好荧光性质且尺寸相对较小的非天然氨基酸荧光探针在生物学研究、病理研究等领域发挥了重要的作用。二苯乙烯荧光团具有π共轭有机体系,荧光量子产率较高,其物理、光学和电子性质可通过结构设计进行调节[8],已被广泛用于荧光探针的设计。Pradeep等[9]设计并合成了一系列含有二苯乙烯结构的荧光非天然氨基酸,可以用作pH和氧化还原反应刺激反应型荧光探针。Ilseung等[10]用紫外线照射含有二苯乙烯结构的无荧光的白藜芦醇,获得了一种新的、高荧光的光致异构产物,可用于生物成像和双光子显微镜。
氟原子具有核磁共振活性的同位素19F的自然丰度为100%,具有很高的核磁灵敏度,其化学位移与化学环境密切相关,而且天然蛋白质中没有氟原子存在导致的背景干扰,因此在氨基酸中引入氟原子后,可以利用它的氟谱研究含氟代氨基酸的蛋白质在不同时间尺度上的动态变化。
结合二苯乙烯荧光团优异的光学特性和氟原子的核磁探针属性,在前期的二苯乙烯氨基酸的合成与性能研究的工作基础上[11],我们计划在分子结构中引入氟原子,使其可以同时作为荧光探针和核磁探针用于相关生物学研究。
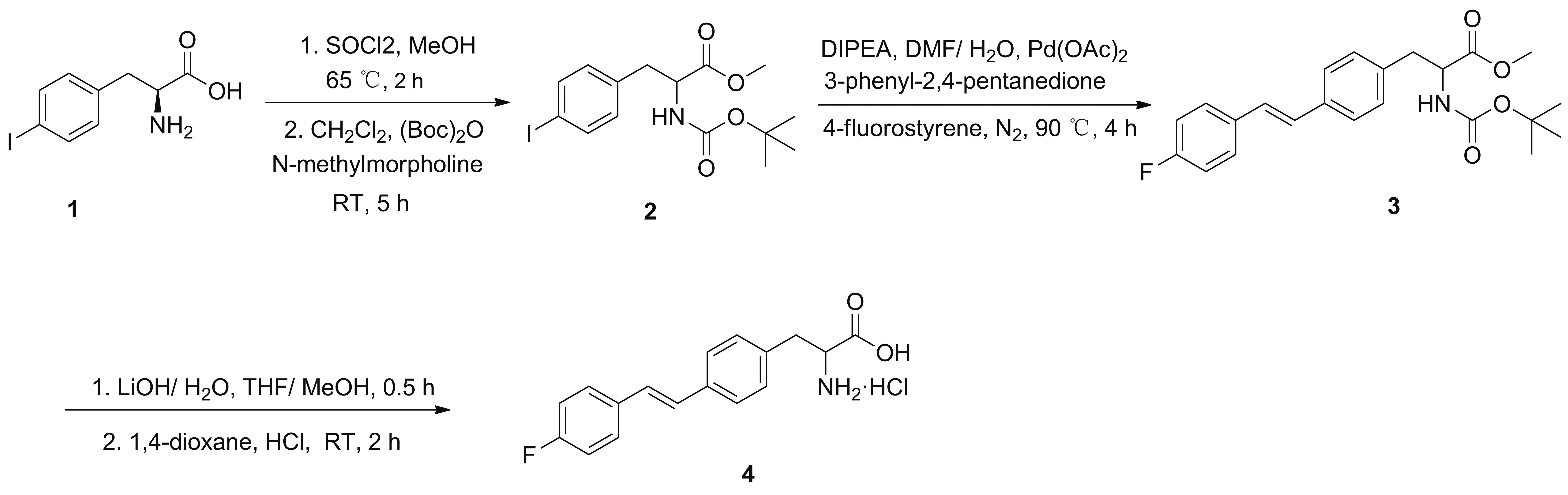
本文首先通过对4-碘-L-苯丙氨酸(1)的羧基和氨基分别进行保护得到甲基-2-((叔-丁氧基羰基)氨基)-3-(4-碘苯基)丙酸酯(2); 2与4-氟苯乙烯在3-苯基-2,4-戊二酮存在的情况下,通过Heck反应得到甲基-(E)-2-((叔-丁氧基羰基)氨基)-3-(4-(4-氟苯乙烯基)苯基)丙酸酯(3); 3首先在LiOH的作用下脱去酯保护基,然后在HCl作用下脱去叔丁氧羰基保护基得到(E)-2-氨基-3-(4-(4-氟苯乙烯基)苯基)丙酸的盐酸盐(4, Scheme 1),产率47.4%,其结构经1H NMR、13C NMR、 IR和MS(ESI-TOF)确证。并研究了4的光学活性。
1 实验部分
1.1 仪器与试剂
X-4型显微熔点仪;UV757CRT型紫外-可见分光光度计;Bruker AVANCE III 500 MHz型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Nicolet iS5型傅里叶变换红外光谱仪(KBr压片);Triple TOFTM5600型质谱仪;G2-XS QTof型质谱仪;WAY型阿贝折光仪;LS55型荧光/磷光/发光分光光度计;ZF-7A型紫外分析仪。
4-碘-L-苯丙氨酸(Ark Pharm);亚硫酰氯(上海秦巴化工有限公司);二碳酸二叔丁酯(Aladdin);N-甲基吗啉(Innochem);醋酸钯(Aladdin); 4-氟苯乙烯(Accela);N,N-二异丙基乙胺(上海秦巴化工有限公司);3-苯基-2,4-戊二酮(TCI);三苯基膦(国药集团化学试剂有限公司)。其余所用试剂均为化学纯或分析纯。
1.2 合成
(1) 2的合成
冰水浴冷却下,将亚硫酰氯2.00 mL(27.40 mmol)缓慢滴加到1 1.60 g(5.50 mmol)的甲醇(10.00 mL)溶液中,滴毕,撤除冰水浴,回流反应2 h。减压蒸除溶剂,粗产物用乙醚洗涤得白色固体4-碘-L-苯基丙氨酸甲酯,不经纯化直接使用。
向4-碘-L-苯丙氨酸甲酯的二氯甲烷(8.00 mL)溶液中依次加入N-甲基吗啉1.82 mL(16.50 mmol)和二碳酸二叔丁酯1.58 g(7.14 mmol),氮气保护,搅拌下反应5 h。减压蒸除溶剂,残余物用乙酸乙酯(100 mL)溶解,依次用饱和碳酸氢钠溶液(60 mL),饱和食盐水(60 mL)洗涤,分液,有机相用无水硫酸钠干燥,过滤,滤液浓缩得白色固体,用甲醇重结晶,收集滤液,蒸除溶剂得白色固体2 1.90 g,产率85.0%, Rf=0.50(石油醚/乙酸乙酯=3/1,V/V), m.p.75.1~76.9 ℃;1H NMRδ: 7.64(d,J=7.5 Hz, 2H), 7.30(d,J=8.0 Hz, 1H), 7.06(d,J=8.0 Hz, 2H), 4.17~4.13(m, 1H), 3.61(s, 3H), 2.97~2.93(m, 1H), 2.82~2.77(m, 1H), 1.32(s, 9H);13C NMRδ: 172.35, 155.34, 137.41, 136.88, 131.55, 92.29, 78.30, 54.86, 51.82, 35.86, 28.07; IRν: 3346, 2964, 1738, 1686, 1526, 1441, 1367, 1291, 1252, 1222, 1166, 1057, 1002 cm-1; MALDI-TOF-MSm/z: Calcd for C15H20NO4I{[M+H]+}428.0329, found 427.9099。
(2) 3的合成
将N-(叔丁氧羰基)-4-碘-L-苯丙氨酸甲酯(2)405.23 mg(1.00 mmol)加入N,N-二甲基甲酰胺和H2O的混合溶剂(DMF/H2O=1/1,V/V, 36 mL)中,加入3 mol%Pd(OAc)26.74 mg(0.030 mmol),N,N-二异丙基乙胺(DIPEA)0.39 g(3.00 mmol)和6 mol%3-苯基-2,4-戊二酮10.3 mg(0.058 mmol),氮气保护下,加入4-氟苯乙烯244.28 mg(2 mmol),于90 ℃反应4 h。加入乙酸乙酯100 mL,用饱和食盐水(2×100 mL),合并有机相,用无水硫酸钠干燥,减压蒸除溶剂,粗产物经硅胶柱层析(洗脱剂:石油醚/乙酸乙酯=5/1,V/V)纯化得黄色固体3 245 mg,产率62.0%, Rf=0.35(石油醚/乙酸乙酯=5/1,V/V), m.p.99.3~100 ℃;1H NMRδ: 7.50~7.40(m, 4H), 7.13(d,J=7.32 Hz, 2H), 7.06(d,J=7.63 Hz, 2H), 7.05~6.99(m, 2H), 5.00(d,J=6.71 Hz, 1H), 4.65~4.54(m, 1H), 3.73(s, 3H), 3.24~3.10(m, 1H), 3.10~2.99(m, 1H), 1.44(br s, 9H);13C NMRδ: 171.26, 162.31, 154.06, 134.99, 132.50, 132.47, 128.66, 127.03, 126.97, 126.91, 126.38, 125.58, 114.69, 114.52, 78.96, 53.38, 51.22, 37.11, 27.29; IRν: 3361, 2983, 1749, 1687, 1599, 1514, 1444, 1367, 1304, 1165, 964, 542 cm-1; MALDI-TOF-MSm/z: Calcd for C23H26NO4F{[M+H]+}399.4624, found 399.4621。
(3) 4的合成
将化合物3 214 mg(0.54 mmol)溶于甲醇(4.0 mL)和四氢呋喃(12.0 mL)的混合溶剂中,于0 ℃缓慢滴加氢氧化锂溶液14.0 mL(1.70 mmol),滴毕,搅拌下反应0.5 h(TLC检测)。滴加1 mol·L-1盐酸至pH<3,蒸除有机溶剂,残余物用乙酸乙酯(3×50 mL)萃取,合并有机相,用无水硫酸钠干燥,旋蒸除溶得白色粗品。不经纯化直接使用。
将粗品溶于1,4-二氧六环(6 mL)中,缓慢滴加12 mol·L-1盐酸2 mL,滴毕,搅拌下反应2 h(TLC检测)。旋蒸除溶,残余物用二氯甲烷(2×40 mL)洗涤,蒸除溶剂得白色固体4 155 mg,产率90.0%, m.p.210~211 ℃;1H NMRδ: 7.68~7.62(m, 2H), 7.56(d,J=8.24 Hz, 2H), 7.29(d,J=8.24 Hz, 2H), 7.24(d,J=5.19 Hz, 1H), 7.22(s, 2H), 7.21~7.18(m, 1H), 4.14(t,J=6.41 Hz, 1H), 3.15~3.08(m, 2H);13C NMRδ: 170.20, 160.64, 135.93, 134.38, 133.62, 133.60, 129.88, 128.32, 128.26, 127.95, 127.93, 127.12, 126.55, 115.62, 115.45, 53.09, 35.38;19F NMRδ: -115.52; IRν: 3379, 3003, 2931, 1745, 1606, 1537, 1512, 1421, 1209, 1016, 962, 837, 696, 540 cm-1; MALDI-TOF-MSm/z: Calcd for C17H16NO2F·HCl{[M+H]+}322.1010, found 322.1015。
1.3 性能测试
(1) 荧光量子产率的测定[12]
待测溶液为1.0 μmol·L-1化合物4的DMSO溶液,标准溶液为2.0 μmol·L-1硫酸奎宁的0.1 mol·L-1硫酸溶液。吸光度使用紫外-可见分光光度计测试,利用荧光光谱仪测试溶液的发射光谱,然后计算发射峰积分面积。测得标准溶液和DMSO的折射率分别为1.3452和 1.4778。
(2) 紫外-可见吸收光谱的测定
用甲醇配制50.0 μmol·L-1化合物4的溶液,然后取3 mL于10 mm×10 mm螺口石英比色皿中用于测定,将ZF-7A手提式紫外分析仪固定在桌面上,作为光源,发射254 nm的光,实验过程中需要避开自然光的照射。在环境温度22 ℃下,照射比色皿中的溶液,光照一段时间后立即测定紫外-可见吸收光谱,并记录光照时间;重复光照操作、测试,直至紫外可见-吸收光谱不再有明显变化为止。
(3) 氟谱的测定
取化合物4 27.5 mg于10 mL样品管中,加入5 mL氘代甲醇溶解配制成溶液,取氟谱内标三氟乙酸乙酯5 μL,加入1 mL氘代甲醇稀释,然后,取150 μL内标溶液于已配制好的化合物4溶液中;最后,取3 mL加入内标之后的化合物4溶液于10 mm×10 mm螺口石英比色皿中用于测定,用固定在桌面上的ZF-7A手提式紫外分析仪作为激发光源发射254 nm的光,照射比色皿中的溶液。按设定的累计光照时间进行照射,每到一个时间节点,取样0.5 mL于核磁管中,立即测定氟谱,且整个实验过程中避开自然光的照射。
2 结果与讨论
2.1 合成
初始原料为4-碘-L-苯丙氨酸,先后通过甲酯化保护羧基,叔丁氧羰基(Boc)酰胺化保护氨基,得到4-碘-L-氨基酸衍生物(化合物2)。原料中含有碘原子,可通过Heck反应构建二苯乙烯结构的乙烯桥。Wittig反应[13-14]、Heck偶联反应[15-16]和Suzuki反应[17]是比较常用的几种构建乙烯桥的方法,但文献[18-19]表明Heck 反应产物的trans选择性更好。化合物2是制备目标产物重要的中间体,其分离纯化可以通过甲醇重结晶进行,总产率为85.0%。
二苯乙烯基荧光基团的构建通过化合物2与4-氟苯乙烯的Heck反应实现。本文使用醋酸钯,3-苯基-2,4-戊二酮(配体)和N,N-二异丙基乙胺作为催化剂,产率较高(化合物3, 62.0%),后处理简单,仅需硅胶柱层析分离(或乙酸乙酯重结晶)即可。当使用本组前期工作所采用的以三苯基膦作配体,醋酸钯、N,N-二异丙基乙胺作为催化剂的方案合成化合物3时,存在副反应多,分离纯化困难,产率较低(产率17.8%)等问题,虽然此方法在苯乙烯与化合物2反应制备二苯乙烯氨基酸时效果很好(产率81.0%)。此外,反应体系的酸碱性以及配体、催化剂的用量都会对反应产生影响,如果加入过量的配体,则容易使催化剂发生聚集,生成没有催化活性的钯黑,因此反应过程中必须严格控制好配体与醋酸钯的比例。最后一步是将化合物3分别在碱性条件和酸性条件下,对羧基和氨基进行脱保护即可得到目标化合物4(产率90.0%)。化合物3和4的IR谱图中在964和962 cm-1处有强吸收峰,对应的是反式烯烃结构的=C—H面外摇摆振动特征峰;在730~650 cm-1处没有观察到顺式烯烃中的弱、宽吸收峰,这进一步证实了双键为反式结构[20]。
2.2 紫外-可见吸收光谱
图1为化合物4的紫外-可见吸收谱图。由图1可知,化合物4在甲醇中吸收峰为296 nm和310 nm,在DMSO中的吸收峰为301 nm和315 nm。出现两个吸收峰的原因在于,分子内存在不同类型的电子跃迁。溶剂效应的影响导致最大吸收波长和吸收强度产生了相应变化。
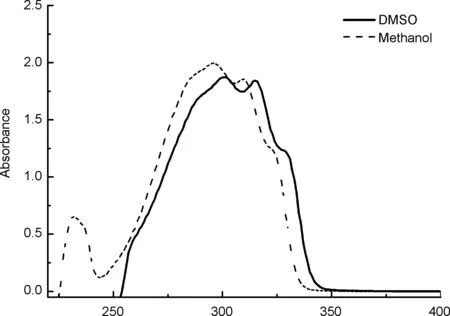
λ/nm图 1 化合物4的UV-Vis谱图Figure 1 UV-Vis spectra of 4
2.3 荧光谱图和荧光量子产率
图2为化合物4在DMSO中的荧光激发、发射谱图。由图2可见,4的激发波长、发射波长分别为314 nm、 355 nm,斯托克斯位移为41 nm。当乙烯基对位没有氟原子取代时,其激发波长、发射波长分别为312 nm、 357 nm,斯托克斯位移为45 nm[11]。表1为化合物4的物理化学性质,其荧光量子产率为0.22,摩尔吸光系数为2.4×104cm-1·mol-1·L,当乙烯基对位没有氟原子取代时,该化合物的荧光量子产率为0.17,摩尔吸光系数为5.2×104cm-1·mol-1·L[11]。由此可见,氟原子的引入使荧光量子产率增加,改变了化合物的荧光性质。

λ/nm

表 1 化合物4的物理化学性质Table 1 Physicochemical properties of 4
λ/nm
2.4 光致顺反异构性
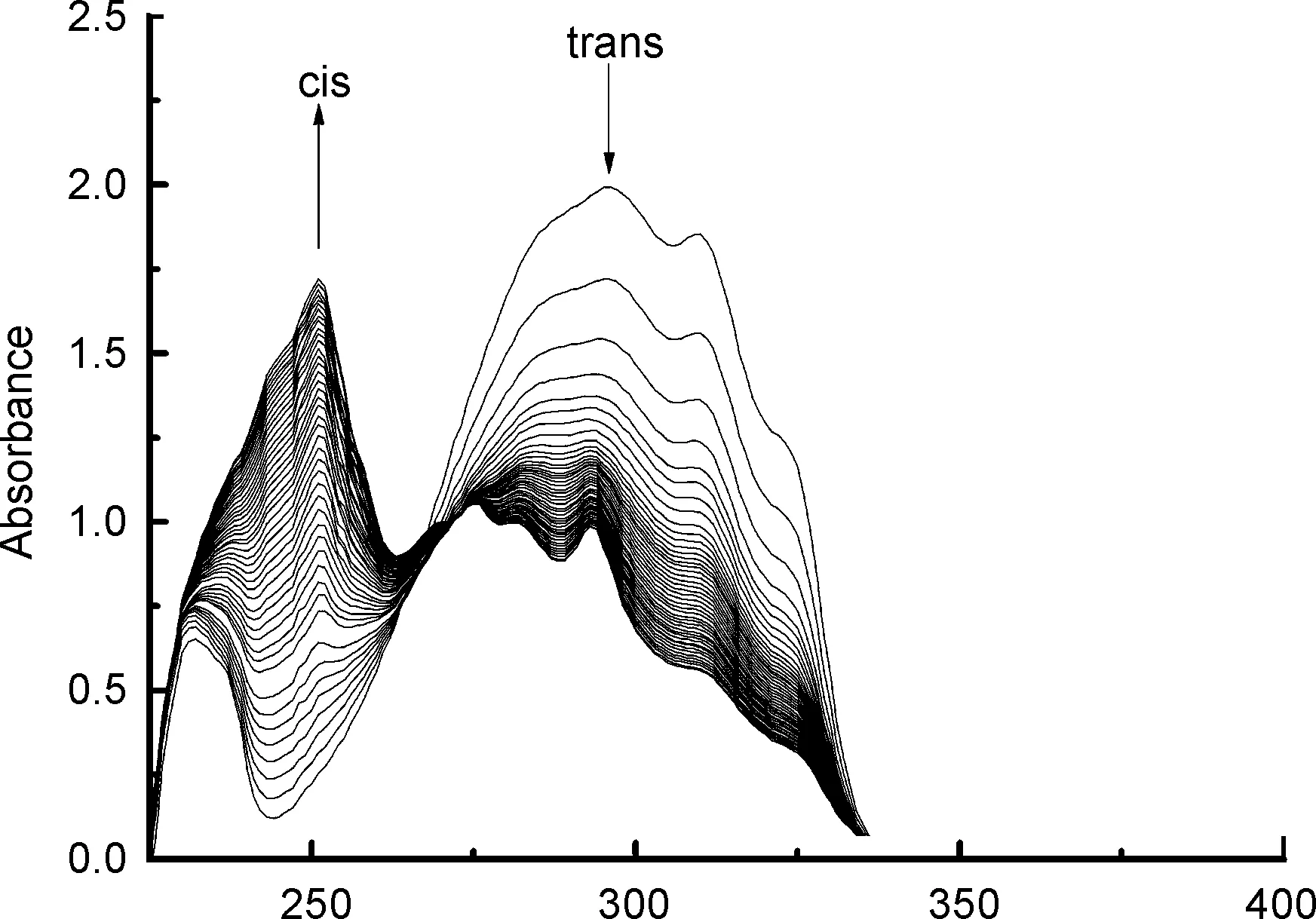
图3为反式化合物4(50.0 μmol·L-1)甲醇溶液光致顺反异构随光照时间变化的紫外-可见吸收谱图。由图3可见,未进行光照射前,化合物4最大紫外吸收波长出现在296 nm处,光照实验开始后,随着光照时间的增长,296 nm处的吸收峰迅速变弱。当累计光照时间t=14 min时,251 nm处出现了一个新的吸收峰,其强度随着累计光照时间增长而增强。当t大于80 min时,紫外吸收光谱再无明显变化,即累计光照时间t=80 min时达到光稳态,此时出现两个等吸收点,分别位于251 nm和293 nm。在相同条件下测试乙烯基对位没有氟原子取代的二苯乙烯氨基酸的光致顺反异构时,累计光照时间t=68 min时就达到了光稳态,两个等吸收点分别为253 nm和295 nm。
根据化合物4光致异构转变一级动力学拟合曲线(曲线略),由文献[19]方法计算得到反式转变为顺式结构速率常数k为0.026 min-1。前期工作对乙烯基对位没有氟原子取代的二苯乙烯氨基酸的光致顺反异构转变进行了拟合[11],计算得到k为0.046 min-1,这说明在相同条件下,无氟取代的二苯乙烯类氨基酸比有氟取代的二苯乙烯类氨基酸(化合物4)具备更快的转变速率。化合物4中由于氟原子的存在,其参与形成的氢键有可能使二苯乙烯结构从反式转变为顺式的活化能变大,导致转换速率降低。
2.5 光致顺反异构氟谱
图4为化合物4随光照时间变化的氟谱。从图4可以看出,在未进行光照之前,化合物4中氟原子的δ为-115.22,经过一段时间的光照后,δ-115.53出现一个新峰,对应的是顺式异构体中氟原子的峰。且随着光照时间的增长,新峰的强度也不断增强。相对于核磁共振氢谱和碳谱,氟谱能够更加清晰地反映顺式/反式结构的变化,因此化合物4可以作为核磁探针用于蛋白质结构的生物学研究。

图4 4因光致顺反异构随光照时间变化的氟谱Figure 4 Light time-dependant 19F NMR spectra of compound 4 due to trans to cis photoisomerization
设计并合成了一种新型氟代二苯乙烯非天然氨基酸(化合物4),斯托克斯位移为41 nm,激发、发射波长分别为314 nm、 355 nm,产率为47.4%,荧光量子产率为0.22,具有较好的荧光性能。化合物4在甲醇溶液中存在光致顺反异构现象,拟合得到的反式转变顺式构型的转变速率常数为0.026 min-1。氟谱表明反式结构和顺式结构中的氟原子的化学位移分别为-115.22和-115.53。因此我们可以通过光照来调控含有非天然氨基酸4的多肽或蛋白质分子的结构,并利用氟谱来研究这些大分子结构中4的片段所含乙烯桥的构象,从而可以探索这些大分子结构的构象与生理活性的关系。
