超高效液相色谱-串联四极杆飞行时间质谱法快速分析东革阿里化学成分
2020-05-09陈秀明周璟明郑孝贤王海龙陈楠楠方东升
陈秀明,周璟明,林 斌,郑孝贤,王海龙,陈楠楠,詹 清,方东升
(福建省微生物研究所,福建省新药(微生物)筛选重点实验室,福建 福州 350007)
东革阿里(EurycomalongifoliaJack)为苦木科(Simaroubaceae)东革阿里属植物,广泛分布于马来西亚、印度尼西亚、越南等东南亚国家,在原产地被称为马来西亚人参、天然伟哥等,与燕窝、锡器并称为马来西亚三大国宝,是东南亚最珍贵的应用植物药之一。东革阿里全株均可入药,常以根入药,具有抗癌、抗疟疾、抗菌、抗寄生虫以及改善男性性功能障碍等功效,还能提升人体机能、减轻疲劳、调节免疫、杀菌、抗溃疡、降血压、抗血管生成、治疗糖尿病、抗焦虑、镇痛抗炎及抗骨质疏松等多种功效[1-2]。
研究表明,东革阿里中含有多种化学成分,以苦木素二萜与β-咔巴啉类生物碱两类化合物为主,此外还含有铁屎米-6-酮类生物碱、木脂素、角鲨烯衍生物、香豆素、氨基酸类、甾醇类等成分。由于含有独特结构类型的化合物和多种重要的生物活性,近年来东革阿里一直备受国内外学者关注[3-15]。目前,东革阿里的研究主要集中在化学成分的提取分离[2,13-15]、少数成分的定量分析[16-23]和药理毒理方面[1,3-12,24],关于东革阿里及其制剂中化学成分的综合定性鉴别却鲜有报道,国内也未见相关文献,因此有必要建立一种快速、高效、全面阐明东革阿里化学成分的分析方法。
本文采用超高效液相色谱-串联四极杆飞行时间质谱法(UPLC-Q-TOF-MS)对东革阿里提取物进行分析研究,结合对照品比对及高分辨质谱数据解析,鉴定出49种化学成分,包括29种苦木素二萜、4种β-咔巴啉类生物碱、12种铁屎米-6-酮类生物碱、3种联苯新木脂素及1种角鲨烯型三萜。该方法快速、可靠、高效,能较全面地反映东革阿里的化学成分,可为深入阐明东革阿里的药效物质基础及其质量标准研究提供可靠的方法,也可为东革阿里的进一步开发与应用提供依据。
1 实验部分
1.1 仪器与试剂
Agilent 1290高效液相色谱系统;Agilent 6545 Q-TOF质谱仪(电喷雾离子源,正离子模式);微型植物试样粉碎机(北京中兴伟业仪器有限公司);KQ-5200DE数控型超声清洗器(昆山市超声仪器有限公司);XSE105十万分之一分析天平(Mettler Toledo公司);Milli-Q超纯水仪(Millipore公司,USA);高速离心机(美国Beckman公司)。
宽缨酮(Eurycomanone)、13α-(21)-环氧宽缨酮(13α-(21)-Epoxyeurycomanone)、东革内酯(Eurycoma lactone)和14,15β-Dihydroxyklaineanone对照品均购自成都普瑞法科技开发有限公司;β-咔巴啉-1-丙酸(β-Carboline-1-propionic acid)对照品购自上海泽叶生物科技有限公司;9-甲氧基-铁屎米-6-酮(9-Methoxycanthin-6-one)对照品购自武汉天植生物科技有限公司。东革阿里药材购自北京博远欣绿生物科技有限公司(规格:80 g,批号:20181001)。乙腈、甲醇、甲酸(色谱纯,德国Merck公司),乙醇(分析纯,国药集团化学试剂有限公司);超纯水由Milli-Q制备。
1.2 实验方法
1.2.1 溶液的制备供试品溶液的制备:将东革阿里根粉碎过筛,称取约5.0 g于250 mL三角瓶中,加入30%乙醇水溶液100 mL于90 ℃水浴中加热提取3次,提取时间分别为2.0、1.5、1.0 h,4 000 r/min离心分离15 min,合并上清液,减压浓缩后,取浓缩液(质量浓度按宽缨酮计为167.85 μg/mL)1.0 mL以0.22 μm微孔滤膜过滤后进行分析。
对照品溶液的制备:取宽缨酮、13α-(21)-环氧宽缨酮、东革内酯、14,15β-Dihydroxyklaineanone、β-咔巴啉-1-丙酸和9-甲氧基-铁屎米-6-酮对照品,精密称定,分别置于10 mL棕色量瓶中,加入适量甲醇超声助溶,放冷后定容至刻度,即得质量浓度分别为203.47、183.34、182.26、247.25、195.03、164.64 μg/mL的单一对照品贮备液。分别精密吸取上述贮备液0.5 mL于10 mL棕色量瓶中,以甲醇稀释至刻度,得质量浓度分别为10.17、9.167、9.113、12.36、9.752、8.232 μg/mL的混合对照品溶液。取混合对照品溶液1.0 mL以0.22 μm微孔滤膜过滤后测定。
1.2.2 UPLC-Q-TOF-MS分析条件色谱条件:色谱柱为Agilent Eclipse Plus-C18RRHD柱(2.1 mm×100 mm,1.8 μm);流动相A为0.1%甲酸,流动相B为乙腈,梯度洗脱:0~3 min,5%B,3~20 min,5%~30%B,20~32 min,30%~98%B,32~35 min,98%B,35~40 min,98%~5%B,40~45 min,5%B;流速:0.2 mL/min,柱温:40 ℃,DAD(G7117A)检测,进样量1 μ L。
质谱条件:ESI离子源,采用正离子检测模式;鞘气温度:350 ℃,鞘气流速:11.0 L/min;喷嘴电压:500 V;毛细管电压:3 500 V;雾化气压力:0.24 MPa(35 psig);干燥气温度:320 ℃,干燥气流速:8.0 L/min;毛细管出口电压:135 V;Skimmer电压:65 V;八级杆电压:750 V;碰撞能量(CE):15~40 V;全扫描模式采集,扫描范围:m/z100~800。
2 结果与讨论
2.1 总离子流图的测定
采用参比溶液校准仪器质量数后,取东革阿里提取液,按“1.2.1”制备供试品溶液,“1.2.2”分析条件进行测定,得到正离子模式下的总离子流图(见图1)。样品经全扫描后,获得东革阿里提取液中各色谱峰的保留时间、准分子离子峰及MS/MS碎片离子的精确相对分子质量信息。通过与部分对照品质谱信息、参考文献数据比对,获得各色谱峰的分子式并进行结构归属,从东革阿里提取液中鉴别出49种化合物,包括29种苦木素二萜、4种β-咔巴啉类生物碱、12种铁屎米-6-酮类生物碱、3种联苯新木脂素及1种角鲨烯型三萜,结果如表1所示(为方便表述,表中碎片离子(MS/MS fragment ion)均以整数表示)。

图1 东革阿里提取液的总离子流图Fig.1 Total ion chromatogram of Eurycoma longifolia Jack extract the peak numbers denoted were the same as those in Table 1

表1 东革阿里化学成分的UPLC-Q-TOF-MS分析结果Table 1 Analysis results of chemical constituents in Eurycoma longifolia Jack by UPLC-Q-TOF-MS

(续表1)
*identified by comparing with reference standards
2.2 东革阿里化学成分的鉴定与分析
2.2.1 苦木素二萜类化合物的鉴定由表1可知,在正离子模式下从东革阿里提取物中共鉴定出29种苦木素二萜,根据结构类别具体包括5种C18laurycomalactone型二萜类(16、37、42~43、45号峰)、7种C19eurycomalactone型二萜类(9、25、29、31~32、36、44号峰)、3种C19longilactone型二萜类(12、18、38号峰)、11种C20eurycomanone型二萜类(3、5~8、10、13~15、19、26号峰)及3种C20klaineanone型二萜类(21、23、27号峰)。根据二级质谱碎片信息、部分对照品信息及文献数据[17,25],可知苦木素二萜类化合物的主要裂解途径为准分子离子[M+H]+脱去H2O、CO中性碎片和呋喃环开裂脱去—CH2O,其中准分子离子单脱水的[M+H-H2O]+碎片多为基峰,以7号峰为例阐述其裂解过程。
7号峰的保留时间为15.057 min,在正离子模式下,一级质谱(图2A)的准分子离子([M+H]+)为m/z409.149 3,[M+Na]+和[2M+Na]+离子的m/z分别为431.131 1和839.273 8,推测其分子式为C20H24O9,误差在±5×10-6范围内。二级质谱(图2B)中可见准分子离子脱水后形成的基峰[M+H-H2O]+m/z391.138 8,该碎片离子进一步脱水形成[M+H-2H2O]+m/z373.129 7碎片离子,其可通过脱水、脱羰基分别形成[M+H-3H2O]+m/z355.115 4和[M+H-2H2O-CO]+m/z345.133 4的碎片离子,前者通过进一步脱羰基或后者通过脱水形成[M+H-3H2O-CO]+m/z327.123 1碎片离子,该碎片离子再通过呋喃环开裂脱去-CH2O和脱水分别生成[M+H-3H2O-CO-CH2O]+m/z297.111 1碎片离子和[M+H-4H2O-CO]+m/z309.111 8,二者可分别通过脱水和脱去-CH2O生成[M+H-4H2O-CO-CH2O]+m/z279.100 4碎片离子,该碎片离子也可由碎片离子[M+H-3H2O]+m/z355.115 4先后脱水脱羰基及呋喃环开裂脱去-CH2O后产生,其可进一步脱去羰基产生[M+H-4H2O-2CO-CH2O]+m/z251.106 9碎片离子(亦可由[M+H-3H2O-CO-CH2O]+m/z297.111 1碎片离子先后脱羰基脱水产生),该碎片离子分别通过脱去-CH2CO和-C2H2生成[M+H-4H2O-2CO-CH2OCH2CO]+m/z209.131 6和[M+H-4H2O-2CO-CH2OC2H2]+m/z225.125 0碎片离子,后者进一步脱CO最终生成[M+H-4H2O-3CO-CH2OC2H2]+m/z197.130 0碎片离子。以上裂解过程与文献报道的宽缨酮的质谱裂解途径一致[17,25]。综合以上信息,推断7号峰的化学成分为C20eurycomanone型二萜类化合物宽缨酮(Eurycomanone),精确分子量为408.142 0,分子式为C20H24O9,其为本次检出的苦木素二萜类化合物中含量最高的组分,常作为东革阿里提取物的指标性成分,因分子结构中含有多个羟基,存在多种可能脱水方式,图3给出了其中一种可能的裂解途径。

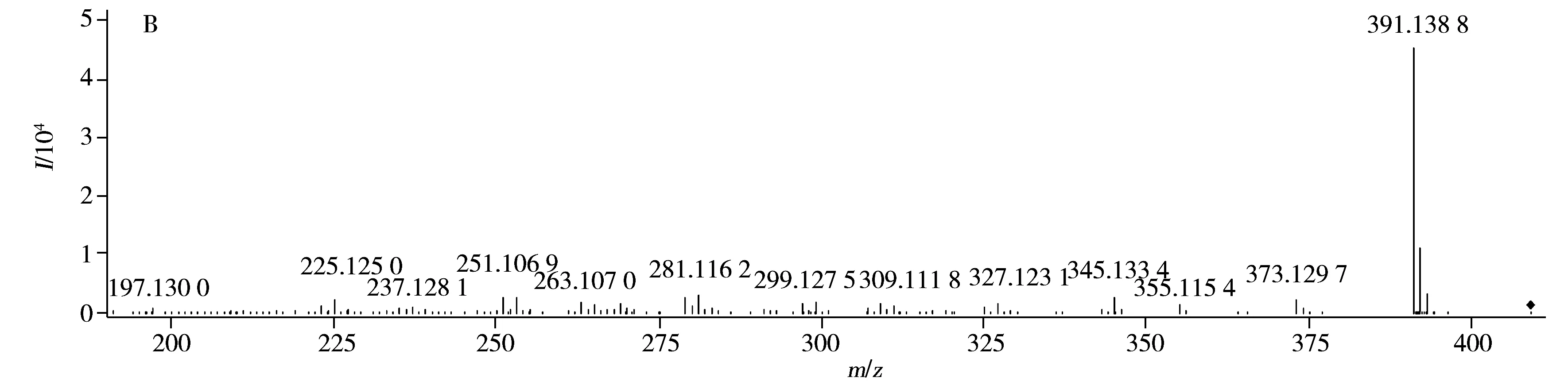
图2 7号峰在正离子模式下的一级质谱图(A)与精确质量数409.149 3峰的二级质谱图(B)Fig.2 MS spectrum of No.7(A) and secondary MS spectrum of 409.149 3(B) in positive ion mode

图3 宽缨酮的可能裂解途径Fig.3 Proposed fragmentation process of eurycomanone
10号峰的保留时间为15.356 min,在正离子模式下的准分子离子为[M+H]+m/z411.165 0,[M+Na]+离子的m/z为433.146 3,推测其分子式为C20H26O9。其结构与宽缨酮相似,结合苦木素二萜类化合物的裂解规律和文献数据[17],推测其为C20eurycomanone型二萜类化合物Eurycomanol(宽缨酮醇)。
2.2.2 生物碱类化合物的鉴定东革阿里植物中分离得到的生物碱大致可分为3类,即β-咔巴啉类生物碱、铁屎米-6-酮类生物碱和铁屎米-5,6-二酮类生物碱。通过比较出峰时间及分析质谱裂解规律,结合参考文献和部分对照品数据信息,在正离子模式下,共鉴定出16种生物碱类化合物,包括4种β-咔巴啉类生物碱、12种铁屎米-6-酮类生物碱。
2.2.2.1β-咔巴啉类生物碱的鉴定β-咔巴啉类生物碱是东革阿里的主要有效成分之一,本次检出4种(1~2、4、11号峰),分别为1-甲氧基甲基-β-咔巴啉(1-Methoxymethyl-β-carboline)、7-羟基-β-咔巴啉-1-丙酸(7-Hydroxy-β-carboline-1-propionic acid)、β-咔巴啉-1-丙酸(β-Carboline-1-propionic acid)和7-甲氧基-β-咔巴啉-1-丙酸(7-Methoxy-β-carboline-1-propionic acid),其中β-咔巴啉-1-丙酸含量最高,7-甲氧基-β-咔巴啉-1-丙酸次之。本类化合物由于分子结构中吡啶环侧链含羧基且吲哚环上多有羟基取代,故极性较大,保留时间较短,在正离子模式下的裂解方式主要为吡啶并吲哚环侧链羧基脱去H2O、CO中性碎片或-CH2O2、-C2H4O2和-C3H6O2碎片,以及吡啶环的α裂解,以4号峰为例阐述其裂解过程。
4号峰的保留时间为13.914 min,在正离子模式下一级质谱(图4A)的准分子离子为[M+H]+m/z241.097 0,推测其分子式为C14H12N2O2,误差在±5×10-6范围内。二级质谱(如图4B)中首先可见准分子离子脱水后形成丰度较低的[M+H-H2O]+m/z223.086 3碎片离子,该碎片离子不稳定可通过脱CO形成丰度较大的[M+H-CH2O2]+m/z195.091 8碎片离子,其可逐级脱去吡啶侧链烯烃的亚甲基生成[M+H-C2H4O2]+m/z181.076 1和[M+H-C3H6O2]+m/z167.064 6碎片离子,二者可进一步发生吡啶环的α裂解脱去1分子HCN,分别生成[M+H-C3H5NO2]+m/z154.065 4和[M+H-C4H7NO2]+m/z140.048 5碎片离子。以上裂解过程与文献[17]报道的β-咔巴啉-1-丙酸(β-Carboline-1-propionic acid)的质谱裂解途径一致。综合以上信息,推断4号峰的化学成分为β-咔巴啉-1-丙酸,精确分子量为240.089 9,分子式为C14H12N2O2,其裂解途径如图5所示。


图4 4号峰在正离子模式下的一级质谱图(A)与精确质量数241.097 0峰的二级质谱图(B)Fig.4 MS spectrum of No.4(A) and secondary MS spectrum of 241.097 0(B) in positive ion mode

图5 β-咔巴啉-1-丙酸可能的裂解途径Fig.5 Proposed fragmentation process of β-carboline-1-propionic acid
1号峰的保留时间为10.750 min,在正离子模式下的准分子离子为[M+H]+m/z213.102 1,推测其分子式为C13H12N2O。通过与β-咔巴啉-1-丙酸类生物碱的裂解规律和文献数据对比[17],推测其为1-甲氧基甲基-β-咔巴啉。2号峰的保留时间为11.794 min,在正离子模式下的准分子离子为[M+H]+m/z257.091 9,相对分子质量、碎片离子和β-咔巴啉-1-丙酸均相差16 Da,推测其分子式为C14H12N2O3。通过与β-咔巴啉-1-丙酸类生物碱的裂解规律和文献数据对比[17],推测其为7-羟基-β-咔巴啉-1-丙酸。
2.2.2.2 铁屎米-6-酮类生物碱的鉴定东革阿里植物中分离得到的铁屎米-6-酮类生物碱按结构类别可细分成3种类型,分别为铁屎米-6-酮类生物碱(Canthin-6-one)、铁屎米-6-酮的3-位氮上形成N-氧化物的季铵类生物碱(Canthin-6-one-3-N-oxide)及铁屎米-5,6-二酮类生物碱(Canthin-5,6-dione)。通过比较出峰时间及分析质谱裂解规律,结合文献和部分对照品数据信息,共鉴定出12种铁屎米-6-酮类生物碱,包括9种铁屎米-6-酮类生物碱(17、28、30、34~35、40、46~48号峰)、2种季铵类生物碱(39、41号峰)、1种报道较少的铁屎米-5,6-二酮类生物碱(22号峰),其中铁屎米-6-酮(46号峰)、9-甲氧基-铁屎米-6-酮(47号峰)的含量最高。该类化合物的主要裂解途径为母环中2-吡啶酮脱去CO或-CHO,其次是2-吡啶酮的逆狄尔斯-阿德尔(retro-Diels-Alder,RDA)裂解和吡啶环的α裂解,此外也可见准分子离子脱去苯环上取代基生成的碎片。以46号峰为例阐述此类化合物的裂解过程。
46号峰的保留时间为28.521 min,一级质谱(图6A)的准分子离子为[M+H]+m/z221.070 8,推测其分子式为C14H8N2O,误差在±5×10-6范围内。二级质谱(图6B)中首先观察到准分子离子分别脱去CO和-CHO后生成的基峰[M+H-CO]+m/z193.075 2和碎片离子[M+H-CHO]+m/z192.068 3,二者可通过RDA裂解脱去-C2H2分别生成碎片离子[M+H-C3H2O]+m/z167.061 0和[M+H-C3H3O]+m/z166.064 1,其中[M+H-C3H2O]+m/z167.061 0也可由准分子离子发生2-吡啶酮的RDA裂解脱去-C2H2生成的碎片离子[M+H-C2H2]+m/z195.083 7进一步脱CO后产生,该碎片离子可进一步发生吡啶环的α裂解脱去1分子HCN后,生成碎片离子[M+H-C4H3NO]+m/z140.048 8。以上裂解过程与文献报道的铁屎米-6-酮(Canthin-6-one)质谱裂解途径一致[17]。综合以上信息并结合文献分析,推断该成分为铁屎米-6-酮,其裂解途径如图7所示。

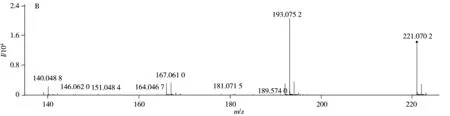
图6 46号峰在正离子模式下的一级质谱图(A)与精确质量数221.070 8峰的二级质谱图(B)Fig.6 MS spectrum of No.46(A) and secondary MS spectrum of 221.070 8(B) in positive ion mode
22号峰的保留时间为19.909 min,在正离子模式下的准分子离子为[M+H]+m/z281.091 7,推测其分子式为C16H12N2O3。结合铁屎米-5,6-二酮类生物碱裂解规律和文献数据结果[17],推测其为9-甲氧基-3-甲基-铁屎米-5,6-二酮(9-Methoxy-3-methylcanthin-5,6-dione)。39号峰的保留时间为26.807 min,在正离子模式下的准分子离子为[M+H]+m/z267.076 1,推测其分子式为C15H12N2O3。结合铁屎米-6-酮-3-N-氧化物(Canthin-6-one-3N-oxide)类生物碱裂解规律和文献数据结果[17],推测其为9-甲氧基-铁屎米-6-酮-3-N-氧化物(9-Methoxycanthin-6-one-3N-oxide)。
此外,在铁屎米-6-酮类生物碱的鉴定过程中发现,部分异构体(30号峰和34号峰)的保留时间和二级碎片离子均极其相似,因此取代基的连接位置不能确定,仅对其进行结构表征,需要进一步获取对照品以进行最终归属。
2.2.3 木脂素类化合物的鉴定东革阿里植物中分离得到的木脂素类化合物,已报道的有6种,其中有4种联苯新木脂素类化合物,本次检出3种(20、24和33号峰)。该类化合物的主要裂解途径为准分子离子脱去苯环上的甲基或甲氧基、苯丙素单元上的羟基或整个基团,其次是苯丙素单元分别发生RDA裂解。以20号峰为例阐述其裂解过程。

图7 铁屎米-6-酮的可能裂解途径Fig.7 Proposed fragmentation process of canthin-6-one
20号峰的保留时间为18.981 min,一级质谱(图8A)的准分子离子为[M+H]+m/z377.159 1,推测其分子式为C20H24O7,误差在±5×10-6范围内。二级质谱(图8B)中首先可见准分子离子分别脱甲基和2分子甲氧基后形成的碎片离子[M+H-CH3]+m/z362.170 5、[M+H-C2H6O2]+m/z315.172 9;其次是准分子离子优先脱去丙三醇基团后形成的碎片离子[M+H-C3H6O3]+m/z287.158 5 ,其进一步脱水生成基峰[M+H-C3H8O4]+m/z269.153 1,同时准分子离子另一侧苯丙素单元的烯丙醇可通过脱水生成[M+H-H2O]+m/z359.110 9碎片离子,其可进一步脱去苯环上2个甲基生成碎片离子[M+H-C2H6]+m/z329.622 8;再次,在质谱图中可观测到准分子离子中两个苯丙素单元发生RDA裂解分别生成[M+H-C5H8O3]+m/z261.433 1和[M+H-C5H6O]+m/z295.126 2碎片离子,后者可分别通过脱水、脱-CH3OH最终分别生成碎片离子[M+H-C5H8O2]+m/z276.899 3、[M+H-C6H10O2]+m/z263.096 9。以上裂解过程与文献报道的2,2′-二甲氧基-4-(3-羟基-1-丙烯基)-4′-(1,2,3-三羟丙基)-二苯醚(2,2′-Dimethoxy-4-(3-hydroxy-1-propenyl)-4′-(1,2,3-trihydroxypropyl)-diphenyl ether)裂解产生的碎片吻合[17]。综合以上信息并结合文献分析,推断该成分为2,2′-二甲氧基-4-(3-羟基-1-丙烯基)-4′-(1,2,3-三羟丙基)-二苯醚,其裂解途径如图9所示。
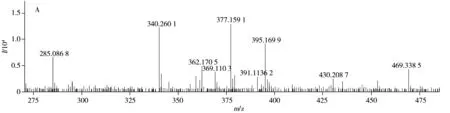
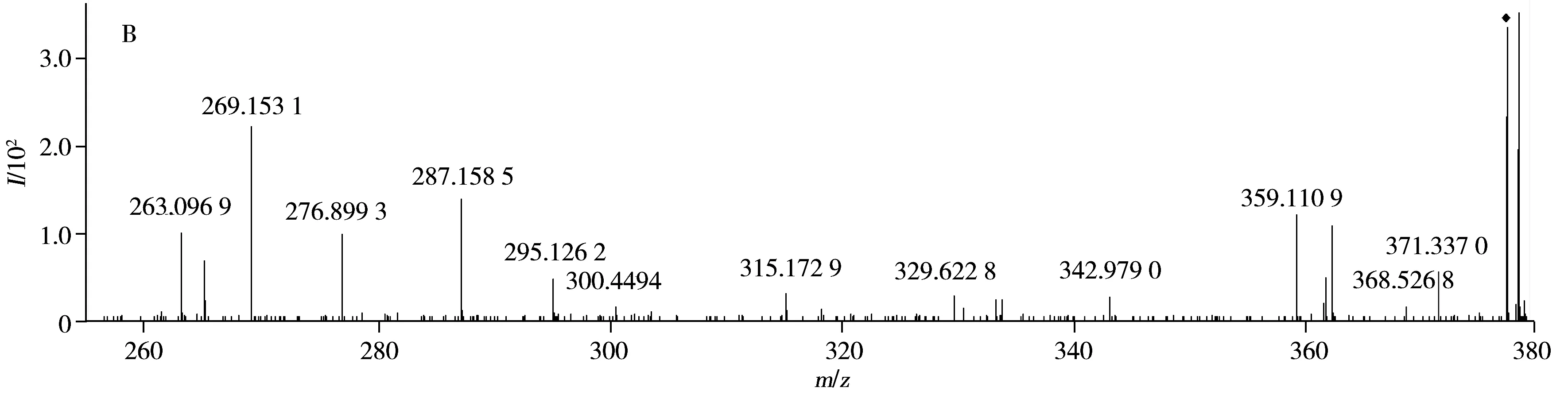
图8 20号峰在正离子模式下的一级质谱图(A)与精确质量数377.159 1峰的二级质谱图(B)Fig.8 MS spectrum of No.20(A) and secondary MS spectrum of 377.159 1(B) in positive mode
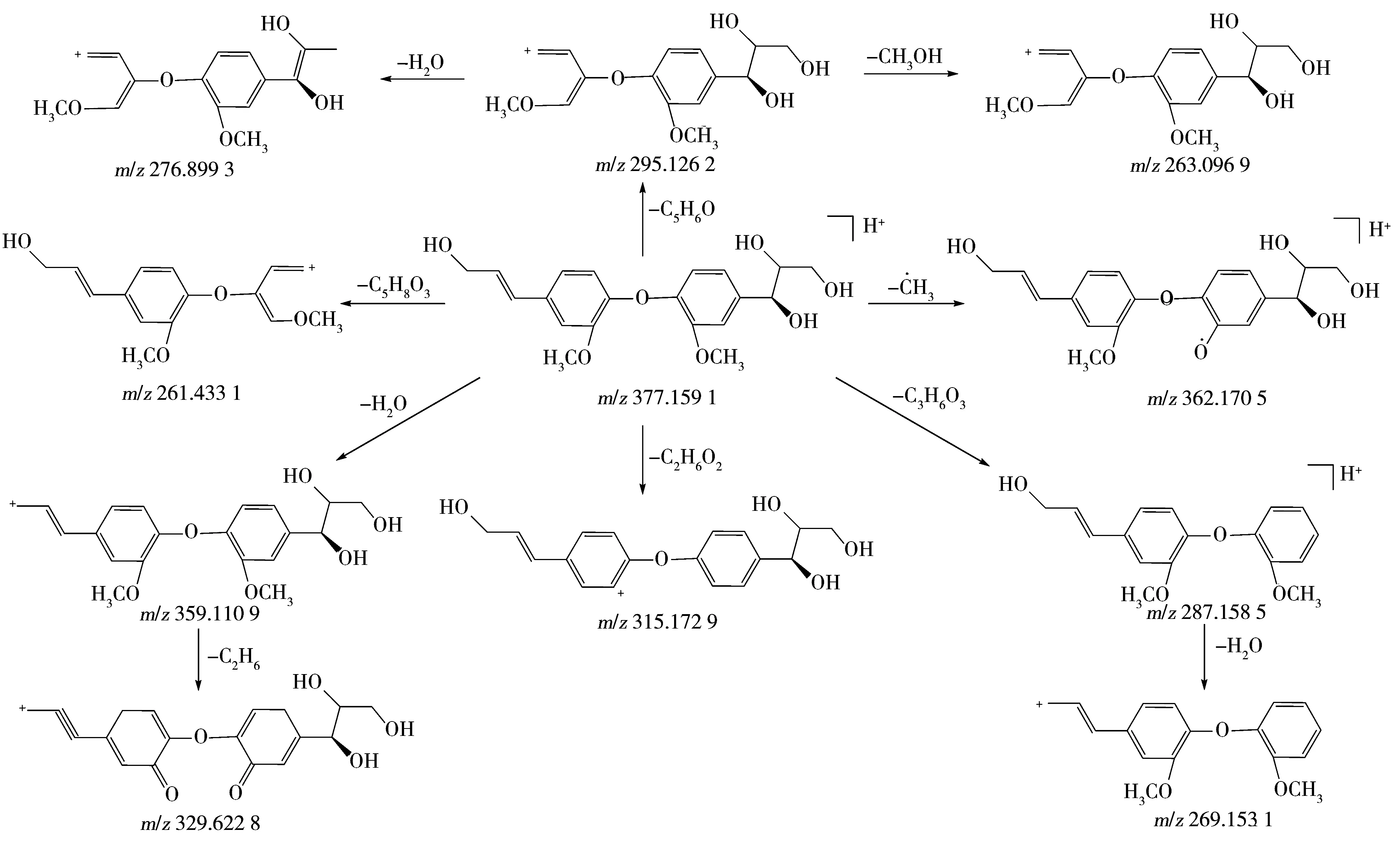
图9 2,2′-二甲氧基-4-(3-羟基-1-丙烯基)-4′-(1,2,3-三羟丙基)-二苯醚的可能裂解途径Fig.9 Proposed fragmentation process of 2,2′-dimethoxy-4-(3-hydroxy-1-propenyl)-4′-(1,2,3-trihydroxypropyl)-diphenyl ether
24号峰的保留时间为20.929 min,在正离子模式下的准分子离子为[M+H]+m/z359.148 5,推测其分子式为C20H22O6。通过与木脂素衍生物的裂解规律和文献数据对比,推测其为2-羟基-3,2′-二甲氧基-4′-(2,3-环氧-1-羟丙基)-5-(3-羟基-1-丙烯基)联苯(2-Hydroxy-3,2′-dimethoxy-4′-(2,3-epoxy-1-hydroxypropyl)-5-(3-hydroxy-1-propenyl)-biphenyl)。33号峰的保留时间为25.237 min,在正离子模式下的准分子离子为[M+H]+m/z389.158 9,推测其分子式为C21H24O7。通过与木脂素衍生物的裂解规律和文献数据对比,推测其为2-羟基-3,2′,6′-三甲氧基-4′-(2,3-环氧-1-羟丙基)-5-(3-羟基-1-丙烯基)联苯(2-Hydroxy-3,2′,6′-trimethoxy-4′-(2,3-epoxy-1-hydroxypropyl)-5-(3-hydroxy-1-propenyl)-biphenyl)。
2.2.4 角鲨烯衍生物类化合物的鉴定东革阿里植物中分离得到的角鲨烯衍生物,已报道的有4种,分别为Eurylene、Longilene peroxide、Teurilene与11/14-Deacetyl eurylene。据报道此类化合物均具有很强的抗癌活性。本实验仅检出1种(49号峰)。
49号峰的保留时间为36.565 min,一级质谱(图10A)的准分子离子为[M+H]+m/z553.409 1,推测其分子式为C32H56O7,误差在±5×10-6范围内。二级质谱(图10B)中首先可见准分子离子逐级脱水后形成的碎片离子[M+H-H2O]+m/z535.397 8、[M+H-2H2O]+m/z517.382 2、[M+H-3H2O]+m/z499.371 4,其中碎片离子[M+H-H2O]+m/z535.397 8可通过脱去—C2H4O2酯基生成碎片离子[M+H-C2H6O3]+m/z475.377 3,该碎片离子可脱水生成基峰[M+H-C2H8O4]+m/z457.365 5(也可由碎片离子[M+H-3H2O]+m/z499.371 4脱去乙酰基产生),其可进一步通过逐级脱水和α裂解分别生成碎片离子[M+H-C2H10O5]+m/z439.354 7、[M+H-C2H12O6]+m/z421.340 1和[M+H-C19H34O6]+m/z195.170 5;其次,准分子离子可脱去甲基和侧链乙酰基后形成碎片离子[M+H-C3H6O]+m/z495.443 7;此外,还可观察到准分子离子直接α裂解生成的碎片离子[M+H-C19H32O5]+m/z213.161 9。综合以上信息并结合文献[17],推断该成分为11-Deacetyl eurylene或14-Deacetyl eurylene,图11以11-Deacetyl eurylene为例列出了其可能的裂解途径。
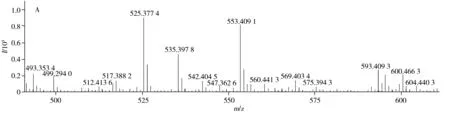

图10 49号峰在正离子模式下的一级质谱图(A)与精确质量数553.409 1峰的二级质谱图(B)Fig.10 MS spectrum of No.49(A) and secondary MS spectrum of 553.409 1(B) in positive ion

图11 11-Deacetyl eurylene的可能裂解途径Fig.11 Proposed fragmentation process of 11-deacetyl eurylene
2.3 化学结构验证
为验证“2.2”中所鉴定化学结构的可靠性,在相同条件下分别测定其色谱保留时间及质谱数据,若目标成分与其对照品的保留时间、准分子离子峰、同位素分布和二级特征离子吻合,则可判定为该化合物。如上文中鉴定精确质量数为409.149 3的7号峰为宽缨酮,则以其标准品为对照,在相同条件下测定宽缨酮对照品的保留时间及质谱数据。结果显示,宽缨酮对照品及东革阿里样品中精确质量数为409.149 3的组分的保留时间均为15.057 min,且宽缨酮对照品的二级质谱图与图2B中的碎片离子完全吻合,证明该峰为宽缨酮,说明推测结果可靠。
3 结 论
本文采用UPLC-Q-TOF-MS法从东革阿里提取液中鉴定出49种化学成分,包括29种苦木素二萜、4种β-咔巴啉类生物碱、12种铁屎米-6-酮类生物碱、3种联苯新木脂素类及1种角鲨烯型三萜,并初步分析了其质谱裂解规律。6种成分(宽缨酮、13α-(21)-环氧宽缨酮、东革内酯、14,15β-Dihydroxyklaineanone、β-咔巴啉-1-丙酸和9-甲氧基-铁屎米-6-酮)经与对照品比对以及结合文献数据而准确鉴定,其中宽缨酮、13α-(21)-环氧宽缨酮、β-咔巴啉-1-丙酸、7-甲氧基-β-咔巴啉-1-丙酸和9-甲氧基-铁屎米-6-酮为本次东革阿里提取液中检出含量最高的5个成分。同时,在铁屎米-6-酮类生物碱的鉴定过程中发现,部分异构体的保留时间和二级碎片离子均极其相似,因此取代基的连接位置不能确定,仅进行了结构表征,未能最终归属,需进一步优化质谱分析参数以获得更详尽的二级质谱或通过获取对照品进行确证。此外,由图1总离子流图可见,东革阿里成分复杂,仍有很多组分(如小分子肽、氨基酸类、香豆素、甾醇等)未能归属,后续将进一步深入此方面的研究。结果表明,UPLC-Q-TOF-MS可系统、高效、准确地对东革阿里中的化学成分进行快速定性分析,能较全面地反映东革阿里中成分的化学组成,为深入研究其药效物质基础和质量控制方法提供了依据。
