血清胱抑素C、NIHSS与首发急性脑梗死患者卒中后抑郁相关性分析
2020-05-06邢立棉李岩松苏东风
邢立棉,李岩松,苏东风
(锦州医科大学解放军北部战区空军医院 a.研究生培养基地; b.神经内科, 辽宁 沈阳 110042)
近年来,脑卒中已成为全球第三大死因,且首发脑卒中人数明显增加,脑卒中包括出血性脑卒中和缺血性脑卒中两类,其中缺血性脑卒中约占70%[1]。卒中后抑郁(post-stroke depression, PSD)为一类脑卒中后常见的情感障碍性综合征,主要表现为一系列以情感低落、兴趣缺失为主的抑郁症状及相应的躯体化症状[2]。有研究发现PSD综合发病率约为30%[3]。PSD的病理生理过程十分复杂,其由脑组织缺血引发的神经生物学障碍以及心理社会困扰共同作用引发。额叶-基底节-脑干通路损伤引起单胺类神经递质系统破坏、急性缺血性脑卒中神经组织损伤、下丘脑-垂体-肾上腺轴应激激活、能量代谢改变(线粒体功能障碍,氧化应激)等均参与PSD的病理生理过程[4]。PSD的危险因素有很多,包括卒中的严重程度、个人精神疾病史、家族精神疾病史、社会和家庭支持、年龄、认知功能障碍、神经质、独立生活能力等[5],近年对于NIHSS和血清胱抑素C(serum cystatin C,Cys C)与PSD的关系成为研究热点。本文就此进行研究。
1 资料与方法
1.1 病例选择 2019年1月1日至2019年6月30日于我院神经内科住院治疗的首次发病的急性脑梗死患者101例,均为连续入组。其中男74例,女27例,年龄35~79岁,平均(63.11±9.65)岁。在发病后1个月时诊断为PSD的患者37例,男25例,女12例,年龄35~79岁,平均(65.78±11.23)岁,发病率36.6%,其中轻度抑郁19例(51.4%),中度抑郁13例(35.1%),重度抑郁5例(13.5%)。所有患者均签署知情同意书。本研究已通过伦理委员会审批。
1.2 纳入及排除标准 纳入标准:年龄≥18岁,且≤80岁;缺血性脑卒中诊断:所有纳入患者均符合《中国急性缺血性脑卒中诊治指南2018》[6]中急性脑梗死的诊断标准;卒中发病后7天内入院;急性缺血性脑卒中为首次发作,既往无缺血性脑卒中及出血性脑卒中病史;患者需能完成1个月随访,且可以完成汉密尔顿抑郁评分量表(Hamilton Depression Rating Scale, HAMD);排除高尿酸血症、痛风及相关代谢疾病;所有患者均自愿加入本研究且取得家属同意,并签署知情同意书。排除标准:年龄>80岁,<18岁;既往有个人精神疾病史及家族精神疾病史;既往出血性脑卒中或缺血性脑卒中病史;有抗抑郁药物或抗精神疾病药物服用史;合并严重心、肺、肾、肝、恶性肿瘤等疾病及其他严重躯体疾病;合并有意识障碍、严重失语、严重听力障碍、智力障碍、理解障碍等不能配合完成者;有酒精、毒品及其他药物滥用史。
1.3 临床资料
1.3.1 一般资料 入院后收集符合纳入标准的患者的性别、年龄、吸烟史、饮酒史、心房颤动史、高血压病史、糖尿病史、冠心病史、高脂血症史等临床资料。
1.3.2 实验室指标测定 入院后第二天对所有研究对象空腹抽取静脉血,检查肝肾功能、血脂、血糖、电解质等生化指标,并收集血清胱抑素C指标。
1.3.3 美国国立卫生研究院卒中量表评分(National Institutes of Health Stroke Scale, NIHSS) 入院后2小时内对所有患者完善NIHSS并记录,以评定其神经系统损伤程度。NIHSS量表为目前临床中应用最广泛的缺血性脑卒中神经功能损伤评定量表。该量表从意识、眼球运动、视野、肢体运动、感觉、反射、语言、构音障碍、肢体共济等11方面对神经系统功能进行评定。通常0~5分为轻度卒中,6~20分为中度卒中,21分以上为重度卒中。
1.4 分组及评估工具 由两名经过训练的神经内科医师对患者发病后1个月进行评估。参照《卒中后抑郁临床实践的中国专家共识》[2]诊断标准,判断研究对象有无抑郁,并根据判断结果分为PSD组和non-PSD组。并应用HAMD 17项评分版本对PSD组患者进行评分,测评抑郁的严重程度。HAMD 17评分结果,分数为>7分且≤17分为轻度抑郁,评分>17分且≤24分为中度抑郁,分数>24分为重度抑郁。依据HAMD17结果将PSD组分为轻度PSD组和中重度PSD组。HAMD由Hamilton于1960年设计制定,为目前临床中应用最广泛的经典抑郁症状他评量表,适用于有抑郁症状的成年患者。该表主要从焦虑/躯体化、认识障碍、阻滞、体重、睡眠障碍、绝望感、日夜变化等7类因子进行评定。据报道该量表的有效度为0.65~0.90[7]。

2 结 果
2.1 基础资料与病史比较 3组在吸烟史、饮酒史、性别、年龄等差异无统计学意义(P>0.05),且3组对象在糖尿病、高血压、冠心病、心房颤动、高血脂等差异无统计学意义(P>0.05),见表1。
2.2 NIHSS、Cys C水平比较 3组间NIHSS及Cys C水平差异有统计学意义(P<0.05),且中重度PSD组的NIHSS、Cys C水平大于轻度PSD组及non-PSD组;轻度PSD组NIHSS、Cys C水平大于non-PSD组(P<0.05),见表2。

表1 3组基础资料与病史比较
注:*:采用Fisher确切概率法
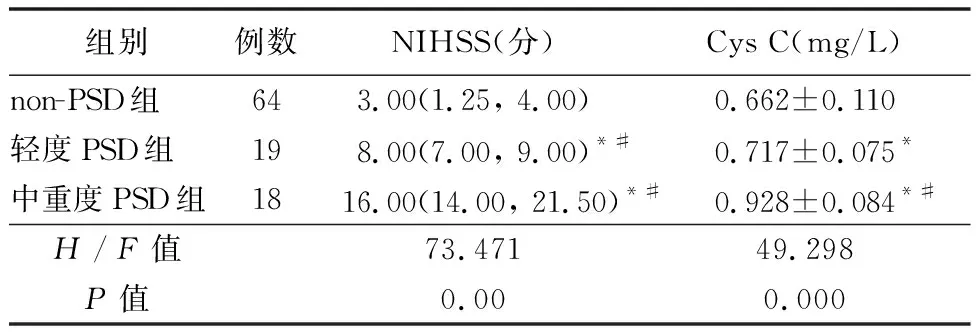
表2 3组NIHSS与Cys C比较
注:与non-PSD组比较,*P<0.01;与轻度PSD组比较,#P<0.01
2.3 R/S相关性分析 首次急性脑梗死患者NIHSS、血清胱抑素C水平与HAMD17评分呈正相关(r=0.766,r=0.511,P<0.05),见表3。

表3 HAMD17评分和各指标相关性分析
2.4 Logistic回归分析 将是否出现PSD作为应变量,将上述有统计学意义的NIHSS、Cys C作为自变量,进行logistic回归分析。NIHSS及Cys C为PSD发生的独立危险因素,见表4。
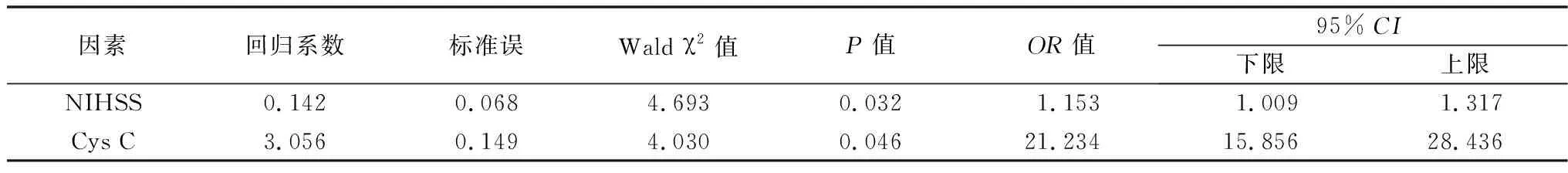
表4 PSD的logistic回归分析
3 讨 论
PSD为脑卒中后常见的并发症,该病除神经系统损伤引发的躯体障碍外,以情绪低落、兴趣缺失的抑郁症状为主,为一类情感障碍性疾病[2]。国外学者对PSD发病率进行Meta分析,发现其发病率有较大差异性,这可能与诊断标准模糊、实验方法、随访周期及随访人群特征有关[8]。我国2016年出版的PSD临床实践的中国专家共识中提到:“PSD可以发生在卒中后急性期(<1个月),中期(1~6个月)和恢复期(>6个月),发病率分别为33%、33%和34%”[2]。本研究结果显示在符合入组的101例患者中,缺血性脑卒中发病后1个月时有37例诊断为PSD,发病率为36.6%且以轻度抑郁为主,这与上述研究相符和。
当前,PSD发病机制尚不清楚,主要有神经递质学说、神经内分泌学说、神经解剖学说、炎性细胞因子学说、遗传背景及社会心理学说等几种,这几种机制不是独立存在,可能是相辅相成[9]。其中神经递质学说和神经解剖学说是指,大脑内存在控制情绪的重要环路系统即边缘-皮质-纹状体-苍白球-丘脑环路(limbic-cortical-striatal-palldal-thalamic circuit, LCSPTC),该环路涉及额叶、基底节区、苍白球、丘脑、扣带回、角回、海马区等重要结构,这些结构中均存在大量的去甲肾上腺素能神经元以及5-羟色胺能神经元,当这两种神经元受到损伤时,导致5-羟色胺(5-hydroxytryptamine, 5-HT)、去甲肾上腺素(norepinephrine, NE)及多巴胺(dopamine, DA)系统受损,引起体内NE和5-HT含量降低,进而引发PSD[10]。有学者[11]研究发现与对照组比较,PSD患者血清和脑脊液中5-HT明显降低。临床上应用选择性5-羟色胺再吸收抑制剂(selective serotonin reuptake inhibitor, SSRI)、5-羟色胺去甲肾上腺素再摄取抑制剂(serotonin-norepinephrine reuptake inhibitor, SNRI)、NE及特异性5-HT能抗抑郁剂(noradrenergic and specific serotonergic antidepressant, NaSSA)等药物治疗PSD后取得不错疗效,这也侧面支持上述机制[12]。近年关于NIHSS、Cys C与PSD关系成为研究热点。
NIHSS已经成为临床中评价缺血性脑卒中神经损伤程度应用最广泛的量表,其操作简单可在短时间内做出评价,能很好地评估神经系统损伤程度,并对是否存在血管闭塞及闭塞血管的位置有一定预测性[13]。国外学者[14]将奥平顿预后量表(Orpington Prognostic Scale,OPS)和NIHSS量表对脑卒中患者未来功能状态预测价值进行对比时发现,入院时NIHSS对患者未来功能状态预测价值低于OPS。入院时NIHSS越高缺血性脑卒中神经功能损伤越重,患者身体机能受到的损伤越大,患者需要外界的帮助就越大,这对患者心理冲击大,易出现负面情绪[15]。国内学者[16]对NIHSS和PSD关系进行研究发现,NIHSS越高PSD患病概率越大,这与本研究结果一致。本研究结果提示,中重度PSD组及轻度PSD组NIHSS明显高于non-PSD组,且中重度PSD组较轻度PSD组NIHSS显著增高(P<0.05),将NIHSS与抑郁程度趋势行相关性分析,结果显示NIHSS和抑郁程度呈正相关(r=0.766,P<0.05),且NIHSS为PSD发生的独立危险因素。
Cys C是一种反映肾脏功能的敏感指标,其以恒定速度产生于全身有核细胞。研究[17]发现大脑小动脉和肾脏入球小动脉在解剖基础及功能上有一定的相似性,且在动脉粥样硬化的早期Cys C参与了破坏血管壁的过程。有学者[18]发现CysC可以和α蛋白在脑小动脉壁周围结合形成淀粉沉淀物,这参与了认知功能障碍的病理过程。另有学者[19]在研究伴有PSD的不同类型缺血性脑卒中与认知功能障碍时发现,PSD的发生与缺血性脑梗死患者出现认知功能障碍有关,且前循环梗死患者更容易出现PSD。研究证实[20]Cys C水平与认知功能障碍严重程度呈正相关,Cys C可能通过引发认知功能障碍的过程参与PSD的病理过程,这需要进一步研究证实。国内学者[21]研究发现Cys C水平和PSD的发生及严重程度呈正相关。本研究发现轻度PSD组、中重度PSD组的血清胱抑素C水平明显高于non-PSD组(P<0.05),且中重度PSD组血清胱抑素C明显高于轻度PSD组(P<0.05),经相关性分析发现Cys C浓度和抑郁程度呈正相关(r=0.511,P<0.05),且高浓度Cys C为PSD发生的独立危险因素,这与上述研究结果相符合。
PSD的发生与NIHSS、Cys C呈正相关。临床中可以通过测定上述指标,预测急性脑梗死患者出现PSD的风险,有助于临床医师早期干预。
