基于FAERS的新型冠状病毒肺炎治疗用药
2020-04-29胡巧织罗敏王华玲吴斌徐珽
胡巧织,罗敏,王华玲,吴斌,徐珽
(1.四川大学华西医院临床药学部,成都 610041;2.四川大学华西药学院,成都 610041)
自新型冠状病毒肺炎(novel coronavirus pneumonia,NCP)疫情发生以来,我国国家卫生健康委员会第一时间制定一系列重大措施抗击NCP,并相继发布多版《新型冠状病毒感染肺炎诊疗方案》(试行)。在近期第五和第六版试行方案中都提及利巴韦林可作为抗病毒药物用于NCP患者的治疗[1]。利巴韦林是一种嘌呤核苷类似物,具有广谱的抗病毒活性。由于能抑制肌苷酸-5-磷酸脱氢酶,阻断肌苷酸转化为鸟苷酸,从而抑制病毒的RNA和DNA合成,对DNA病毒和RNA病毒均有抑制复制作用,利巴韦林在临床上得到广泛使用[2]。在2003年严重急性呼吸综合征(severe acute respiratory syndrome,SARS)流行期间,利巴韦林曾作为中国香港地区的推荐抗病毒药物之一和糖皮质激素联合使用来治疗SARS[3]。目前该药主要用于呼吸道合胞病毒感染以及联合α-干扰素治疗丙型肝炎[4]。但利巴韦林相关的药品不良事件(adverse drug event,ADE)高发,其中以贫血最常见,这也限制该药的临床应用。
目前,基于上报制度来研究药物安全信号的机构及其数据库有很多,如世界卫生组织(WHO)国际药品监测协作中心、美国不良事件报告系统(adverse events reporting system,AERS)、加拿大药物不良反应监测系统等。其中美国FDA不良事件报告系统(FAERS)因数据量大且对公众免费开放,常被用于药品不良事件信号挖掘研究[5]。在利巴韦林长期使用过程中,国外临床积累大量该药ADE数据,因此,笔者在本研究拟基于FAERS对利巴韦林的安全性进行分析,为该药在NCP患者中的安全应用提供依据。
1 资料与方法
1.1数据来源 本研究数据来源于FAERS数据库。该数据库2004年开始对外公开,每季度对其数据进行更新,以ASCII或XML形式存储。选择2004年至2019年64个季度ASCII数据进行分析[6]。每季度的ASCII数据均包含数据库说明和7个子文件,子文件分别是包括选择个人信息记录(DEMO)、不良事件记录(REAC)、药物使用记录(DRUG)、治疗结果记录(OUTC)、报告来源(RPSR)、治疗时间(THER)以及诊断(INDI)。本研究选择其中的DEMO、REAC、DRUG和OUTC数据表进行后续分析。
1.2数据处理 根据FAERS说明文件去除DEMO表的重复报告,并映射到DRUG、REAC和OUTC表。采用美国Vanderbilt大学开发的Medex_UIMA_1.3.7系统进行药品名称标准化和RxNorm编码(RxCUI)[7-8]。FAERS 不良事件数据采用《ICH国际医学用语词典》(Medical Dictionary for Regularly Activities,MedDRA)首选语(Preferred Terms,PT)编码。本研究下载MedDRA 21.1版,用于PT、高位语(High Level Term,HLT)、高位组语(High Level Group Term,HLGT)、系统器官分类(System Organ Class,SOC)编码和语言汉化[9]。
1.3数据提取 限定上报为“首要怀疑药品(primary suspect drug)”,筛选标准化DRUG表中RxCUI = 9344(Ribavirin)的记录作为目标药品。根据上述得到的报告编码和病例编码映射REAC表,筛选出对应报告事件并通过SOC映射到系统分类
1.4数据分析 采用比例失衡法(Disproportionality Methods)中报告比值比法(reporting odds ratio,ROR)和比例报告比值法(proportional reporting ratio,PRR)进行信号检测。该方法基于四格表(表1),通过比较目标药品的目标事件发生比例与其他所有药品的目标事件的发生比例(背景数据),以检测潜在ADE信号。PRR法报告数≥3,PRR≥2,且χ2≥4提示信号;ROR法双侧检验95%置信区间(CI)下限>1提示信号[10],即药品和事件之间潜在关联性。计数资料采用例数和构成比描述。统计分析采用SPSS 20.0版软件和Microsoft Excel 2016版软件。
表1 比例失衡法四格表
Tab.1Four-foldtableofdisproportionalitymethods

项目目标不良事件报告数其他不良事件报告数合计目标药物aba+b其他药物cdc+d合计a+cb+dN=a+b+c+d
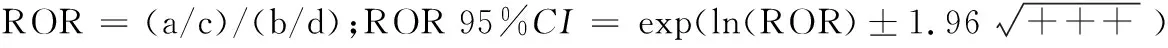

2 结果
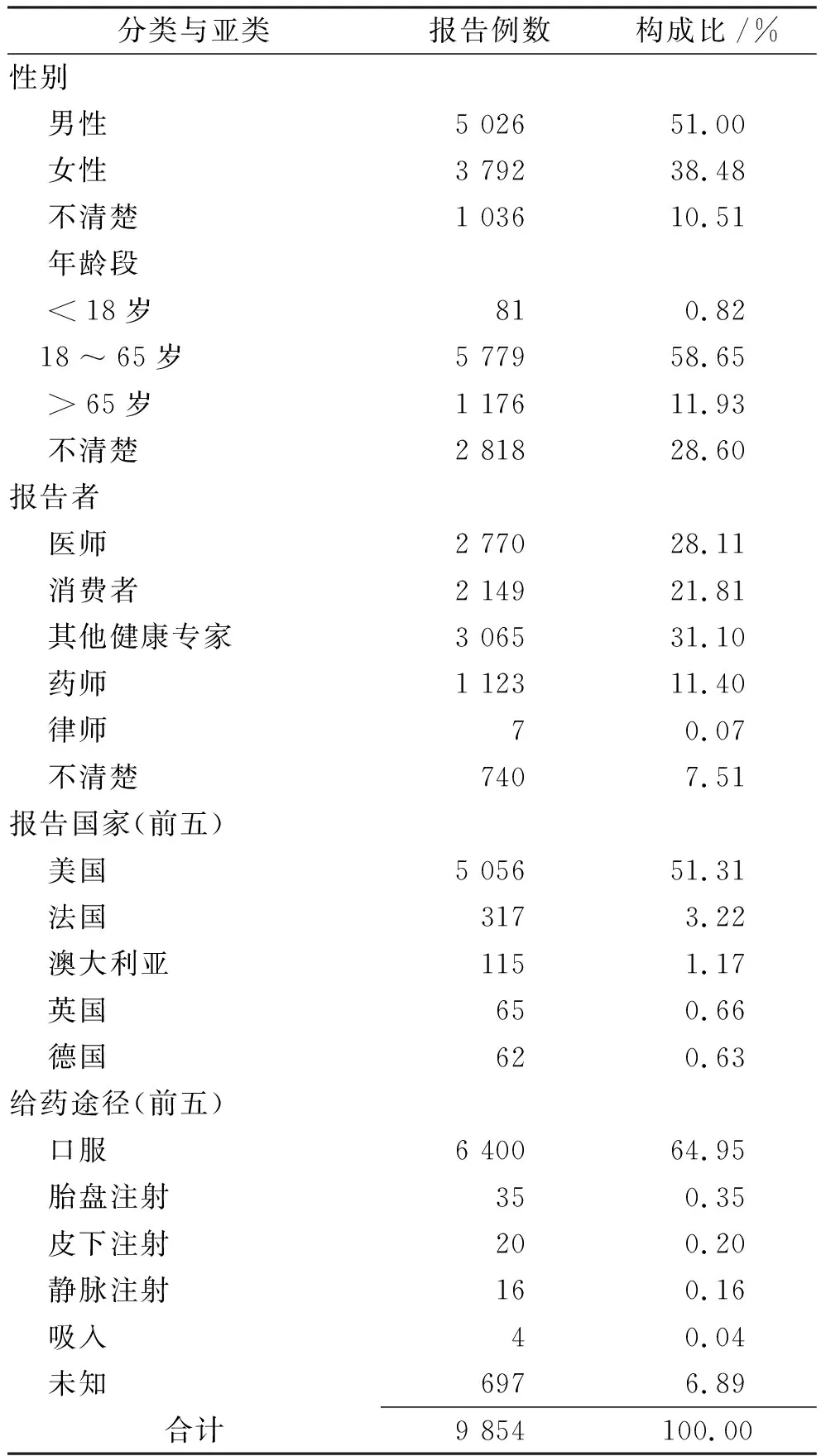
2.1药品不良事件报告情况 数据处理结果显示2004—2019年报告ADE共11 450 529例,其中以利巴韦林为首要怀疑药品的报告有9854例。9854例报告中男性占51.00%,男女比例为1.32,平均年龄为54.01岁。报告者多为从事健康相关的工作人员,其中医师报告2770例,占28.11%。报告国家前五位分别是美国、法国、澳大利亚、英国和德国,中国仅报告44例,占0.45%。用药途径多为口服给药,其次为经胎盘、皮下、静脉以及吸入给药,见表2。历年报告数显示,该药的报告数在2012开始增加,在2013年最多达1887例后呈逐年下降趋势。见图1。
2.2各系统器官分类不良事件报告及信号检测情况 对以利巴韦林为首要怀疑药品的不良事件报告进行信号分析并根据系统器官分类(SOC)进行分类排序得到各SOC项下报告数排名前三的事件及其信号分析结果,见表3。结果显示SOC报告例数排名前五的分类依次为全身性疾病及给药部位各种反应、胃肠道系统疾病、各类检查、血液及淋巴系统疾病以及各类神经系统疾病。其中全身性疾病及给药部位各种反应、各类检查、血液及淋巴系统疾病以及肝胆系统疾病项下报告数前3位事件均检出信号。
表2 2004—2019年FAERS数据库中利巴韦林相关不良事件报告基本信息
Tab.2Primaryinformationofribavirinrelatedeventsreportedfrom2004to2019inFAERS
分类与亚类报告例数构成比/%性别 男性5 02651.00 女性3 79238.48 不清楚1 03610.51 年龄段 <18岁810.82 18~65岁5 77958.65 >65岁1 17611.93 不清楚2 81828.60报告者 医师2 77028.11 消费者2 14921.81 其他健康专家3 06531.10 药师1 12311.40 律师70.07 不清楚7407.51报告国家(前五) 美国5 05651.31 法国3173.22 澳大利亚1151.17 英国650.66 德国620.63给药途径(前五) 口服6 40064.95 胎盘注射350.35 皮下注射200.20 静脉注射160.16 吸入40.04 未知6976.89合计9 854100.00
2.3前20位不良事件报告及信号情况 对以利巴韦林为首要怀疑药品的报告事件进行统计并采用PRR和ROR法进行分析。报告数排名前20的不良事件多为血液及淋巴系统疾病、各类神经系统疾病、胃肠系统疾病、全身性疾病以及皮肤及皮下组织类疾病。见表4。
2.4不良事件结局 分析利巴韦林为首要怀疑药品的不良事件报告结局结果显示,该药导致入院或延长住院时间的报告例数为2 889例(29.32%),死亡513例(5.21%),威胁生命336例(3.41%),需要干预以预防永久性损伤100例(1.01%),先天畸形58例(0.59%),另外发生其他重要医学事件和结局不清楚的报告共5 746例(58.31%)。
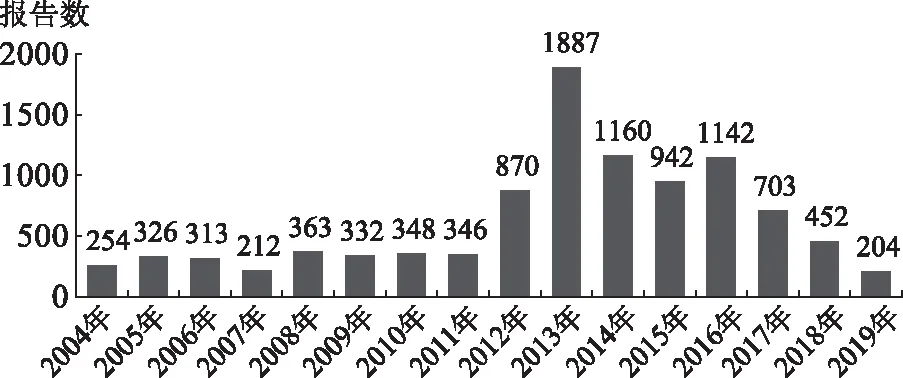
图 1 2004—2019年FAERS数据库中利巴韦林相关不良事件逐年报告数量
Fig.1Yearlyreportsofribavirinrelatedeventsreportedfrom2004to2019inFAERS
3 讨论
利巴韦林因其抗病毒谱广、活性强、耐药率低、价格低廉和疗效确切等特点,是治疗病毒性传染病的一线药物,临床上常用于病毒性腮腺炎、肝炎、带状疱疹、流行性感冒的治疗中[11]。此次新型冠状病毒来袭,“老药新用”成为疾病治疗的一个热点,但利巴韦林的不良反应发生率也较高,一定程度上限制该药的使用。本次研究纳入的以利巴韦林为首要怀疑药品的9854例病例报告中,超过半数病例来自美国报告,病例平均年龄为54.01岁。病例年龄集中在18~64岁。由于无法得知利巴韦林使用总人群的情况,因此上述情况可能与使用者的性别、年龄或地域分布差异有关,尚不能得到不同类型患者不良反应发生率情况。
在本研究纳入的利巴韦林报告中,以全身性疾病及给药部位各种反应(如疲乏、发热、体质量降低)、胃肠系统疾病(如恶心、呕吐、腹泻)、血液及淋巴系统事件(贫血、血小板减少症、中性粒细胞及白细胞计数降低、血红蛋白降低)报告例数相对较多。上述不良事件不仅可能导致危重症患者病程误判还可能加重患者病情,因此在使用利巴韦林治疗NCP患者时应密切监护不良反应并定期进行血常规监测。报告病例转归情况分析结果显示,利巴韦林相关的不良事件多导致入院或住院时间延长,死亡或威胁生命的事件仅占5.21%。该结果提示利巴韦林导致的不良事件多为可逆事件,停药可缓解[12]。
本研究存在一定局限性:①FAERS数据库为自发呈报系统,存在低报漏报情况,可能导致信号被低估;②无法计算药品不良事件总体以及在不同人群中的发生率;③FAERS数据库的部分数据项存在缺失,导致部分数据无法分析;④药品不良事件与药品因果关系尚不明确,仍需要经过进一步研究。
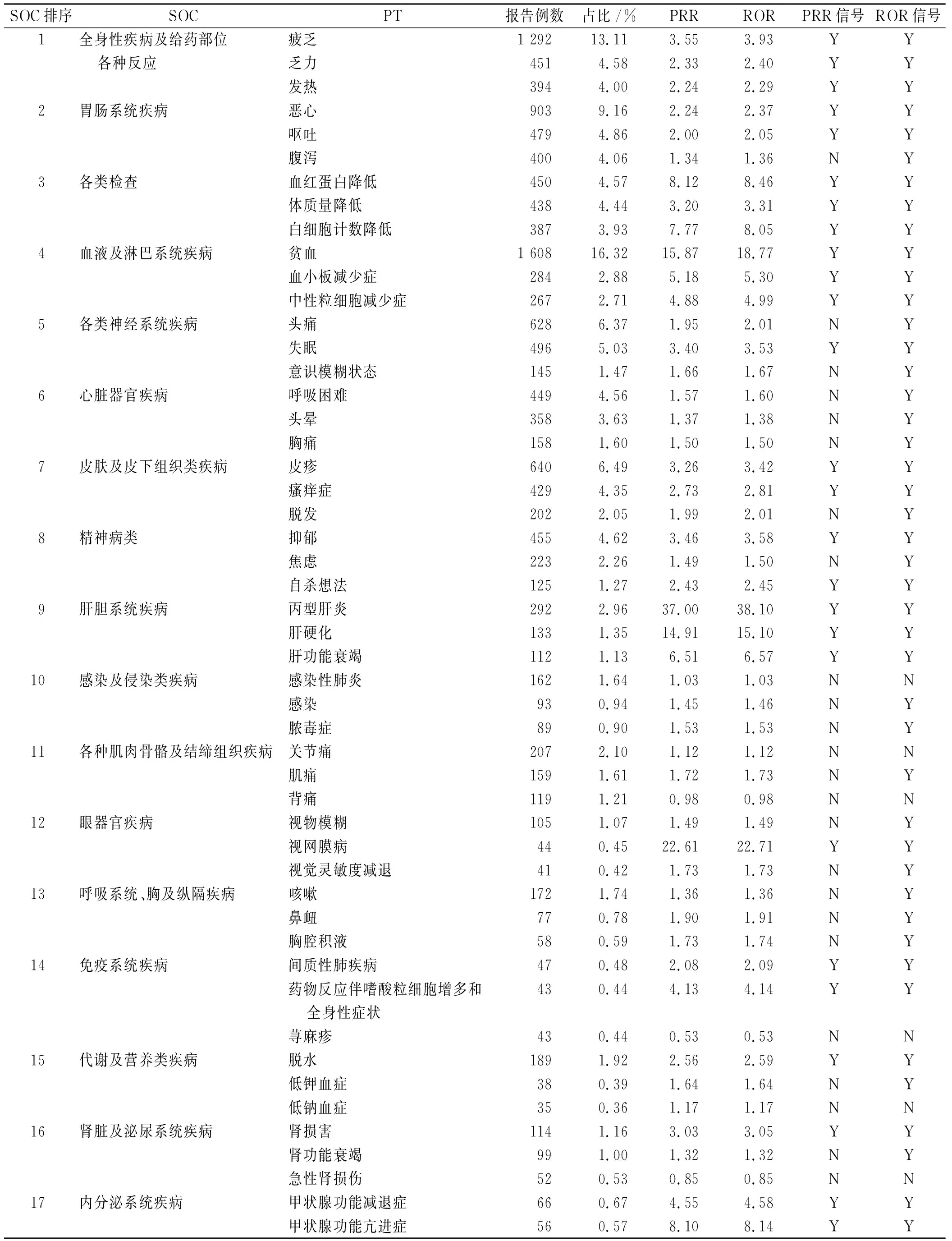
表3 SOC项下利巴韦林报告例数前3位事件及其信号分析

续表3 SOC项下利巴韦林报告例数前3位事件及其信号分析
“Y”代表检出信号;“N”代表未检出信号。
“Y” respresents the detected signal;“N” means the signal is not detecteal.

表4 FAERS中利巴韦林报告例数前 20 位信号事件
综上所述,本研究基于信号挖掘方法对NCP治疗药物利巴韦林不良事件进行全面展示。利巴韦林用于NCP治疗时应密切监护不良反应并定期进行血常规监测,以避免因不良反应导致的停药或疾病进程误判。
