胃癌全胃切除术后早期肠内营养支持的临床效果观察
2020-04-13顾文斌
顾文斌
无锡市锡山人民医院,江苏 无锡 214000
全胃切除术是根治胃癌患者的首选疗法,虽然可控制癌症病情,但同时也是对患者机体的生理性损伤[1],应激反应明显,术后易发营养不良而导致免疫力下降,对病情康复不利。如何确保营养支持是保证患者机体康复的关键。本研究对45例病患进行研究,分析全胃切除术后予以早期肠内营养支持的有效性,报道如下。
1 资料与方法
1.1 一般资料 选择2019年1月-2019年6月在我院接受全胃切除术的胃癌患者45例,均在术后予以早期肠内营养支持。入选对象中男性24例,女性21例,年龄54-77岁,平均年龄(63.29±4.30)岁。所有入选对象均排除合并严重肝肾功能不全、合并高血压等心血管慢性病者[2]。入选者均对本次研究内容充分知情且自愿参与,符合伦理学要求。
1.2 方法 所有病患均进行消化道重建,调整导管置于空肠-空肠吻合口20-25cm处;手术结束后经腹壁穿孔,将空肠营养管置于韧带远端15cm空肠处,经肠壁下穿行5cm后即可进入腹腔,导管到达预期位置后将导管缝合固定于肠壁部位,再将无菌敷料覆盖遮挡皮肤上的伤口,进行肠内营养支持。
营养液选用肠内营养混悬液TRF,初始输注剂量为每日500mL,滴速控制在25-30mL/h,根据患者耐受酌情调整输注量,一般可在3-4d内过渡至完全肠内营养(每日1500-2000mL);持续肠内营养7-9d,直至患者可经口进食半流质食物。
1.3 观察指标 观察统计患者的肛门排气时间、进流食时间、住院时间、并发症发生情况;同时在予以早期肠内营养前后测量患者体重、免疫球蛋白A(IgA)、免疫球蛋白M(IgM)水平。
1.4 统计学处理 采用统计学软件SPSS14.0进行处理,计量资料以平均数±标准差表示;计数资料以率表示;计量资料采用t检验,计数资料采用卡方检验,P<0.05为有统计学差异。
2 结果
2.1 临床恢复情况分析 45例患者的住院时间(13.95±5.03)d,其胃肠功能均恢复较快,均在手术后(37.69±5.22)h成功肛门排气,在早期肠内营养(68.44±6.02)h后进流食,有2例主诉腹胀,经调整滴速后逐渐缓解。本组并未发现感染性并发症。
2.2 肠内营养前后的体重、免疫功能指标对比 如表1所示,45例患者在予以肠内营养前后体重有所下降,P<0.05;免疫功能指标变化不显著,P>0.05。
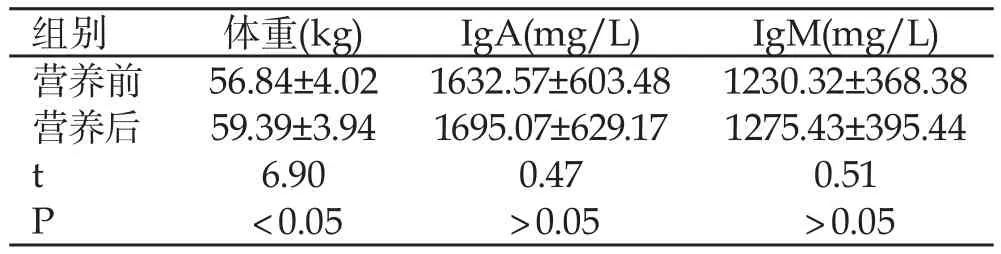
表1 肠内营养前后的体重、免疫功能指标对比(n=45)
3 讨论
在全胃切除术后予以营养支持毋庸置疑,是确保患者正常生理功能康复的关键。研究表明,相比肠外营养,肠内营养与人体正常的生理特征更相符。通过肠内营养可避免肠内屏障功能衰竭、免疫功能发生变化,还能促进肠道蠕动,同时肠内营养液还可同时满足患者对营养底物的需求,以及机体胃肠道黏膜的营养需求[3-4],避免机体内环境中细菌移位,促进康复。本次研究显示,入选病患的住院时间(13.95±5.03)d,其胃肠功能均恢复较快;肠内营养后体重与营养前相比有轻微上升,P<0.05;免疫功能指标变化不显著,P>0.05。但也有学者认为早期肠内营养对患者的免疫功能无确切影响,推断不一致的研究结果与病理选取、免疫功能指标检测准确性等相关,后续研究中需进一步完善改进。
综上所述,对接受全胃切除术的胃癌患者在手术后予以早期肠内营养,有利于病情康复和免疫力恢复,有临床意义。
