不可逆电穿孔技术联合导管电极用于组织消融的研究进展
2020-04-10周一坤韩轩任冯刚李青山陈雪初大可吴荣谦吕毅
周一坤,韩轩,任冯刚,李青山,陈雪,初大可,吴荣谦,吕毅
1 西安交通大学第一附属医院精准外科与再生医学国家地方联合工程研究中心,西安市,710061
2 西安交通大学第一附属医院陕西省再生医学与外科工程研究中心,西安市,710061
3 西安交通大学 宗濂书院,西安市,710061
4 西安交通大学第一附属医院 肝胆外科,西安市,710061
5 西安交通大学第一附属医院 消化内科,西安市,710061
0 引言
不可逆电穿孔(Irreversible Electroporation,IRE)是近年来新兴的一种组织物理消融技术[1]。IRE基于微秒方波脉冲电场生物学效应原理,通过对生物组织施加一定强度的脉冲电场导致细胞死亡,进而实现组织物理消融的目的。尽管IRE导致细胞死亡的内在机制仍不十分明确,但由于脉冲电场作用导致细胞膜跨膜电位破坏导致细胞凋亡或坏死的过程已被广泛接受[2]。由于脉冲电场作用于细胞膜磷脂双分子层结构的特点,IRE在组织消融过程中可以不依赖热量,不会引起组织不可逆性热损伤,可以保留细胞内大分子、组织支架和纤维结构等。因此,IRE是一种与射频消融(Radiofrequency Ablation,RFA)、微波消融、激光消融等传统物理消融技术完全不同的组织消融形式[3]。
方波脉冲电场刺激引起的“电穿孔”现象在1950年代就已被发现,当时被描述为一种“膜击穿”效应,可以引起细胞膜传导率和通透性的增加[4]。在此之后,强脉冲电场对于微生物的非热杀伤作用被发现,并且广泛应用于食品工业领域。20世纪90年代以来,电穿孔技术被应用于细胞生物学领域,通过电穿孔效应使细胞膜表面出现微孔,进而可以使外源性物质(如DNA)进入细胞内,在外加电场撤离后细胞膜结构可以恢复,这也被称作“可逆性电穿孔(Reversible Electroporation,RE)”[5]。在此基础上,电穿孔技术联合化疗药物也被用作肿瘤治疗领域[6]。
2000年以来,我国重庆大学孙才新院士[7]和美国UC Berkeley大学Rubinsky教授[1]相继提出利用基于微秒脉冲电场生物学效应实现肿瘤组织物理消融的设想,并通过体外、体内实验证实了其安全性和有效性。研究发现,当脉冲电场场强超过500~750 V/cm时,脉冲作用一段时间后细胞膜电穿孔无法恢复,最终引起细胞死亡[1-2,7]。2009年,AngioDynamics公司研制的首台微秒脉冲电场肿瘤治疗仪NanoKnife问世,2012年获FDA批准进行临床应用,同年12月获得欧盟临床许可,2015年获得我国CFDA批准,我国自行研发同类仪器也进入临床研究阶段。当前,IRE已在局部进展的肝癌、胰腺癌和前列腺癌等实体肿瘤的治疗中表现出良好效果。由于IRE非热能组织消融的特点,在肿瘤消融中具有一些特殊优势:脉冲作用时间短,整体治疗过程迅速,对机体损伤小,利于术后康复;不受热沉效应影响,可以用于大血管周围肿瘤组织;不损伤组织支架结构,不导致血管、神经等的不可逆性损伤;消融后组织可以通过再生修复等。因此,IRE可以有效应用于当前热消融技术无法应用的临床场景中[8]。
长期以来,RFA等热消融技术主要应用于实质器官中,对于胃肠道、胆管、胰管以及泌尿道等结构无法适用[4]。最主要的原因是由于热效应会导致管壁的破坏性损伤,进而引起管壁穿孔,影响治疗的安全性;而降低能量强度则可能会影响治疗的有效性。虽然已有一些基于RFA原理的技术应用于食管、胆道等的组织消融,但由于其热效应的原理,消融能力有限,且易引起感染、穿孔等并发症。IRE基于其非热能组织消融的原理,可以有效保护组织支架结构不受损伤,而这个特点对于胃肠道等管腔结构组织来说具有重要临床意义。然而,目前IRE主要采用一组阵列式针状电极的形式,通过排布于肿瘤组织周围构成消融区域实现作用,而针状电极无法应用于管腔结构,因而尚无IRE应用于消化道的临床研究报道。
近年来,国内外已有多个团队致力于IRE联合导管电极用于消化道和心脏组织消融的研究,相继开展了大量动物实验,初步证实了其可行性、安全性与有效性,为IRE联合导管电极的临床应用奠定了基础。本研究综述了IRE联合导管电极用于组织消融的研究进展,并对其关键技术与未来发展方向进行了展望。
1 电脉冲产生
向生物组织施加符合能量强度要求的电穿孔脉冲是实现电穿孔的关键。电穿孔脉冲由脉冲电源发生器生成,也称电脉冲源。电脉冲源的结构通常包括高压脉冲电源、脉冲放大器、控制单元、输出模块和交互界面等几个部分。在充电阶段,经过长时间积累大量电能储存在储能元件(如电容)中。在放电阶段,储存的电能快速释放至负载,从而形成电脉冲。有多种元件可以用于放电,包括直接电容放电、脉冲形成线、变压器、磁能储存电感器、谐振电路等。根据输出脉冲特征的不同,脉冲源可以分为微秒脉冲源、纳秒脉冲源、双极性脉冲源和复合脉冲源等。电穿孔的结局与电脉冲参数和细胞或组织的生物物理参数密切相关,包括脉冲波形、脉冲幅值、持续时间和极性。在电穿孔研究中通常有两种波形:方波脉冲和指数衰减脉冲。方波脉冲也称陡脉冲,是IRE最常用的脉冲波形,理想的方波脉冲形状呈矩形,包括高电平和零电平。单脉冲的生物效应是有限的,IRE通常需要将一定数量的电脉冲按序列输出来实现消融目的。
2 电极结构与配置
电穿孔脉冲经由电极输送至靶组织,因此电极配置与IRE的消融结局密切相关。电极结构主要包括四种:针式、板式、钳夹式和导管式。电极性质包括阳极(高电位)和阴极(接地)两种,电极与生物负载接触后构成电场回路。针状电极的治疗途径主要包括开腹、经腹腔镜和经皮穿刺,这三种治疗途径已经在临床上得到应用,主要用于实体肿瘤消融。导管电极结合内镜技术和介入技术进行消化道、泌尿道、呼吸道和心血管组织消融是近年来的热点研究方向。导管电极可与内镜或介入技术结合用于管腔组织消融,目前已有多种IRE导管电极用于腔内或心肌组织消融。导管电极通常为双极或阵列式电极结构,可以从管腔内对局部组织上皮进行消融,不引起管壁穿孔,不影响管道通畅性,对于管腔肿瘤消融具有重要意义。导管电极的结构和配置包含以下关键点:①电极结构需符合内镜或介入器械的设计理念,满足内镜或介入操作环境对导管直径和柔韧性的要求。②电极需适合腔内肿瘤的解剖特点,消融区域可以对腔内肿瘤实现适形覆盖。③电极配置与其形成的消融电场范围严密相关,因此导管电极必须符合IRE电极的设计要求,需要包含一个高压端、一个接地端。同时,二者的相对位置、电极的间距、尺寸、几何形状同样对电场形成起重要作用。电极设计过程中,可结合计算机辅助设计、有限元分析和数值模拟等技术,分析电极形成的电场特点,对电极结构进行评估和调整。④电极材料应与应用环境和承载电压匹配,针对消化道的导管电极需要抗酸腐蚀,电极整体需具备足够的耐压强度。除以上几点以外,导管电极在释放电穿孔脉冲的基础上,还可加装多种生物传感器,实时反馈消融过程中的生物物理信息。
3 联合内镜技术用于消化道组织消融
我国每年新发消化道恶性肿瘤146万例,死亡人数108万例,疾病负担严重[9]。从起源上来说,黏膜层来源的消化道肿瘤较为常见,且恶性度高;黏膜下起源肿瘤以胃肠道间质来源肿瘤为主,预后较好。目前,消化道肿瘤的治疗手段主要包括手术切除、化学治疗、靶向治疗和内镜下治疗等。外科手术切除是早期胃肠道肿瘤根治性治疗的主要手段,中晚期消化道肿瘤丧失手术切除机会,多采用化疗或靶向治疗等方法。内镜下治疗主要包括内镜下黏膜切除术和内镜黏膜下剥离术,利用高频电刀原位移除肿瘤组织。对于早期胃癌,有研究发现内镜下治疗可以获得与手术切除相当的远期效果。但是内镜下治疗难度大,对于术者技术要求高,学习曲线较长,治疗中极易出现穿孔或出血等并发症,限制了应用。内镜操作管道为多种治疗器械微创下置入消化道提供了便捷的通道,例如将RFA设备经内镜应用于消化道组织消融,其典型代表有Medtronic研发的Barrx系统和Boston Scientific研发的Habib Endo HPB系统。这两种系统均包含一个可经内镜置入的导管,用于消融食管、胃的异常组织及胆管癌,但这种治疗方式消融深度控制差,过度消融容易导致消化道穿孔、管壁瘢痕形成[10-11]。
近年来,国内外多个研究机构通过联合IRE与内镜技术,设计了多种适用于消化道组织消融的导管电极,并且在胃肠、胆道和食管等部位开展了动物实验研究。西安交通大学吕毅教授设计了磁锚定式导管电极用于胃组织消融。磁锚定电极分为内磁体和外磁体两部分,每部分由锚定磁体和消融电极两部分组成。锚定磁体由钕铁硼材料制成,电极为医用不锈钢,均为圆盘型。内磁体固定于胃管前端,在透视指导下置入胃腔内,外磁体在开腹条件下借助磁力与内磁体锚定吸引。磁锚定电极在消融过程中可以克服肌肉受电刺激抖动所引起的电极脱位,稳固锚定电极在胃壁内外两侧,可以实现胃组织全层消融,见图1(a)[12]。

图1 用于消化道组织消融的导管电极Fig.1 Catheter-based electrode for digestive tract
UESHIMA等[13]通过改造胆道球囊扩张导管,在该导管上加装了长度为20 mm的单极电极,皮肤表面固定阴极板作为接地电极,通过ERCP技术将电极逆行插入胆总管进行胆道组织消融,见图1(b)。除此之外,SRIMATHVEERAVALLI团队[14]还设计了适用于直肠组织消融的电极,该电极利用注射器改造而成,包含单极和双极两种模式。电极经肛门置入直肠,可以实现浅层和深层直肠组织消融,见图1(c)。NEVEN等[15]设计了吸盘式电极用于食管组织消融,电极由一包裹在吸盘中的线性电极组成,在开胸手术下电极的吸盘经胸骨上切口吸附于食管外膜,对食管外壁进行了消融实验,见图1(d)。除了消化道外,KODAMA等[16]在肺脏的支气管中使用网篮状的导管电极进行了研究,电极在X线或CT引导下经气管插管置入主支气管并进行组织消融。
消化道等管腔结构器官各区域均具有相似的结构特征,包括黏膜层、黏膜下层、固有肌层和浆膜层等结构,其厚度因位置和生理状态的不同有所差异。从组织学上来说,经过相应的IRE作用后,消化道组织呈现出了相似的组织学变化:大体可见黏膜表面出现了与周围正常组织界限清晰的消融区域;组织学染色可见消化道管壁出现浅表或透壁组织消融,消融的深度与脉冲强度相关。从安全性上来说,内镜引导下的IRE手术过程顺利,围手术期动物生理状态良好,消融区术后并未出现管壁扩张、穿孔、出血等严重并发症。吕毅教授利用磁外科技术设计锚定消融电极,有效解决了IRE过程中电极移位的问题。整体上说,IRE用于消化道等管腔组织消融是安全可行的。表1汇总了IRE应用于管腔结构组织消融的研究方案。
4 联合介入技术用于心血管组织消融
除恶性肿瘤之外,物理消融技术也常用于异常组织的原位消融中,最常见的是RFA用于恶性心律失常的治疗。心律失常是一种较为常见的心脏疾病,冠心病、心率衰竭与高血压性心脏病是引发该疾病出现的主要原因。药物治疗、导管RFA及植入心脏转复除颤器是常用的治疗方法[19]。导管RFA联合介入技术可以在微创条件下对异常心脏组织进行治疗,具有创伤小、操作精准、消融迅速等优点。但是由于RFA热消融的原理,在消融过程中可能因为损伤冠状动脉邻近组织而产生严重并发症,如血栓形成、血管狭窄、心肌梗死等。从消融方法上看,单极射频消融可能造成透壁损伤,在跳动的心外膜消融时,血液循环带来的“热沉效应”使其难以形成透壁消融。而双极射频消融只能在两个电极之间作用,难以进行钳夹的部位就很难进行消融。因此,射频消融在恶性心律失常的治疗过程中仍存在一定局限[20]。常用导管电极如图2所示。

表1 不可逆电穿孔应用于管腔结构组织消融的研究方案汇总Tab.1 Summary of the application of IRE in the ablation of lumen structures and tissues
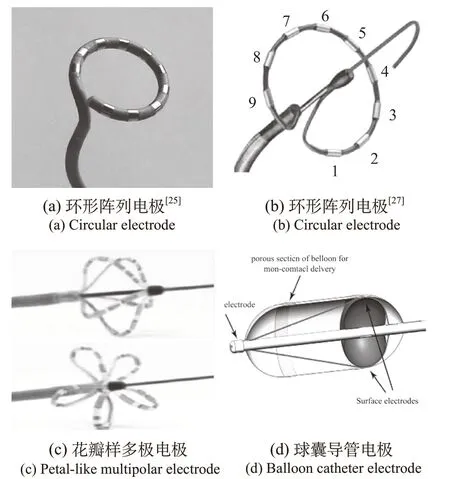
图2 用于心血管组织的导管电极Fig.2 Catheter-based electrode for cardiovascular tissue
近年来已有团队开展了IRE用于心脏组织消融的研究。荷兰乌德勒支大学医学中心WITTKAMPF等[21]设计了直径20 mm的环形导管电极对猪进行了肺静脉开口部的消融,发现低能量的不可逆电穿孔可以在此处安全消融。NEVEN等应用导管电极经心包穿刺进行了心包内心外膜消融的实验,发现IRE可造成深度可控、连续透壁的心肌损伤且不对冠状动脉造成明显损害。因此,IRE可以解决RFA最突出的问题:冠状动脉及其附近组织的安全消融,证实了导管电极联合IRE用于心脏消融的安全性和有效性,使得应用IRE进行室性心动过速治疗成为可能[22-23]。此外,该团队也证实了线形电极向心外膜输送的脉冲能量的水平与平均心肌损伤深度、宽度之间存在显著关系[24]。
上述研究大都是在开胸或离体动物心脏上进行的,手术入路创伤较大。近年来一些团队尝试通过联合介入技术将电极送至心内目标区域进行消融治疗。DRIEL和WITT等[25-26]使用导管电极在肺静脉内消融,证实IRE术后不影响肺静脉直径,见图2(a)和图2(d)。STEWART等[27]则证实IRE可以产生局限的心脏纤维化损伤,见图2(b)。REDDY等[28]首次开展了IRE进行心肌组织消融的临床研究,证实IRE可以优先破坏心肌组织而不影响邻近结构。此外,通过优化的双相波形,IRE术后可以实现持久的肺静脉隔离,见图2(c)。综上,IRE用于心脏组织消融的安全性整体尚可,但是在部分实验中出现过包括发热、发绀以及心包填塞等并发症,也有动物在治疗过程中出现死亡。因此,对于该技术用于恶性心律失常的研究还需要进一步开展。表2汇总了IRE应用于心血管组织消融的研究方案。

表2 不可逆电穿孔应用于心血管组织消融的研究方案汇总Tab.2 Summary of the application of IRE in the ablation of cardiovascular tissues
5 展望与结论
IRE是近年来最受关注的物理消融技术,但是基础研究与临床研究主要局限于实质器官肿瘤治疗。基于其非热能组织消融的特点,在消融过程中不会破坏组织支架结构,不受血流“热沉效应”的影响,可以突破现有热消融技术的诸多禁区,具有重要的临床意义。内镜技术与介入技术在消化道、泌尿道、呼吸道和心血管疾病中应用广泛,可以为多种诊疗技术提供微创、便捷的操作通道。IRE与RFA在治疗原理上存在明显差异,不能简单地将RFA消融导管用于IRE。因此,进一步研究IRE的作用原理,优化脉冲形式,设计适用于不同临床场景的IRE导管电极,可以充分发挥IRE的优势,为临床治疗提供新的解决方案。
