超声引导下囊内消融与刺穿囊壁消融治疗甲状腺良性囊实性结节的对比研究
2020-11-16韦文姜田作富李立恒唐迎红徐谷根肖承江
韦文姜,田作富,李立恒,唐迎红,徐谷根,肖承江*
1.广东省第二人民医院介入科,广东广州 510317;2.广东省第二人民医院内分泌科,广东广州 510317; *通讯作者 肖承江xxx196610@163.com
甲状腺囊实性结节是结节内同时存在实性成分和囊性成分,占外科切除标本的18%~35%[1],常归为良性病变。随着对甲状腺囊实性结节认识的不断提高,发现其存在一定的恶性率[2]。鉴于较大结节对外观和颈部感觉的影响以及可能发生结节恶变,临床常选择对囊实性结节进行处理。乙醇、射频、微波等微创消融治疗甲状腺结节较手术治疗有一定的优点[3-6]。热消融治疗甲状腺囊实性优于乙醇治疗[7-9];而甲状腺囊实性结节热消融囊壁方法的差异对比研究较少。本研究拟比较甲状腺囊实性结节抽液后,囊内消融囊壁与穿刺囊壁消融囊壁的疗效,探索治疗甲状腺囊实性结节的最佳囊壁消融方法。
1 资料与方法
1.1 研究对象 回顾性分析2014年8月—2018年6月于广东省第二人民医院细针穿刺活检证实为甲状腺良性囊实性结节及行甲状腺囊实性结节抽液+消融治疗的患者。纳入标准:①甲状腺囊实性结节最大径≥1.5 cm,囊性部分≥50%;②有颈部疼痛、颈部异物感等不适,或颈部肿大影响美观者;③经超声引导下穿刺活检并经病理证实为良性囊实性结节。排除标准:①复查资料缺失者;②甲状腺囊实性结节最大径<1.5 cm,囊性部分<50%;③病理结果为恶性或不确定者。最终纳入93例患者共98枚囊实性结节,根据囊实性结节囊壁的消融方式分为囊内消融组(抽液、囊内消融、紧贴囊壁消融)与刺穿囊壁消融组(抽液、囊内消融、刺穿囊内消融)。囊内消融组37例40枚结节,其中男2例,女35例;年龄21~67岁,平均(42.16±7.62)岁;结节体积1.33~28.37 ml,平均(15.52±3.91)ml。刺穿囊壁消融组56例58枚结节,其中男4例,女52例;年龄17~65岁,平均(41.34±6.89)岁,结节体积1.62~30.92 ml,平均(16.81±3.45)ml。两组患者性别、年龄及结节体积比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 检查方法 患者取仰卧位,开放静脉通道,充分暴露颈部,常规消毒铺洞巾。以2%利多卡因在超声监视下局部浸润麻醉穿刺点、穿刺路径上的组织及甲状腺包膜使甲状腺浅面、颈动脉侧形成液体隔离区(图1A)。以1.2 mm 注射器针头(18G)于拟穿刺点刺破皮肤后,再将1.6 mm、100 mm 微波消融针沿穿刺点送入。在超声引导下经甲状腺峡部穿刺插入结节囊性部分。随后用20 ml 注射器经消融针穿刺点旁穿刺进入甲状腺结节囊性部分,并负压抽尽囊液后消融(图1B)。囊内消融组患者抽尽囊液后通过实时超声查看消融针位于囊内位置,按背侧向腹侧、足侧向头侧的顺序进行囊内消融(包括囊内实性部分);消融囊实性结节边缘时,消融针紧贴囊壁消融(图2A)直至结节边缘被高回声覆盖后停止消融(图2B),消融功率30 W。刺穿囊壁消融组患者抽尽囊液后通过实时超声查看消融针位于囊内位置,按背侧向腹侧、足侧向头侧的顺序进行囊内消融(包括囊内实性部分);消融囊实性结节边缘时,将消融针刺穿囊壁直接消融囊实性结节边缘(图3A)直至结节边缘被高回声覆盖后停止消融(图3B),消融功率30 W。在消融过程中,消融靠近危险三角时均用生理盐水建立液体隔离带并于消融时让患者持续发“一”的声音。若有声音改变则停止该点消融,并用地塞米松10 mg 静脉注射与甘露醇125 ml 快速静脉滴注。
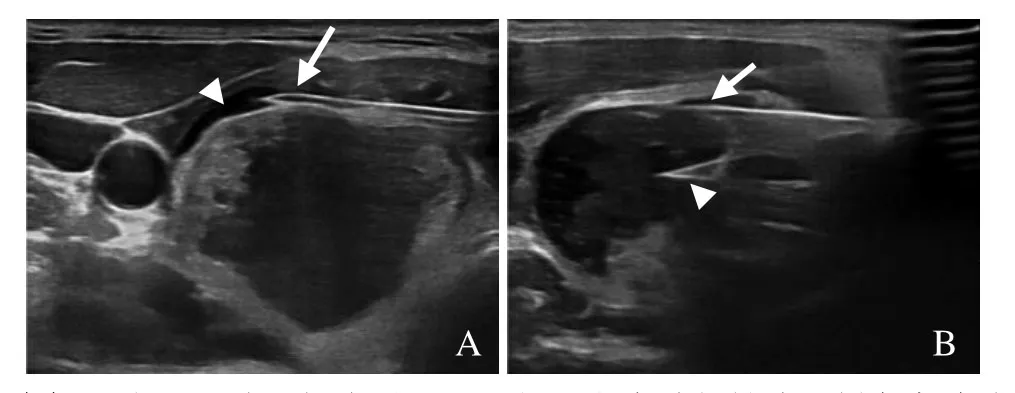
图1 女,41岁,超声引导下局部浸润麻醉与抽液(刺穿囊壁消融组)。局部浸润麻醉甲状腺包膜(箭示麻醉针头)并使甲状腺浅面、颈动脉侧形成液体隔离区(箭头,A);消融针(箭,B)位于结节囊性部分后再用1.2 mm 针头(箭头,B)穿刺抽液

图2 女,39岁,囊内消融组。消融针先消融囊内,随后紧贴囊壁对囊壁进行消融,高回声热量不易向囊壁弥散(箭,A);消融针紧贴囊壁多点消融后,高回声消融区覆盖囊壁,囊壁轮廓隐约显示(箭,B)

图3 女,41岁,刺穿囊壁消融组。消融针先消融囊内,随后多点刺穿囊壁对囊壁进行移动消融,高回声热量迅速向囊壁弥散(箭,A);消融针刺穿囊壁多点消融后,高回声消融区覆盖囊壁及囊壁显示不清(箭,B)
1.3 参数测量 根据公式(1)计算术前和术后即刻、1、6、12个月的甲状腺结节体积[6]。根据公式(2)计算甲状腺结节体积减小率。记录术中囊内出血、声嘶,术后疼痛、囊内出血情况;术后1个月与12个月分别抽取静脉血检查甲状腺功能。
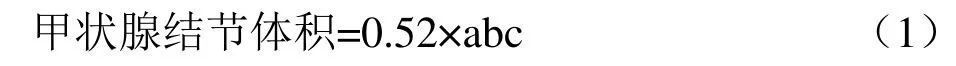
其中,a为结节的最大直径,b、c为相互垂直且均与最大直径垂直的结节径线。

1.4 统计学方法 采用SPSS 18.0 软件,计量资料以±s表示。两组结节体积缩小率比较采用独立样本t检验;计数资料组间比较采用χ2检验或Fisher 确切概率法。P<0.05表示差异有统计学意义。
2 结果
2.1 甲状腺结节消融后缩小情况 两组术后即刻与1个月结节缩小率差异均无统计学意义(P>0.05);术后6个月与12个月刺穿囊壁消融组结节体积缩小率大于囊内消融组,差异有统计学意义(P<0.05,表1)。
2.2 并发症 刺穿囊壁消融组与囊内消融组患者术中声音嘶哑、术中囊内出血、术后疼痛、术后囊内出血的发生率比较,差异均无统计学意义(P>0.05),见表2。所有消融患者术后1个月与12个月甲状腺功能均正常。
表1 囊内消融组与刺穿囊壁消融组患者结节体积缩小率比较(±s,%)
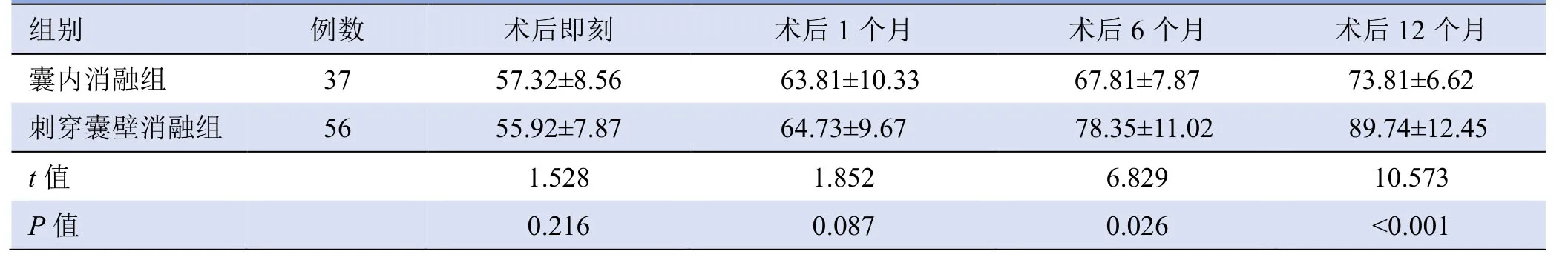
表1 囊内消融组与刺穿囊壁消融组患者结节体积缩小率比较(±s,%)
组别例数术后即刻术后1个月术后6个月术后12个月囊内消融组 37 57.32±8.56 63.81±10.33 67.81±7.87 73.81±6.62 89.74±12.45 t值 1.528 1.852 6.829 10.573刺穿囊壁消融组56 55.92±7.87 64.73±9.67 78.35±11.02 P值0.216 0.087 0.026<0.001

表2 囊内消融组与刺穿囊壁消融组患者并发症发生情况比较[例(%)]
3 讨论
本研究纳入囊内消融组与刺穿囊壁消融组患者术后12个月结节体积缩小率分别为(73.81±6.62)%与(89.74±12.45)%,故认为两种消融方法均取得成功。囊内消融组与刺穿囊壁消融组相比,术后即刻结节体积均显著缩小,两组术后即刻结节缩小率差异无统计学意义,推测由于囊液抽出后结节即刻缩小所致,与既往研究[5,10]报道的甲状腺囊实性结节抽液后再行乙醇消融治疗与射频消融治疗对比结节缩小差异无统计学意义相符。因此,囊液的抽取情况直接影响结节缩小率。
囊内消融组与刺穿囊壁消融组术后即刻与术后1个月结节缩小率差异无统计学意义,推测原因为甲状腺结节消融后凝固性坏死吸收缩小需要时间,以及消融后的甲状腺结节吸收快慢与结节成分及消融程度有关[11-12]。术后6个月与12个月刺穿囊壁消融组患者结节体积缩小率显著大于囊内消融组,其原因可能与甲状腺结节壁结构有关。王晨琛等[13]提出甲状腺结节壁结构的概念。超声二维灰阶指标包括边缘、边界及周边,统称为甲状腺结节的交界带,其中边界指结节与非结节(通常指围绕结节的甲状腺组织)之间的连接面。边缘指临近边界的结节区域,周边指紧挨边界的甲状腺组织。甲状腺囊实性结节的壁结构可能在边界存在假包膜,甲状腺囊实性结节的假包膜可能会延缓结节消融后的吸收。本研究中囊内消融组在消融囊实性结节壁结构时,消融针紧贴囊壁消融直至结节壁结构被高回声覆盖后需要的消融时间延长。消融时间延长易出现局部过度消融碳化而不易吸收缩小;消融针紧贴囊壁消融壁结构时也容易出现壁结构消融不均匀导致结节壁结构消融不全而出现残留,特别是有假包膜存在的情况下。甲状腺结节局部过度消融碳化与结节消融不全会导致结节消融后吸收不良[14-17]。既往研究认为甲状腺囊实性结节射频消融并不优于乙醇消融[5,10];另有研究认为乙醇消融具有不定向扩散与扩散不均的特点,在消融结节壁结构时易出现消融不完全导致复发单次治疗后复发率高达38.3%[9]。本研究认为刺穿囊壁消融甲状腺囊实性结节壁结构的热消融(射频/微波)方法具备完全消融优势;刺穿囊壁消融组在消融囊实性结节壁结构时,消融针刺穿囊壁直接消融囊实性结节壁结构直至其被高回声覆盖后所需要的消融时间短,不易局部过度消融碳化;且刺穿囊壁消融时可见高回声热量沿结节壁结构迅速向周边弥散,消融均匀使结节边缘完全消融。本研究囊内消融组1例患者消融术后1个月服用阿司匹林1 周后出现消融结节内出血复发需二次抽液+消融治疗,可反向说明囊内消融组中的消融针紧贴囊壁消融时,有导致结节边缘消融不全出现残留的可能。
总之,甲状腺囊实性结节微波消融安全、有效。在超声引导下采用先将消融针在超声引导下经甲状腺峡部穿刺插入结节囊性部分,随后用20 ml 注射器经消融针穿刺点旁穿刺进入甲状腺结节囊性部分并负压尽囊液后再消融,消融针在结节囊内消融后,再将消融针刺穿囊壁直接消融囊实性结节壁结构更能完全消融结节,降低局部过度消融碳化率,更有利于结节消融后的吸收,结节消融体积缩小更明显,值得临床进一步推广应用。本研究为回顾性研究,样本量相对较少,资料尚有偏差的可能。期待后期前瞻性研究探讨甲状腺囊实性结节壁结构完全消融的安全性与重要性。
