建立“模型认知”核心素养在《物质结构》中的应用
——以金刚石模型为例
2020-03-30薛晓燕
薛晓燕
(陕西省西安市西安外国语大学附属西安外国语学校 710061)
“模型认知”是高中化学核心素养重要构成要素,该能力建立在证据推理素养基础上,依据物质结构、组成、变化特点提出假设,使学生可通过推理、分析、思考,将研究对象具体化,以该体系为依据建造认知模型,在模型中展示各个构成要素之间的关系及本质特征,使化学现象可通过模型解释,得出化学规律及现象本质,使学生在掌握化学知识基础上,达到培养其“模型认知”思维等核心素养的目的,凸显高中化学教育创新实践价值.
笔者以金刚石模型为例,浅谈一下建立“模型认知”的应用.
一、建立金刚石晶体结构单元模型
1.金刚石晶体中正四面体结构单元
(1)如何理解金刚石结构?
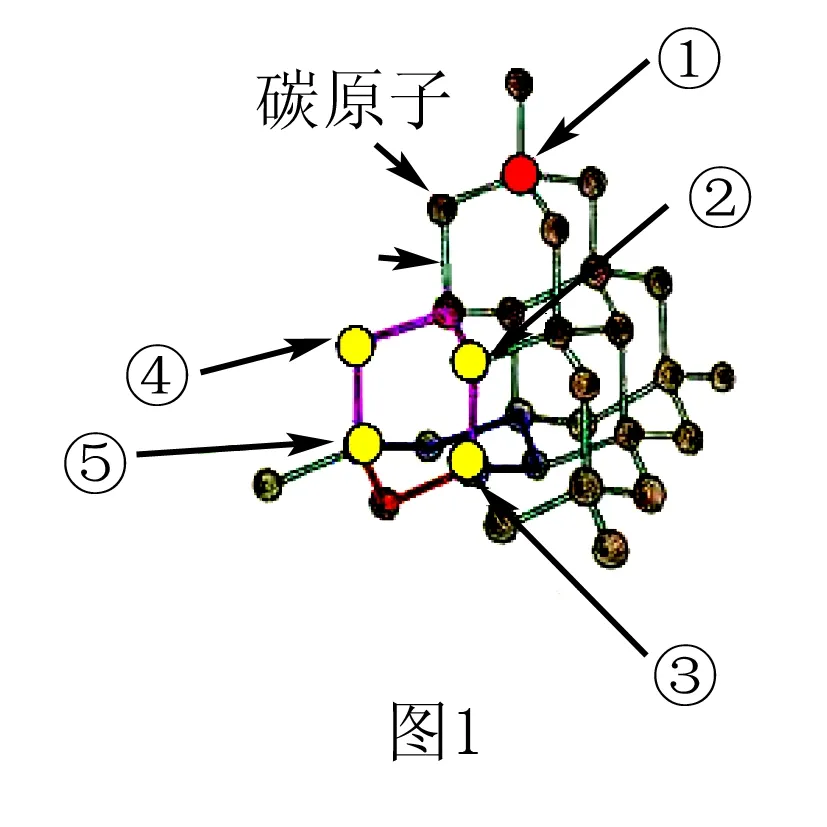
金刚石结构中的每个原子与相邻的4个原子形成正四面体.在金刚石晶体中,每个碳原子的4个价电子以sp3杂化方式形成4个完全等同的原子轨道,与最相邻的4个碳原子形成共价键.这4个共价键之间的角度都相等,为109°28.
(2)如何理解正四面体中心这个碳原子(①号碳原子)参与形成4个C—C单键,每个碳原子对一个C—C单键的“贡献”都是1/2,所以数目相当于4×1/2=2,故金刚石中1 mol C原子形成2 mol C-C单键.除金刚石以外,还有硅、锗等.
2.金刚石晶体中网状结构六元环
如何理解金刚石晶体中每个碳原子被12个六元环共有?
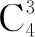
二、金刚石晶胞结构
1.认识金刚石晶胞结构

金刚石晶胞结构为立方晶系,碳原子分布于8个顶角和6个面心,同时在晶胞内部有4个碳原子位于4条体对角线的1/4、3/4处.每个碳原子周围都有4个碳原子,配位数为4,碳原子之间形成共价键,为正四面体构型.
原子坐标参数,表示晶胞内部各原子的相对位置,用坐标参数来分析一下金刚石的结构.其中原子坐标参数A为(0,0,0);B为(1/2,1/2,0);D为(1/4,1/4,1/4);C为(1/4,3/4,1/4)
2.金刚石晶胞中碳原子数是多少?
每个晶胞中含有碳原子数8个顶角×1/8+6个面心×1/2+内部4个碳原子=8,所以每个晶胞实际含有8个碳原子.
三、晶体边长a与碳原子半径r的关系及金刚石晶胞中碳原子空间利用的计算
1.晶体边长a与碳原子半径r的关系

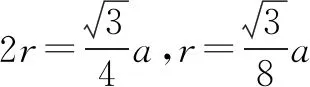
2.晶胞中碳原子空间利用率的计算
(1)空间利用率:指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比.

(2)空间利用率的计算步骤:
第一步:计算晶胞中的微粒数
第二步:计算晶胞的体积
第三步:找出球的半径r与晶胞边长a的关系
四、利用晶胞常数计算晶体密度
1.晶体密度的计算
(2)计算步骤:
第一步:确定晶胞中的粒子数
第二步:确定晶胞体积
第三步:代入公式进行计算
(3)注意长度单位的换算
常见长度单位换算关系:1cm=10-2m 1nm=10-9m=10-7cm 1pm=10-12m=10-10cm
2.应用模型
将所需论证的化学问题套用在该模型中,为学生系统认知化学问题提供路径,充实原有化学思维,提高学生化学学习能力,扩展“模型认知”思维辐射范围,提升学生模型认知能力,达到培养其核心素养教育目的.
例1 高考链接一(2015全国1卷节选)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:
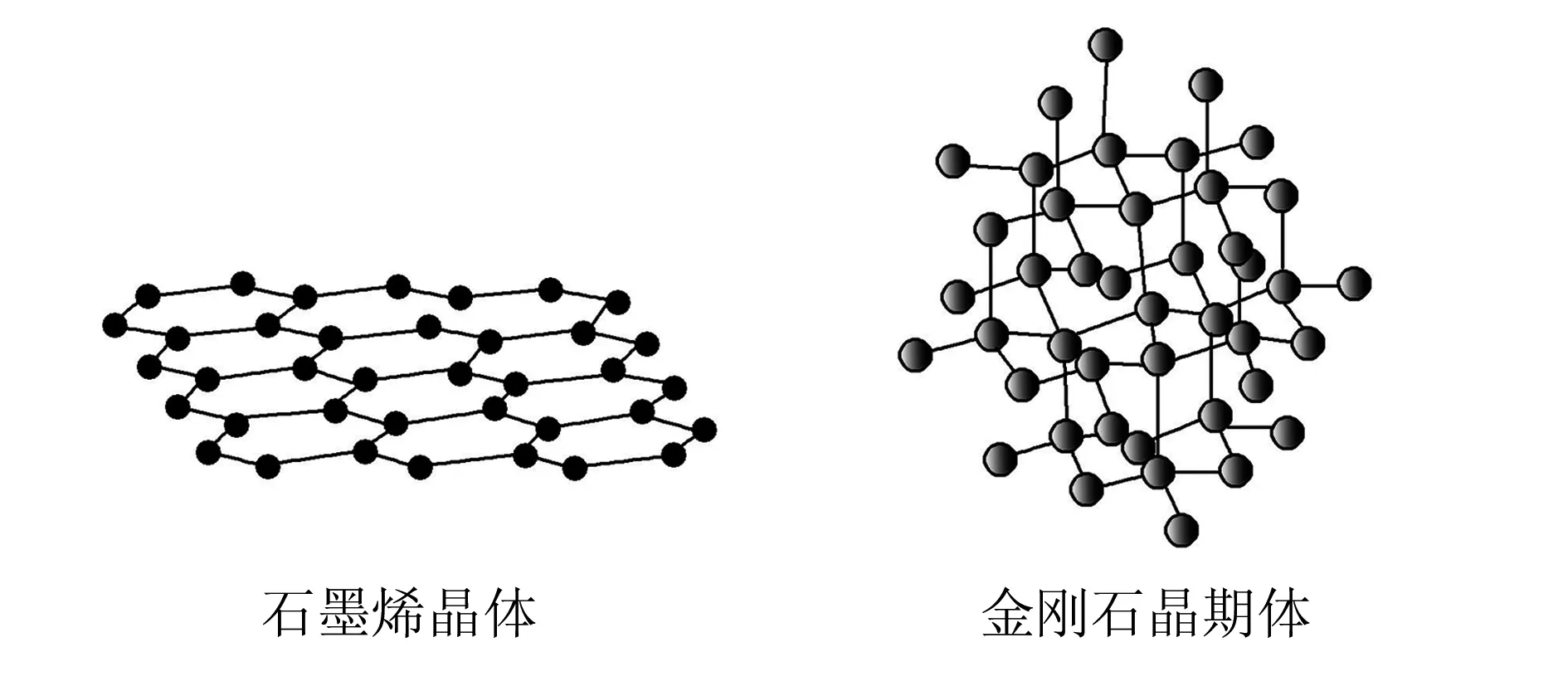
(1)在石墨烯晶体中,每个C原子连接____个六元环,每个六元环占有____个C原子.
(2)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接____个六元环,六元环中最多有____个C原子在同一平面.
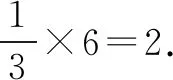
(2)由金刚石的结构可知,每个C可参与形成4条C—C键,其中任意两条边(共价键)可以构成2个六元环.根据组合知识可知四条边(共价键)任选其中两条有6组,6×2=12.因此每个C原子连接12个六元环.六元环中C原子采取sp3杂化,为空间六边形结构,最多有4个C原子位于同一平面.
例2 高考链接二(2019全国1卷第35题节选)
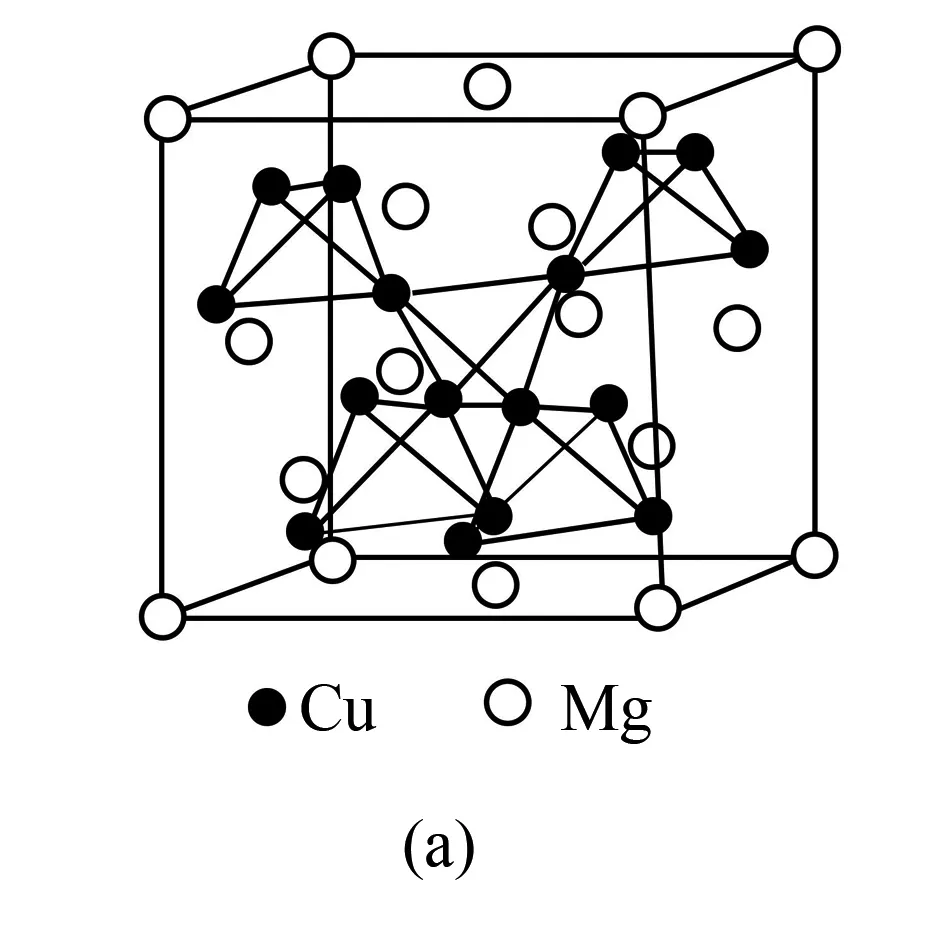
图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu.图(b)是沿立方格子对角面取得的截图.可见,Cu原子之间最短距离x=____pm,Mg原子之间最短距离y=____pm.设阿伏加德罗常数的值为NA,则MgCu2的密度是____g·cm-3(列出计算表达式).
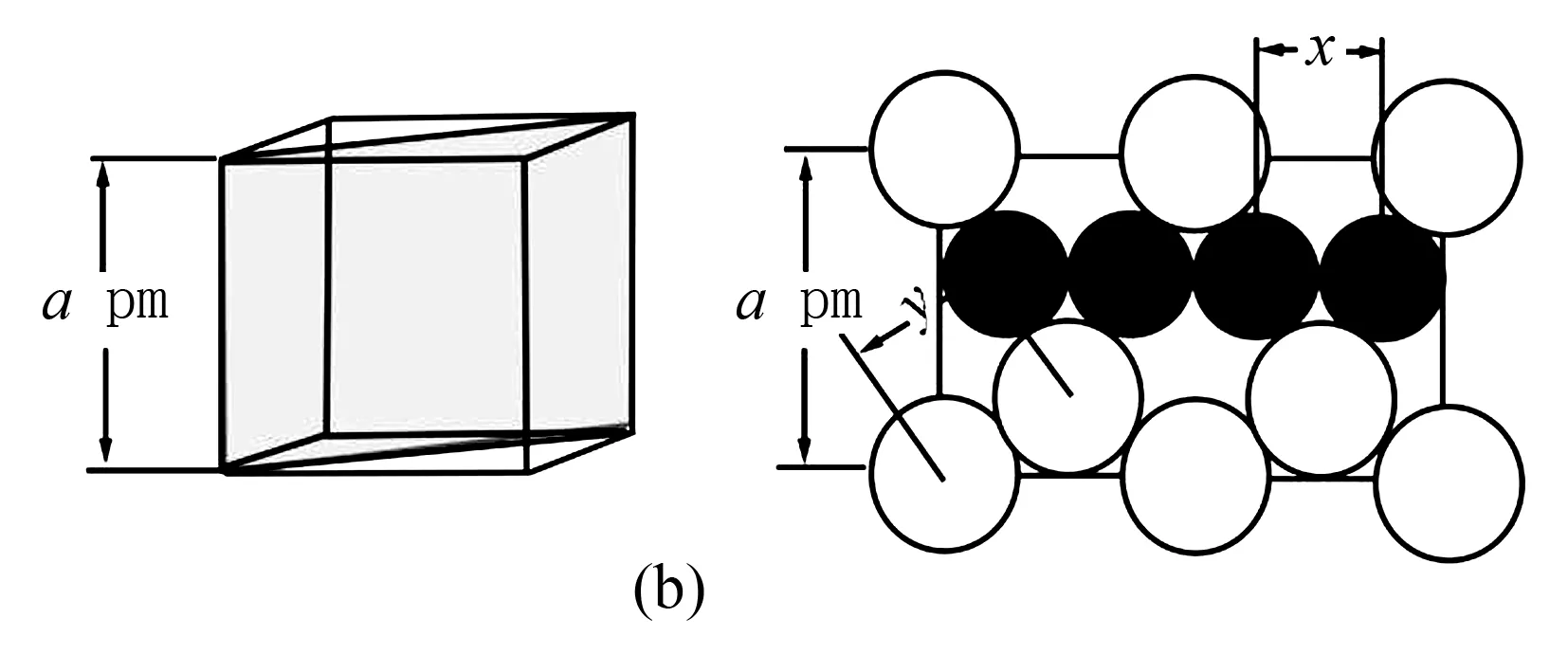
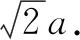
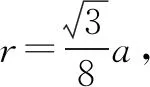
该晶胞中含有8个Mg原子和16个Cu原子,也就是有8个MgCu2基本单元.
所以,MgCu2的密度为
综上所述,高中化学核心素养“模型认知”思维在教学中若想得到有效培养,教师需秉持以人为本教育理念,关注学生化学知识学习动向,引导学生善用化学思维,组就“模型认 知”思维体系,通过建模准备、提出假设、建立模型、检验模型及应用模型,使学生掌握建模方法,体悟建模过程,形成建模意识,达到建立“模型认知”思维体系的目的.
