口腔修复膜材料在牙种植中引导骨再生的临床效果和安全性
2020-03-28米尔阿迪力阿不都卡地尔古丽奴尔沙吾提迪里夏提吐拉洪
米尔阿迪力·阿不都卡地尔,古丽奴尔·沙吾提,迪里夏提·吐拉洪
(1.新疆维吾尔自治区人民医院口腔科,乌鲁木齐 830001;2.新疆医科大学第五附属医院口腔科,乌鲁木齐 830000)
口腔出现创伤性牙缺失后,由于气体的生理性吸收作用会导致骨骼组织缺少,从而使部分牙槽过小或有缺陷,所以在牙种植手术时会出现穿孔现象[1]。而采用修复膜材料在骨缺损处进行覆盖,引导骨再生为骨组织缺损的修复治疗提供了新思路,其中屏障膜材料的应用能不同程度地增强骨组织的再生能力,已成为牙种植过程中的一种常用治疗手段[2-3]。在骨缺损处覆盖一层高分子的生物膜作为屏障,可确保骨缺损区骨的修复,将修复膜材料精确放置在骨缺损处,特别是牙槽嵴颊侧,可以引导骨再生,抑制骨吸收,也可以提高植入物的长期存活率[4-6]。同时,使用修复膜也可有效保护患者的血液凝结,减小覆盖组织的压力,并有效增加修复膜和牙龈表面组织的接触空间,从而有效提高牙齿破损骨骼组织的再生能力。此外,采用修复膜材料还可以增加骨量。因此,引导骨组织再生术在临床得到越来越多的开发和应用。目前,多种生物材料运用于临床并发挥屏障膜作用,早期的修复膜材料一般采用聚四氟乙烯膜,比例为30%~40%[7]。近年来开始采用钛膜材料,但这些材料均不可吸收,需再次进行手术去除[8]。而采用可吸收材料制作口腔修复膜材料能避免再次手术。其中,胶原蛋白膜由于具有更长的降解时间、更好的骨再生效果,在临床应用广泛[9]。本研究主要探讨口腔修复膜材料在牙种植中引导骨再生的临床效果和安全性。
1 资料与方法
1.1一般资料 选取2017年1月至2018年1月在新疆维吾尔自治区人民医院口腔科接受牙种植的患者49例作为研究对象。纳入标准:①年龄≥18岁;②单颗牙缺失;③接受择期牙种植修复术。排除标准:①牙周组织活动性感染;②孕妇或哺乳期妇女;③对于新型胶原蛋白口腔修复膜材料和传统钛膜材料中的任何成分过敏。上述患者按照治疗方法不同分为观察组(24例)和对照组(25例)。本研究经新疆维吾尔自治区人民医院医学伦理委员会批准,患者均签署知情同意书。
1.2治疗方法 治疗前两组患者均接受X线检查,牙科检查(包括测量牙槽骨的厚度和高度,植骨厚度和成骨厚度),然后进行CT扫描获得牙槽图像,以明确牙槽骨的厚度和高度情况,并评估患者的软组织和硬组织损坏状况。
患者保持仰卧位,由消毒人员对口腔内外进行消毒,对手术部位进行局部浸润麻醉,切开翻瓣。两组患者行牙种植引导骨再生均根据常规手术步骤放置植入物,将骨粉浸入0.9% NaCl注射液中,然后将其放置在植入物侧的骨缺损区域,再根据患者牙骨缺损创面的形状和大小选择口腔修复膜材料。其中,观察组采用的材料为海奥胶原蛋白口腔修复膜(烟台正海生物技术有限公司生产,型号:C3,规格:2 cm×1.5 cm),对照组采用传统钛膜(西安中邦钛生物材料有限公司生产,型号:IG1W4509,规格:2.5 cm×2.5 cm)。
两组均在放置好植入物的边缘处覆盖2.0~3.0 mm,充分松弛牙龈软组织瓣后,用缝线闭合切口。手术完成后,使用抗生素预防发生感染,并在手术后7~10 d将缝合线移除。
1.3观察指标 修复手术结束后6个月,对两组患者手术前后的骨缺损情况(骨缺损高度,定义为最终修复前后的牙槽嵴厚度与术前牙槽嵴厚度之差),修复后植骨厚度与成骨厚度(采用10分度游标卡尺测量)以及不良反应发生情况进行评估。

2 结 果
2.1两组患者的一般资料比较 两组患者的性别、年龄、吸烟状况、牙周病史及种植部位比较差异无统计学意义(P>0.05)。见表1。
2.2两组患者手术前后的骨缺损情况比较 手术后两组患者的骨缺损高度均低于手术前,且观察组的骨缺损高度低于对照组(P<0.05),两组间、时点间及组间和时点间交互作用比较差异均有统计学意义(P<0.01)。见表2。

表1 两组接受牙种植患者的一般资料比较
对照组:采用传统钛膜治疗;观察组:采用海奥胶原蛋白口腔修复膜治疗;a为t值,余为χ2值


组别例数手术前手术后对照组255.1±2.12.3±0.5观察组245.0±1.92.1±0.7 组间F=19.032 P<0.001 时点间F=54.467 P<0.001 组间·时点间F=57.315 P<0.001
对照组:采用传统钛膜治疗;观察组:采用海奥胶原蛋白口腔修复膜治疗
2.3两组患者修复后植骨厚度与成骨厚度的比较 观察组植骨厚度和成骨厚度显著高于对照组(P<0.01)。见表3。

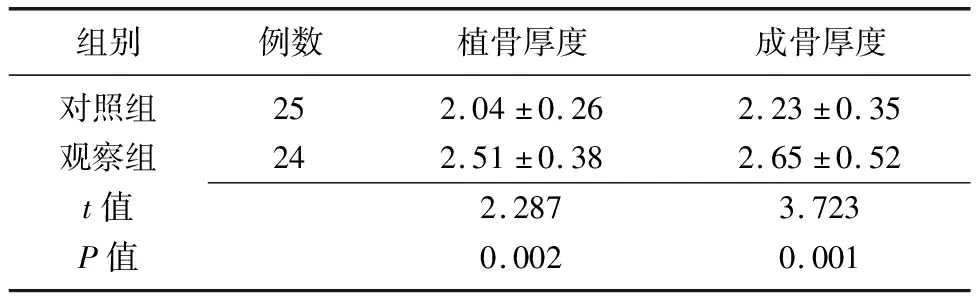
组别例数植骨厚度成骨厚度对照组252.04±0.262.23±0.35观察组242.51±0.382.65±0.52t值2.2873.723P值0.0020.001
对照组:采用传统钛膜治疗;观察组:采用海奥胶原蛋白口腔修复膜治疗
2.4两组患者的不良反应发生情况比较 两组患者的切口裂开、修复膜暴露、牙周组织红肿及总不良反应发生率比较差异无统计学意义(P<0.05)。见表4。
3 讨 论
近年来,采用修复膜材料在骨缺损处进行覆盖,引导骨再生已成为牙种植的常用治疗方法。引导骨再生是一种使用生物膜在软组织和牙龈的骨缺损之间人为地建立生物屏障的过程,该生物膜由生物材料制成,软组织中的成纤维细胞和上皮细胞在屏障外生长。其目的是尽量闭合植入物的咬合-颊侧角的空间。闭合空间对于骨再生非常重要,因为缝合的皮瓣会产生一定的压力,将骨移植材料推入周围区域,可能影响骨再生。而口腔修复膜可以固定颗粒状移植材料,防止这一问题的发生。研究显示,无修复膜固定时,颗粒状移植材料在切口闭合期迁移到周围组织,严重影响骨再生[10]。近年来,多采用胶原蛋白修复膜或钛膜作为牙骨槽缺损的修复膜,将骨移植物固定在所需要的位置[11-12]。

表4 两组接受牙种植患者的不良反应发生情况比较 [例(%)]
对照组:采用传统钛膜治疗;观察组:采用海奥胶原蛋白口腔修复膜治疗;a为校正χ2值
新型胶原蛋白口腔修复膜是一种可生物降解的新材料。它可以被口腔组织吸收,从而避免再次手术。此外,新型胶原蛋白口腔修复膜的降解时间长,生存期较长,且降解产物没有细胞毒性。它的生物结构保证了可与牙周软组织密切接触,完全有效地闭合了植入物的咬合-颊侧角的空间[13-15]。同时,它又具有高密度的孔隙(160 μm),保证了植骨生长区域的血流灌注,从而使新生成的骨组织贴合至生物膜上,最终新生骨能与自体骨紧密结合[16-17]。张自强等[18]研究显示,术后1个月覆盖膜的动物骨缺损有不同程度修复,而不覆盖膜的骨缺损明显存在,且骨缺损内有肌肉长入;同时,该研究发现喜勒可吸收生物膜与市售生物修复膜均能有效阻挡软组织进入骨缺损区生长,表明该修复膜可以作为骨细胞载体促进骨修复[18]。
本研究结果显示,手术后观察组的骨缺损高度低于对照组(P<0.05)。其原因主要为在口腔软组织与骨骼组织之间,口腔修复膜可以作为机械性的生物屏障,牙根缔结与上皮组织细胞被该屏障阻挡在骨缺损区外,保证具有较高生命潜力且运动速度缓慢的成骨细胞可以率先进入骨缺损区;同时该生物屏障还具有血凝块保护作用,使覆盖组织承压减小,在修复膜与种植体外部,为成骨细胞生长保留足够的空间,从而使骨缺损区形成新骨。应用钛膜骨缺损修复效果较差,主要原因为钛膜与骨面的贴合效果较差,可以通过延长钛膜使其超过骨边缘的长度,保证其贴合的紧密性,也可以采用固定的钛钉,加强钛膜边缘的稳固性。由于牙槽骨具有较强的自成骨能力,使用修复膜后,成骨速度加快。
本研究结果显示,观察组的植骨厚度和成骨厚度均明显高于对照组(P<0.01)。其主要原因为钛膜不被患者吸收,故患者的血液无法进入植骨区,影响植骨区对血液中营养的吸收,从而引起各种并发症。新型胶原蛋白口腔修复膜具有多孔层,可以与骨组织紧密接触(包含血液)。血液能有效地进入骨移植物的生长区域,为骨移植物的正常生长提供必要的营养,促进新的骨组织与生物膜之间的密切贴合,确保新骨与自体骨的正常生长,使细胞正常进入缺损区域,并有效增强空间稳定性[19]。本研究中,两组患者的切口裂开、修复膜暴露、牙周组织红肿发生率比较差异无统计学意义(P>0.05),提示采用胶原蛋白口腔修复膜并不会导致更多的不良反应。
综上所述,可吸收生物膜具有较好的安全性。海奥胶原蛋白口腔修复膜移植4个月后开始被吸收,6个月后被完全吸收,缓慢吸收有效促进了大范围骨缺损能及时被提供足够的新骨,从而提升种植效果[20]。故在牙种植引导骨再生过程中,新型胶原蛋白口腔修复膜材料的应用保证了修复的成功率,骨与植骨均可得到较好的生长发育,并在不良反应发生率得到控制的前提下,保证了牙周软组织的健康。因此,它是一种可靠的牙种植体引导骨再生材料,具有良好的应用前景。
