无模板剂介孔锆基固体碱的制备及其催化合成甘油碳酸酯性能
2020-03-27路文学王振华蒋希希张学兰王登峰
柏 冬, 路文学, 王振华, 蒋希希, 张学兰, 王登峰
(1.枣庄学院 化学化工与材料科学学院,山东 枣庄 277160;2.兖矿水煤浆气化及煤化工国家工程研究中心有限公司,山东 济南 250101)
化石能源的大量消耗加剧了能源危机和环境污染[1],这使得具有可再生、低燃烧排放和易生物降解等优点的生物柴油产业得到了迅猛发展。然而,生产10 kg生物柴油会副产1 kg甘油[2]。因此,开发高附加值甘油下游产品利于生物柴油产业良性发展。甘油碳酸酯(GC)是甘油衍生物重要一环,其沸点和闪点较高,挥发性低,常被用作绿色有机溶剂。同时,GC也是一种高反应活性有机合成中间体[3]。传统合成GC的光气法由于光气剧毒性已被淘汰[4]。以廉价、无毒的二氧化碳和甘油直接合成GC极具发展潜力。然而,该路线反应条件苛刻、转化率低[5]。为克服上述缺点,众多学者研究了尿素醇解法合成GC,但该技术需在真空条件下将副产的氨气移出以推动GC合成[6]。另一方面,碳酸二甲酯(DMC)可替代剧毒光气和硫酸二甲酯作为绿色羰基化试剂使用。因而,以甘油和DMC为原料经酯交换法合成GC是一条环境友好型路线,符合绿色化学的发展[7]。尽管诸如NaOH、KOH和Na2CO3等均相催化剂可催化酯交换合成GC,但它们与产物分离困难,其工业化应用受到了限制[8]。文献[9]报道,与酸性催化剂相比,碱性催化剂更有利于酯交换反应的发生。因此,开发出碱性较强的催化剂可促进GC合成。CaO、MgO和La2O3等简单金属氧化物初始活性高,但其碱性位易被空气中水蒸气和二氧化碳污染而失活。且这些金属氧化物的比表面积小,活性位点暴露不足,催化剂活性还有待改善[10]。解决上述问题的有效途径是选择合适载体,以提高催化剂活性和稳定性。在诸多催化剂载体中,氧化锆由于其显著的热稳定性和高比表面积,一直是人们研究的热点[11]。刘水刚等[12]报道了 MgO-ZrO2催化合成二丙二醇甲醚;刘卓等[13]发现Na2O-ZrO2在催化环氧丙烷合成1,2-丙二醇中具有优异的催化性能。但是,此类催化剂需以正丙醇锆为锆源,且要借助昂贵的P123为模板剂,才能获得较高的比表面积[12-14]。同时,催化剂制备方法繁琐,极大地限制其工业化应用。
笔者以廉价的硝酸锆为锆源,无需使用模板剂,即可通过简单的共沉淀法制备出3种不同组成的锆基固体碱催化剂。借助X射线衍射(XRD)、N2吸附-脱附、透射电镜(TEM)和二氧化碳程序升温脱附(CO2-TPD)等手段,对催化剂的物化性质进行了表征。并在反应釜中考察了它们催化甘油和DMC合成GC的反应性能,优化了反应条件。结合催化测试和CO2-TPD表征结果,阐明了催化剂催化性能和碱性质之间的内在联系。考察了具有最佳催化效果的MgO-ZrO2催化剂的重复使用性,获得了合成GC的理想多相催化剂。
1 实验部分
1.1 试剂及原料
本实验中所用化学试剂和原料均为分析纯,未经任何预处理。Mg(NO3)2·6H2O、Ca(NO3)2·4H2O、Zr(NO3)4·5H2O、碳酸二甲酯(DMC)和甘油,国药集团化学试剂有限公司产品;La(NO3)3·6H2O和NaOH,天津科密欧试剂有限公司产品。
1.2 催化剂制备
在无模板剂作用下,利用共沉淀法制备具有不同组成的锆基固体碱催化剂。催化剂前驱体金属起始摩尔比n(M)/n(Zr)=0.5(M为Ca、Mg或La)。以制备MgO-ZrO2催化剂为例,典型的制备过程如下:将Mg(NO3)2·6H2O和Zr(NO3)4·5H2O按上述比例溶于50 mL去离子水;剧烈搅拌下,与 2 mol/L 的NaOH溶液(50 mL)同时滴加到500 mL烧杯中,在此过程中保持混合液pH=10。将混合液在25 ℃下老化6 h、抽滤,去离子水洗涤数次至滤液中性,将沉淀在去离子水中于80 ℃回流 24 h。经抽滤将所得滤饼100 ℃下干燥24 h获得催化剂前驱体。最后,在N2气氛中于500 ℃煅烧6 h即得到MgO-ZrO2催化剂样品。CaO-ZrO2、La2O3-ZrO2和ZrO2的制备过程与MgO-ZrO2的类似:对于前2种材料而言,分别用Ca(NO3)2·4H2O和La(NO3)3·6H2O替代Mg(NO3)2·4H2O;制备ZrO2时,只使用单一的Zr(NO3)4·5H2O,而不加入其他金属组分。
1.3 催化剂表征
采用日本理学D/max-rA型X射线衍射仪测得催化剂样品的XRD谱图,CuΚα辐射,Ni滤光片,管电压和管电流分别为40 mV和40 mA。采用美国Micromeritics公司Tristar型3000自动物理吸附仪对催化剂样品进行N2吸附-脱附实验。实验前,将样品在300 ℃真空预处理3 h,液氮温度下获得吸附-脱附曲线。催化剂的比表面积通过BET方法计算获得;孔径分布曲线由Barrett-Joyner-Halender(BJH)方法确定。采用JEOL JEM-2010型透射电镜获得催化剂样品的TEM照片。采用自制的化学吸附仪进行CO2程序升温脱附(CO2-TPD)实验。在U形管里放入200 mg催化剂,500 ℃下预处理3 h,冷却至25 ℃,脉冲吸附CO2(2 h,30 mL/min)后,氩气吹扫物理吸附的CO2。最后,以10 ℃/min的升温速率加热至600 ℃。在此过程中,采用瑞士Balzer公司Omnistar-2000型质谱仪采集信号。
1.4 催化性能评价
甘油和DMC合成GC反应在带有磁力搅拌和温控仪的50 mL高压不锈钢反应釜中进行。称取5.4 g的DMC、1.84 g甘油和质量分数为反应物总量5%的催化剂加入反应釜,快速加热至120 ℃,打开磁力搅拌器,开始计时。待反应结束,关闭搅拌器,反应釜温度降至25 ℃后,取出反应物,过滤除去固体催化剂。采用带有HP-5色谱柱和FID检测器的 GC-950 型气相色谱分析液体产物组成。然后,以甘油转化率(xGlycerol)、GC收率(yGC)和选择性(sGC)、缩水甘油(GD)收率(yGD)和选择性(sGD)评价催化剂活性。
(1)
(2)
(3)
(4)
(5)
式(1) ~(5)中,nGlycrol,0为反应开始时反应体系中甘油的物质的量,mol;nGlycerol、nGC和nGD分别为反应结束后液体产物中甘油、GC和GD的物质的量,mol。
1.5 重复性实验
以MgO-ZrO2为模板催化剂,当反应完成后,将混合液离心,经无水乙醇多次洗涤,除去催化剂表面吸附的有机物种。然后,再将试样放入烘箱于80 ℃干燥12 h后,直接用于下一轮反应。
2 结果与讨论
2.1 催化剂结构和织构表征
图1(a)为所制备的锆基固体碱催化剂样品的广角XRD谱图。可以看出,4种催化剂样品均在2θ为31°、50°和60°出现了属于ZrO2四方相晶型(t-ZrO2)晶相的衍射峰。通常,ZrO2在25 ℃至1170 ℃范围内以单斜晶相(m-ZrO2)存在,四方晶相(t-ZrO2)在此温度范围内属于一种亚稳相[15]。然而在本研究中,四方相结构至500 ℃亦未发生转变。这可归因于Ca2+、Mg2+和La3+离子对t-ZrO2稳定化作用[12,16]。同时,对催化剂前驱体的水热处理也可大幅度提高t-ZrO2结构稳定性[17]。更为重要的是,这些离子能够取代载体部分Zr4+进入其四方相晶格形成稳定的固溶体结构[12-17]。因此,掺杂这些金属后的固体碱样品也只呈现出t-ZrO2晶相,而没有检测到属于CaO、MgO或La2O3单一物种衍射峰。因而,催化剂固溶体结构不但保证了碱性位的引入,还能阻止出现游离碱性位,为催化剂结构稳定性的提高奠定了结构基础。4种锆基固体碱催化材料的小角XRD谱图如图1(b)所示。不难看出,所有固体碱样品皆在2θ=1°附近出现了明显衍射峰,说明Ca、Mg和La金属的掺杂并没有完全破坏ZrO2介孔结构,有利于材料催化活性和稳定性的提高[12-14]。但客体金属的引入会导致该位置衍射峰强度出现不同程度的减弱。尤其是 La2O3-ZrO2催化剂,其衍射峰强度降低得最为明显,说明La的加入使ZrO2的介孔规整度受到的破坏程度最大。
表1为不同锆基固体碱催化材料的织构和表面碱量。由表1可知,与单一的ZrO2相比,引入碱性位后,固体碱催化剂的比表面积均有不同程度的下降。其中,La2O3-ZrO2样品的比表面积最低,这可归因于La的加入对材料介孔规整度破坏最大(如图1(a)所示)。尽管如此,这3种锆基固体碱催化剂比表面积均超过了180 m2/g,远远大于文献报道的CaO、MgO和La2O3催化剂的比表面积[18]。这有助于碱性位在催化剂表面的分散和暴露,为催化剂表面碱量和催化剂活性的提高提供了保证。
图2为不同锆基固体碱催化剂样品的N2吸附-脱附等温吸附和孔径分布。由图2(a)可知,4种催化材料都呈现典型的VI型吸附-脱附等温曲线和H2类滞后环,再次证明了它们都具有规整介孔结构[19]。而且,它们的孔径分布范围集中在20 nm以内(如图2(b)所示)。然而,与ZrO2相比,3种复合氧化物样品的孔径分布范围都有不同程度的增加,与XRD小角表征结果相一致。
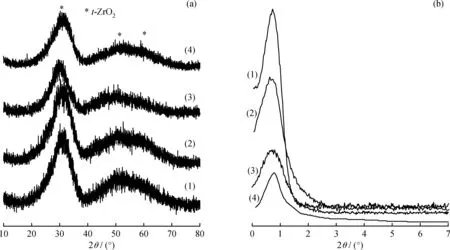
图1 不同锆基固体碱催化剂的XRD谱图Fig.1 XRD patterns of various Zr-based solid bases catalysts(a) Wide angle; (b) Low angle(1) ZrO2; (2) MgO-ZrO2; (3) CaO-ZrO2; (4) La2O3-ZrO2
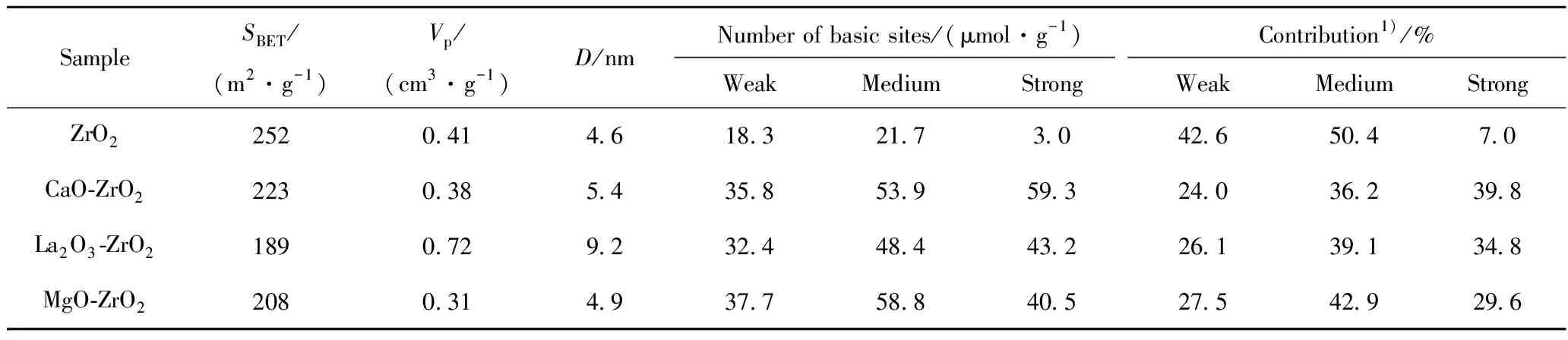
表1 不同锆基固体碱催化剂的织构和表面碱量Table 1 The textural and surface basic amount of various Zr-based solid bases catalysts
Vp—Pore volume;D—Average pore diameter
1) The value is the contribution of single basic sites to the total number of total basic sites.
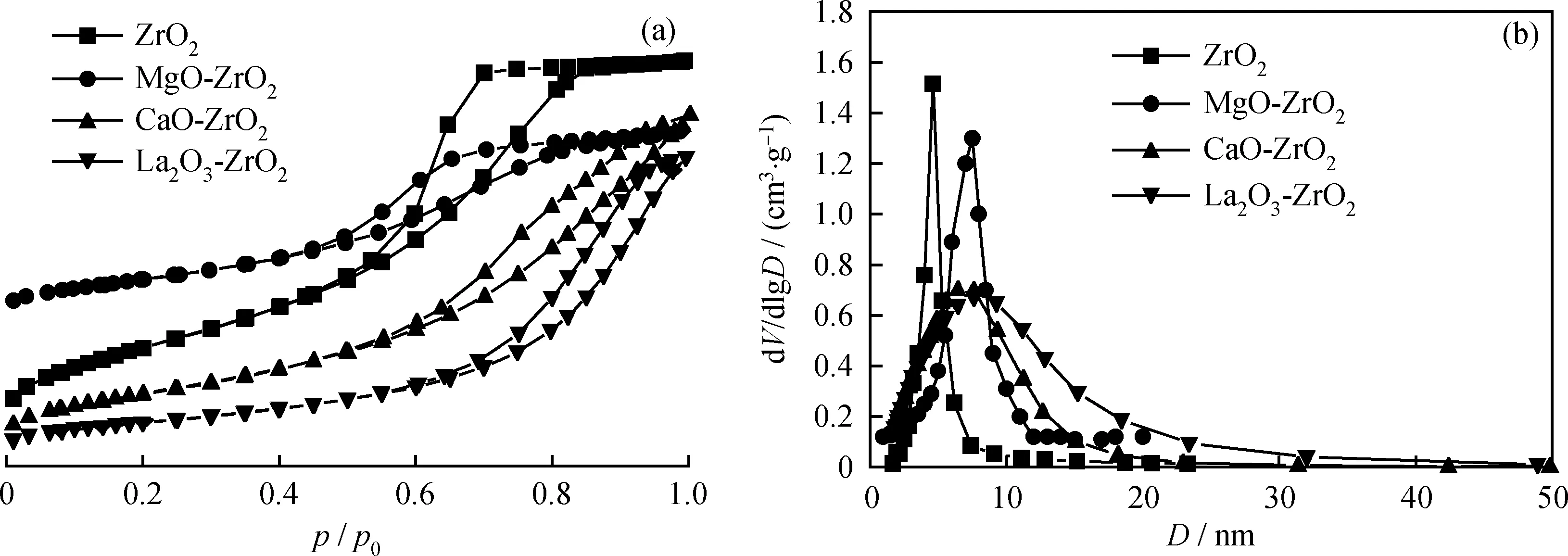
图2 不同锆基固体碱催化剂的N2吸附-脱附等温线和孔分布曲线Fig.2 N2 adsorption-desorption isotherms and pore contribution of various Zr-based solid bases catalysts(a) N2 adsorption-desorption isotherms; (b) Pore contribution
图3为不同锆基固体碱催化剂样品的TEM照片。不难看出,所有样品都具有孔径在5~20 nm的类似于海绵状疏松结构,说明它们都具有完好的多孔孔道。同时,ZrO2和各种金属氧化物混合较为均匀,避免了碱性氧化物颗粒的团聚。这也表明Ca2+、Mg2+和La3+都进入了t-ZrO2晶格,形成了稳定的固溶体结构[12-15]。

图3 不同锆基固体碱催化剂样品的TEM照片Fig.3 The TEM images of various Zr-based solid bases catalysts(a) CaO-ZrO2; (b) MgO-ZrO2; (c) La2O3-ZrO2
2.2 催化剂表面碱性质和催化性能
采用CO2-TPD技术考察了所制备的锆基固体碱催化剂的表面碱性位强度和碱量分布,如图4所示。可以看出,所有曲线都可以分解为3个Gaussian峰,分别对应催化剂的弱碱性位(<200 ℃)、中强碱性位(200~400 ℃)和强碱性位(>400 ℃)。文献[20-21]报道:复合氧化物的弱碱性位产生于表面OH-基团;中等碱性位是由金属-氧离子对(Zr-O和M-O)产生的;而强碱性位是由不饱和O2-离子产生。不难发现,在加入3种金属离子后,锆基固体碱中强碱位和强碱性位都向右出现了不同程度的位移,说明碱性金属的掺杂有利于催化剂碱强度的增加。特别是CaO-ZrO2催化剂,它的强碱性位脱附温度达到了542 ℃。同时,对于这些催化材料来说,它们的强碱性碱强度从高到底的顺序为CaO-ZrO2、La2O3-ZrO2、MgO-ZrO2、ZrO2。另一方面,如表1所示,加入碱性金属后催化剂的碱性位分布也有了明显的变化。对单一的ZrO2载体来说,其弱碱性位所占比例较高,可达到42.6%。与此不同的是,其他3种锆基固体碱复合氧化物催化剂的中强碱性位和强碱性位数量有了明显增加,催化剂表面的弱碱性位被大幅覆盖。导致该现象的原因如下:首先,Ca2+、Mg2+和La3+离子的加入会引起金属-氧离子对(M-O)数量的增加,进而使中等碱性位数量增加;其次,在催化剂制备过程中,上述3种金属的硝酸盐分别与硝酸锆混合,NaOH作用下形成沉淀。在后续烘干和煅烧过程中,3种金属离子取代了部分Zr4+,进入到t-ZrO2晶格。由于Zr4+比Ca2+、Mg2+和La3+带有更多正电荷,随着这些客体金属离子的加入,形成了M-O-Zr结构,增强了晶格氧的负电性。因而,O1s结合能会不断降低,不饱和O2-离子数目也随之增加,进而提高了催化剂强碱性位数量[14]。所以,在弱碱性位数量基本保持一致的前提下,催化剂表面碱性位总量、中碱性位和强碱性位所占比例都得到了大幅提高。需要指出的是,这些样品的表面碱性位数量从高到低的顺序为:CaO-ZrO2、MgO-ZrO2、La2O3-ZrO2、ZrO2。
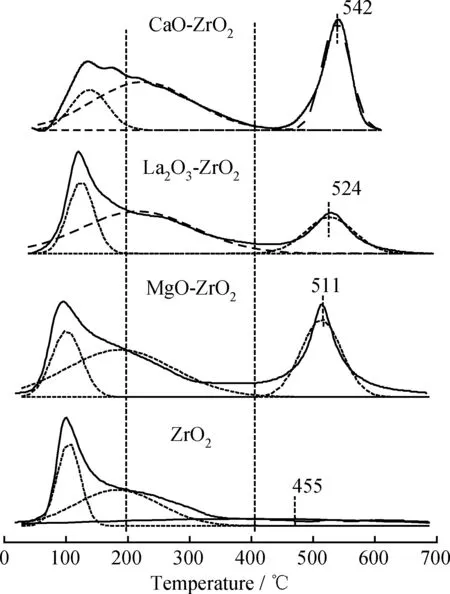
图4 不同锆基固体碱催化剂的CO2-TPD曲线Fig.4 CO2-TPD profiles of various Zr-basedsolid bases catalysts
文献[22]指出,甘油和DMC酯交换反应网络可由图5描述。在催化剂作用下,DMC和甘油在生成GC的同时,释放出甲醇分子。另外,除上述主要产物外,目标产物GC会在碱性位作用下,脱CO2生成副产物缩水甘油(GD)。不同锆基固体碱催化剂催化GC合成的催化性能如表2所示。在无催化剂作用时,反应很难发生,甘油转化率仅为3.2%。在ZrO2作用下,甘油转化率有了一定的提高,然而,GC收率依然很低。在加入客体金属离子后,催化剂活性有了明显的改善,且催化性能与所掺杂的金属离子种类有关。以La2O3-ZrO2为催化剂,甘油转化率有了明显的改善(79.5%)。在相同的反应条件下,CaO-ZrO2具有最高的反应性能,甘油转化率可达到97.6%。然而,需要注意的是,在La2O3-ZrO2和CaO-ZrO2作用下,GC选择性大幅降低。由此相对应的是,副产物GD的选择性有了明显的提高。与这2种催化剂不同,尽管MgO-ZrO2催化剂反应活性小于CaO-ZrO2,然而以GC收率为评价指标,其催化性能最佳,GC收率可达到88.2%。
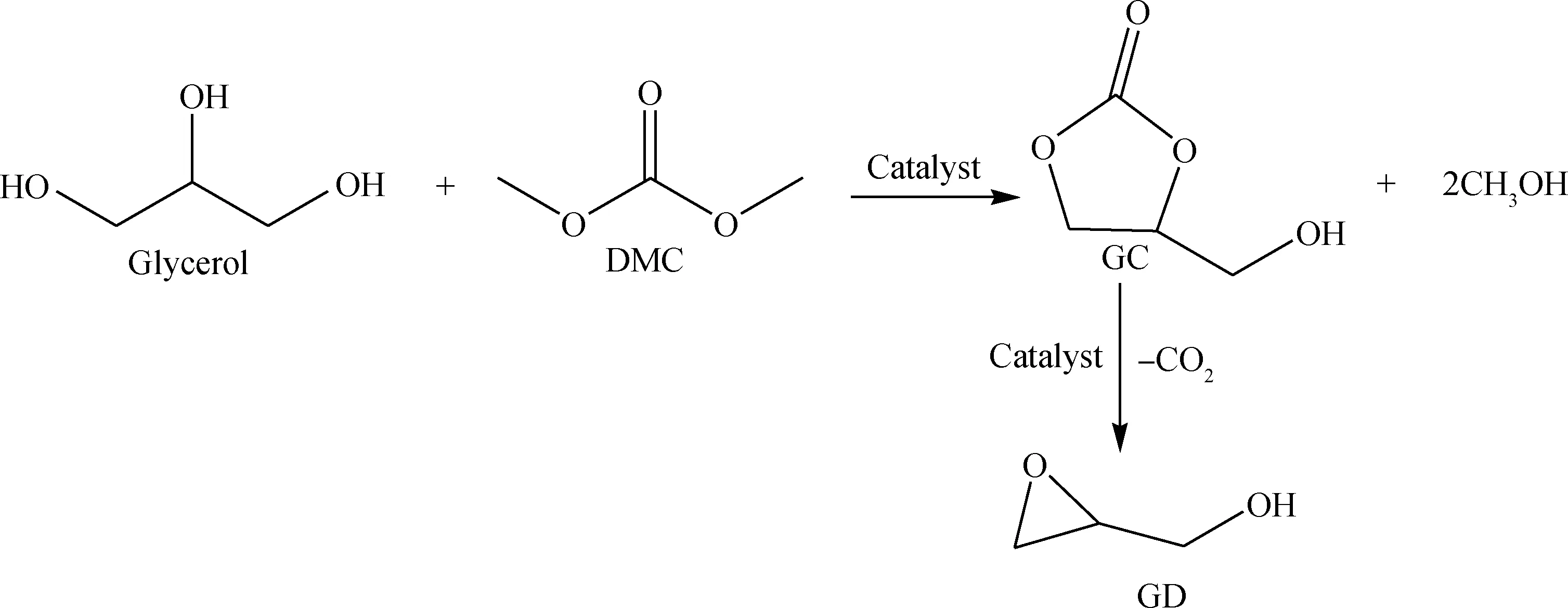
图5 甘油和DMC的反应网络[22]Fig.5 The reaction system of glycerol and DMC[22]GC—Glycerol carbonate; GD—Glycidol

表2 不同锆基固体碱催化剂催化甘油和DMC反应生成GC的催化性能Table 2 The catalytic performance of various Zr-basedsolid bases catalysts for GC synthesis byreaction of glycerol with DMC
Reaction condition:mGlycerol=1.84 g;mDMC=5.4 g;wCatalyst=5%;T=120 ℃;t=3 h
对催化材料来说,其比表面积的提高有利于表面活性位的暴露,进而有益于其催化能力的增强。由前面讨论可知,催化材料的比表面积从高到低的顺序为:ZrO2、CaO-ZrO2、MgO-ZrO2、La2O3-ZrO2;然而,它们的催化活性从高到低遵循以下顺序:CaO-ZrO2、MgO-ZrO2、La2O3-ZrO2、ZrO2。因此,在本研究中,催化剂的比表面积不是催化剂活性的决定因素。考虑到碱性金属的添加利于增强催化剂表面碱性,因而,笔者系统考察了反应刚开始2 h的催化剂反应性能与其表面碱性质之间的关系(见图6)。很明显,催化剂的活性与催化剂表面碱性位总数目有关。当以表面碱性位总数目较低的ZrO2为催化剂时,甘油转化率仅为24.0%;与此相比,具有较高碱性位数目的MgO-ZrO2和La2O3-ZrO2的催化活性有了大幅提高。特别是CaO-ZrO2催化剂,由于其具有最多的碱性位,甘油转化率也就最高,可达到97.6%。然而,文献报道,在强碱性位的作用下,GC会大幅分解为GD,从而引起GC选择性的降低[6,21-22],这也被图6(b)所证明。在具有最强碱强度的CaO-ZrO2作用下,GC选择性最低;当以碱强度最弱的ZrO2为催化剂时,GC选择性最高。笔者系统考察了反应刚开始2 h各催化剂的反应性能,结果见表3。结合表1所列出的催化剂表面碱量,由表3可知,当以表面碱性位总数目较低的ZrO2为催化剂时,甘油转化率仅为24.0%;与此相比,具有较高碱性位数目的MgO-ZrO2和La2O3-ZrO2的催化活性有了大幅提高。特别是CaO-ZrO2催化剂,由于其具有最多的碱性位,甘油转化率也就最高,可达到80.7%。然而,文献[6,21-22]报道,在强碱性位的作用下,GC会大幅分解为GD,从而引起GC选择性的降低,这也被笔者所证实。从图4可知,CaO-ZrO2具有最高的碱强度,当以CaO-ZrO2为催化剂时,GC选择性最低,只有79.2%(见表3)。当以碱强度最弱的ZrO2为催化剂时,GC选择性最高,GC选择性可达到100%。因而,可以得出以下结论,催化剂的活性取决于其表面碱性位数量,催化剂表面碱性位越多,其催化能力也就最强。然而,GC选择性决定于催化剂的碱强度,催化剂碱强度过高,反而不利于GC的选择性合成。对于MgO-ZrO2样品而言,在其表面存在较多的碱性位,同时它又具有合适的碱强度。因而,以GC收率为评价基准,其催化性能最佳,GC收率可达到73.6%。
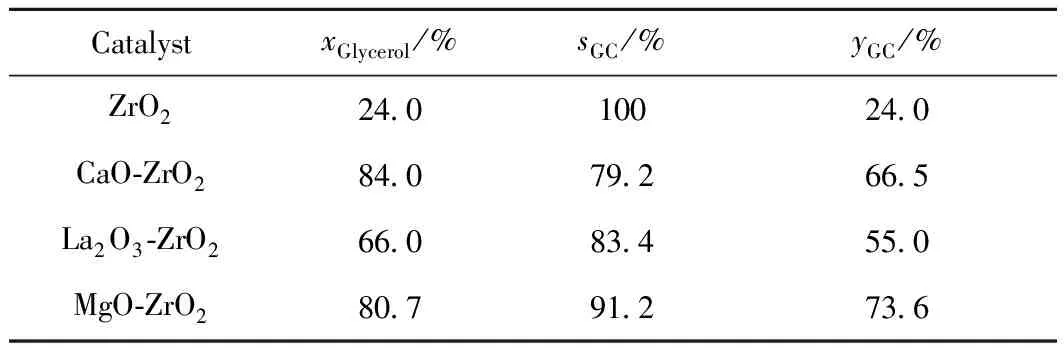
表3 不同催化剂在反应2 h时的催化性能Table 3 The catalytic performance of different catalysts atthe beginning 2 h of the reaction
Reaction condition:m(Glycerol)=1.84 g;m(DMC)=5.4 g;wCatalyst=5%;T=120 ℃;t=2 h
2.3 反应条件对GC合成的影响
以催化性能最优的MgO-ZrO2为模板催化剂,考察了反应温度、反应时间和催化剂用量对GC合成的影响。
2.3.1 反应时间对GC合成的影响
在甘油和DMC的起始质量分别为1.84和5.4 g、反应温度为120 ℃、催化剂质量分数为反应物总量5%条件下反应时间对GC合成的影响如图6所示。在上述条件下,当反应时间为3 h时,甘油转化率可以达到94%。在此过程中,GC收率也快速增加。然而,进一步延长反应时间到4 h,GC收率会出现一定的下降。因而,合成GC最佳反应时间为3 h。
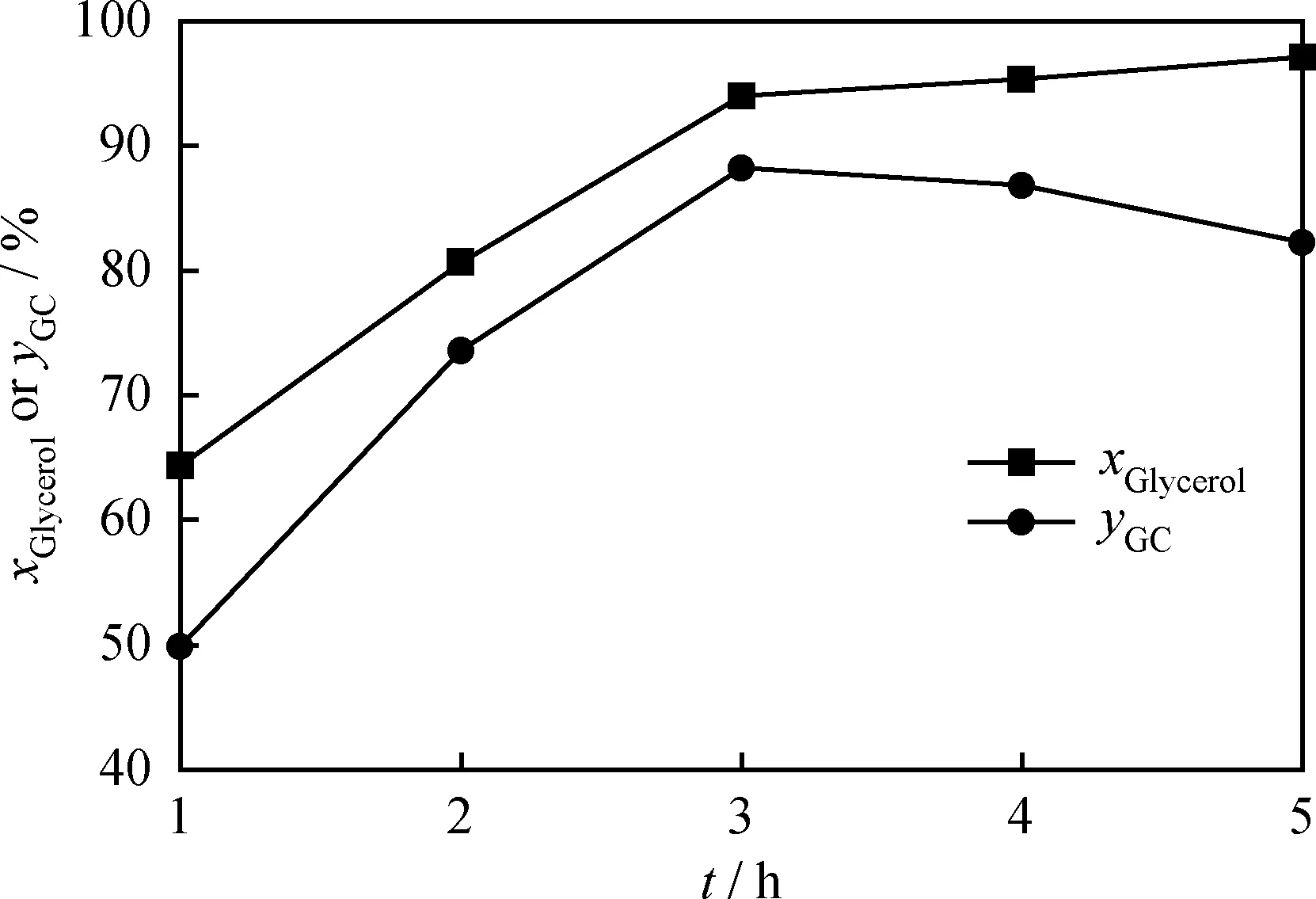
图6 以MgO-ZrO2为催化剂时反应时间对GC合成的影响Fig.6 The influence of reaction time on theGC synthesis over MgO-ZrO2 catalystsReaction condition: mGlycerol=1.84 g; mDMC=5.4 g;wCatalyst=5%; T=120 ℃
2.3.2 反应温度对GC合成的影响
在甘油和DMC的起始质量分别为1.84和5.4 g、反应时间为3 h、催化剂质量分数为反应物总量5%条件下反应温度对GC合成影响规律如图7所示。可以看出,在温度低于60 ℃时,随反应温度的增加,GC收率增长较为缓慢。当超过该温度后,由于甲醇易从液体反应体系逸出,推动了反应向右进行,从而GC收率随温度的进一步升高而快速提高。在反应温度为120 ℃时,可获得最高的GC收率。当温度超过120 ℃,GC收率会出现小幅下降,这可能是由于高温有利于GC分解为GD的缘故。因而,最佳反应温度为120 ℃。
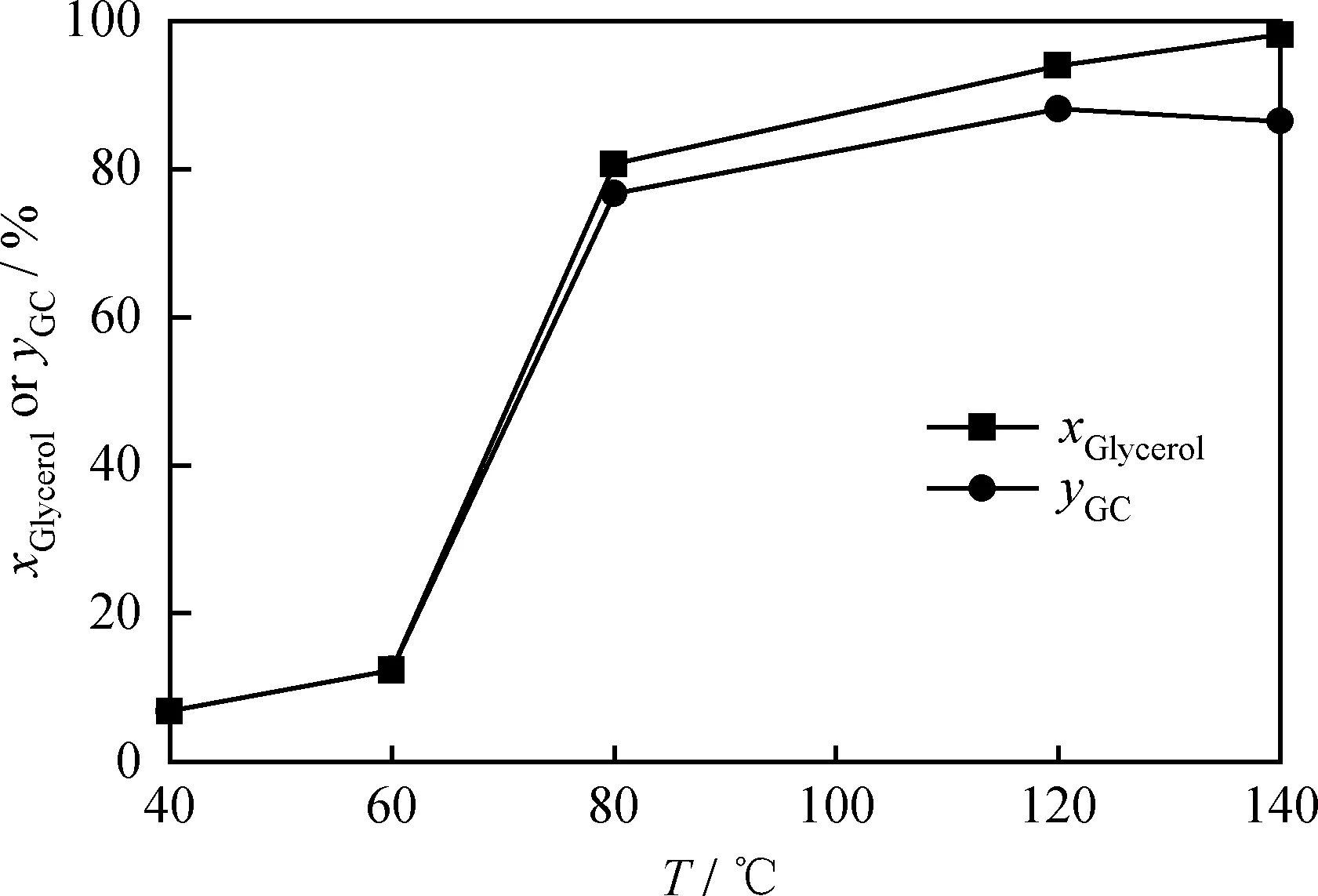
图7 以MgO-ZrO2为催化剂时反应温度对GC合成的影响Fig.7 The influence of reaction temperature on theGC synthesis over MgO-ZrO2 catalystsReaction condition: mGlycerol=1.84 g; mDMC=5.4 g;wCatalyst=5%; t=3 h
2.3.3 催化剂用量对GC合成的影响
在甘油和DMC的起始质量分别为1.84和5.4 g、反应时间为3 h、反应温度为120 ℃条件下,考察了催化剂用量对反应的影响(见图8)。可以看出,随着催化剂用量的增加,GC收率持续增加,当催化剂质量分数为反应物总量5%时,GC收率达到最高。进一步增加催化剂用量,GC收率会有小幅度下降。因而,催化剂最佳用量为质量分数5%。

图8 以MgO-ZrO2为催化剂时催化剂用量对GC合成的影响Fig.8 The influence of catalyst amount on theGC synthesis over MgO-ZrO2 catalystsReaction condition: mGlycerol=1.84 g; mDMC=5.4 g;t=3 h; T=120 ℃
2.4 MgO-ZrO2重复使用性实验结果
对于多相催化剂来说,重复使用性能是评价其工业化应用的重要指标。因而,对于催化性能最优的MgO-ZrO2样品进行了重复使用性实验。笔者所开发的MgO-ZrO2催化剂在使用4次后,其催化活性基本保持不变(见图9)。这说明MgO-ZrO2催化剂具有较高的催化稳定性,是催化DMC和甘油合成GC的理想多相催化剂。其原因在于催化剂制备过程中Mg2+能进入ZrO2晶格,形成了稳定的固溶体。显然,这种结构上的碱性位由于被晶格紧固的“锚定”,不容易流失,从而使催化剂稳定性大大提高。
3 结 论
(1)以硝酸锆为锆源,NaOH为沉淀剂,在无模板剂情况下,采用共沉淀法制得了3种不同组成的介孔锆基固体碱催化剂。研究表明,在催化剂制备过程中,Ca2+、Mg2+和La3+可进入四方相氧化锆,形成稳定的固溶体结构。同时,催化剂表面碱性质取决于所引入的金属种类,它们的表面碱性位数量由高到低的顺序为CaO-ZrO2、MgO-ZrO2、La2O3-ZrO2、ZrO2,碱强度由高到低的顺序为CaO-ZrO2、La2O3-ZrO2、MgO-ZrO2、ZrO2。
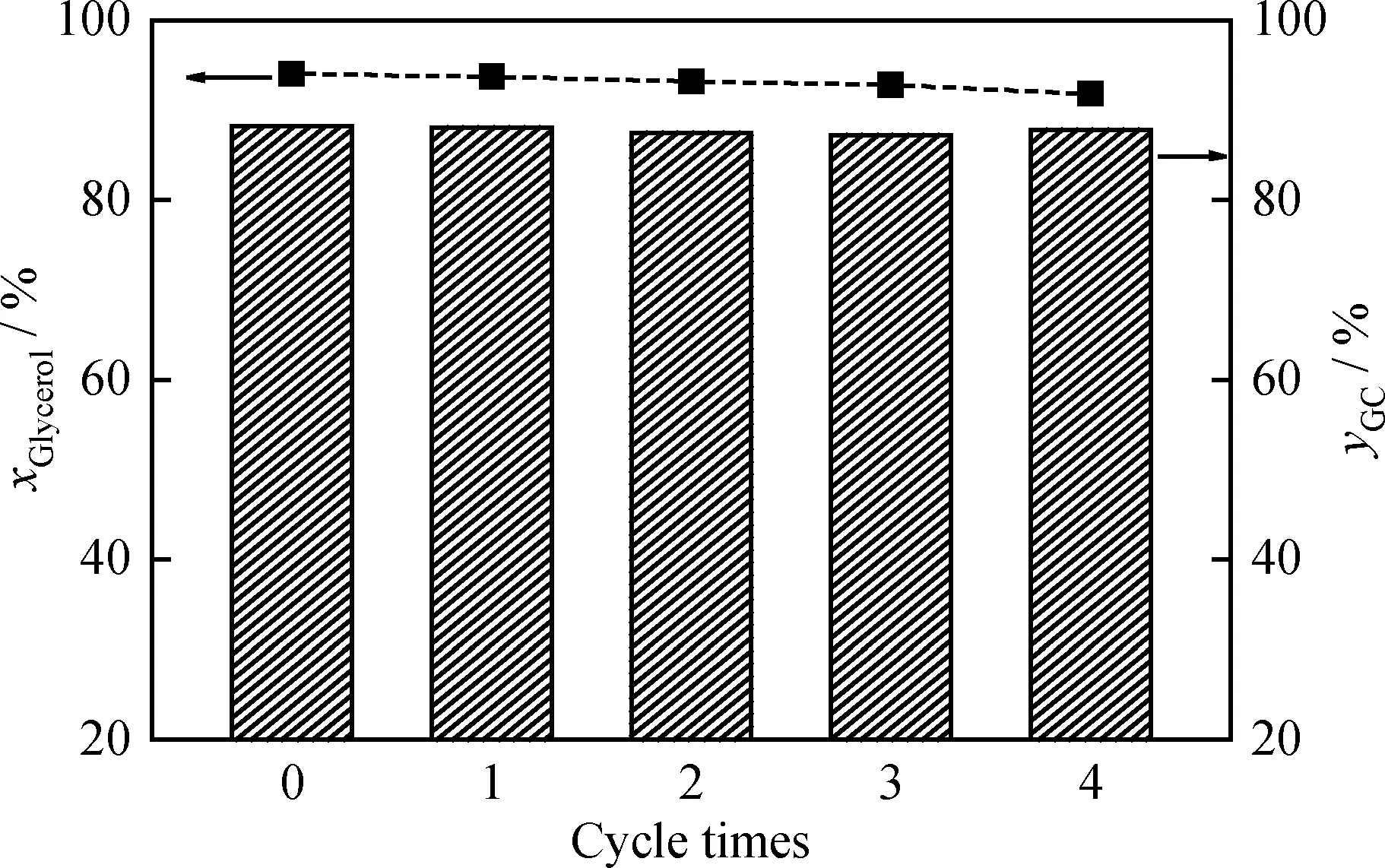
图9 MgO-ZrO2催化剂催化GC合成的重复使用性Fig.9 Catalytic reusability of the MgO-ZrO2 catalystfor the synthesis of GCReaction condition: mGlycerol=1.84 g; mDMC=5.4 g;wCatalyst=5%; t=3 h; T=120 ℃
(2)锆基固体碱催化剂样品催化DMC和甘油合成GC的活性与其表面碱性位总数目成正比。然而,GC选择性随着催化剂碱强度的增加而降低。这是由于GC在强碱性位上发生分解反应造成的。在所制备的催化材料中,MgO-ZrO2具有最适宜的碱性质,因此,其在相同反应条件下,所获得的GC收率最高。
(3)以MgO-ZrO2为模板催化剂,在反应温度120 ℃、反应时间3 h、催化剂用量为总反应物的5%(质量分数)条件下,GC收率可达88.2%。
(4)由于共溶体结构的存在,使碱性位进入了载体晶格。因而,该催化剂在重复使用4次后,催化活性基本保持不变,是合成GC的理想多相固体催化剂。
