剪刀型内镜切开刀在困难部位内镜黏膜下 剥离术治疗中的应用*
2020-03-12徐凯徐萍张黎杨静于海滨
徐凯,徐萍,张黎,杨静,于海滨
[南京医科大学上海松江临床医学院(上海市松江区中心医院) 1.消化内科; 2.病理科,上海 201600]
内镜黏膜下剥离术(endoscopic submucosal dissec- tion,ESD)与传统的内镜下黏膜切除术(endoscopic mucosal resection,EMR)相比,不受病灶大小的限制,即使较大的病变也可做到整块完整切除,有利于术后的病理分析,是当前消化道早癌及癌前病变的首选内镜微创治疗方法。但ESD 操作难度大,在纤薄的消化道管壁进行剥离切开稍有不慎即可发生消化道穿孔等严重并发症,特别是一些操作困难部位的ESD,即使是经验丰富的医师操作仍十分棘手,更是初级操作者的禁忌,限制了这项技术的推广开展。临床上为了解决这一难题,相继开发了新型内镜切开刀(如水刀、flush 刀等)和新的切开技术(如牙线辅助法、隧道法等)。
VS 刀为近年来应用于ESD 治疗的一种新型剪刀型内镜切开刀,其操作类似于使用内镜活检钳,大大降低了ESD 操作的难度,提高了安全性。本研究旨在探讨VS 刀对一些消化道操作比较困难部位进行ESD治疗的可行性和安全性。
1 资料与方法
1.1 一般资料
选取2015年6月-2018年6月因发现消化道早癌及癌前病变拟于本科行ESD 治疗,但术前评估判断为操作困难的病例共29例。其中,男15例,女14例,年龄40 ~84岁,平均(67.10±12.05)岁。病变位于食管14例,胃食管交界2例,胃体上段小弯2例,大肠侧方发育型病变11例(直肠病变累及肛管2例、直肠病变伴有瘢痕1例,右半结肠6例,回盲部2例)。病变最大径2 ~6cm,平均(3.70±1.09)cm。
ESD 操作困难病例[1-2]:经术前评估考虑病变位于直肠肛管附近、胃窦幽门区域、胃食管交界区域和食管入口等,因操作空间狭小,内镜操作困难;病变位于食管、回盲部及右半结肠、胃体上段小弯且病变范围大;伴随有瘢痕改变的病变,预计行黏膜下注射困难。
1.2 方法
1.2.1 器械 ESD 治疗内镜系统使用Olympus CLV-260 型主机,带有附送水功能的Olympus GIF-Q260J型电子胃镜和PCF-Q260JI 型电子肠镜;高频电工作站使用ERBE VIO 200D 电外科工作站;一次性高频内镜切除刀使用日本住友电木株式会社MD-47703 Jr型VS 刀(图1);其他器械包括Alton AF-D2423PN内镜注射针、Olympus FD-410LR 止血钳、ERBE 2200直喷氩气喷头和治疗用内镜头端透明帽等。

图1 MD-47703 Jr 型VS 刀(剪刀型刀头)Fig.1 MD-47703 Jr type of VS knife
1.2.2 内镜操作 所有患者术前均签署手术知情同意书。术中患者采用气管插管全身麻醉,左侧卧位。手术步骤采用传统的ESD 操作步骤:①沿病灶边界外侧约0.50cm 的正常黏膜处以直喷氩气喷头行环周型标记,大肠病变边界清晰者可不标记;②黏膜下注射:以1 ∶10 000 肾上腺素甘油果糖溶液(加入少许靛胭脂溶液)行黏膜下注射,并观察病灶非抬起征是否阳性;③环周切开:以Jr 型VS 刀沿标记点外缘约0.50cm 行环周形切开;④黏膜下剥离:以VS 刀沿黏膜下层切开剥离,直至将病变完整切除,切开和剥离的方法均以VS 刀钳夹黏膜下组织并提起判断深度合适未累及固有肌层后,给予电切模式切开剥离(图2);如遇较粗大血管或有活动性出血时,以VS刀钳夹并给予电凝模式灼烧止血,再给予电切模式切开,如此反复直至病变全部切除;⑤创面处理,以VS刀将创面裸露血管钳夹,并给予电凝模式灼烧,以预防术后迟发性止血。

图2 VS 刀钳夹黏膜下组织提起后行切开剥离Fig.2 The submucosa tissue was lifted by VS knife clamp and dissection
1.2.3 病理学分析 充分伸展标本,保持病灶的完整性,边缘用细针完整的固定于泡沫板上,并标记在体内的相对位置(口/肛侧、前/后壁等),以4%甲醛溶液充分浸泡固定12 ~48 h。先确定距病灶最近的切缘,以此为基准,垂直与切线方向切割,从其旁侧1 mm 开始按大约2 mm 的距离平行切割,并按顺序进行组织包埋及切片来进行组织病理学分析,包括病变性质和垂直切缘/水平切缘情况,如病变为恶性,还应判断最大浸润深度、有无血管、淋巴管及神经累及。整块切除定义为将目标病变一次性完整切除;治愈性切除定义为垂直切缘和侧切缘均阴性,恶性病变无黏膜下层深部浸润(食管< 200μm,胃< 500μm,大肠< 1 000μm),无血管、淋巴管和神经累及。对非治愈性切除患者建议追加外科手术治疗[3]。
2 结果
2.1 手术情况
29例患者均成功完成ESD 操作并获得整块切除,未发生消化道穿孔和大出血等治疗相关并发症。ESD操作时间(从开始行环周标记至病变全部切除的时间,未标记病变为自黏膜下注射至病变全部切除)为35 ~112 min,平均(64.83±17.77)min。病灶平均大小(3.70±1.09)cm。
2.2 术后病理
①14例食管病变中,食管鳞癌6例,3例累及黏膜固有层(M2),2例累及黏膜肌层(M3),1例累及黏膜下层浅层(SM1);4例为食管鳞状上皮高级别上皮内瘤变,4例为食管鳞状上皮低级别上皮内瘤变;②2例胃食管交界病变为腺上皮低级别上皮内瘤变;③2例胃体病变分别为绒毛-管状腺瘤伴高级别上皮内瘤变及高分化腺癌(病变位于黏膜固有层,M2);④11例大肠病变中,4例大肠管状腺瘤,1例大肠管状-锯齿状腺瘤,6例大肠绒毛-管状腺瘤,其中2例伴高级上皮内瘤变。
2.3 术后病理学检查
所有患者垂直切缘及水平切缘均为阴性。术后证实癌变的7例患者血管、淋巴管及神经均为阴性,虽然2例食管M3、1例食管SM1 的患者为ESD 的相对适应证,但术后病理判断切缘、脉管及神经均未累及,且浸润深度最深未超过黏膜下层200 μm,故所有病例均判断为治愈性切除,不需追加外科手术治疗。见图3。
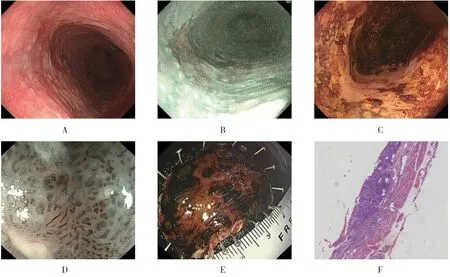
图3 表浅型食管鳞癌的ESD 治疗Fig.3 ESD treatment of superficial esophageal squamous cell carcinoma
2.4 随访
所有患者随访6 ~42 个月,平均(27.69±12.31)个月,均未发现复发。
3 讨论
ESD 自1988年被报道应用于胃早期肿瘤以来,因其整块切除率高、不受病变大小的限制和创伤小等优势,具有较高的治愈性切除率和恶性极低的复发率,已成为消化道早癌及癌前病变内镜微创治疗的首选方法[4-5]。但ESD 需要在狭窄的消化道腔内进行剥离,对操作的技术要求较高,稍有不慎可能发生消化道穿孔及出血。ESD 导致消化道穿孔的发生率东、西方国家分别为3.11%和3.38%,大肠病变的术中穿孔和术后迟发性穿孔发生率分别为4.20%和0.22%,食管穿孔率报道为1.50%~5.00%[6-9]。大部分通过内镜下金属夹夹闭可治愈,但仍有部分治疗失败,甚至可能发生纵隔、腹腔感染等严重并发症[10]。特别是对于一些操作困难的部位,如胃食管交界、肛管和回盲部等部位,即使经验丰富的医师也十分棘手,而对于一些经验不足的操作者来说更是禁忌。因此,在一定程度上限制了该技术的推广应用。
VS 刀为近年应用于临床的剪刀型内镜切除刀,剪刀型的刀头具有电切、电凝功能。VS 刀操作类似内镜活检钳,在切开时可像活检钳一样将拟切开组织夹起,确认未累及深层组织及固有肌层后,再给予高频电切,整个切除过程与内镜下活检过程相似,易于掌握,且大大降低了ESD 操作过程中的穿孔风险。此外,当发现切除部位有较大的血管时,可先钳夹给予电凝灼烧后再切开,降低了操作中的出血风险,并可以像热止血钳一样对术中发生的活动性出血随时给予钳夹电凝止血,且无需更换器械。上述优势使VS 刀在应用于操作困难部位的ESD 治疗时,较传统内镜切除刀更容易掌握,且有着更高的安全性[11-12]。
笔者近期对29例操作困难部位的病变开展了应用Jr 型VS 刀进行ESD 治疗的尝试。因病变位于胃食管交界、胃体小弯、直肠并累及肛管、或病变伴随有瘢痕改变等原因,术前评估认为行ESD 操作比较困难,从而应用Jr 型VS 刀进行ESD 治疗。尽管笔者对上述病变操作经验较欠缺,以往较少独立操作,但因Jr 型VS 刀可在每次切开操作前预先将组织钳夹提起,待确认层次正确后再进行切开,故保证了安全性,所有患者均成功地进行了ESD 操作,且全部获得了一次性整块切除,未发生消化道穿孔、大出血等治疗相关并发症,初步证实了VS 刀在困难ESD 操作中的可行性和安全性。
目前,对ESD 的疗效评价一般涉及整块切除率、治愈性切除率和复发率等。整块切除率是随后对切除病变进行系统病理分析,判断其完全切除率和治愈性切除率,从而进一步评判治疗后的复发风险,及是否需要进一步追加内镜或手术治疗。有文献[13]分析了近年来东西方关于ESD 疗效的报道,其中整块切除率为92.00%~97.00%,治愈性切除率为73.60%~94.70%。 本组患者均为相对操作困难的病例,但通过应用VS刀获得了100.00%的整块切除,使随后的病理分析成为可能。术后病理评估所有患者均达到治愈性切除,无需追加外科手术治疗,所有患者随访至今未见复发。
在应用VS 刀的过程中笔者发现,在进行多次的电切、特别是长时间电凝后,易导致刀头无法张开而需反复取出器械进行清洗,同时在操作过程中,需要助手经常旋转刀头的方向,以调整合适的角度进行切开,这导致了操作时间的延长。但VS 刀易于操作、可有效控制术中出血,降低了出血发生率使内镜视野干净清晰,又相应地节省了操作时间。本组患者的操作时间为35 ~112 min,平均(64.83±17.77)min,与应用其他器械进行ESD 治疗比较无明显的延长[14-15]。且随着操作经验的进一步丰富,术者与助手配合默契度提高,还有可能进一步缩短操作时间。
综上所述,应用VS 刀进行ESD 治疗的经验显示,操作简单,无需掌握特殊的ESD 技巧,整块切除率高,并发症发生率低,使ESD 操作的难度降低,安全性提高。即使经验少,也能对一些较为困难复杂的病变进行安全的ESD 操作,大大降低了其门槛,有利于临床的推广普及。
