腹腔镜辅助经肛全直肠系膜切除术治疗中低位直肠癌的临床分析(附32例报告)*
2020-03-12龙飞欧阳军陈向恒赵晓春刘泳周新栋陈浪邓江平
龙飞,欧阳军,陈向恒,赵晓春,刘泳,周新栋,陈浪,邓江平
(南华大学附属第一医院 胃肠外科,湖南 衡阳 421001)
经肛全直肠系膜切除术(transanal total mesorectal excision,TaTME)是基于经自然腔道内镜手术(natural orifice transluminal endoscopic surgery,NOTES)的理念,利用经肛的操作平台,采用“由下而上”的操作路径,并遵循全直肠系膜切除(total mesorectal excision,TME)原则而实施的经肛腔镜直肠癌切除手术[1]。该术式自2007年提出以来[2],在经过动物试验和尸体试验的反复论证后,最终于2010年进入临床研究[3-4]。2013年,TME 理念的提出者HEALD[5]评价:TaTME利用自下而上的独特视角,可能成为解决老问题的新方法。近十年的临床实践也证明,对于男性、前列腺肥大、肥胖、肿瘤直径>4.00cm、直肠系膜肥厚、低位直肠前壁肿瘤、骨盆狭窄、新辅助放疗引起的组织平面不清晰等“困难骨盆”的直肠癌患者,TaTME可能具有独特的优势[6-10]。在我国,一些大型的胃肠中心也陆续开展并报道了完全TaTME 和腹腔镜辅助TaTME 手术的临床实践和经验总结[11-13]。南华大学附属第一医院胃肠外科从2017年开始,在湖南省率先开展了此项技术,至2018年共完成32例中低位直肠癌的腹腔镜辅助TaTME 术。现报道如下:
1 资料与方法
1.1 一般资料
回顾性分析南华大学附属第一医院胃肠外科2017年12月-2018年12月采用腹腔镜辅助TaTME 术治疗的中低位直肠癌患者32例。其中,男21例,女11例;年龄46 ~63岁,平均(54.65±3.24)岁;体质指数(body mass index,BMI)20.75 ~27.64 kg/m2,平均(23.76±1.82)kg/m2。32例患者术前均完善肠镜并行活检,明确病理诊断为腺癌,其中高分化9例,中分化16例,低分化7例;通过肠镜、肛门指诊及MRI确定肿瘤下缘距肛缘的距离为2.00 ~10.00cm,平均(4.94±1.32)cm;肿瘤大小为1.50 ~5.00cm,平均(3.12±0.87)cm。术前均行胸腹部增强CT 和盆腔MRI,并根据美国癌症联合委员会(American Joint Committee on Cancer,AJCC)/国际抗癌联盟(Union for International Cancer Control,UICC)第8 版结直肠癌TNM 分期系统进行临床分期(cTNM)[14],其中Ⅰ期15例,Ⅱ期11例,Ⅲ期6例;有1例直肠系膜筋膜(mesorectal fascia,MRF)阳性。依据中国卫计委结直肠癌诊疗规范(2017年版)[15],17例(Ⅱ、Ⅲ期)有新辅助放化疗指征,其中11例行新辅助放化疗并获得明显降期,6例拒绝行新辅助放化疗。
1.2 方法
1.2.1 手术方法 手术均由同一组医师序贯完成,具体手术操作参照“直肠癌经肛全直肠系膜切除专家共识及手术操作指南(2017 版)”[16]。手术主要分为三个部分:①经腹操作部分:采用常规腹腔镜辅助TME的手术操作,到达腹膜返折水平后转为经肛手术;②经肛操作部分:经过充分扩肛后置入圆盘拉钩牵开肛门,距肿瘤下缘1.00 ~2.00cm 处行荷包缝合,关闭肠腔;在荷包缝合的远端切开直肠壁全层,进入盆底,并循盆筋膜脏层与壁层间的“神圣平面”自下向上游离直肠系膜,直到与腹部操作平面会合,完成TME;③标本移除及消化道重建:经肛拖出直肠癌TME 手术标本,离断近端的结肠,移除标本,并使用器械或手工吻合完成消化道重建。术前术后均按照加速康复外科(enhanced recovery after surgery,ERAS)的理念和营养支持的要求进行管理[17-18]。TaTME 手术操作要点见图1。
1.2.2 术后随访 术后1 个月随访1 次,之后每3 个月随访1 次,随访内容包括患者生存情况、生活质量情况和肿瘤复发转移情况,随访时间截至2019年6月。
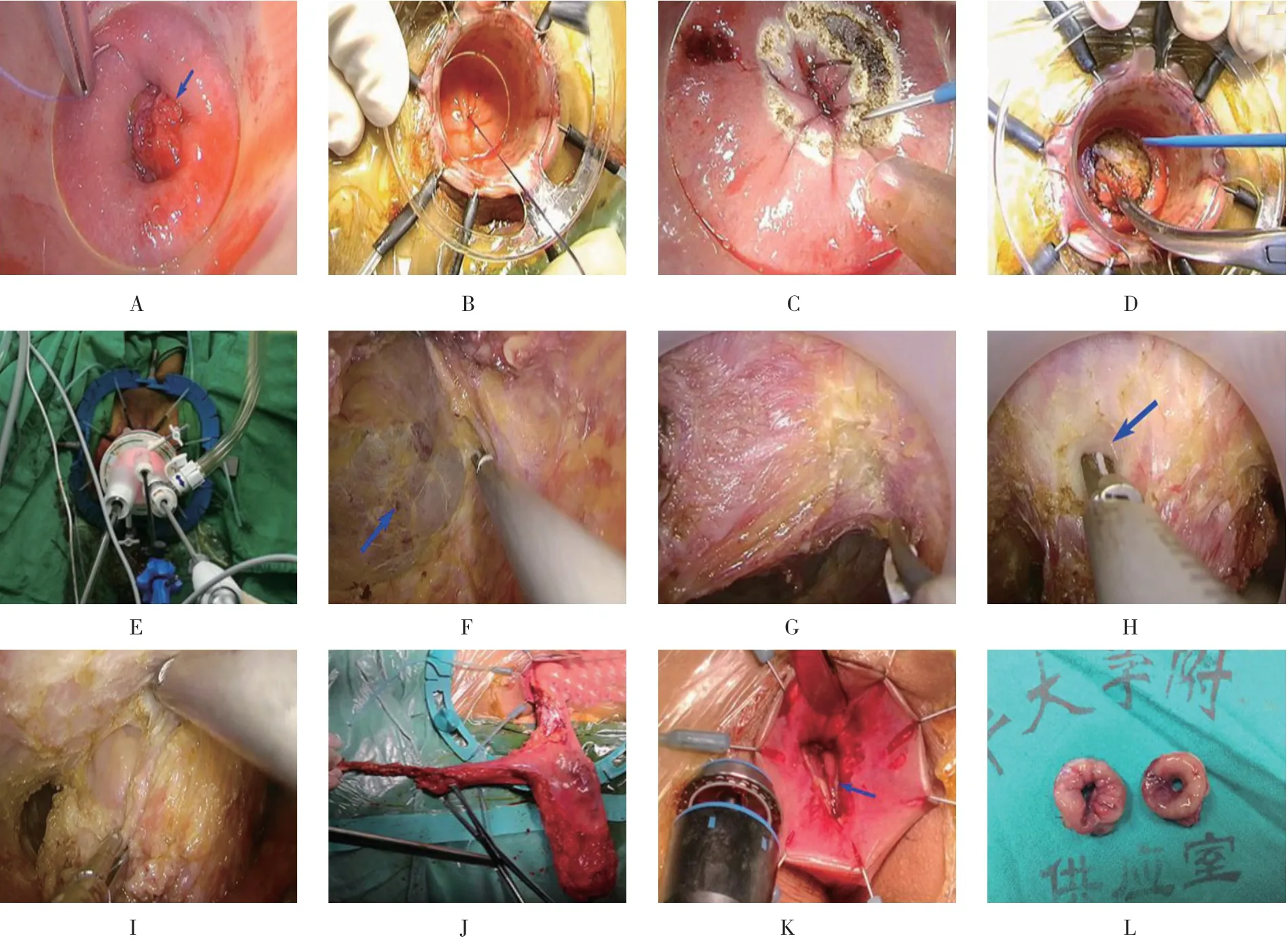
图1 TaTME 手术操作要点Fig.1 Operation points of transanal total mesorectal excision
2 结果
32例患者均顺利完成手术,无中转开腹者;手术时间145 ~480 min,平均(257.50±32.60)min;术中出血量30 ~250 ml,平均(76.56±15.64)ml。经腹经肛操作相继完成者27例,同时进行者5例;高位结扎肠系膜下动脉者24例,低位结扎者8例;进行结肠脾曲松解者7例,未松解者25例;肠道重建中,器械吻合者17例,手工吻合者15例。术后常规留置盆腔引流管和肛管,并行保护性末段回肠造口。术后病理均为腺癌,分化程度与术前活检病理基本一致,部分合并黏液腺癌或印戒细胞癌。标本长度6.80 ~27.20cm,平均(11.25±3.47)cm;远端切缘距离0.50 ~3.50cm,平均(1.85±0.83)cm;淋巴结检出数目10 ~34 个,平均(15.50±4.68)个;TME标本质量优良者(评价为3 级/2 级[19])占96.88%(31/32),环周切缘(circumferential resection margin,CRM)阴性率为96.88%(31/32),远切缘阴性率为100.00%。见图2。术后病理分期(pathological TNM,pTNM),Ⅰ期17例,Ⅱ期11例,Ⅲ期4例[14];11例为患者行术后辅助化疗,其中有1例(TME 标本质量为1 级且CRM 阳性)追加放疗。术后大部分患者恢复良好,排气时间1 ~5 d,平均(1.69±0.54)d;开始进食时间1 ~3 d,平均(1.56±0.45)d;首次下床活动时间1 ~3 d,平均(1.34±0.28)d;引流管拔除时间4 ~32 d,平均(7.63±3.26)d;术后住院时间8 ~21 d,平均(12.87±1.56)d。术后3例出现肛周感染,6例出现吻合口瘘,并发症发生率28.13%,但有盆腔引流管和保护性造口,未造成严重后果,参照Clavien-Dindo 分级[20]均为Ⅰ~Ⅱ级,予以冲洗引流、抗感染和肛门坐浴等对症治疗后基本恢复;无腹部切口感染、腹腔出血、肠梗阻、肺部感染和下肢静脉血栓等并发症,无再次手术及死亡病例。所有患者均获得随访,中位随访时间6 ~18 个月,平均11.5 个月,均未见局部复发及远处转移。18例已行回肠造口还纳,且术后根据低前切除综合征(low anterior resection syndrome,LARS)评分[21]判断,无/轻度LARS 者占66.67%,提示大部分肛门功能尚可,生活质量相对较高。

图2 TME 手术的切口外观和标本质量Fig.2 Incision appearance and specimen quality of transanal total mesorectal excision
3 讨论
3.1 TaTME 的适应证
TaTME 手术一般适用于中低位直肠癌,尤其是低位直肠癌,并且对于“困难骨盆”的直肠癌患者,TaTME 可能更具优势[16]。对于初学者,更应严格把握TaTME 的适应证,筛选合适的病例谨慎开展该术式。对此,笔者的经验是:①肿瘤下缘距肛缘的距离≤7.00cm(通过肛查和MRI 确定),因为大于7.00cm的患者通常经腹操作即可顺利完成,并且此时经肛操作也有一定困难;②肿瘤浸润深度为T3以内(T1和T2最佳),部分T3和T4、N+的患者通过新辅助放化疗获得降期后也适用TaTME,但近齿状线区域并侵犯肛门外括约肌或肛提肌的T4直肠癌除外;③“困难骨盆”患者,传统开腹或腹腔镜TME 手术难度大;④无严重基础疾病,心肺功能储备良好;⑤术前肛门括约肌功能良好。
3.2 TaTME 的术前准备
3.2.1 术者准备 TaTME 手术难度较大,对术者要求较高。初学者必须具备丰富的直肠癌综合诊治经验,以及过硬的腹腔镜操作技术、单孔腹腔镜操作技术和扎实的经肛操作基础,否则不能贸然开展该术式[22]。本中心自2003年起,逐步开展手辅助腹腔镜/腹腔镜辅助/完全腹腔镜/单孔腹腔镜胃肠肿瘤手术,积累了丰富的腹腔镜手术经验;并且在早期直肠癌局部切除术和肛门良性疾病手术的长期实践中,掌握了熟练的经肛操作技巧。在此基础上,通过查阅文献、观看手术视频、前往中山六院进行规范化培训和现场观摩手术以及充分的调研后,笔者于2017年12月顺利开展了第1 台腹腔镜辅助TaTME 术,之后陆续完成了30 余台。
3.2.2 设备准备 除了常规的腹腔镜设备和器械,TaTME 手术还需要一些特殊的设备和器械,例如:恒压气腹机、单孔腹腔镜手术入路装置、扩肛器、窥肛器、圆盘拉钩、小型号的切口保护器等。本中心采用的是施爱德(厦门)医疗器材有限公司的一次性多通道单孔腹腔镜穿刺器和环形牵开器,术野暴露较好。此外,由于本院尚未购置恒压气腹机,故暂时使用的是普通脉冲式气腹机。经肛操作空间狭小,使用脉冲式气腹机容易使术野扑动。所以,笔者对其进行了改良,利用塑料保护套做成缓冲气囊连接气腹机,从而可以产生相对恒压的持续气流,基本消除了术野的扑动,但在消除术野烟雾上仍不及恒压气腹机。因此,建议有条件的医院配置恒压气腹机。
3.3 TaTME 的术式选择
根据是否有腹腔镜的辅助,TaTME 可分为完全TaTME 和腹腔镜辅助TaTME。完全TaTME 虽然在技术上可行且更加符合NOTES 理念,但是技术难度相对较大,学习曲线较长;更为重要的是,完全TaTME由于“先处理肿瘤再离断血管”且无法彻底探查腹腔,有悖于直肠癌根治手术的基本原则,目前在国内开展得越来越少[23]。所以,我国专家就TaTME 的手术入路达成如下共识:在遵循直肠癌根治手术的基本原则以及TME 理念的前提下,基于当前的腹腔镜设备及手术器械,更倾向于腹腔镜辅助TaTME 手术[16]。本中心的实践经验也认为,腹腔镜辅助TaTME 能发挥经腹和经肛入路的各自优势,可相继或同时完成经腹和经肛的手术操作,学习曲线相对更短,更易实施和推广。
3.4 腹腔镜辅助TaTME 的操作要点
3.4.1 操作顺序 腹腔镜辅助TaTME 主要分为经腹操作部分和经肛操作部分。按照直肠癌根治手术的基本原则,一般推荐先经腹操作再经肛操作。但对于部分适合先经肛操作的病例以及一些习惯先经肛操作的术者,也可以考虑先腹腔镜探查,再经肛操作,最后再经腹操作。有条件的医院(具备大的手术间、两套主机及显示屏、两套腔镜设备及操作器械、两个直肠癌腔镜手术团队)建议经腹经肛同时进行[24]。本中心有5 台TaTME 采用了经腹和经肛操作同时实施的手术方式,不仅大大缩短了手术时间(平均148.60 min),又能协同工作,便于寻找TME 的正确解剖层面。
3.4.2 经腹操作 经腹操作部分与常规腹腔镜辅助TME 手术相同,但有三个关键点需要特别注意。①肠系膜下动脉(inferior mesenteric artery,IMA)的离断位置:尽管TME 已然成为直肠癌手术的金标准,但对于肠系膜下动脉的处理仍存在争议,TaTME 也不例外[25-26];通常为了获得足够的肠管长度,习惯从根部进行离断,但对于合并高血压、高血脂、糖尿病和动脉粥样硬化等高危因素的老年患者,笔者建议尽量保留左结肠血管,防止近端肠管缺血,降低吻合口瘘的风险;②系膜的裁剪:为了使肠管顺利拖出肛门,术中应充分游离并裁剪乙状结肠系膜,但由于腔镜下难以准确判断肠管切除的位置,故应暂时保留边缘血管弓,待标本拖出体外并确定上切缘的位置后,再离断边缘血管弓;③脾曲的松解:对于乙状结肠比较短的患者,常需游离结肠脾曲,以保证标本经肛拖出时无张力;松解脾曲后,还能增加近端肠管的切除长度和血运,尤其对于新辅助放疗后的患者,有望减少术后吻合口并发症及相关功能障碍的发生率[27-28]。
3.4.3 经肛操作 经肛操作部分是TaTME 的重点和难点,也是初学者最难跨越的坎,主要分为两个阶段。
起始阶段:包含四个基本手术步骤,即荷包缝合关闭肠腔(缝)、切断肠壁全层(切)、分离肌间隙(分)、放置Port。应根据肿瘤下缘距离肛缘的长度决定这四个步骤的具体顺序,以便进入正确的操作平面。对此,笔者的经验是:①距离<3.00cm 时,建议顺序为直视切→分→缝→Port;②距离为3.00 ~5.00cm时,建议顺序为直视缝→切→分→Port;③距离为5.00 ~7.00cm 时,建议顺序为Port →腔镜缝→切→分。此外,由于直肠下段及肛管的血运极其丰富,切、分和缝均极易出血,会使术野血肉模糊,影响后续操作。所以,确切止血相当重要,可以选择双极电凝或者超声刀,配合使用小纱布压迫止血;助手要灵活使用小S 拉钩,充分暴露术野,配合吸引器持续吸引和生理盐水冲洗,保持术野清晰。能否妥善处理起始阶段将直接关系手术的成败。
游离阶段:此阶段的关键是“神圣平面”的把握,否则难以获得高质量的TME 标本。对此,笔者的经验是按照“后方→侧方→前方→前侧方”的顺序进行游离,即最后分离10 至11 点和1 至2 点处的系膜,可避免损伤该处的血管神经束,保护泌尿生殖功能。
经肛操作部分是TaTME 的精髓所在,如能熟练掌握上述要点,将会大大缩短学习曲线。
3.4.4 经腹经肛的交汇点 经腹操作和经肛操作的交汇点建议选在腹膜返折水平,前方可达精囊腺或阴道后穹隆,然后向侧方、后方游离包抄。如果经腹操作在达到该水平之前手术已经很困难,可以终止腹部手术,转为经肛手术。
3.4.5 消化道重建 消化道重建也是TaTME 的关键步骤,主要有两种吻合方式,应根据残端长度、术者习惯以及经济因素等综合考虑。①器械吻合:对于直肠或肛管残端长度大于3.00cm 的病例,可以使用圆形吻合器完成消化道重建,如吻合有张力,可在腹腔镜下补充游离近端肠管,并在腹腔镜辅助下完成肠管的端端吻合;②手工吻合:当残端长度<3.00cm 时,多难以使用器械吻合,可在直视下完成结肠-直肠或结肠-肛管的手工吻合;手工吻合的要点是先在上下左右四个点用2-0 的薇乔线将残端的肌层与近端肠管的浆肌层固定四针,再用3-0 的倒刺线全层连续缝合两肠管断端,最后再用3-0 的薇乔线间断全层加固。
3.4.6 引流管的留置和保护性造口 行TaTME 的病例绝大部分为中低位直肠癌,通常为低位甚至超低位吻合,并且部分患者术前还行了新辅助放化疗,故吻合口瘘的风险大大增加[29]。另外,经肛操作也可能会增加腹腔感染和肛周感染的风险。故TaTME 术后建议留置盆腔引流管和肛管,开展初期也建议行保护性末段回肠造口[12],待度过学习曲线后(多数需要30例[30],少数只需10 ~15例[24]),则视患者吻合口的安全性以及肛门功能的完好性来决定是否需行保护性末段回肠造口。这些措施的采用一方面可以减少吻合口瘘的发生[31-32];另一方面一旦发生上述并发症,不至于造成严重后果。笔者的经验是:在吻合之前经会阴部或腹部放置引流管至盆底,达到低位引流的效果,并且最好选用双套管,以便于冲洗引流;肛管应外包凡士林纱布,这样可以适当压迫吻合口及肛管的创面,以减少渗血和促进愈合。本中心在开展TaTME 的早中期,先后出现3例肛周感染和6例吻合口瘘,但因有上述保护措施,在予以冲洗引流、抗感染和肛门坐浴等对症治疗后,基本恢复。
3.5 腹腔镜辅助TaTME 的注意事项
“无菌原则”和“无瘤原则”是肿瘤外科手术最基本的原则。TaTME 因其手术部位和操作方式的特殊性,更应严格遵守这两项规范,否则容易造成肛周感染和腹腔感染,并增加肿瘤播散的风险,而无菌技术和无瘤技术的巧妙运用是避免这些并发症发生的重要举措。对此,笔者的经验是:①术前行充分的肠道准备,保证肠腔清洁,必要时可以口服甲硝唑或庆大霉素,抑制肠道细菌生长;②经肛操作时必须再次会阴区消毒,络合碘反复冲洗肠腔,距离肿瘤下缘1.00 ~2.00cm 处行荷包缝合,以关闭肠腔并隔离肿瘤;③在标本拖出离断以及消化道重建时,应经肛置入保护套或小型号的切口保护器来隔离标本,保护切口,并且经常用络合碘和生理盐水反复冲洗术野和清洗肠腔;④倘若肿瘤过大或者直肠系膜过于肥厚难以经肛拖出,不宜强行挤压,可以经预造口处取出。
3.6 腹腔镜辅助TaTME 的安全性及有效性
本中心的临床实践经验表明,对于中低位直肠癌患者,尤其是“困难骨盆”的患者以及保肛欲望强烈的患者,施行腹腔镜辅助TaTME 术是安全可行的,在保证肿瘤根治性切除的前提下能大大提高保肛率,并且本文的随访数据(中位随访时间为11.5 个月)显示近期效果良好。由欧美多个国家开展的国际多中心登记研究结果也表明:TaTME 手术解剖远端直肠系膜是安全有效的,能够获得高质量的TME 手术标本,且手术后的短期效果也是满意的[33]。此外,MARKS 等[34]于2017年6月首次发表了TaTME 手术后直肠癌患者的长期生存数据,该单中心研究纳入了373例直肠癌TaTME 手术病例,TME 手术标本质量评价为“完整”和“接近完整”者占96.0%,CRM 阴性者占94.0%,标本远切缘阴性者占98.6%,患者的5年局部复发率为7.4%,5年总生存率达90.0%,显示出TaTME 手术带来的高质量手术标本和良好的远期效果。
综上所述,TaTME 作为一项新技术,由于理念和术式的不同,必然会存在争议[35]。但不可否认的是,不管从理论上还是从目前的临床实践上来看,TaTME都有着较好的应用前景。尤其对于“困难骨盆”的中低位直肠癌患者,TaTME 是一种安全有效的补充术式,并且在游离腹膜返折以下的直肠系膜时具有独特的优势,从而增加术者的保肛信心。但对于初学者,必须严格掌握TaTME 的适应证,并在做好充分准备的前提下谨慎开展,同时注意细节的把握,以缩短学习曲线。
