遗传性弥漫性白质脑病合并轴索球样变1例报告及文献复习
2020-02-19刘蓥琪张立霞邱志皓王朝霞
刘蓥琪, 张立霞, 邱志皓, 李 静, 王朝霞
1 临床资料
患者,女,29岁。因“右侧肢体麻木6 m,记忆力减退4 m,言语欠清2 m”于2019年2月1日入院。现病史:患者缘于6 m前,无明显诱因及原因出现右足麻木,时有头晕,4 m前出现记忆力减退,伴右侧偏身麻木,2 m前出现言语欠清且记忆力明显下降,无法正常工作。发病以来体重无明显变化,二便正常。患者2015年曾行肺结核手术且有输血史。2018年6月开始接种乙肝疫苗。否认家族中有遗传倾向疾病。神经系统查体:意识清楚,轻度构音障碍,计算力、记忆力下降,右侧肢体浅感觉减退,四肢肌力5-级,右上下肢腱反射(),双侧Babinski征、Chadocki征(+),双侧指鼻试验、快速轮替试验、跟膝胫试验欠稳准。简易精神状态检查(MMSE)评分26/30 分。辅助检查:血常规、血生化、血沉、C-反应蛋白、HIV抗体、梅毒螺旋体抗体、结核杆菌抗体、维生素B12、叶酸等正常或阴性。脑脊液常规、生化正常,脑脊液免疫学、蛋白学监测分析:白蛋白和免疫球蛋白定量结果正常,IgG生成指数正常,未见寡克隆区带。血清及脑脊液AQP4抗体IgG阴性、抗MOG抗体IgG阴性、抗MBP抗体IgG阴性。脑脊液及血清其它免疫组化:抗NMDA-R抗体、抗CASPR2抗体、抗AMPA1-R抗体、抗AMPA2-R抗体、抗LGI1抗体、抗GABAB-R抗体及抗GAD65抗体均阴性。颈椎MRI(2018年11月13日):C5/6颈椎间盘突出。颅脑MR(见图1)显示:双侧放射冠、半卵圆中心、侧脑室周围脑白质及胼胝体可见多发对称性片状略长T1略长T2信号,T2FLAIR呈高信号,DWI为高信号,ADC值无明显减低,脑室池扩大,脑沟裂增宽。DTI显示胼胝体纤维丢失(见图2)。颅脑增强MRI示异常信号未见明显强化。脑电图:异常脑电图(慢波阵发,前部为主)。肌电图检测正常。视觉诱发电位示:双眼全、半(鼻,颞)视野P100波形分化差,重复性差,P100潜伏期延长,波幅正常,提示双侧视觉传导径路异常。诊断和治疗:患者住院期间,结合症状与辅助检查,考虑中枢神经系统脱髓鞘性病变,不除外多发性硬化,予甲泼尼龙抗炎、抑制免疫,维生素B1、B12营养周围神经,患者病情未见明显好转于2019年2月17日自动出院。2019年3月26日患者及其父亲基因检测结果示(见图3、图4):血液样本在CSF1R基因外显子区域存在一处杂合突变:c.2381T>C(胸腺嘧啶>胞嘧啶),导致氨基酸改变p.I794T(异亮氨酸>苏氨酸),家系验证结果显示此杂合突变来自于其父。患者父亲未表现出临床症状。根据患者临床表现、辅助检查,尤其结合基因检测结果,目前诊断为遗传性弥漫性白质脑病合并轴索球样变(Hereditary diffuse leukoencephalopathy with spheroids,HDLS)。出院4 m后电话随访,患者肢体麻木症状减轻,言语欠清加重,记忆力较住院期间无明显改变,近期记忆力减退,远期记忆相对保留,计算力明显减低。现未行特殊治疗。
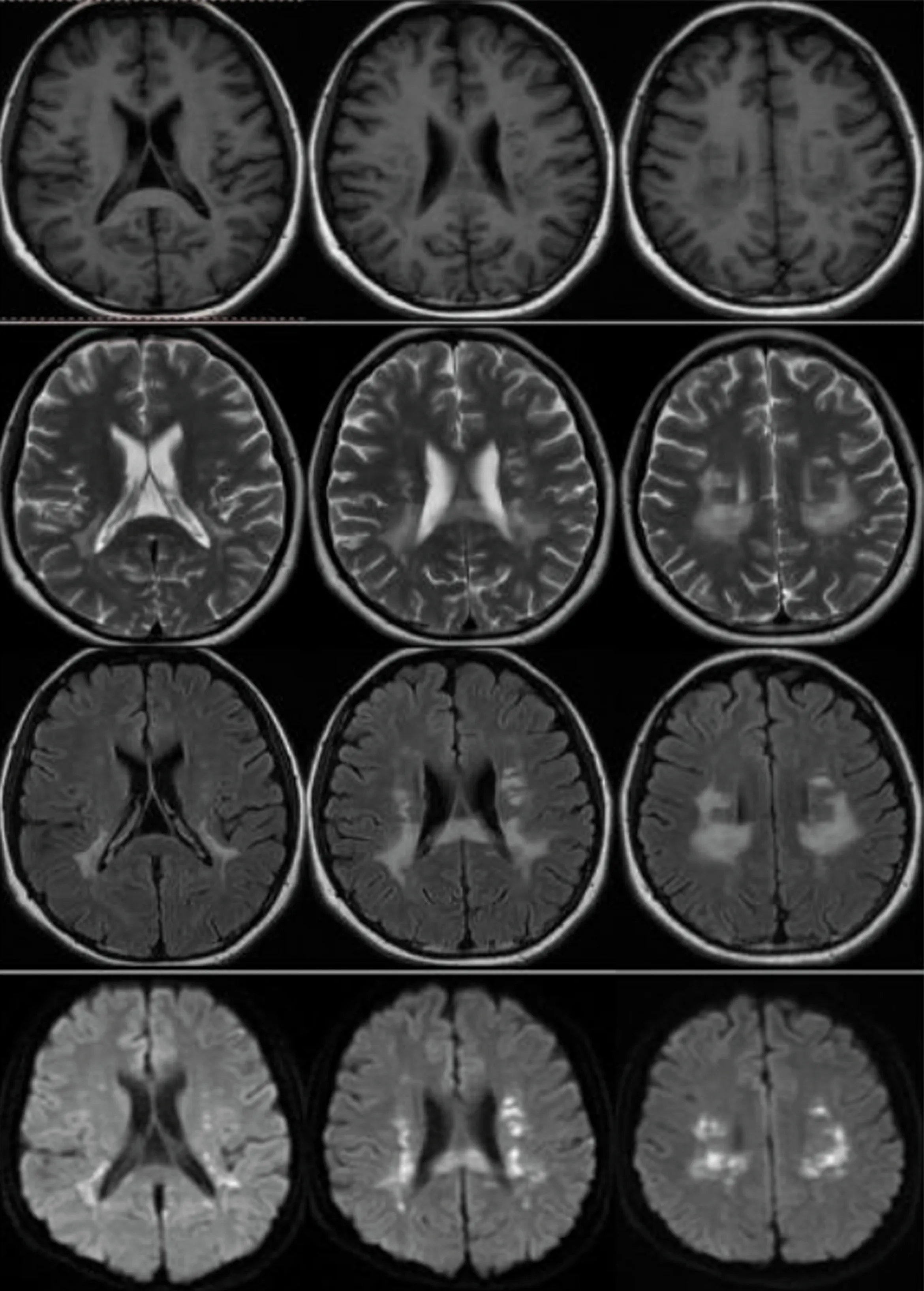
图1 双侧放射冠、半卵圆中心、侧脑室周围脑白质及胼胝体可见多发对称性片状异常信号,T1呈略低信号、T2呈略高信号、FLAIR呈高信号、DWI呈高信号,脑室池扩大,脑沟裂增宽

图2 A:T2示胼胝体膝部、压部高信号;B:弥散张量成像(DTI)示胼胝体压部纤维束缺失
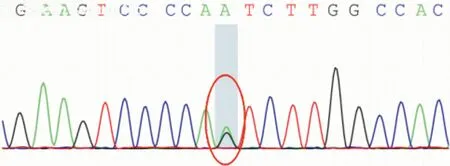
图3 患者(NGQX1900345301-1)chr5:149435843存在c.2381T>C的杂合突变

图4 患者父亲(NGQX1900345301-1)chr5:149435843存在c.2381T>C的杂合突变
2 讨 论
遗传性弥漫性白质脑病合并轴索球样变(Hereditary diffuse leukoencephalopathy with spheroids,HDLS)是一种罕见的遗传性中枢神经系统白质变性病,集落刺激因子1受体(CSF1R)基因是其常见的致病基因,目前已报道70余种致病性CSF1R基因突变类型[1,2]。该病发病年龄15~78岁,平均35~40岁,病程1~30 y[3,4]。其病理特征是广泛的白质脑病伴轴索球样变和脱髓鞘。发病机制可能与小胶质细胞有关,研究显示[5]CSF1R主要调节小胶质细胞密度和分布,小胶质细胞的早期丢失可能参与HDLS发病,因此基因突变可能使小胶质细胞丧失正常的生理功能[1]。
HDLS临床表现多样,主要包括人格改变、认知障碍、精神行为异常、癫痫和帕金森样症状等。相关文献报道HDLS首发症状主要是神经精神症状[6],而本患者首发症状为感觉异常,于晓攀[7]对46例HDLS患者临床症状进行总结,以感觉异常为首发症状的仅有1例。由于个体间的临床症状差异显著,家族史常被忽略,易被误诊或漏诊。
HDLS患者影像学改变,颅脑CT白质病变中可见多发斑点状钙化灶,且钙化主要分布在侧脑室前角附近的额叶白质,具有很高的特异性。磁共振成像的特点是双侧不对称性的前额、额顶叶病变、脑室扩大的中心性萎缩和胼胝体变薄,通常不累及皮质下U型纤维[8],深部灰质、外囊和脑干很少受累[9]。随病情进展,病灶逐渐融合呈片状,并呈对称性分布。典型MRI表现[10]:(1)脑室周围白质病变以额叶、顶叶为主;(2)与年龄不符的侧脑室扩大;(3)胼胝体变薄和异常信号;(4)内囊和大脑脚等投射纤维异常信号;(5)进行性脑沟增宽和皮质萎缩。Konno等[11]发现1例患者在发病5 y前颅脑MR就已出现脑白质和胼胝体的异常变化,表明影像学改变可能先于临床症状。胼胝体变薄常出现在发病后6~36 m,T2加权像和FLAIR像膝部和压部可见高信号[12]。白质病变的异常高信号在DWI序列通常持续数月或更长时间[13]。磁共振波谱显示N-乙酰天冬氨酸和谷氨酸浓度下降,胆碱、乳酸和肌醇浓度升高,无症状CSF1R基因突变携带者中也可观察到胆碱浓度升高,这表明代谢变化在无症状状态就已经发生[14,15]。因此,疾病的早期阶段,mRs可能会成为分析HDLS代谢和病理生理学机制的潜在有用工具。2016年我国首次报道了累及视神经的1例HDLS[16],该患者视神经MRI显示双侧视神经病变,视觉诱发电位(VEP)示双侧P100波幅降低;双眼视野检查可见部分象限缺失。本患者未表现出相关临床症状,未行视神经MRI及视野检查,根据VEP异常,推测可能累及双侧视神经。白艳艳等[17]报道了1个基因诊断的HDLS家系,患者脑电图均为局灶性慢波改变。本患者脑电图示慢波阵发、前部为主,说明前部脑功能下降可能,与影像所示病变部位相符。目前尚未有文献报道本病有特异性脑电图改变。
Konno等[18]在2018年提出了特异性较高的诊断标准,核心特征:(1)发病年龄≤60岁。(2)至少具备以下2种症状与体征:①进行性认知功能障碍或人格改变/行为异常;②锥体束征;③帕金森样症状;④癫痫发作。(3)常染色体显性遗传形式或散发病例。(4)头部CT和(或)MRI显示:①双侧脑白质病变;②胼胝体变薄。(5)排除导致脑白质病变的其他原因,如血管性痴呆、多发性硬化、脑白质营养不良等。支持依据有:(1)临床表现或认知功能评价提示额叶功能障碍;(2)进展迅速,通常在发病后5 y内卧床;(3)颅脑CT显示脑白质内点状钙化灶;(4)符合HDLS的神经病理学改变。排除依据:(1)发病年龄≤10岁;(2)合并显著的周围神经病变;(3)两次以上的中风样发作,癫痫除外。根据以上特征,分为确定的诊断:满足核心特征(2)、(3)及(4)中的①,且存在CSF1R基因突变或HDLS典型神经病理学发现;很可能的诊断:满足核心特征(1)~(5),但未行基因检测及神经病理学检测;可能的诊断:满足核心特征中(2)中的①、(3)和(4)中的①,但未行基因检测及神经病理学检测。
HDLS 鉴别诊断:较多文献提到HDLS需与多发性硬化(MS)鉴别,两者症状具有相似性,但后者脑脊液寡克隆带多为阳性,诱发电位多异常,MRI可见侧脑室周围、半卵圆中心及胼胝体的类圆形病灶。本例患者予激素治疗后无明显好转,且MRI病灶不符合MS的特点,脑脊液各项指标阴性均不支持多发性硬化的诊断。HDLS一般不累及皮质下U形纤维,MS易累及皮质下U形纤维。Sundal等[4]首次在HDLS中发现寡克隆带,因此HDLS可能会被误诊为MS,在诊断MS时有必要检测CSF1R基因以排除HDLS。本病还需与视神经脊髓炎谱系疾病(NMOSD)鉴别,因HDLS也可累及视神经,后者脑脊液细胞数增多,血清AQP4抗体多为阳性,多数患者VEP 异常,颅脑MRI病灶多位于皮质下区、下丘脑、丘脑、三脑室、四脑室周围及大脑脚等。本患者颈椎MRI髓内未见异常颅内病灶不符合NMOSD影像特点,血清AQP4抗体阴性,脑脊液细胞数正常,激素治疗无效,均不支持NMOSD。除此之外,本病还需与遗传性成人型脑白质病如异染性脑白质营养不良、肾上腺脑白质营养不良、伴有皮质下梗死和白质脑病的常染色体显性遗传性脑动脉病(CADASIL)等遗传病鉴别,除特征性影像表现之外,HDLS与上述疾病均可通过基因检测方法以鉴别。
HDLS 的治疗,目前尚无特殊有效治疗方法可以阻止或改变HDLS进展,临床主要对症支持治疗。康复治疗可能有助于患者保持身体机能。一旦病情恶化,重点在于营养管理和防治继发性感染。造血干细胞移植可能对本病有治疗作用[19],有文献报道[20]1例快速进展的成年发病的白质脑病伴轴索球样变和色素胶质细胞(ALSP)患者,在干细胞移植术后病情得到有效控制,6 m其神经功能恶化停止,30 m DWI病灶逐渐消退,但其长期疗效尚待进一步研究。此外,如果小胶质细胞与CSF1R相关白质脑病存在相关性,那么针对小胶质细胞的靶向治疗将是一种理想方法[1]。
