基于处方挖掘与药效团模型的新型冠状病毒RdRp抑制成分筛选
2020-02-02韦缤琪李可馨苏学燕张志锋
李 婧,韦缤琪,李可馨,苏学燕,3,张志锋,3*
1西南民族大学药学院;2四川大学生物治疗国家重点实验室,成都 610041;3四川省羌彝药用资源保护与利用技术工程实验室,成都 610225
2019年12月,一种新型冠状病毒疾病在武汉市暴发,截止到2020年10月21日,全世界已累计有4 000多万人被感染,死亡110万余人,给全世界人民的生命和健康构成巨大威胁,目前已被世界卫生组织(WHO)评估认定为进入全球大流行状态。2020年2月11日,WHO将该疾病命名为新型冠状病毒疾病(COVID-19),是一种由新型冠状病毒(SARS-CoV-2)引起的急性感染性肺炎[1],患者初始症状多为呼吸道症状、发热、咳嗽、气促和呼吸困难等,重症患者可导致肺炎、严重急性呼吸综合征、肾衰竭,甚至死亡[2]。2020 年3 月4 日,国家卫健委发布了《新型冠状病毒肺炎诊疗方案(试行第七版)》[3],治疗主要采用α-干扰素、洛匹那韦/利托那韦、利巴韦林、磷酸氯喹、阿比多尔等抗病毒药物治疗,同时推荐采用连花清瘟胶囊、清肺排毒汤等中药联合治疗。然而,目前针对SARS-CoV-2 感染尚无特效药物,因此,研究针对抗COVID-19 疗效显著的新治疗方法和药物十分迫切。
COVID-19具有强烈的传染性和流行性,以“湿、热、毒、瘀”为主要特征,治疗原则为早治疗、早诊断,重祛邪,防传变[4]。根据《新型冠状病毒肺炎诊疗方案(试行第七版)》推荐中药包括:清肺排毒汤、藿香正气胶囊、金花清感颗粒、连花清瘟胶囊、疏风解毒胶囊、喜炎平注射液以及多种中药复方[3]。在临床实践中,各大医院根据其临床经验及病人的情况采用中西药结合进行个性化治疗,也总结出一系列具有较好临床疗效的中药处方。这些复方的疗效经过了临床检验,在我国抗COVID-19 的过程中发挥了独特的作用,为寻找抗新冠活性成分提供了丰富的物质和理论基础。
SARS-CoV-2是一种RNA病毒,病毒自身编码的RNA依赖性RNA聚合酶(RNA-dependent RNA polymerase,RdRp),在病毒的RNA复制过程中起到关键作用。因此RdRp抑制剂可作为抗RNA 病毒的广谱抗病毒药物[5],目前疗效明确的新冠RdRp抑制剂包括瑞德西韦、利巴韦林及法匹拉韦[6]等。近期“清华大学-上海科技大学抗新冠病毒联合攻关团队”在全世界率先成功解析新型冠状病毒“RdRp-nsp7-nsp8复合物”近原子分辨率的三维空间结构,揭示了该病毒遗传物质转录复制机器核心“引擎”的结构特征,为开发针对新冠肺炎的药物奠定了重要基础。
药效团模型是一种基于配体的药物设计工具,从已知活性化合物的结构出发寻找共有的药效特征信息,从而指导新化合物的理性设计或虚拟筛选[7]。近年来,药效团模型被广泛应用于中药活性成分的筛选[8]。本文收集了目前几种疗效确切的RdRp小分子抑制剂作为训练集,利用HipHop方法建立三维药效团模型。将产生的药效团与常用抗新冠处方药材中活性成分进行匹配,预测“抗新冠候选活性成分”中具有潜在新冠病毒RdRp抑制作用的成分及其与该靶标的结合模式,并且建立一种快速高效的新冠病毒RdRp抑制剂筛查模型,为后续实验研究及临床应用提供参考。
1 材料与方法
1.1 常用中药处方挖掘及药材候选活性成分数据库建立
根据《新型冠状病毒肺炎诊疗方案(试行第七版)》以及全国各地新型冠状病毒处方全面搜集抗新冠中药处方,根据研究报道筛选临床疗效较好的处方作为候选处方。根据对处方中的药材进行搜集及用药频次统计,以高频药材作为重点研究对象,建立候选药材数据库。通过中药系统药理学分析平台数据库(TCMSP)搜集候选药材数据库中每种药材的主要化学成分。以口服生物利用度(oral bioavailability,OB)≥30%,类药性(drug-like,DL)≥0.18为参考评估候选化合物。此外,在CNKI及PubMed数据库中查候选药材相关文献,搜集每种药材主要活性成分,与在TCMSP数据库筛选到的活性物质进行整合及确证,建立“抗新冠候选活性成分数据库”,并在TCMSP数据库及PubChem数据库下载化合物3D结构,确认结构无误后保存。
1.2 药效团的构建及验证
1.2.1 训练集化合物的选取及HipHop药效团模型建立
Discovery Studio 软件中Pharmacophore项下Common Feature Pharmacophore Generation 模块可用于发现一系列配体小分子化合物共有的化学特征,根据这些共同特性结构比对叠合自动生成药效团模型[9]。参照Liu等[10]的药效团构建方法,本研究使用Discovery Studio 2016软件构建基于小分子配体的HipHop药效团模型。根据文献报道选取6个具有RdRp抑制活性的小分子化合物作为训练集[5,6,11,12],训练集化合物结构及RdRp抑制活性(EC50)见图1,其中rbavirin、remdesivir、favipiravir及penciclovir 的EC50值为对SARS-CoV-2抑制活性,Galidesivir的EC50值为对SARS病毒(SARS-CoV)抑制活性,sofosbuvir的EC50值为对丙型肝炎病毒(HCV)的抑制活性。基于训练集中小分子的共同特征结构比对叠合自动生成药效团模型。将训练集中SARS-CoV-2 RdRp抑制活性最高的化合物瑞德西韦(remdesivir,EC50=0.77 μM)Principal值预设为2,作为建立药效团的建模时主要需参考配体的构象,其他5个化合物Principal 值预设为1,作为建立药效团的建模时次要需参考配体的构象。所有化合物MaxOmitFeat 值设为1,表示建模结果可以有一个特征元素与之不匹配。在HipHop模块输入参数时选择氢键受体(hydrogen bond acceptor,A)、氢键供体(hydrogenbond donor,D)、疏水基团(hydrophobic region,H)、正电中心(positive ionizable,PI)、芳环(ringaromatic,R)等5项作为药效团的特征元素,每个药效元素的范围设定为0~5,药效团模型设定为采用Best模式进行叠合,经过运算后得出10个得分最高的药效团模型作为候选模型。
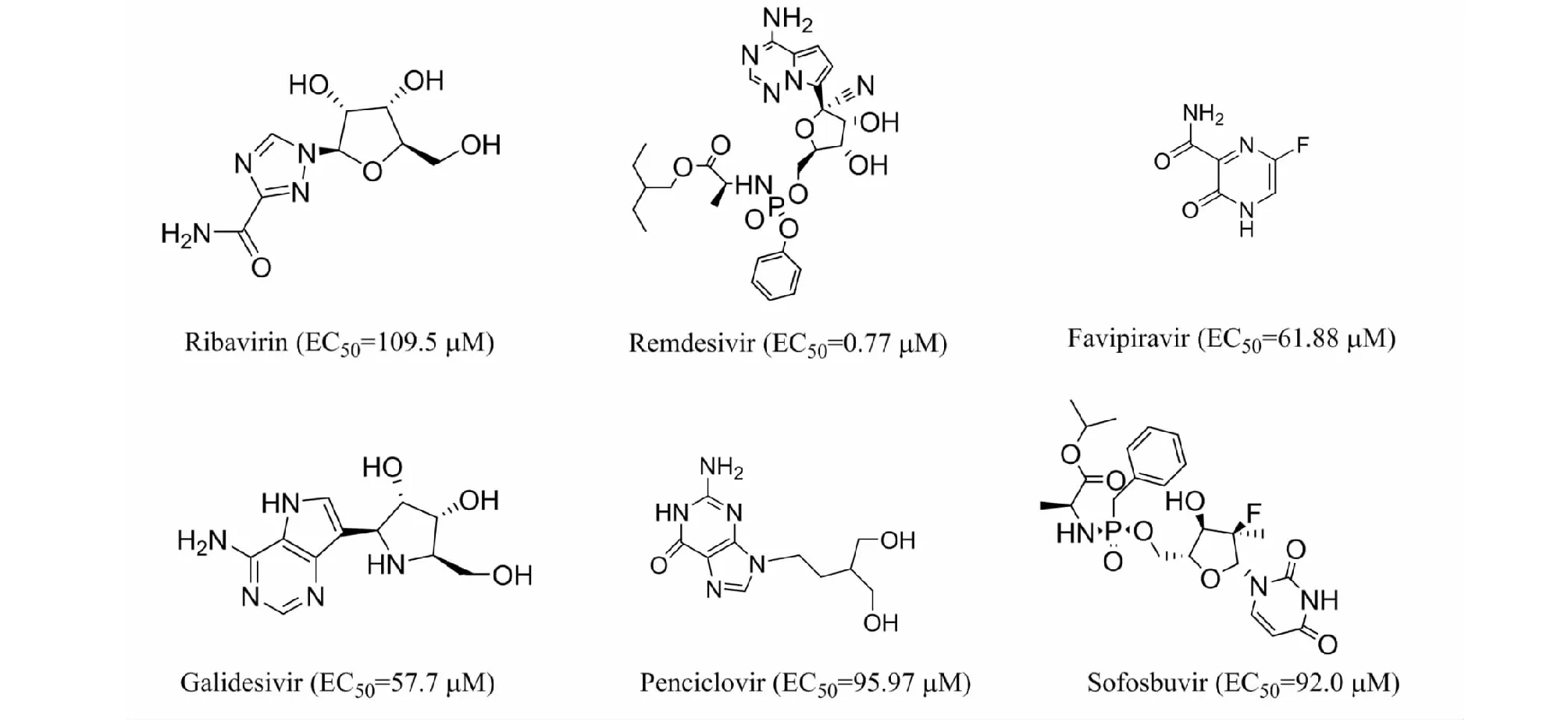
图1 训练集化合物的结构与EC50Fig.1 Chemical structures and EC50 of training set compounds
1.2.2 药效团模型的评价验证
选取具有RdRp抑制活性的6种化合物和30种未见RdRp抑制活性报道的化合物组成测试集。用测试集化合物对药效团模型的性能进行评价,采用Discovery Studio中Pharmacophore 项下的Ligand Profiler 模块,选择Best 模式进行评价,选取在评分值尽可能高的情况下与活性化合物匹配度高及与非活性化合物匹配度较低的药效团作为优选药效团模型。
1.2.3 基于药效团模型SARS-CoV-2 RdRp抑制活性成分虚拟筛选
得到优选药效团后,将“1.1”项中得到的“抗新冠候选活性成分数据库”中活性成分结构与优选药效团采用Discovery Studio进行匹配并分析结果。模式为Best Search,MaxOmitFeat 值设为0,其余为默认参数。选取匹配值(FitValue)较高的化合物作为潜在活性化合物。
1.3 潜在活性化合物的分子对接验证
将“1.2.3”中得到的潜在活性化合物小分子化合物3D坐标文件,在pymol中检查空间结构无误后,利用openbabel转换为pdb格式。将结构文件载入autodocktool 1.5.6程序,添加原子电荷,分配原子类型,所有柔性键均默认可旋转。保存为pdbqt格式,作为对接配体。本研究靶蛋白“SARS-CoV-2病毒RdRp-nsp7-nsp8复合物”蛋白结构由上海科技大学饶子和院士团队提供。采用AutoDock Tools1.5.6 软件删除RdRp蛋白中水分子,分离配体和受体,添加非极性氢,计算Gasteiger电荷,保存为pdbqt文件。根据研究报道的remdesivir与SARS-CoV-2病毒RdRp蛋白结合位点设置RdRp蛋白对接的Gridbox坐标及大小[13]。以SARS-CoV-2病毒RdRp蛋白作为受体,以潜在活性化合物为配体,采用AutoDock Vina进行分子对接,根据对接结果初步评价小分子配体与受体的结合情况。
2 结果与分析
2.1 根据常用中药处方建立“抗新冠候选活性成分数据库”
根据《新型冠状病毒肺炎诊疗方案》及全国各地新型冠状病毒常用处方筛选到31个中药处方作为候选处方。分析处方药材并进行药材使用频数统计,使用频数≥5的药材作为高频使用药材。共搜集到候选药材92种,其中高频使用药材21种,包括甘草、藿香、黄芩、麻黄、石膏、连翘、厚朴、黄芪、杏仁、白术、半夏、金银花、柴胡、苍术、茯苓、陈皮、生姜、草果、葶苈子、栀子及槟榔。以高频使用药材为重点搜集对象,通过TCMSP 数据库以OB≥30%,DL≥0.18为标准筛选得到的候选活性成分与文献收集的主要成分及抗病毒活性成分相整合,共得到1 384个候选成分,建立“抗新冠候选活性成分数据库”。候选活性成分筛选流程图见图2。
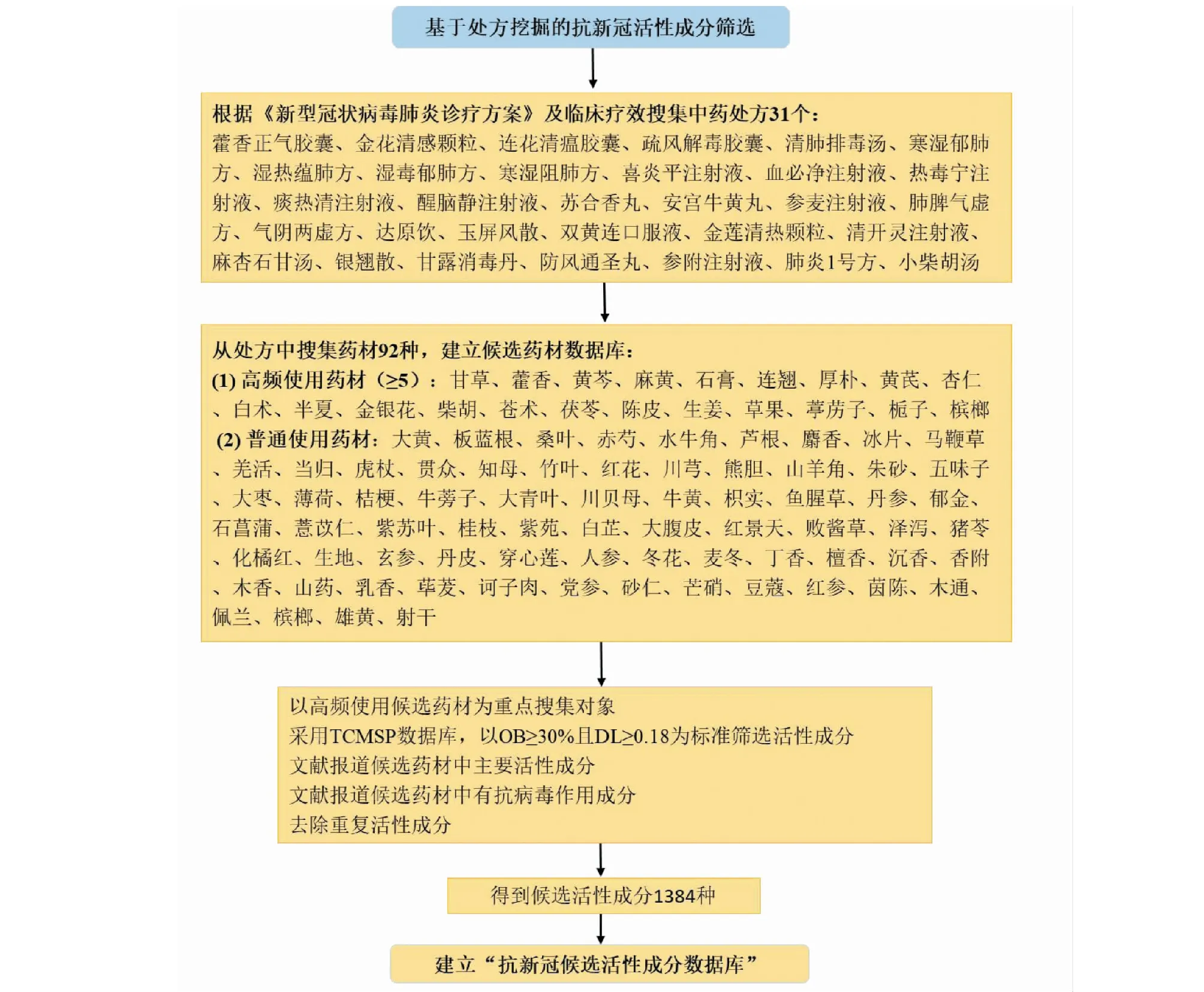
图2 抗新冠候选活性成分筛选流程图Fig.2 Screening flow chart of the candidate active ingredients against COVID-19
2.2 HipHop药效团模型建立及验证
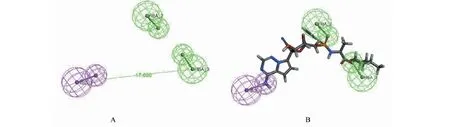
以训练集6个活性化合物采用HipHop方法共产生10个药效团模型,结果参数见表1。评分值参考了训练集分子与药效团模型的匹配度,第01、02、03、07、08、09号药效团药效特征为DAA,第04、05、06、10号药效团药效特征为DDA,6个化合物有5个与所有药效团完全匹配,1个部分匹配。生成的10个药效团评分都超过了40分,说明测试集所选的分子共同特征较为明显,排前几位的药效团评分较为接近,因此结合图3中药效团热图的结果选取最佳药效团,其中冷色调代表对配体响应较低,而暖色调代表药效团对配体响应度较高。由图可见,匹配共命中10个化合物,其中编号1001~1006的5个化合物为活性化合物(1001-ribavirin、1002-remdesivir、1004-galidesivir、1005-penciclovir、1006-sofosbuvir),其他5个化合物为非活性化合物。药效团02对于测试集中活性化合物的响应度较高,而对于非活性化合物的响应值较低,符合本研究对于药效团的要求,结合图3中几种药效团打分情况,02药效团打分(Rank)最高,故选择药效团02作为优选药效团模型进行后续研究。优选药效团模型如图4A,由图可见,优选药效团02主要由1个氢键供体(HBD)和2个氢键受体(HBA)和构成。而整个模型的氢键供体与远端的氢键配体距离为17.698Å,对所匹配的小分子配体的尺寸有一定的限制作用。活性最强的化合物remdesivir与优选药效团的FitValue为3.0,与药效团叠合效果见图4B。
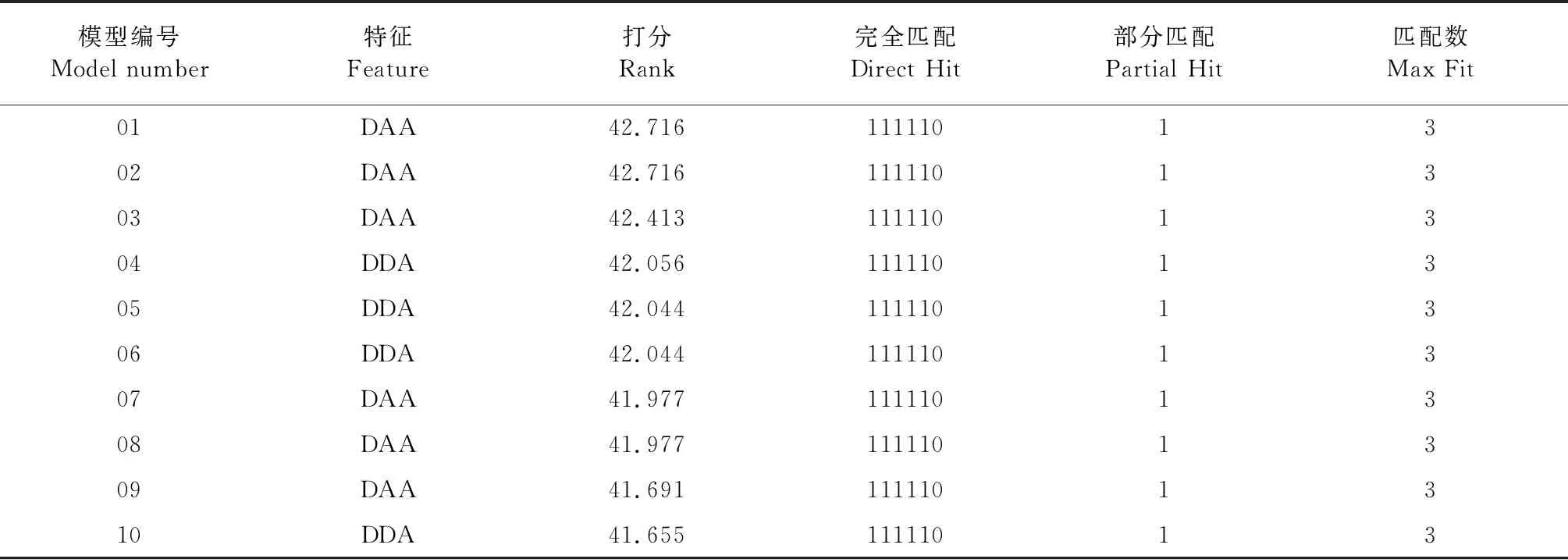
表1 10个基于分子共同特征的药效团的结果参数Table 1 The parameters of ten common features of pharmacophore
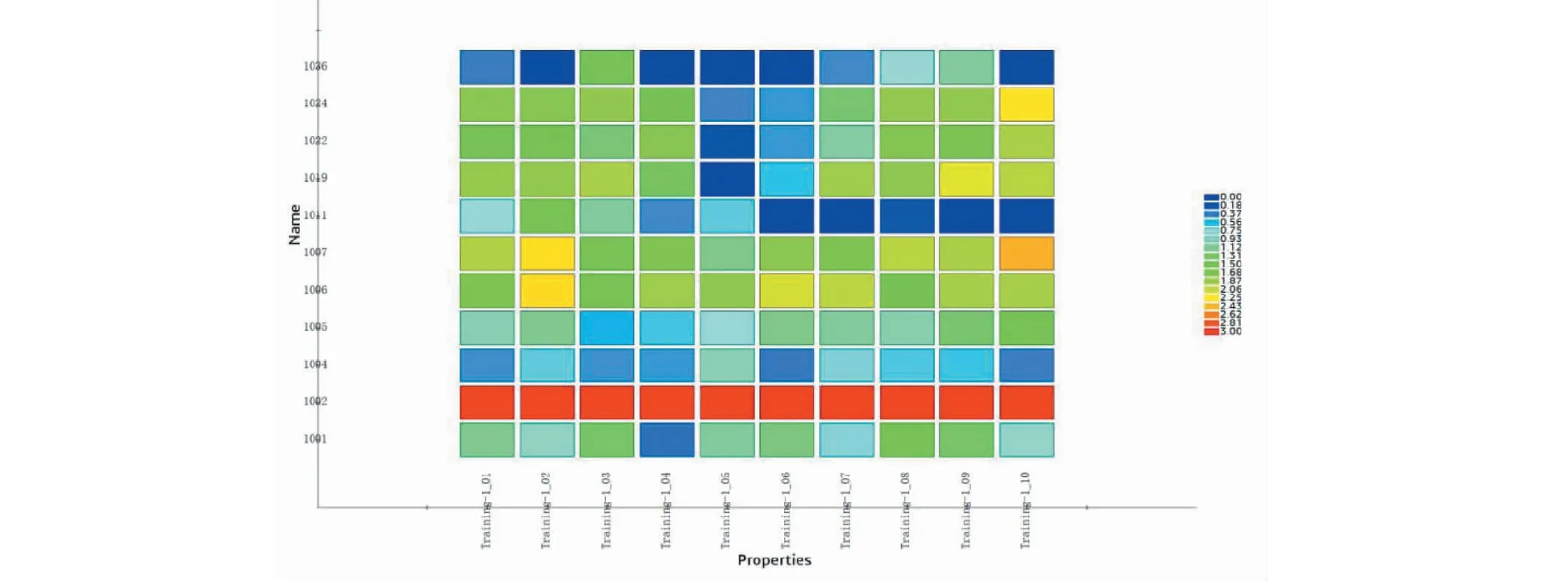
图3 10个生成的药效团对测试集分子的验证热图Fig.3 Heat map of 10 generated pharmacophore models evaluated by test set注:1001-Ribavirin;1002-Remdesivir;1004-Galidesivir;1005-Penciclovir;1006-Sofosbuvir。
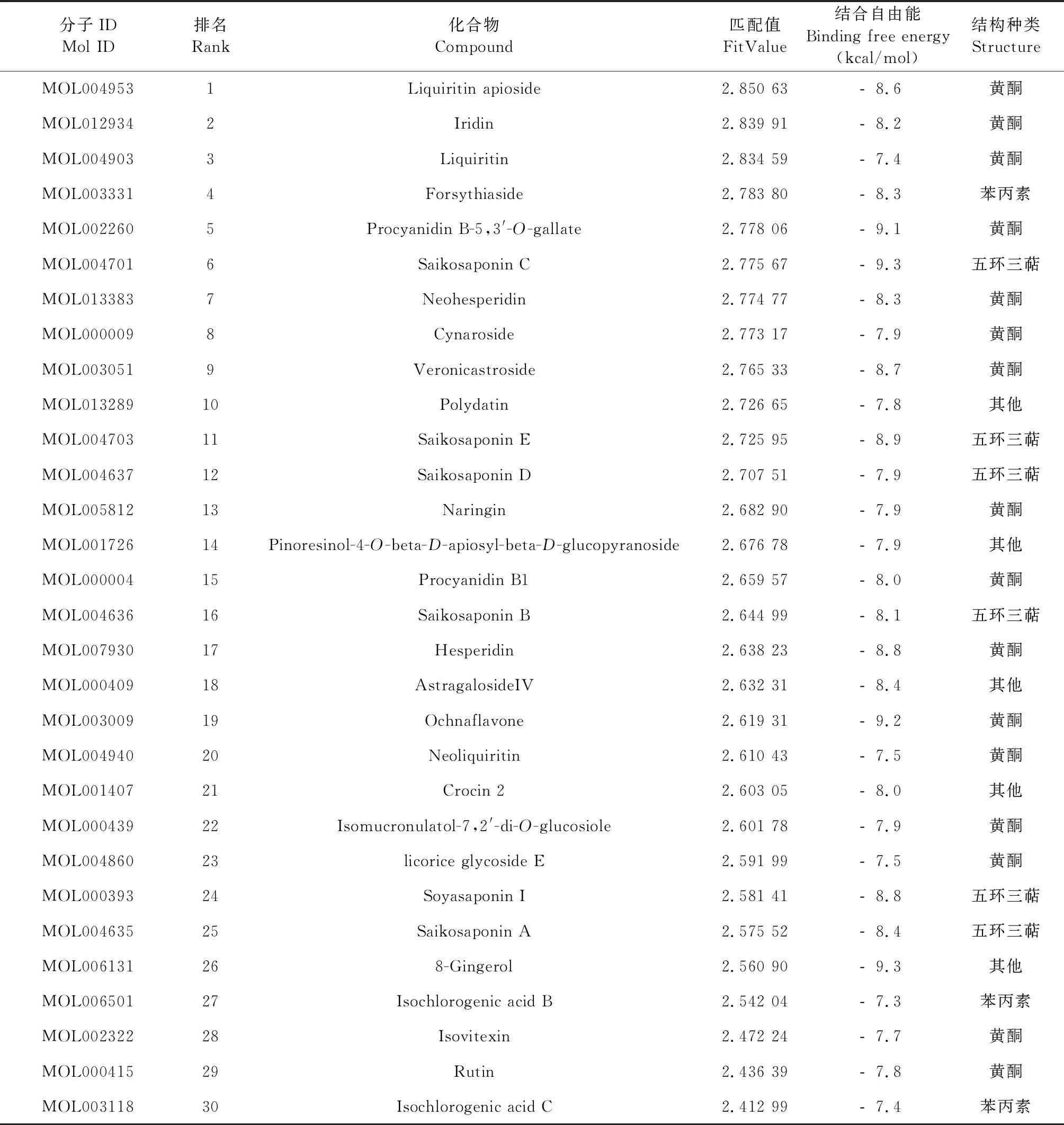
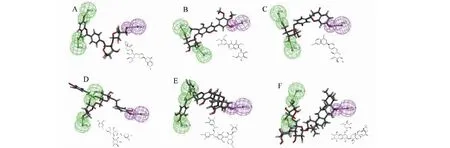
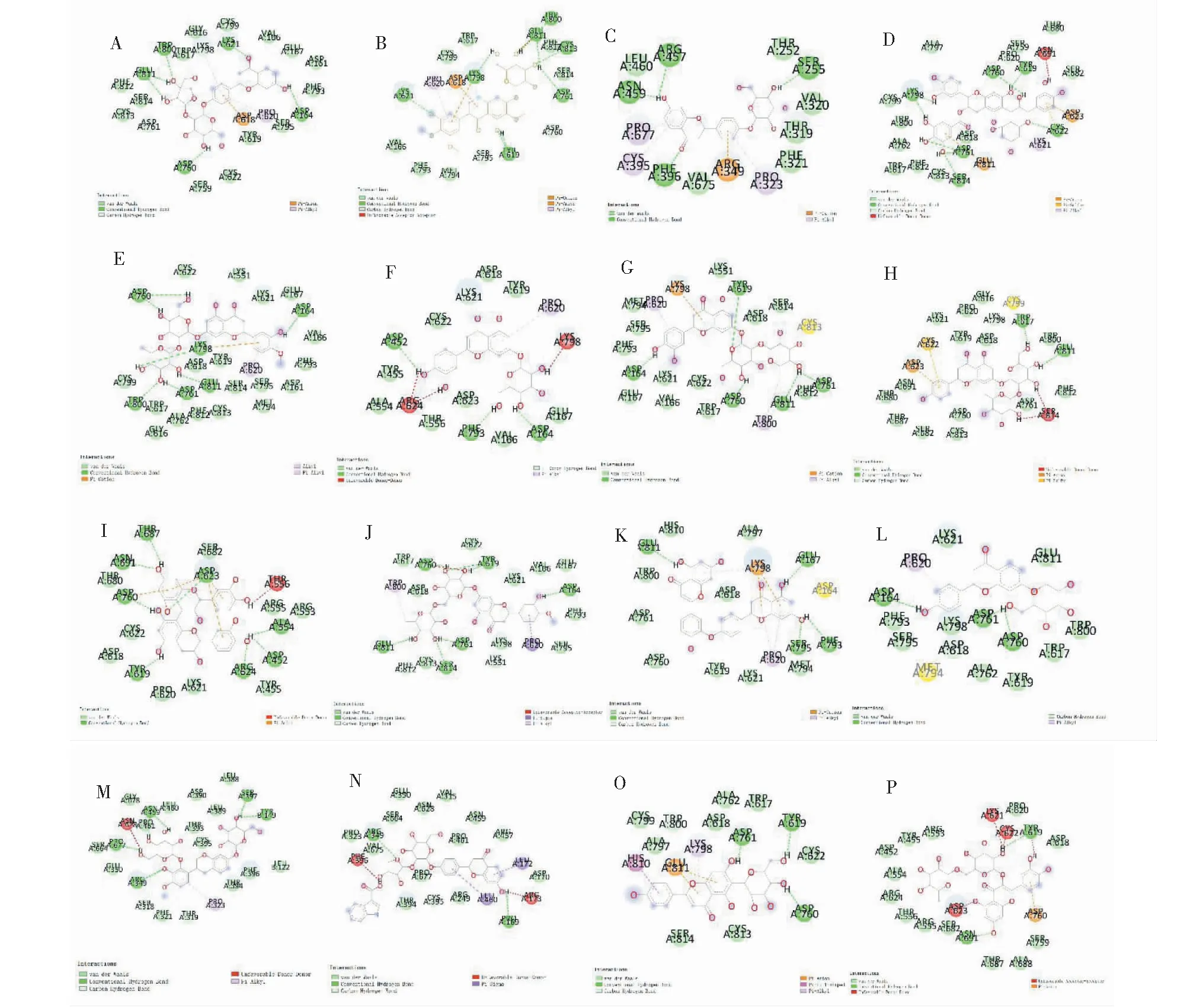
表2 候选活性成分中FitValue排名前30且结合自由能低于remdesivir的主要活性成分信息Table 2 Basic information of the potential active ingredients in candidate active ingredients ranking according to FitValue (top 30) and binding free energy ( 用“2.1”中优选的RdRp抑制剂药效团模型对“1.1”中得到的“抗新冠活性成分数据库”中1 384种成分进行虚拟筛选,命中104个化合物,选取其FitValue排名前30的化合物(FitValue>2.3)作为新型冠状病毒RdRp潜在抑制活性成分进行后续研究,潜在活性化合物信息见表2,表中为FitValue排名前30且与RdRp结合自由能低于remdesivir(<﹣7.2 kcal/mol)的重要潜在活性化合物。药效团匹配到的FitValue最高的6种潜在活性化合物见图5,由图可见,从图中可以看出6种化合物药效团的3个特征元素都能很好地匹配,主要为酚羟基对应氢键供体,羟基或羰基对应氢键受体。 图4 HipHop产生的最优药效团模型(A)及其与remdesivir叠合结果(B)Fig.4 The optimized pharmacophore model (A) and mapping of compound remdesivir on it (B) 图5 药效团02匹配到的候选成分中FitValue最高的6种潜在活性化合物Fig.5 The matching pattern diagram between pharmacophore model 02 and top 6 potential active constituents from candidate ingredients注:A.Liquiritin apioside;B.Iridin;C.Liquiritin;D.Forsythiaside;E.Procyanidin B-5,3′-O-gallate;F.Saikosaponin C。 以“2.2”中得到的“抗新冠候选成分数据库” 中RdRp抑制作用潜在活性成分为配体,以SARS-CoV-2病毒RdRp蛋白为受体,根据研究报道[13]的remdesivir与SARS-CoV-2病毒RdRp蛋白结合位点设置RdRp蛋白对接的Gridbox坐标及大小,配体设置为柔性,受体刚性,采用AutoDock Vina 1.1.2进行分子对接。选取打分最高(affinity数值最低)的构象作为对接构象,利用pymol对对接构象进行可视化分析。每种活性成分对接结果几种结合构象中,选取结合能较低且构象较好的结果作为分子对接结果。分子对接结合自由能越小说明受体配体之间亲和力越大,我们以remdesivir与RdRp的结合自由能(-7.2 kcal/mol)作为参考来判定待测化合物的亲合力。候选成分中RdRp抑制作用潜在活性成分对接结果见表2(结合自由能低于remdesivir)。FitValue最高的6种潜在活性化合物与SARS-CoV-2病毒RdRp蛋白分子对接图如图6。根据研究报道[13],SARS-CoV-2病毒RdRp蛋白与remdesivir结合的活性口袋位于RdRp复合物蛋白中心的空腔,潜在结合位点包括545、555、682、623、687、691、759、760、761等。由图6可见,以上6种化合物能与报道的SARS-CoV-2病毒RdRp蛋白中心活性口袋结合,并与以上关键结合位点中的多个发生了相互作用。图中liquiritin apioside 及iridin均在LYS-621位点产生氢键作用;liquiritin apioside 及pocyanidin B-5,3′-O-gallate均在ASP-760位点产生氢键作用;Iridin及procyanidin B-5,3′-O-gallate均在ASP-761位点产生氢键作用;liquiritin apioside及forsythiaside均在ASP-164位点产生氢键作用;liquiritin apioside及Iridin均在GLU-811及TRP-800位点产生氢键作用;iridin及procyanidin B-5,3′-O-gallate均在LYS-798位点产生氢键作用;iridin、procyanidin B-5,3′-O-gallate及saikosaponin C均在TYR-619位点产生氢键作用。 此外以上多个化合物与PRO-620发生Pi-Alkyl相互作用,与ASP-618发生Pi-Cation相互作用。以上这些位点可能是活性成分与RdRp蛋白作用的潜在位点。 我们将表2中FitValue排名前30且结合自由能低于remdesivir(-7.2 kcal/mol)的化合物进行分类,发现其中53%的化合物骨架类型为黄酮类,主要为黄酮、二氢黄酮、双黄酮、黄酮醇类。提示黄酮类化合物可能具有潜在SARS-CoV-2 RdRp抑制活性。RdRp抑制剂主要有两类,即核苷/核苷酸类似物(NI)和非核苷抑制剂(NNI)。NI能成为RNA依赖的RNA聚合酶的底物,可参入到RNA链中抑制病毒。NNIs与RdRp变构位点之一结合,这种结合改变酶的3D构象,从而在起始步骤破坏聚合酶活性[11,12]。有研究表明,多种黄酮类化合物对HCV病毒的RdRp具有抑制活性[13]。该研究发现黄酮醇、黄酮、二氢黄酮及其苷类对HCV病毒的RdRp具有不同程度的抑制活性,与本研究筛选到的黄酮类化合物结构上具有一定的相似性。 此外,该研究以槲皮素为例进行了多项实验,发现槲皮素能在病毒RNA模板通道的入口处与病毒结合,通过非核苷抑制作用抑制RNA与酶的结合发挥RdRp抑制作用,可能是一种与高泛基因组活性和高抗性屏障有关的新作用机制。该研究也为黄酮类物质的化学改良和大规模基于结构的抗病毒药物分子筛选提供了参考。还有研究表明,黄酮类物质水飞蓟素对HCV病毒RdRp有抑制作用,水飞蓟素可能不是通过阻断HCV细胞系与细胞的结合,而是抑制了病毒假颗粒(pp)的进入,从而抑制了HCVpp与脂质体的融合发挥抑制病毒作用[14]。还有研究表明双黄酮类化合物对登革病毒聚合酶DENV-NS5 RdRp具有抑制作用[15],本研究筛选到procyanidin B1与procyanidin B-5,3′-O-gallate为双黄酮类成分,且与RdRp结合自由能均<﹣8 kcal/mol,提示这两种化合物与RdRp可能具有潜在作用。以上研究为本研究结果提供了相关实验证据,然而黄酮类化合对于SARS-CoV-2 RdRp是否有抑制作用尚需后期实验证实。 从对接的结果可以看出,由于黄酮类结构含有多个富电子的氧原子,易于与RdRp 靶点残基中的供电子基团形成氢键,故黄酮类结构作为潜在的抗RdRp活性化合物的骨架是合理的。我们把FitValue排名靠前且结合自由能低于remdesivir的30个黄酮类化合物作为重要黄酮类活性成分进行分析,与RdRp蛋白残基互作图见图7。在黄酮活性化合物中,氢键多在黄酮骨架上A 环的C-7位(liquiritin apioside、liquiritin、procyanidin B-5,3′-O-gallate、rutin、isovitexin、ochnaflavone、Procyanidin B1及licorice glycoside E)及C环的C-3位(iridin、procyanidin B-5,3′-O-gallate、hesperidin、neohesperidin、procyanidin B1、ochnaflavone及isomucronulatol-7,2′-di-O-glucosiole)或C-4位(cynaroside、veronicastroside、neoliquiritin 及procyanidin B1)上产生,由此推测上述位置的取代基可能对化合物的活性有一定影响。 图7 潜在活性成分中重要黄酮类成分与RdRp蛋白残基互作图Fig.7 Interaction of protein residues between RdRp and the important flavonoids in potential active ingredient注:A.Liquiritin apioside;B.Iridin;C.Liquiritin;D.Procyanidin B-5,3′-O-gallate;E.Neohesperidin;F.Cynaroside;G.Veronicastroside;H.Naringin;I.Procyanidin B1;J.Hesperidin;K.Ochnaflavone;L.Neoliquiritin;M.Isomucronulatol-7,2′-di-O-glucosiole;N.Licorice glycoside E;O.Isovitexin,P. Rutin。 COVID-19属于“瘟疫”范畴,以“湿、热、毒、瘀”为主要特征,并与运气、地理、气候和人群的易感性相关,其病位在膜原,涉及三焦、肺、脾、胃,采用清热除湿解表药在新冠肺炎的防治中有重要的作用[16]。本研究对于临床常用的31个抗新冠常用中药处方的组成药物进行频次统计,其中使用频次≥5 的有21味中药(图1)。使用频次较高的药材大致归纳为:补气健脾药、清热药、解表药、祛湿药。补气健脾药(黄芪、甘草、白术、厚朴、杏仁);清热药(金银花、甘草、连翘、麻黄、黄芩、石膏、葶苈子、栀子);解表药(金银花、连翘、藿香、麻黄、柴胡、生姜);祛湿药(白术、藿香、陈皮、苍术、黄芩、茯苓、厚朴、半夏、草果、槟榔)等。 SARS-CoV-2 属于β属的新型冠状病毒,SARS-CoV-2可通过刺突糖蛋白(S蛋白)的S1亚基上的受体结合域(RBD)与宿主细胞表面的血管紧张素转化酶2(ACE2)之间的结合,通过内吞作用进入宿主细胞[17]。SARS-CoV-2病毒进入细胞后,核衣壳与病毒自身的正义链RNA释放到细胞质中,由木瓜蛋白酶样蛋白酶(PLpro)和主蛋白酶(3CLpro)参与裂解,最终产生包括螺旋酶(Helicase)和RNA 依赖性RNA 聚合酶(RdRp)在内的非结构蛋白,参与病毒转录、复制过程[18]。病毒自身编码的RNA依赖性RNA聚合酶(RdRp)在SARS-CoV-2病毒的RNA复制过程中起到关键作用,RdRp也是目前针对SARS-CoV-2作用明确且研究较多的靶点。本研究探索从常用抗新冠中药材中寻找RdRp抑制剂,也为更好的阐明中药抗新冠作用机制提供参考。本研究根据TCMSP数据库及文献挖掘搜集了常用抗新冠药材中1384种候选活性成分,根据已报道的具有RdRp抑制活性的6种化合物构建了药效团模型并进行了验证,选取最优药效团模型与“抗新冠候选活性成分”进行了虚拟筛选,在匹配得到的化合物中选取FitValue较高的化合物作为潜在RdRp抑制活性成分,本研究发现lquiritin apioside、iridin、liquiritin、forsythiaside、procyanidin B-5,3′-O-gallate、saikosaponin C等成分具有较高的FitValue,可作为RdRp抑制的潜在活性成分。通过分类分析发现筛选产物中有较多黄酮类成分,与文献报道的黄酮类化合物抑制病毒RdRp作用有一定相似性,提示黄酮骨架可能具有抑制SARS-CoV-2 RdRp的活性。我们还筛选到一些五环三萜类成分,主要是saikosaponin,有研究报道saikosaponins A、C、B、D具有抗流感、HBV、HCV等病毒活性[19-21]。研究还发现一些有苯丙素类具有RdRp潜在抑制活性,主要包括forsythiaside(连翘苷)及绿原酸类似物,有研究报道连翘苷A可通过抑制病毒复制控制甲型流感病毒感染[22];连翘苷A还可通过影响小鼠肺免疫细胞中RLRs信号通路,减轻流感病毒FM1株在小鼠肺中引起的炎症反应[23]。Isochlorogenic acid A及chlorogenic acid具有抗流感病毒、HBV等病毒活性[24,25]。然而五环三萜及苯丙素类成分是否对病毒RdRp具有抑制活性尚未见报道,需进一步试验研究证实。本研究采用remdesivir作为重要模板进行活性基团模型构建,有研究报道remdesivir三磷酸化后的形式为其活性形式[13],但考虑到remdesivir三磷酸化物的不稳定性,因此研究采用了remdesivir原型作为药效团模型。 综上,本研究通过对抗新冠常用中药处方挖掘及数据库搜集,建立了“抗新候选活性成分数据库”,基于已报道的具有RdRp抑制活性的化合物构建了HipHop药效团模型并对候选成分进行匹配,对FitValue排名并进行分子对接验证,选取FitValue较高且结合自由低于对照药物remdesivir的前30种化合物进行分析,得到具有RdRp潜在抑制活性的化合物及活性结构。本研究结果为抗SARS-CoV-2活性成分筛选提供了新思路及参考。2.3 优选药效团对“抗新冠活性成分数据库”中SARS-CoV-2 RdRp潜在抑制成分的虚拟筛选
2.4 RdRp抑制作用潜在活性成分分子对接验证
2.5 基于筛选结果的潜在活性结构分析
3 讨论
