不同剂量重组人脑利钠肽对行经皮冠状动脉介入治疗的急性心肌梗死患者影响的对比研究
2020-01-17曾宪国罗亮宋景春
曾宪国,罗亮,宋景春
急性心肌梗死(AMI)指在冠状动脉粥样硬化不稳定斑块病变基础上继发斑块破裂、血栓形成导致冠状动脉血管完全阻塞而引起的大量心肌细胞坏死、凋亡,可引发心功能不全、神经内分泌紊乱、心肌细胞重塑和心力衰竭等[1]。经皮冠状动脉介入治疗(PCI)是挽救缺血心肌、保护心功能的有效方法,可有效降低AMI 患者病死率,但PCI 后部分AMI 患者心力衰竭可能依然持续。重组人脑利钠肽(rhBNP)与心室肌细胞分泌的内源性肽—脑钠肽(BNP)具有相同的氨基酸序列和调节机制。研究表明,rhBNP 可促进心力衰竭患者血管扩张、利尿、排钠,降低心脏前负荷,纠正血流动力学紊乱,同时可通过抑制肾素-血管紧张素-醛固酮系统(RAAS)和刺激交感神经系统而改善心功能,进而缓解心力衰竭[2]。因此,目前rhBNP 已被广泛应用于AMI 患者的围术期。目前,临床报道的rhBNP 治疗AMI 的最佳剂量尚不统一:PAN 等[3]采用低剂量rhBNP(0.005 μg·kg-1·min-1静脉泵注)、XIONG等[4]采用标准剂量rhBNP(2.0 μg/kg 静脉注射,继而以0.01 μg·kg-1·min-1的速率静脉泵注)、CHENG 等[5]采用较大剂量rhBNP(1.5 μg/kg 静脉内注射,继而以0.007 5 μg·kg-1·min-1的速率静脉泵注)治疗AMI 患者,结果均证实rhBNP治疗AMI 患者的临床效果较好。本研究旨在比较不同剂量rhBNP 对行PCI 的AMI 患者的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2015 年1 月—2018 年1 月中国人民解放军第九四医院和中山大学附属第七医院收治的AMI 患者216 例,均符合《中国心力衰竭诊断和治疗指南(2018)》[6]中的AMI 诊断标准。纳入标准:(1)年龄18~75 岁;(2)具备PCI 指征[6];(3)发病24 h 内行PCI;(4)PCI 后1 h血流动力学稳定且冠状动脉血运重建成功。排除标准:(1)合并肺部炎症、肺栓塞、慢性阻塞性肺疾病者;(2)收缩压<90 mm Hg(1 mm Hg=0.133 kPa)或出现心源性休克者;(3)既往心电图检查结果提示陈旧性心肌梗死、慢性心力衰竭、肥厚性心肌病、左房室瓣返流或先天性心脏病者;(4)合并急慢性肾脏疾病(尿量<30 ml/h)者;(5)合并恶性肿瘤或精神障碍者。采用随机数字表法将所有患者分为对照组(n=54)、A 组(n=54)、B 组(n=54)、C 组(n=54)。四组患者年龄、性别、体质指数(BMI)、Killip 分级、心血管风险因素、梗死血管比较,差异无统计学意义(P>0.05,见表1),具有可比性。本研究经中国人民解放军第九四医院医学伦理委员会审核批准,所有患者或家属签署知情同意书。
1.2 方法 所有患者入院后完善心电图、心脏彩超、胸部X线、呼吸功能、生化常规、血常规等常规检查,并给予吸氧、控制水盐摄入、控制感染及使用利尿剂、血管紧张素转化酶抑制剂、血管紧张素Ⅱ受体拮抗剂、β-受体阻滞剂、醛固酮拮抗剂等治疗,同时密切观察所有患者生命体征。
所有患者于发病24 h 内行PCI,PCI 前2 h 口服氯吡格雷〔赛诺菲安万特(杭州)制药有限公司生产,国药准字H20056410〕75 mg/kg 和阿司匹林(宁夏金太阳药业有限公司生产,国药准字H64020045)300 mg/kg。在此基础上,对照组患者于PCI 前2 h 给予硝酸甘油(广州白云山明兴制药有限公司生产,国药准字H44020569)静脉滴注,初始剂量为5 μg·kg-1·min-1,10 min 后 增 加 至10 μg·kg-1·min-1;A 组患者于PCI 前2 h 给予小剂量rhBNP(成都诺迪康生物制药有限公司生产,国药准字S20050033),即rhBNP 0.005 μg·kg-1·min-1静脉泵注72 h;B 组患者于PCI 前2 h 给予中等剂量rhBNP,即rhBNP 1.5 μg/kg 负荷剂量于1~3 min 内静脉注射,继而以0.007 5 μg·kg-1·min-1的速率静脉泵注72 h;C 组患者于PCI 前2 h 给予较大剂量rhBNP,rhBNP 2.0 μg/kg 负荷剂量于1~3 min 内静脉注射,继而以0.01 μg·kg-1·min-1的速率静脉泵注72 h。治疗过程中发生肺水肿、低血压、心力衰竭加重、严重过敏反应、休克等严重不良反应者需立即给予相应治疗,必要时退出本研究。
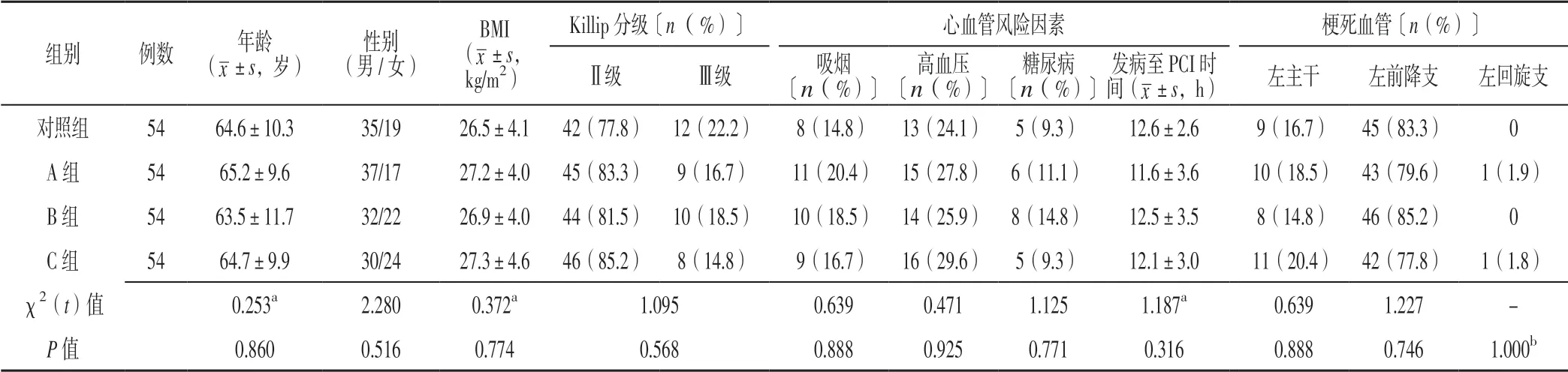
表1 四组患者一般资料比较Table 1 Comparison of general information in the four groups
1.3 观察指标
1.3.1 生命体征 比较四组患者给药时及给药后0.5、1、3、6、12、24、48、72 h 生命体征,包括心率、收缩压(SBP)、舒张压(DBP)。
1.3.2 心功能指标 采用超声心动图观察四组患者给药时及给药后24、48、72 h 心功能指标,包括左心室射血分数(LVEF)、左心室舒张末期内径(LVEDD)、左心室舒张末期容积(LVEDV)、左心室收缩末期容积(LVESV)、每分钟搏出量(SV)。
1.3.3 心肌损伤标志物 给药后72 h 抽取四组患者空腹肘静 脉 血5 ml,室 温 下3 500 r/min 离 心15 min(离 心 半 径5 cm),留取上层血清并置于-20 ℃冰箱中保存待测;采用酶联免疫吸附试验(ELISA)检测肌酸激酶(CK)、肌酸激酶同工酶(CK-MB)、心肌肌钙蛋白I(cTnI),试剂盒均购自北京杰辉博高生物技术有限公司。
1.3.4 肾功能指标 分别于治疗后24、48、72 h 抽取四组患者空腹肘静脉血5 ml,室温下3 500 r/min 离心 15 min(离心半径5 cm),留取上层血清并置于-20 ℃冰箱中保存待测;采用ELISA 检测血肌酐(Scr)、血尿素(Sur)、β2-微球蛋白(β2-MG)、胱抑素C(Cys C),试剂盒均购自北京杰辉博高生物技术有限公司。
1.3.5 不良反应 观察四组患者治疗期间不良反应发生情况。
1.4 统计学方法 采用SPSS 21.0 统计学软件对数据进行分析,计量资料以(x± s)表示,组间比较采用单因素方差分析,两两比较采用SNK-q 检验,重复测量资料采用双因素重复测量方差分析;计数资料分析采用χ2检验或Fisher's 确切概率法。以P<0.05 为差异有统计学意义。
2 结果
2.1 生命体征 时间与方法在SBP、DBP 上存在交互作用(P<0.05),在心率上无交互作用(P>0.05);时间、方法在SBP、DBP 上主效应显著(P<0.05),在心率上主效应不显著(P<0.05)。A 组、B 组、C 组患者给药后1、3、6 h SBP 低于对照组,B 组、C 组患者给药后12、24、48、72 h SBP 低于对照组,B、C 组患者给药后1、3、6、12、24、48 h SBP 低于A 组,C 组患者给药后72 h SBP 低于A 组且给药后1、3、6、12、72 h SBP低于B组,差异有统计学意义(P<0.05)。A 组、B 组、C 组患者给药后1 h DBP 低于对照组,B 组、C 组患者给药后3、6、12 h DBP 低于对照组且给药后3、6 h DBP 低于A 组,B 组患者给药后24 h DBP 低于对照组,C 组患者给药后24、48、72 h DBP 低于对照组、A 组、B 组,差异有统计学意义(P<0.05,见表2)。
2.2 心功能指标 时间与方法在LVEF、LVEDD、LVEDV、LVESV、SV 上存在交互作用(P<0.05),时间、方法在LVEF、LVEDD、LVEDV、LVESV、SV 上主效应显著(P<0.05)。B 组、C 组患者给药后24 h LVEDD 短于对照组、A 组,C 组患者LVEDD 短于B 组,差异有统计学意义(P<0.05);A 组患者给药后48 h LVEDV、LVESV 小于对照组,差异有统计学意义(P<0.05);B 组、C 组患者给药后48 h LVEF 高于对照组,LVEDD 短于对照组、A 组,LVEDV 小于对照组、A 组,LVESV 小于对照组,差异有统计学意义(P<0.05);C 组患者 给 药 后48 h LVEF 高 于A 组,LVEDD 短 于B 组,LVEDV小于B 组,LVESV 小于A 组、B 组,SV 大于对照组、A 组、B 组,差异有统计学意义(P<0.05);给药后72 h,A 组、B 组、C 组患者LVEF 高于对照组,LVEDD 短于对照组,LVEDV 小于对照组,B 组、C 组患者LVEDD 短于A 组,LVEDV 小于A 组,LVESV 小于对照组、A 组,SV 大于对照组、A 组,C 组患者LVEF 高于A 组、B 组,LVEDV、LVESV 小于B 组,差异有统计学意义(P<0.05,见表3)。
表2 四组患者不同时间点心率、血压比较(±s)Table 2 Comparison of heart rate and blood pressure in the four groups at different time points

表2 四组患者不同时间点心率、血压比较(±s)Table 2 Comparison of heart rate and blood pressure in the four groups at different time points
注:SBP=收缩压,DBP=舒张压;与对照组比较,aP<0.05;与A 组比较,bP<0.05;与B 组比较,cP<0.05
组别 例数 心率(次/min)给药时 给药后0.5 h 给药后1 h 给药后3 h 给药后6 h 给药后12 h 给药后24 h 给药后48 h 给药后72 h对照组 54 66.3±6.5 67.8±6.1 68.6±6.0 68.2±5.8 69.1±5.9 67.9±6.1 68.1±5.9 68.1±5.3 67.5±5.4 A 组 54 65.2±5.6 66.7±6.1 68.4±6.1 67.9±5.8 69.7±6.2 69.2±6.2 67.6±5.8 68.4±5.5 66.4±5.3 B 组 54 65.8±6.4 66.2±5.7 66.8±5.9 67.1±6.0 68.1±5.8 66.5±5.7 66.7±5.5 67.6±5.0 67.5±6.0 C 组 54 66.9±6.1 67.5±5.9 67.2±5.9 66.9±6.1 70.3±5.9 68.4±6.1 68.4±5.8 68.2±5.1 68.1±5.9 F 值 F时间=2.658,F组间=3.484,F交互=2.514 P 值 P时间=0.684,P组间=0.258,P交互=0.617组别 SBP(mm Hg)给药时 给药后0.5 h 给药后1 h 给药后3 h 给药后6 h 给药后12 h 给药后24 h 给药后48 h 给药后72 h对照组 130±22 127±14 125±11 125±11 119±11 118±12 122±11 122±12 120±12 A 组 129±21 125±15 120±10a 120±10a 113±10a 115±10 118±10 120±11 119±11 B 组 130±22 122±12 112±11ab 110±12ab 111±10ab 108±13ab 109±11ab 111±10ab 111±10a C 组 129±22 123±13 109±10abc 103±11abc 105±9abc 103±12abc 106±11ab 109±10ab 107±10abc F 值 F时间=98.658,F组间=136.58,F交互=171.25 P 值 P时间<0.01,P组间<0.01,P交互<0.01组别 DBP(mm Hg)给药时 给药后0.5 h 给药后1 h 给药后3 h 给药后6 h 给药后12 h 给药后24 h 给药后48 h 给药后72 h对照组 88±18 80±10 82±11 80±11 80±9 76±11 76±11 73±10 75±7 A 组 86±18 80±12 78±10a 77±9 76±9 73±11 73±10 74±9 73±8 B 组 82±18 80±13 74±10a 70±11ab 71±10ab 70±11a 72±9a 71±8 72±9 C 组 84±18 79±10 71±10a 71±10ab 71±9ab 70±11a 68±10abc 68±8abc 69±7abc F 值 F时间=146.365,F组间=168.241,F交互=123.28 P 值 P时间<0.01,P组间<0.01,P交互<0.01
2.3 心肌损伤标志物 四组患者给药后72 h CK、CK-MB、cTnI 比较,差异有统计学意义(P<0.05);A 组、B 组、C 组患者CK、CK-MB、cTnI 低于对照组,B 组、C 组患者CKMB、cTnI 低于A 组,C 组患者CK-MB 低于B 组,差异有统计学意义(P<0.05,见表4)。
2.4 肾功能指标 时间与方法在Scr、Sur 上存在交互作用(P<0.05),在β2-MG、Cys C 上不存在交互作用(P>0.05);时间、方法在Scr、Sur 上主效应显著(P<0.05),在β2-MG、Cys C 上主效应不显著(P>0.05)。给药后24 h A 组、B组、C 组患者Scr、Sur 高于对照组,B 组、C 组患者Scr、Sur高于A 组,C 组患者Scr、Sur 高于B 组,差异有统计学意义(P<0.05);给药后48 h B 组、C 组患者Scr、Sur 高于对照组、A 组,C 组患者Scr、Sur 高于B 组,A 组患者Sur 高于对照组,差异有统计学意义(P<0.05);给药后72 h,C 组患者Scr、Sur 高于对照组、A 组、B 组,A 组、B 组患者Sur 高于对照组,B 组患者Sur 高于A 组,差异有统计学意义(P<0.05,见表5)。
2.5 不良反应 治疗期间对照组患者无一例出现低血压;A 组患者出现低血压1 例,不良反应发生率为1.9%;B 组患者出现低血压1 例,不良反应发生率为1.9%;C 组患者出现低血压5 例,不良反应发生率为9.3%。四组患者治疗期间不良反应发生率比较,差异有统计学意义(χ2=8.711,P=0.033);C 组患者不良反应发生率高于对照组,差异有统计学意义(χ2=5.243,P=0.022)。
表4 四组患者给药后72 h 心肌损伤标志物比较(±s)Table 4 Comparison of markers of myocardial injury in the four groups 72 hours after drug delivery

表4 四组患者给药后72 h 心肌损伤标志物比较(±s)Table 4 Comparison of markers of myocardial injury in the four groups 72 hours after drug delivery
注:CK=肌酸激酶,CK-MB=肌酸激酶同工酶,cTnI=心肌肌钙蛋白I;与对照组比较,aP<0.05,与A 组比较,bP<0.05;与B 组比较,cP<0.05
组别 例数 CK(mol/L) CK-MB(mol/L) cTnI(μg/L)对照组 54 1 587±748 162±42 15.67±2.40 A 组 54 1 342±695a 134±34a 13.54±2.28a B 组 54 1 168±721a 113±35ab 10.35±2.34ab C 组 54 988±635a 99±31abc 9.64±2.08ab F 值 7.172 30.774 82.451 P 值 <0.01 <0.01 <0.01
3 讨论
随着科技发展,AMI 的诊断和治疗已从建立冠状动脉疾患护理单元(CCU)模式发展到静脉溶栓再到直接PCI,并使AMI 患者病死率降低了约30%[7],但近10 年来AMI 住院患者病死率和主要并发症发生率并没有明显降低[8],因此,为进一步提高AMI 患者临床治疗效果,直接PCI 联合新的治疗方法或药物可能是一个切实可行的方法。BNP 是由心脏合成和分泌的一种循环激素,存于心房、心室肌细胞和血管内皮细胞。BNP 可与效应细胞膜上的鸟苷酸环化酶耦联钠尿肽受体A 结合并激活鸟苷环化酶,继而将鸟苷三磷酸转化为环磷酸鸟苷(cGMP);cGMP 作为第二信使可激活下游酶信号通路cGMP 依赖的蛋白激酶1,进而发挥多种生物学效应。BNP 是一种天然神经内分泌拮抗剂,可抑制肾素、醛固酮、去甲肾上腺素和内皮素等的激活,进而抑制神经内分泌系统过度激活。同时,BNP 也是一种天然抗心肌重塑因子,可通过调节纤维化基因的表达而调节细胞因子和炎性因子。此外,BNP 还可直接作用于心肌成纤维细胞,减少心肌细胞外基质,
减轻间质纤维化和心肌肥厚;同时,BNP 可选择性地扩张冠状动脉并降低肺循环阻力,有利于增加冠状动脉血流量,减少心肌耗氧量。本研究旨在比较不同剂量rhBNP 对行PCI 的AMI 患者的影响,以进一步明确rhBNP 的最佳使用剂量。
表3 四组患者不同时间点心功能指标比较(±s)Table 3 Comparison of index of cardiac function in the four groups at different time points

表3 四组患者不同时间点心功能指标比较(±s)Table 3 Comparison of index of cardiac function in the four groups at different time points
注:LVEF=左心室射血分数,LVEDD=左心室舒张末期内径,LVEDV=左心室舒张末期容积,LVESV=左心室收缩末期容积,SV=每分钟搏出量;与对照组比较,aP<0.05;与A 组比较,bP<0.05;与B 组比较,cP<0.05
组别 例数LVEF(%) LVEDD(mm)给药时 给药后24 h 给药后48 h 给药后72 h 给药时 给药后24 h 给药后48 h 给药后72 h对照组 54 49.87±9.24 49.98±8.94 50.61±6.84 51.76±7.05 58.13±1.89 57.91±1.92 58.42±1.95 57.74±1.42 A 组 54 50.34±10.32 51.45±9.25 52.41±8.58 54.61±7.21a 58.34±1.91 58.34±1.06 57.65±1.85 56.55±1.48a B 组 54 51.28±10.34 50.64±10.01 54.09±3.58a 55.93±3.52a 57.64±1.88 57.21±1.03ab 56.21±1.37ab 55.62±1.34ab C 组 54 49.54±9.13 51.64±9.45 55.07±3.57ab 58.07±3.65abc 58.19±1.96 56.54±1.21abc 55.47±1.43abc 55.13±1.37ab F 值 F时间=168.54,F组间=205.54,F交互=186.74 F时间=188.657,F组间=149.658,F交互=152.364 P 值 P时间<0.01,P组间<0.01,P交互<0.01 P时间<0.01,P组间<0.01,P交互<0.01组别LVEDV(ml) LVESV(ml) SV(ml)给药时 给药后24 h 给药后48 h 给药后72 h 给药时 给药后24 h 给药后48 h 给药后72 h 给药时 给药后24 h 给药后48 h 给药后72 h对照组 81.24±7.28 80.05±5.11 80.02±5.24 80.13±5.25 29.96±3.79 29.85±3.87 29.99±3.51 29.89±3.47 47.65±7.54 48.22±6.05 47.83±6.64 50.72±4.78 A 组 81.64±6.94 78.62±5.05 75.82±5.11a 74.15±5.91a 29.76±3.78 29.11±2.94 27.63±3.46a 28.62±3.06 46.86±7.11 48.66±6.13 48.61±5.38 51.14±4.98 B 组 80.67±7.64 78.28±5.37 72.76±4.96ab 70.25±5.18ab 30.14±3.94 29.89±2.73 26.40±2.94a 25.98±2.87ab 48.14±7.08 49.04±6.26 49.27±5.08 53.91±4.53ab C 组 81.48±7.35 78.14±5.21 70.25±5.01abc 68.54±5.54abc 29.76±3.88 28.62±2.86 24.64±3.16abc 23.64±3.32abc 48.08±6.94 50.57±6.28 51.68±5.07abc 54.62±4.53ab F 值 F时间=86.658,F组间=103.684,F交互=162.248 F时间=81.354,F组间=96.567,F交互=163.584 F时间=68.658,F组间=135.547,F交互=106.352 P 值 P时间=0.005,P组间<0.01,P交互<0.01 P时间=0.006,P组间=0.004,P交互<0.01 P时间=0.015,P组间<0.01,P交互<0.01
表5 四组患者不同时间点肾功能指标比较(±s)Table 5 comparison of index of renal function in the four groups at different time points
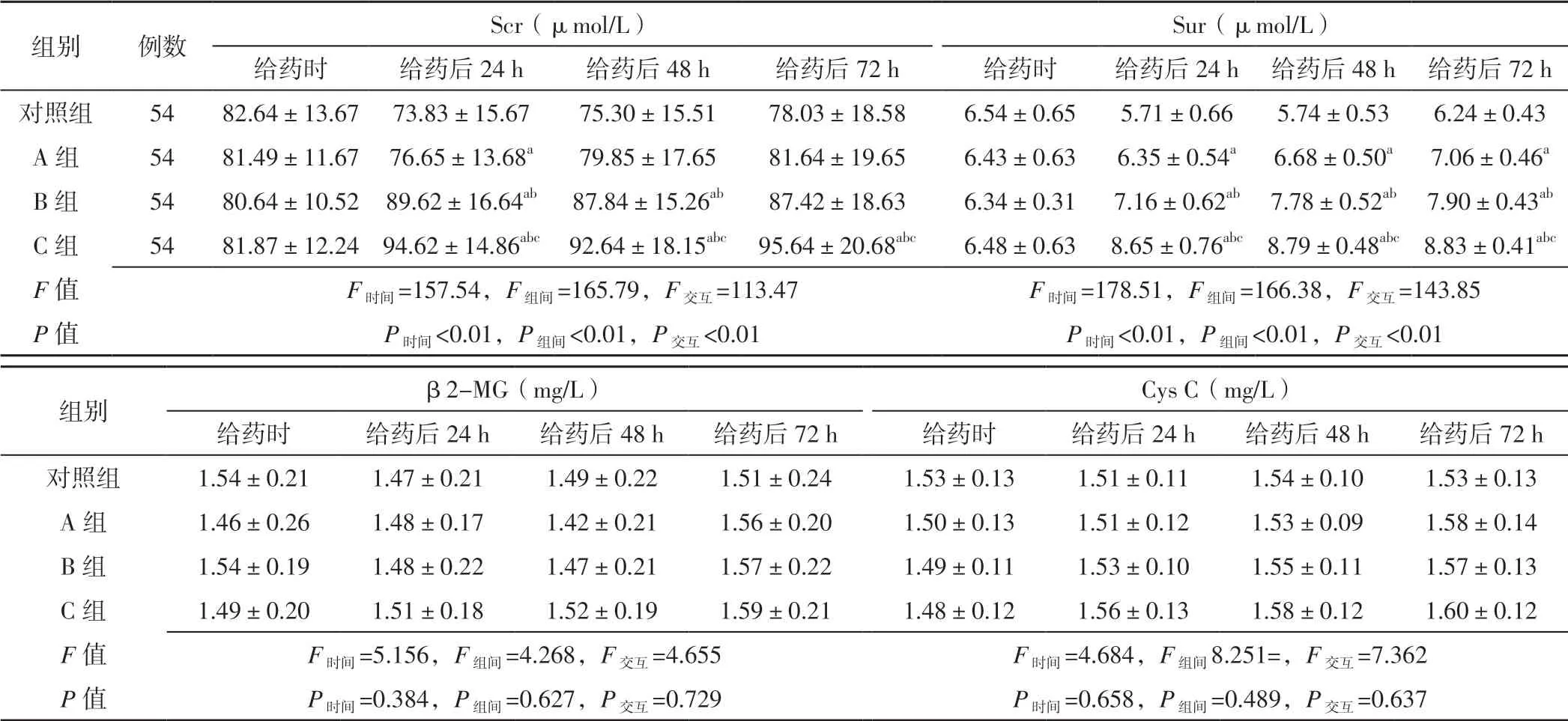
表5 四组患者不同时间点肾功能指标比较(±s)Table 5 comparison of index of renal function in the four groups at different time points
注:Scr=血肌酐,Sur=血尿素,β2-MG=β2-微球蛋白,Cys C=胱抑素C;与对照组比较,aP<0.05;与A 组比较,bP<0.05;与B 组比较,cP<0.05
组别 例数 Scr(μmol/L) Sur(μmol/L)给药时 给药后24 h 给药后48 h 给药后72 h 给药时 给药后24 h 给药后48 h 给药后72 h对照组 54 82.64±13.67 73.83±15.67 75.30±15.51 78.03±18.58 6.54±0.65 5.71±0.66 5.74±0.53 6.24±0.43 A 组 54 81.49±11.67 76.65±13.68a 79.85±17.65 81.64±19.65 6.43±0.63 6.35±0.54a 6.68±0.50a 7.06±0.46a B 组 54 80.64±10.52 89.62±16.64ab 87.84±15.26ab 87.42±18.63 6.34±0.31 7.16±0.62ab 7.78±0.52ab 7.90±0.43ab C 组 54 81.87±12.24 94.62±14.86abc 92.64±18.15abc 95.64±20.68abc 6.48±0.63 8.65±0.76abc 8.79±0.48abc 8.83±0.41abc F 值 F时间=157.54,F组间=165.79,F交互=113.47 F时间=178.51,F组间=166.38,F交互=143.85 P 值 P时间<0.01,P组间<0.01,P交互<0.01 P时间<0.01,P组间<0.01,P交互<0.01组别 β2-MG(mg/L) Cys C(mg/L)给药时 给药后24 h 给药后48 h 给药后72 h 给药时 给药后24 h 给药后48 h 给药后72 h对照组 1.54±0.21 1.47±0.21 1.49±0.22 1.51±0.24 1.53±0.13 1.51±0.11 1.54±0.10 1.53±0.13 A 组 1.46±0.26 1.48±0.17 1.42±0.21 1.56±0.20 1.50±0.13 1.51±0.12 1.53±0.09 1.58±0.14 B 组 1.54±0.19 1.48±0.22 1.47±0.21 1.57±0.22 1.49±0.11 1.53±0.10 1.55±0.11 1.57±0.13 C 组 1.49±0.20 1.51±0.18 1.52±0.19 1.59±0.21 1.48±0.12 1.56±0.13 1.58±0.12 1.60±0.12 F 值 F时间=5.156,F组间=4.268,F交互=4.655 F时间=4.684,F组间8.251=,F交互=7.362 P 值 P时间=0.384,P组间=0.627,P交互=0.729 P时间=0.658,P组间=0.489,P交互=0.637
本研究结果显示,给药后72 h B 组、C 组患者心肌损伤标志物及心功能指标均优于对照组及A 组;提示与小剂量rhBNP 比较,中等剂量或较大剂量rhBNP 可有效改善行PCI 的AMI 患者心功能,与最近一项循证医学研究结果较为一致[9]。本研究结果还显示,A 组患者给药后72 h 心肌损伤标志物与心功能指标优于对照组,提示小剂量rhBNP 对改善行PCI 的AMI 患者心功能指标具有一定优势;此外笔者还发现,随着rhBNP 剂量增加,心功能改善程度也越明显,可能是心功能与rhBNP 有一定剂量依赖效应。
在AMI 患者的治疗中,导致急性肾功能障碍的极重情况如下:低血压引起的肾灌注减少、血管收缩因子导致髓质缺血及PCI 使用的造影剂,而急性肾功能障碍发生时会有大量肾性物质堆积,可导致AMI 患者病情加重,并严重威胁患者生命安全。目前研究表明,rhBNP 静脉给药对血管舒张、钠排泄、利尿均有一定优势[10],但rhBNP 对肾脏的影响尚存在争议。Scr 是预测急性肾功能障碍的主要生物学标志物;Sur 是一种新的、敏感的早期肾功能障碍标志物。本研究结果显示,C 组患者给药后72 h Scr、Sur 高于对照组、A 组、B 组,提示较大剂量rhBNP 会损伤行PCI 的AMI 患者肾功能。本研究结果还显示,A 组患者给药后24 h Scr、Sur 高于对照组,提示小剂量rhBNP 也可导致行PCI 的AMI 患者肾功能损伤,笔者推测肾功能损伤可能与rhBNP 剂量也有一定依赖效应,这与既往研究结果相似[4,11-12]。有研究表明,低剂量rhBNP对AMI 患者或心脏手术患者的肾功能具有保护作用[11,13-14],分析本研究结果与之不同的原因可能是纳入的AMI 患者基线资料不一致,如入院时的肾功能、基础疾病等。有研究表明,rhBNP 给药后发生急性肾功能障碍的主要原因可能是低血压[15-16],本研究结果显示,A、B、C 组患者SBP、DBP 与rhBNP 也呈一定剂量依赖效应。
随着rhBNP 在围术期的运用,AMI 患者预后获得了较大益处,但鉴于rhBNP 的药理作用,仍需注意药物的不良反应,临床在应用rhBNP 时需要严格控制剂量。因此,笔者建议在PCI 后AMI 患者治疗中,首先给予低剂量rhBNP,72 h 内复查肾功能,并根据复查结果逐渐增加rhBNP 剂量,以确保AMI 患者获得更多的心功能益处。
综上所述,与小剂量、中等剂量rhBNP 比较,较大剂量rhBNP 可更有效地降低行PCI 的AMI 患者血压,改善患者心功能,减轻患者心肌损伤,但有可能使肾功能损伤发生风险升高,因此,rhBNP 的剂量调整在行PCI 的AMI 患者中有着重要作用,动态调整rhBNP 剂量可使患者获得最大益处;但本研究为回顾性研究,结果结论可能存在信息偏倚,且本研究只评估了患者左心功能,并未评估患者右心功能,rhBNP 对行PCI 的AMI 患者整体心功能的影响仍需要进一步深入探讨。
