高温烟气中煤焦气化行为
2020-01-15宋伟明周建安王宝李数杨健
宋伟明,周建安,王宝,李数,杨健
(1 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北武汉430081;2 武汉科技大学湖北省冶金二次资源工程技术研究中心,湖北武汉430081)
中国作为世界上最大的煤炭生产国和消费国之一[1]。煤炭所带来的资源与环境问题已经成了国民经济高速、健康发展的制约因素,并对能源、经济、环境的协调发展构成了严重威胁[2-3]。因此,开发煤炭的高效清洁利用技术迫在眉睫。煤气化技术作为一种高效清洁技术,能够促进煤炭资源综合利用,并能减少CO2排放量,提高气体的品质[4]。目前,以煤炭为燃料的发电企业、电池企业、钢铁企业、化工企业等行业会产生高CO、CO2、N2含量的高温烟气[5-6]。若直接排放到空气中不仅污染环境,同时也会造成资源的浪费。
如果以高温烟气作为气化剂来气化煤焦,不仅可以减少CO2排放,还可以制备高品质可燃气体,降低能耗。气化得到的H2和CO一部分可作为化工原料,另一部分可作为燃料来发电。
为实现上述过程,需要对煤与高温烟气的实际过程进行相关研究。煤气化反应过程研究多采用CO2、H2O 作 为 气 化 剂[7]。Kim 等[8]在 自 制 的 固 定 床反应器上进行了煤焦的CO2气化反应,并对气体分析,研究了煤阶对气化反应的影响,建立了相应的动力学模型。Fermoso 等[9]在反应温度为850~1050℃,实验升温速率为50℃/min,热重分析仪上研究了煤焦的水蒸气气化特性。Ewerson 等[10]利用热重分析仪,对南非煤焦与水蒸气及CO2共气化反应进行了相关研究,表明煤焦与水蒸气和煤焦与CO2气化反应分别发生在不同的活性位上,共气化反应速率为单一气氛下反应速率的加和。目前的研究多采用热重分析仪,升温速度比较慢且样品处于堆积的条件下进行,传热和传质情况与实际气化生产过程中有较大区别[11-13]。而沉降炉装置具有升温速度快、样品分散程度好、能很好模拟工业流化床等优点。
许多研究者利用流化床对煤焦在氧气和二氧化碳气氛中的燃烧气化特性进行了报道。Ahn等[14]和Kajitani 等[15]利用滴管炉对煤焦的二氧化碳气化反应进行了研究,并建立了相应的动力学模型。Zhang 等[16]研究了煤颗粒在流化床内燃烧和煤粒的破碎情况。还有部分学者利用流化床对煤焦的水蒸气气化行为进行了研究[17-19]。目前煤焦在单一气氛下研究较多,在高温混合气氛下研究较少,特别是CO/CO2/N2这种高温烟气下报道较少。
本文通过软件FactSage 6.1 来分析各组分发生反应的可能性,然后通过热重实验探究煤焦的气化行为,最后通过沉降炉实验来模拟高温烟气,探究煤焦在不同反应温度、气氛配比、粒径条件下的高温反应特性和气体成分的变化规律。该研究结果可为煤焦在高温烟气中的应用提供理论指导,最大限度地提高资源利用率,减少温室效应。
1 实验材料和方法
1.1 实验材料
在N2保护气氛下,将鄂州钢铁集团高炉喷煤所用的无烟煤粉加入高温管式炉内进行热解,在常压下,以10℃/min 速率升温到900℃,保温时间30min,冷却至室温,取出煤焦粉后研磨备用。粒径为100~400 目(150~38μm)。试验前,将实验原料放置在105℃鼓风干燥箱内烘干24h,以降低水分含量。用Vario EL元素分析仪分析煤焦中各元素含量。煤焦粉的工业分析和灰熔点温度的结果见表1。用美国康塔公司Autosorb-1-MP 型分析仪测出煤焦的比表面积A、孔容V及平均孔径D,见表2。

表1 煤焦粉的工业分析和元素分析
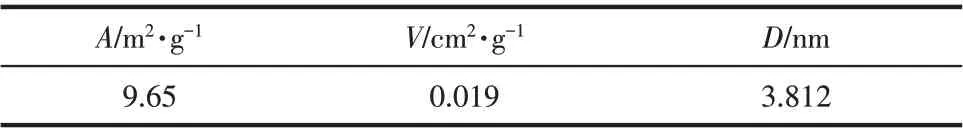
表2 煤焦比表面积、孔容、平均孔径
1.2 实验方法
1.2.1 热力学计算
煤焦粉在高温混合气体中发生热解和气化反应,主要生成CO、CO2、CH4、H2O、H2、焦炭、灰分等组分[20]。为确定各组分反应温度、反应顺序,利用FactSage 6.1 中的Reaction 模块,对不同温度下反应的ΔG进行理论计算。煤焦气化过程可以用式(1)~式(4)所示的反应来表示。

为确定煤焦粉在高温混合气体中高温反应特性,采用FactSage 6.1 中的Equilib 模块,对不同温度下的气体产物进行理论计算分析。煤焦化学式由元素组成来确定,设置煤焦摩尔数为1mol。控制混合气体CO、CO2、N2比例为5∶3∶2,进而设置混合气体CO、CO2、N2物质的量分别为2.5mol、1.5mol、1mol,计算结果为进一步研究奠定了基础。
1.2.2 热重实验
采用热重分析仪(STA449C)记录样品在连续加热过程中的失重率和失重速率,作为理论研究的一部分。热重实验结果可以很好地体现煤焦CO2气化行为,为沉降炉实验起到指导作用。实验过程中,将约10mg 样品放置于氧化铝坩埚中,在流速为50mL/min的CO2气氛中将样品以10℃/min的升温速率从室温加热至1400℃。
1.2.3 沉降炉实验
为了进一步研究煤焦在高温烟气下的高温反应行为,用沉降炉实验来模拟高温烟气。通过沉降炉实验研究了煤焦在不同温度、气氛和粒度下的反应特性,实验装置如图1所示。首先,打开冷却系统并设置升温程序将沉降炉加热到设定温度。当加热到设定温度时,向反应器中通入氮气以排除空气气氛,接着通入CO 和CO2气体,调节流量计以控制气体流速和气体比例,混合气体流量为5L/min,并通过烟气分析仪进行验证气体成分。同时,打开进料装置,调节转速为0.8g/min的速率将试样添加到反应器中,并开启真空泵将反应后的气氛从炉底抽出,通过烟气分析仪(VARIO PLUS)实时监测反应体系中CO、CO2、CH4和H2浓度。为减小误差,反应连续进行16min,数据每分钟记录1 次。每个实验重复3次,取3次实验的平均值作为最终实验表征值。具体工况见表3。
1.3 评价指标
由于这种特殊的气体环境,为进一步反映高温烟气对煤焦气化的影响,实验以可燃气体的上升率α和CO2下降率β这两个指标来表征煤焦的转化。
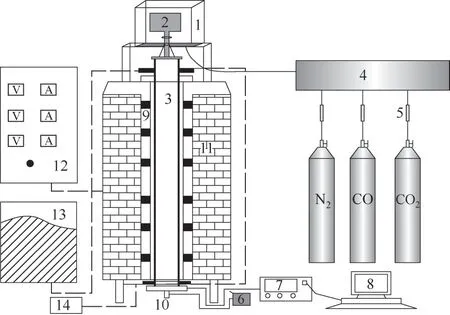
图1 实验装置
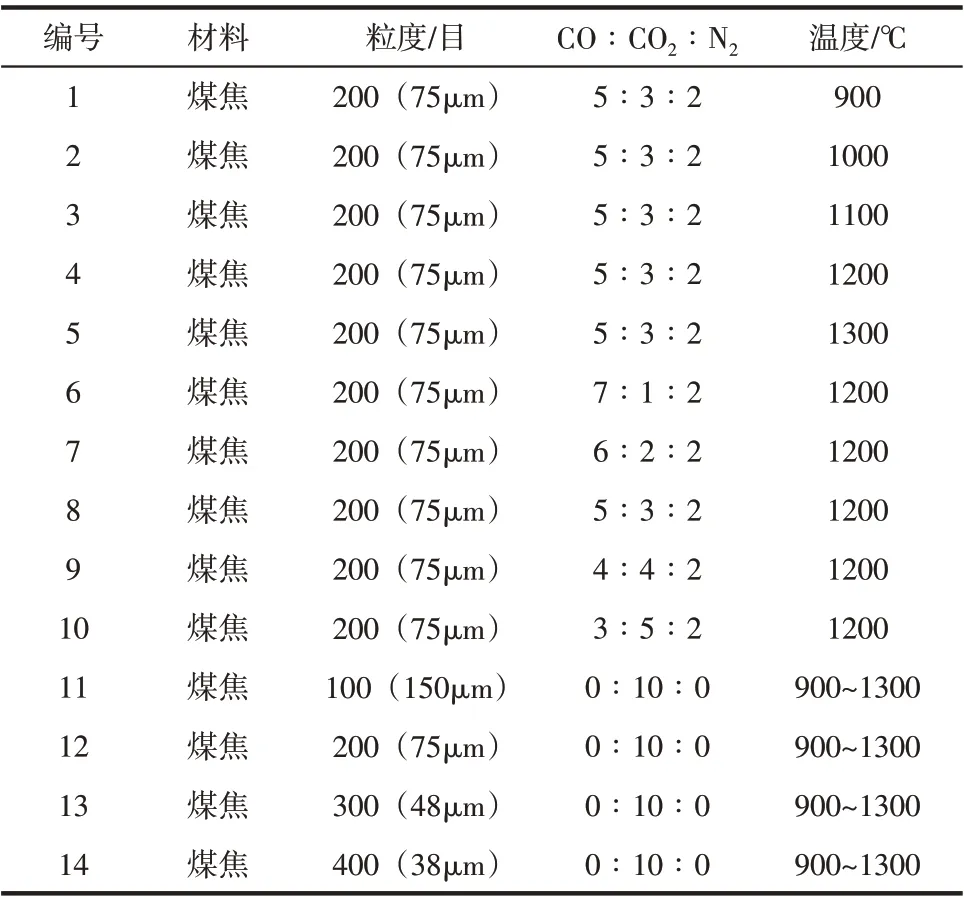
表3 沉降炉实验方案
(1)可燃性气体包括CO、H2和CH4;α定义见式(5)。

式中,φ1为反应前可燃气体的总体积分数,%;φ2为反应后可燃气体的总体积分数,%。
(2)二氧化碳下降率β的定义见式(6)。

式中,v1为反应前CO2的总体积分数,%;v2为反应后CO2的总体积分数,%。
(3)可燃性气体的低位热值LHV(MJ/m3)定义见式(7)[21]。
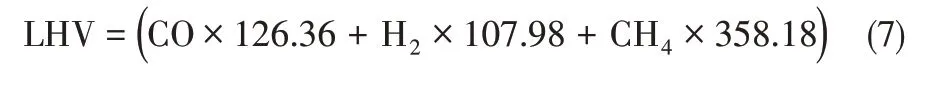
式中,CO、H2和CH4为气体产物中组分的摩尔分数,%。
2 实验结果与讨论
2.1 热力学计算分析
利用FactSage 6.1 中的Reaction 模块,对不同反应温度下的ΔG进行计算,如图2(a)所示。随着温度的升高,反应式(1)、反应式(2)、反应式(4)的吉布斯自由能不断减小,所以升高温度有利于反应的进行;反应式(3)的吉布斯自由能不断增大,所以升高温度不利于反应的进行。此外,当温度大于727℃时,反应式(1)、反应式(2)、反应式(4)的吉布斯自由能都小于0,这表明三个反应均能发生,进而促进CO、H2气体的产生。与此同时,从反应式(4)可以看出CH4在高温下不稳定存在,易发生裂解。
利用FactSage 6.1 中的Equilib 模块,对不同温度下的气体产物进行理论计算分析,如图2(b)所示。随着温度的升高,气体产物CO 的量不断增加,气体产物H2的量增加程度较小。当温度大于1127℃时,气体产物H2、CO 增加幅度较小。而气体产物CO2随温度升高不断减少,这主要是由于发生反应式(1)导致CO2量减少和CO 量升高。当温度大于1000K时,随着温度升高气体产物CH4先升高后降低,这是因为煤焦中残余挥发分热解生成CH4,温度继续升高CH4在高温下不稳定存在,进而导致CH4先升高后逐渐降低。气体总量(GAS)也随温度升高不断增加,只是各温度段增加幅度不同。热力学模拟结果表明,高温有利于气体CO、H2的生成,不利于CH4稳定存在。

图2 吉布斯自由能和气体产物随温度的变化曲线
2.2 热重分析
煤焦CO2气化的TG 和DTG 曲线如图3 所示。整个气化过程主要分为以下两个阶段:第一阶段为899℃以内,煤焦质量缓慢失重,这是由于煤焦中水分蒸发与残余挥发分的析出[22]。在第二阶段为899~1400℃,煤焦质量出现明显的失重,是因为煤焦中的残余碳与CO2发生气化反应,热重实验结果与热力学计算结果相一致。当温度为1237℃时,失重速率出现最大峰值。通过TG、DTG 数据分析可为沉降炉实验设计提供参考。

图3 煤焦在CO2气氛下TG和DTG曲线
2.3 沉降炉实验
2.3.1 不同温度对气体产物的影响
为了进一步探讨温度对气体产物的影响,选择反应气氛CO、CO2、N2的比例为50∶30∶20,煤焦粒度为200 目(75μm)。温度为900℃、1000℃、1100℃、1200℃、1300℃。气体产物的变化如图4(a)所示,气化产物中H2和CO含量随温度升高有逐渐增加的趋势。这是由于温度升高增加了煤焦中碳原子的能量,使构成煤的芳香环中的碳键易断裂,另外从反应式(1)也可以看出温度升高有利于CO2气化反应的进行[23]。H2含量的增加主要是由于煤焦中残余挥发物的析出以及水煤气反应,从反应式(2)可以看出温度升高有利于H2的生成。当温度从900℃升至1200℃,H2和CO 产量迅速增加,而1200℃之后增速放缓。有研究结果表明这是由于煤焦在高温下会出现熔融现象,进而降低煤焦的气化反应活性[24]。然而,气化产物CH4含量随温度升高有逐渐下降趋势,从热力学角度看出CH4在高温下不稳定存在易发生裂解反应,所以随着温度升高CH4含量降低。
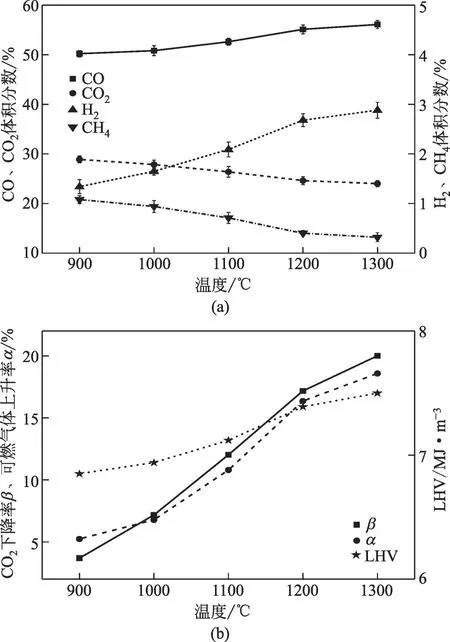
图4 气体产物、α、β、LHV随温度的变化
CO2下降率β、可燃气体上升率α、低温热值LHV(标况下)随温度的变化如图4(b)所示,都随温度的升高而增加,这与气体产物CO、H2变化保持一致。β、α、LHV 值分别由900℃的3.70%、5.24%、 6.85MJ/m3上 升 到 1200℃的 12.03%、18.58%、7.50MJ/m3。主要是因为CO、H2含量随温度升高而增加,进而提高了混合气体的热值和可燃气体上升率。
2.3.2 不同气氛比例对煤焦气化的影响
由于高温烟气中CO 和CO2含量存在波动,因此非常有必要研究煤焦在不同气氛下的反应情况。保持温度为1200℃,煤焦粒度为200 目(75μm)。设置CO2、CO、N2比例分别为10∶70∶20、20∶60∶20、30∶50∶20、40∶40∶20、50∶30∶20条件下,探究气体产物和可燃气体上升率α、CO2下降率β和低温热值LHV 的变化。如图5(a)所示,随着CO2/CO 比值的升高,CO 的增加量分别为0.3%、2.86%、7.51%、8.10%、9.82%;CO2的下降 量 分 别 为1.08%、 2.77%、 5.39%、 8.99%、12.35%。可以看出,CO 的增加量和CO2下降量都逐渐增大。一方面,是由于CO2含量的增加,反应能消耗更多的CO2生成更多的CO;另一方面,是由于CO 含量的减少,对反应式(1)的抑制程度减弱,生成CO 的趋势更大。部分学者利用H2O 作气化剂也得到相似的观点,H2对煤焦气化行为也起到抑制作用[25]。与此同时,随着CO2/CO 比值的增大,CH4量、H2量变化不明显,CO2/CO 比值对H2和CH4含量的影响较小。
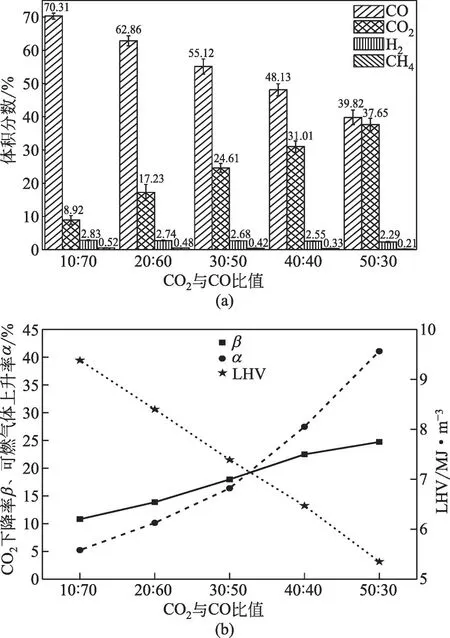
图5 气体产物、α、β、LHV随气氛的变化
图5(b)可以看出,CO2下降率β、可燃气体上升率α随CO2/CO 比值的增大而逐渐增加。β、α值分别由CO2/CO 比为10∶70 时的10.80%、5.21%增加到CO2/CO比为50∶30时的24.71%、41.06%。可以看出,随着CO2含量增大,可燃气体上升率快速增加。与此同时,LHV 值随着CO2/CO 比值的增大却出现逐渐减少的趋势。这是因为设置原料气氛CO2/CO 比值增大时,使初始气体CO 的含量大量减少,进而导致可燃气体成分相对含量降低。虽然低CO含量对反应式(1)抑制作用减弱,但是相比于初始气氛来说影响较小,所以LHV 值是逐渐减少的。由此可以得出,LHV值主要是由外在条件决定的,内在条件只是起到促进作用。
2.3.3 不同粒径对煤焦气化的影响
不同温度下煤焦的粒径对煤焦气化的影响如图6 所示。由于实验时初始通入气体CO2体积分数较高,进而导致生成的气体几乎都是CO2和CO。因此,本实验中只统计CO 体积分数来计算低温热值。在相同温度下,随着煤焦粒径的减小,CO2体积分数逐渐减小,CO 体积分数逐渐升高。这说明随着煤焦粒径的减小,气化反应CO2进入煤焦颗粒内部孔隙的扩散阻力降低[26],有利于气体CO 的生成。在900℃时,CO2和CO 体积分数变化不明显,温度大于1000℃时,CO2体积分数快速下降,CO体积分数迅速升高。可以看出,低温不利于气化反应进行。从TG曲线也可以看出,温度在899℃时煤焦气化反应才开始进行。在相同温度时,100 目(150μm) 与200 目(75μm) 的曲线间隔较大,300 目(48μm)与400 目(38μm)的曲线间隔较小。这表明在一定范围内,随着煤焦粒径的减小,煤焦气化反应活性增加量变小。同时煤焦粒径越小,制备成本就越高。因此,在实际应用中要综合考虑煤焦制备成本和反应性能等因素。通过以上两个因素的考虑,在实际应用中选用粒径为300 目(48μm)比较合适。

图6 CO2和CO体积分数随温度和粒径的变化
图7 显示了CO2下降率β和低温热值LHV 随温度和粒径的变化。较高反应温度和减小煤焦粒径,都有利于煤焦CO2气化反应进行,进而导致CO2下降率升高。在煤焦粒径为200目(75μm)时,温度从900℃增加到1300℃,β值增加量分别为1.49%、8.69%、15.69%、18.19%。然而,当反应温度为1200℃时,煤焦粒径从100目(150μm)减小到400目(38μm)时,β值增加量分别为2.6%、3.7%、4.2%,其他粒径和温度对比也出现相似的情况。因此,可以得出反应温度对煤焦气化反应的影响要远大于煤焦粒径。粒径为200目(75μm)时,低温热值LHV随温度的变化如图7(b)所示,低温热值LHV随温度的升高不断增大。当温度大于1200℃时,低温热值LHV 随温度升高增加程度较小,这是由于大于1200℃时,气化反应活性增加量较小。
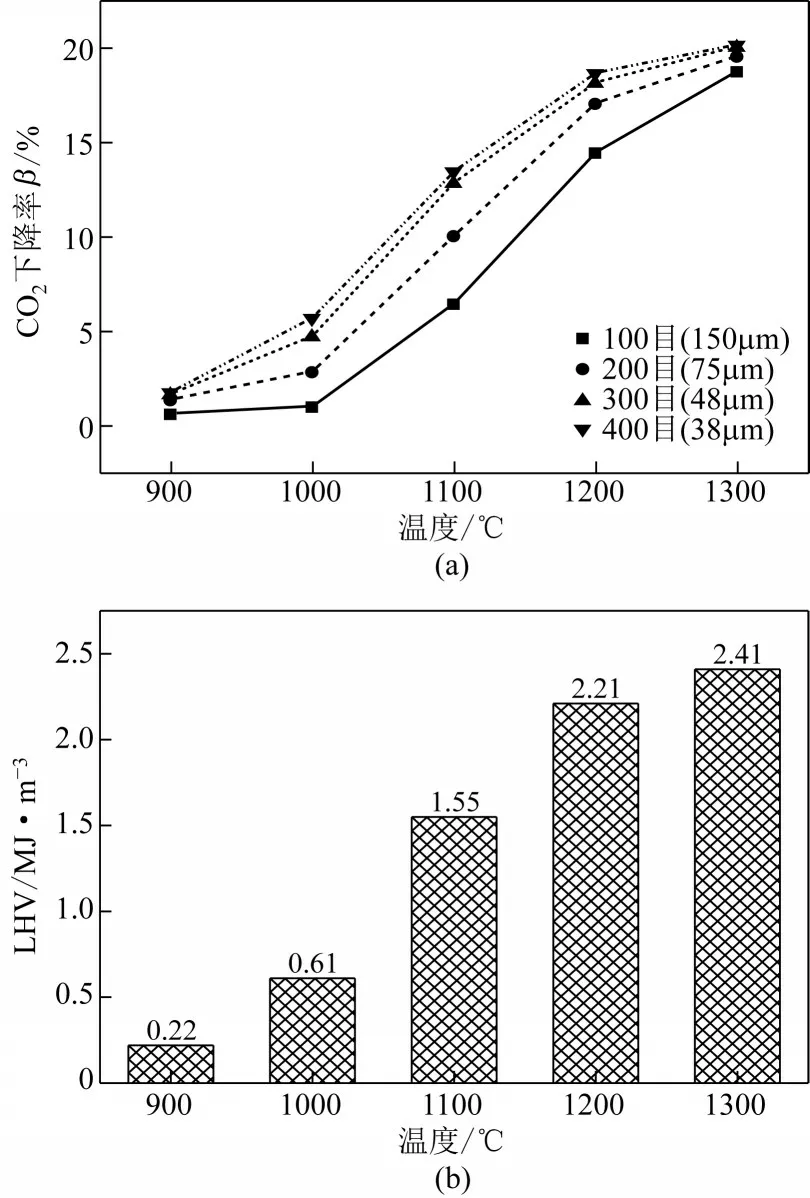
图7 CO2下降率和低温热值随温度和粒径的变化
3 结论
(1)热力学计算结果表明随着温度的升高,有利于CO2气化反应的进行,气体产物H2和CO 含量不断增加。然而CH4含量随温度升高逐渐下降,是由于CH4在高温下不稳定存在,易发生裂解。
(2)热重实验结果表明煤焦气化反应主要分为两个阶段:第一阶段为899℃以内,主要是煤焦中水分蒸发与残余挥发分的析出;在第二阶段为899~1400℃,主要是因为煤焦中的碳与CO2发生气化反应。失重速率最大峰值温度为1237℃。
(3)沉降炉实验结果表明随着温度的升高,H2和CO 的含量增加,CH4和CO2的含量下降。β、α、LHV 值分别由900℃的3.70%、5.24%、6.85MJ/m3上升到1200℃的12.03%、18.58%、7.50MJ/m3。在温度为1200℃时,随着CO2/CO比值的升高(由10∶70 分别升至20∶60,30∶50,40∶40,50∶30),CO的增加量分别为0.3%、2.86%、5.51%、8.10%、9.82%; CO2的 下 降 量 分 别 为1.08%、 2.77%、5.39%、8.99%、12.35%;CH4和H2含量变化不明显。相同温度下,CO2含量随煤焦尺寸的减小而降低。反应温度大于煤焦粒径对煤焦CO2气化反应的影响。综合分析,在实际应用中焦粉粒径为300目(48μm)、气化温度为1200℃比较适宜。
