铝空气电池用6061和7075铝合金阳极电化学性能
2020-01-15杨亚刚俞小花张磊史春阳庄晓东谢刚
杨亚刚,俞小花,张磊,史春阳,庄晓东,谢刚,2,3
(1昆明理工大学冶金与能源工程学院,云南昆明650093;2昆明冶金研究院有限公司,云南昆明650503;3共伴生有色金属资源加压湿法冶金技术国家重点实验室,云南昆明650503)
人类对资源能源需求的增长,现有资源能源日趋减少,环境污染日益严重的问题已成为阻碍国家发展、企业兴亡、人民幸福的重要因素。因此,努力开发高效绿色清洁可再生能源势在必行。铝空气电池是一种金属燃料电池,具有理论能量密度高(8200Wh/kg)、成本低、产量大、绿色环保、阳极材料储量大等优点[1-2]。在过去50 年里,铝空气电池的研究取得了长足的进展,获得了多项专利,并在电力、水下航行器、储能载体、军工等领域得到了一定应用,且有望得到进一步的应用和发展[3-6]。铝空气电池的研究包括选择合适的阳极[7-16],高催化活性的阴极[17-23]和制作最有效的电解液[24-27]这3部分。其中在碱性电解液中阳极表现出活性更高、电极电位更负的特点,具有很高的研究和应用价值,但由于铝阳极在碱性体系中与水易发生还原反应而导致阳极自腐蚀严重,极大限制了铝空气电池的发展。因此,采用铝合金作阳极替代纯铝来降低阳极材料的自腐蚀速率进而提高阳极的利用率,已成为铝阳极研究的热点。已经产业化的铝合金具有成熟的生产工艺,能够有效降低开发新型阳极合金所带来的工艺转变的经济负担。6061 合金和7075 合金中,除了Al 外一般还含有不同比例的Mg、Mn、Cu、Si、Zn、Ti、Cr 和Fe 等元素。相较于纯铝,6061 合金和7075 合金具有易加工、强度高、耐腐蚀等特性,能有效阻碍阳极的溶解,减少腐蚀损失,提高铝空气电池的效率。
本文旨在研究纯铝、6061 合金和7075 合金作为阳极在4mol/L NaOH中的电化学性能,确定适合碱性铝空气电池的阳极材料,采用电化学阻抗法、电流-电位曲线、恒放电实验对阳极材料在碱性介质中的放电性能进行表征。
1 实验材料和方法
1.1 电极制备
工作电极为纯铝(99.99%)、工业6061铝合金(6061)和航空7075铝合金(7075)。3种阳极材料的元素成分如表1所示。
电极工作面积为1cm2,非工作面涂环氧树脂,铜线导电。对工作面进行机械抛光,然后用蒸馏水清洗,干燥。

表1 3种阳极材料的元素成分表(质量分数)
1.2 电化学性能测试
采用瑞士万通PGSTAT-204电化学工作站对材料进行电化学性能测试,测试时采用三电极体系,其中辅助电极为1.5cm×1.5cm 铂片电极,参比电极为Hg/HgO (1mol/L NaOH)电极。分别以6061、7075和纯铝为工作电极在4mol/L NaOH溶液中进行开路电位、阻抗曲线和电位极化曲线测量。极化曲线电压范围为-2~-1V,扫描速率为0.01mV/s。阻抗曲线范围0.1~105Hz,测试信号为幅值10mV 的正弦波,数据拟合软件为瑞士万通Nova2.13。
1.3 放电性能测定
组装成半电池进行放电性能测试,电池阳极分别为6061、7075和纯铝板,阴极是以MnO2为催化剂的空气电极,有效面积为16cm2。电解液为4mol/L NaOH 溶液。室温下,采用蓝电电池测试系统CT2001A对电池进行不同电流密度下连续恒流放电测试,来检测不同电流密度下的放电电压,计算阳极连续放电的腐蚀速率va和能量密度w,阳极消耗的质量为阳极放电前后的质量差,放电后阳极在稀硝酸中用毛刷刷洗,再用蒸馏水清洗,干燥后再称重。
阳极腐蚀速率和能量密度的计算见式(1)和式(2)[28]。

式中,va为腐蚀速率,g/(cm2·h);w为能量密度,W·h/kg;j为电流密度,mA/cm2;W0为实际损失质量,g;U为对应电流密度的放电电压,V;S为阳极板的有效面积,cm2;t为放电时间,min。
1.4 表面微观形貌分析
采用日本岛津EPMA-1720 电子探针显微镜观察阳极放电前后的表面形貌,并采用波谱仪分析基体和第二相的成分;放电前的阳极观测之前用砂纸(800目-1000目-1500目-2000目)进行抛光处理,放电后的阳极在称重时已进行处理。
2 结果与讨论
2.1 电化学性能
铝的氧化反应是铝空气电池的基础,相对于标准氢电极的电势为-2.31V,在碱性介质中阴极表面发生氧还原的电位为+0.40V,电池的理论放电电位为2.7V。铝空气电池在碱性介质中的活性明显高于在其他介质中的活性[29],由于铝阳极在碱性介质中的自腐蚀损耗严重,导致铝空气电池的效率降低,故碱性铝空气电池的研究方向应该是在兼顾电极电位的基础上来降低阳极腐蚀率[30]。图1 为纯铝、6061 和7075 在4mol/L NaOH 溶液中的电位极化曲线,可看出7075 的腐蚀电位最正,其次是6061,纯铝最负,这种电位正移提高了阳极腐蚀所需的条件,使腐蚀更难发生;同时可以看出,3种阳极腐蚀电流由大到小的顺序为i7075<i6061<i纯铝,说明6061 和7075 极化较纯铝严重,抗腐蚀性能较好。表2为3种阳极的极化曲线测试数据,可以看出,阳极所对应的腐蚀速率、极化电阻腐蚀电位和传递系数与图1极化曲线图所对应的腐蚀电流密度和阳极极化的腐蚀电流趋势相同,即6061 和7075在碱性体系中具有较好的抗腐蚀性能,其中6061电极电位和缓蚀的兼容性更好。
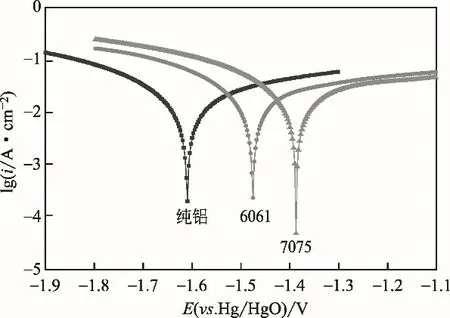
图1 纯铝、6061铝和7075铝在4mol/L NaOH溶液中的电位极化曲线
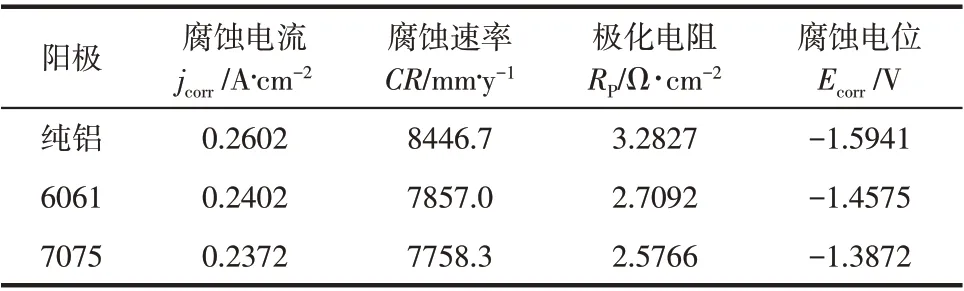
表2 纯铝及6061铝合金和7075铝合金在4mol/L NaOH溶液中的电位极化曲线测试数据
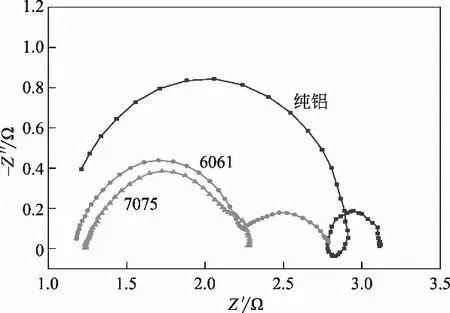
图2 纯铝及6061和7075在4mol/LNaOH溶液中的阻抗曲线
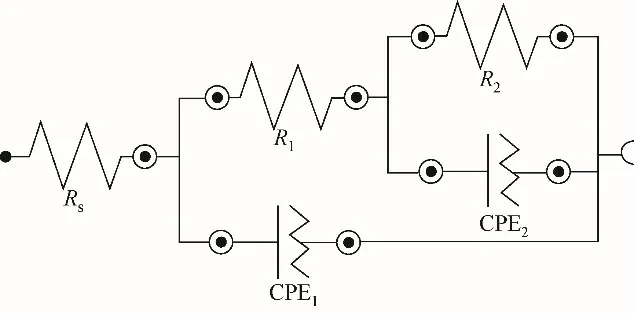
图3 阻抗曲线等效电路图
对于铝合金阳极的阻抗曲线开始处的电阻是溶液电阻(Rs),将曲线水平外推得到的电阻值是极化电阻(Rp)。极化电阻(Rp)包括薄膜电阻Rf和碱腐蚀引起的孔隙电阻Rpor[Rpor=Rct(电荷转移电阻)+Rdl(扩散层电阻)+Ra(所有其他累积种类,如腐蚀产物、任何现有分子或离子等)][31-32]。图2为纯铝及6061和7075在4mol/L NaOH溶液中的阻抗曲线,图3为所对应的拟合电路图。在图2可以看到两个电容环,第一个是高频电容环,其代表的是薄膜电阻Rf,对应图3 中的电阻值(R1)和薄膜形成的非理想电容(CEP1),由于合金电极在电化学反应时表面会发生微观起伏,因其弥散效应,故电路中电容元件全部用常相位角元件CEP 代替,相关性能分别用相对应的Y0和弥散指数n两个参数表征;第二个是低频区电容环,其代表的是孔隙电阻Rpor,对应图3 中的电阻值(R2)和非理想电容(CEP2)组成[33]。表3 为等效电路的拟合数据,纯铝、6061和7075 的Rf值分别为1.725Ω/cm2、1.093Ω/cm2和0.166Ω/cm2,合金阳极的Rf值小于纯铝阳极,表明合金元素对铝阳极具有活化作用,这是由于合金元素能够减小合金表面所形成的薄膜厚度而降低电阻。纯铝、6061 和7075 的Rpor值分别为0.291Ω/cm2、 0.479Ω/cm2和1.101Ω/cm2, 纯 铝 的Rpor值最小。
2.2 放电性能
图4为纯铝、6061和7075在4mol/L NaOH溶液中的恒流放电曲线,各电流密度下的放电测试结果如表4所示。各电流密度下,6061的放电电压都比纯铝和7075的放电电压平稳。3条放电曲线的开始静置电压都存在逐渐降低直至平稳的过程,且刚开始的静置电压比放电后再次静置的电压略高,这是因为铝阳极和碱液反应产生氧化层的速率与氧化层在碱液中的溶解速率有一个平衡过程,达到平衡之前氧化层的生成速率大于溶解速率,氧化层变厚,氧化层电阻变大,放电电压降低;达到平衡之后氧化层厚度稳定,放电电压趋于平稳。不同的电流密度下阳极氧化层的生成速率、溶解速率以及氧化层厚度也不同,放电后再次静置时前一步放电产生的厚氧化层未来得及溶解变薄,造成放电后再次静置时的电压较低。纯铝和6061 在小于80mA/cm2的电流密度下放电电压才有效,且6061 在相同电流密度下的放电电压高于纯铝,7075 只在电流密度小于60mA/cm2时才能使用,且相同电流密度下的放电压小于纯铝和6061。对照3种阳极在不同电流密度下连续放电的综合能量密度可发现,6061 的能量密度最高,为901.16Wh/kg。说明6061铝更适合作为铝空气电池阳极材料。
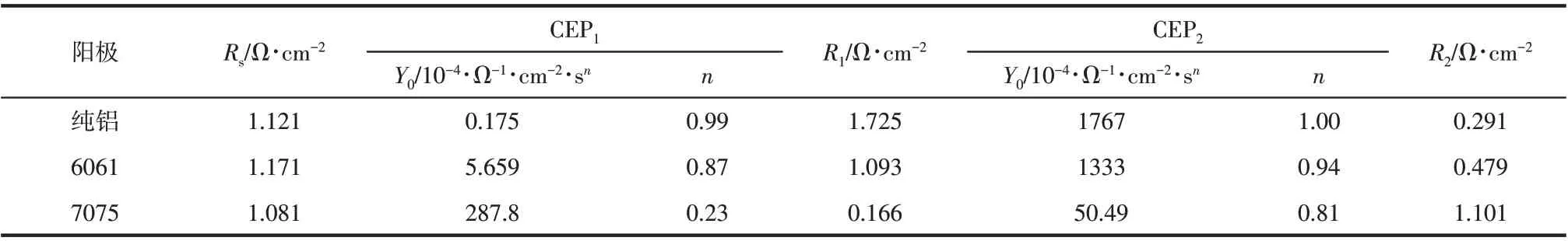
表3 纯铝及6061和7075在4mol/L NaOH溶液中的阻抗曲线拟合数据
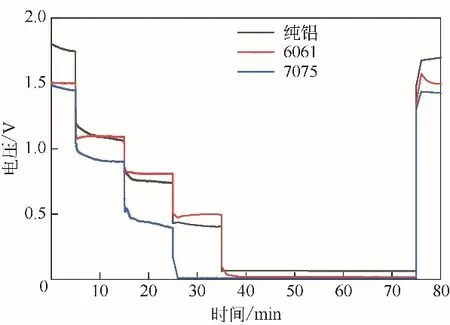
图4 纯铝及6061和7075在4mol/L NaOH溶液中的恒流放电曲线
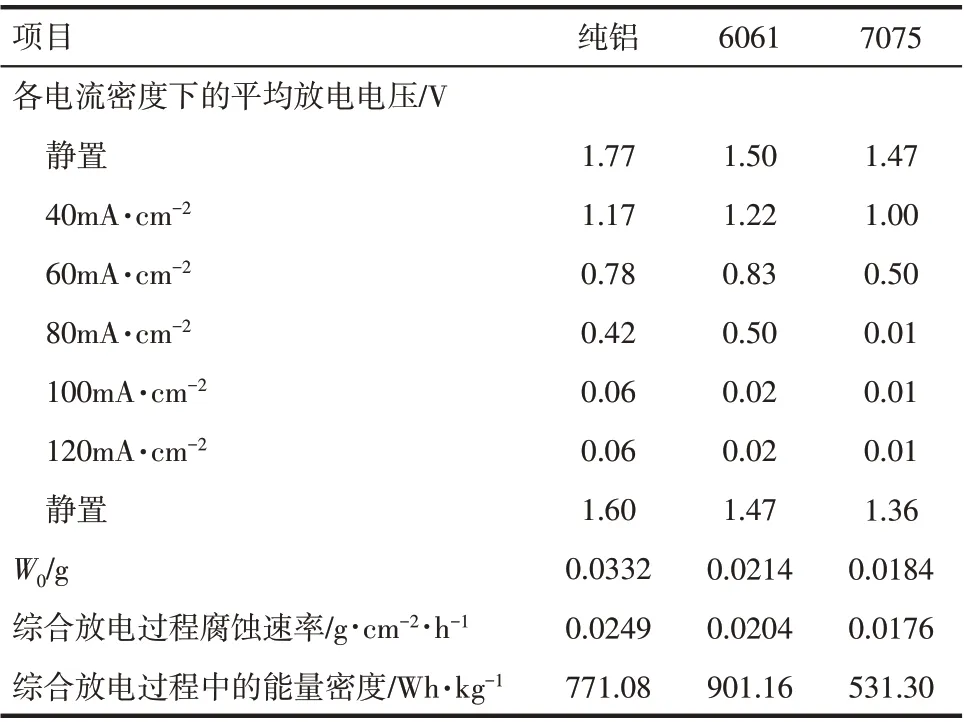
表4 纯铝及6061和7075在4mol/L NaOH溶液中的恒流放电测试结果
2.3 微观形貌分析
图5 为3 种阳极放电前后的表面微观形貌,几种表面微观局域的波谱分析结果如表5。可以看到,放电前3种阳极表面都存在缺陷,纯铝的缺陷为阳极轧制变形缺陷,无杂质,组织呈纤维状;6061 和7075 的缺陷为孔洞状,该缺陷可能是阳极制作时拉丝造成的;同时两种阳极中均存在偏析相,6061 的偏析相以Al、Mg、Si 为主,偏析相颗粒较小且分布均匀密集;7075的偏析相以Al、Fe、Cu、Zn 为主,偏析相颗粒较大,分布均匀但较稀疏。从图5可以看出,放电后3种阳极的表面形貌都发生了巨大的变化,纯铝的表面变成了多个巨大块体,这是因为该阳极从纤维缺陷处开始反应,使得阳极表面被分割,最终形成完整的块体;且表面有极少数杂相,其成分以Al 和Ca 的氧化物为主,由于该杂相很少且分布不均,故对阳极反应的影响可忽略。6061 表面褶皱和孔洞极多,偏析相颗粒较细,分布均匀且密集,适量的Mg 元素能够细化合金晶粒,改善微观组织结构,有利于阳极的均匀溶解和极化性能的提高[34];Mg 元素的高析氢过电位对阳极的析氢也有一定的限制作用,少量Si 也能够提高合金阳极的腐蚀均匀性。这种形貌能够增加阳极反应的有效面积,使得有效面积在3种阳极中最大,有助于反应的进行,偏析相中的合金元素对阳极反应能起到活化的作用,基体中的Mg 元素对阳极的自腐蚀能起到抑制作用[35]。7075的表面具有大量凹坑,有棱角偏析相较少,这可能是由于基体中Mg 元素含量过高导致合金颗粒变大,使得阳极活性不足,腐蚀速率慢,能量密度低;阳极表面初始形貌对阳极的腐蚀也有影响,但电解液为高浓度NaOH 与阳极润湿性较好且反应剧烈,故Mg 含量对腐蚀速率的影响程度更大。

图5 合金阳极放电前后的表面微观形貌
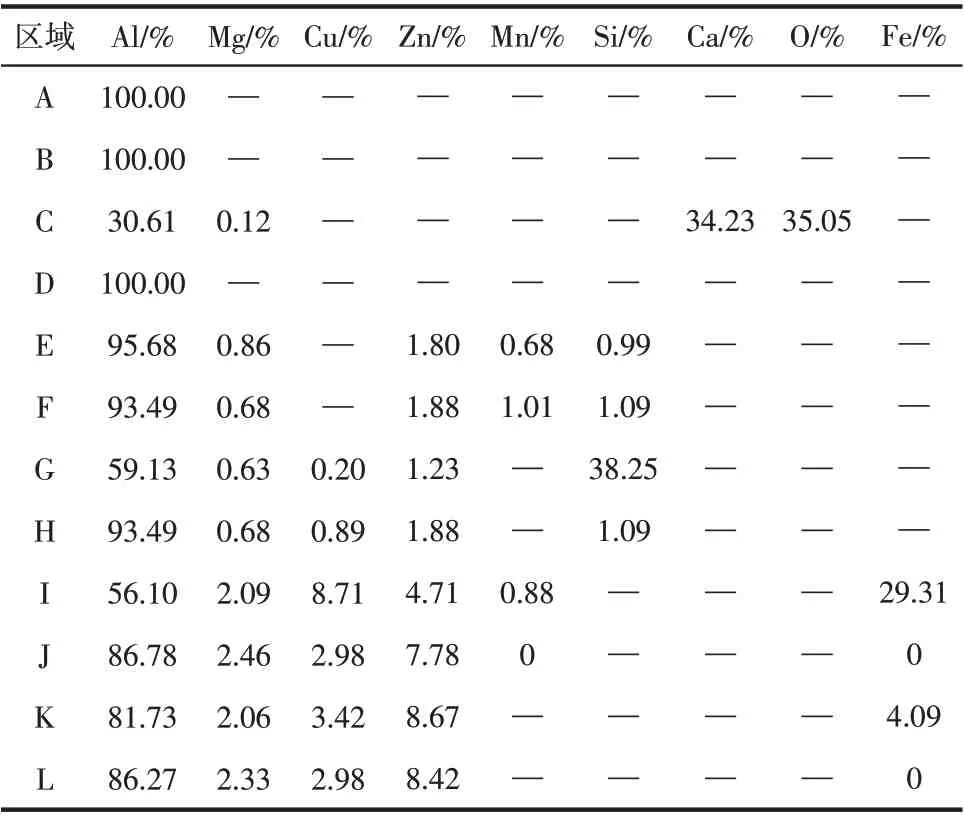
表5 合金阳极放电前后部分区域元素成分(质量分数)
3 结论
本文研究了3 种阳极的电化学性能,并对3 种阳极放电前后的表面微观形貌进行了分析对比,得出以下结论。
(1)纯铝、6061 和7075 这3 种阳极在开路电位下,6061 和7075 的自腐蚀电位相对于纯铝都有正移,薄膜电阻Rf减小,空隙电阻Rpor增大,腐蚀速率降低,具有很好的缓蚀性,但活性降低。其中6061在抗腐蚀和电极活性的兼容性上更好。
(2)在不同电流密度下连续恒流放电时,3种电极都只适合在小于80mA/cm2的电流密度下放电。在这个范围内同电流密度下6061 阳极的放电电压最高,综合能量密度最高。
(3)阳极恒流放电后,阳极的表面形貌都发生了变化,造成形貌变化的主要因素为阳极自身特性和所含元素共同决定的。其中6061 的合金元素含量最佳,使得合金元素在阳极和基体中分布合理,缓蚀和活化得到兼顾,表现出较好的阳极性能。
