尼莫地平负荷 SPECT脑血流灌注显像在急性非致残性脑血管病中的诊断价值
2019-12-25张秋洪陈汉水马琪林
张秋洪 陈汉水 岳 岑 马琪林
厦门大学附属第一医院神经内科,福建 厦门 361000
2016年Lancet杂志发表的《2015年全球疾病负担研究》指出,在我国脑血管病占疾病病死率的第1位,约占20.1%[1]。《Global stroke statistics》同样指出,我国脑卒中的发病率、患病率、复发率、病死率均在逐年增高,中国卒中经济负担也在不断提高[2]。急性非致残性脑血管病[短暂性脑缺血发作[3](TIA)和轻型卒中[4](NIHSS≤3分)]在脑血管病中最常见[5],急性非致残型脑血管病因其“非致残性”特点,常常出现“救治不及时、不规范”等问题[6]。因此,加强对非致残性脑血管病的诊治及预防显得尤为重要。本文对比分析MRI、SPECT静息、尼莫地平负荷后显像,分析尼莫地平药物负荷脑血流灌注成像技术在非致残性脑血管病中的临床应用价值。
1 资料与方法
1.1一般资料选择2017-01-01—2017-11-01就诊于厦门大学附属第一医院神经内科的急性非致残性脑血管病患者共35例,男21例,女14 例;年龄(62.9±2.0)岁;轻型卒中25 例,短暂性脑缺血发作10例。所有患者均行1.5T或3.0T常规磁共振(T1、T2、T2-FLAIR、DWI、ADC、MRA),同时完善静息及尼莫地平负荷SPECT脑血流灌注显像。收集患者一般资料,包括年龄、性别、血糖、血压、BMI、血脂、吸烟史、血清同型半胱氨酸。
1.2纳入标准伴有以下危险因素中的1种或以上的TIA或轻型卒中(NIHSS≤3分)患者:年龄≥60岁;肥胖(BMI>24);高血压;糖尿病;高甘油三酯(≥2.3 mmol/L);高低密度脂蛋白(≥4.1 mmol/L);吸烟史>10 a;高同型半胱氨酸血症(HCY≥10 μmol/L)。
1.3排除标准(1)尼莫地平药物过敏史;(2)血压偏低(收缩压≤100 mmHg和或舒张压≤80 mmHg);(3)急性冠脉综合征;(4)2度及3度房室传导阻滞、频发室性早搏、室性心动过速、病态窦房结综合征);(5)妊娠或哺乳期女性;(6)存在其他可影响脑血流情况的症状(痴呆、帕金森等)。
1.4方法
1.4.1 试剂与显像方法:要求脑血流灌注放射性药物99mTc-双半胱乙脂(ECD)浓度为1 480~1 850 MBq/mL,剂量740~1 110 MBq/mL,标记率>95%,体积<1 mL。
1.4.2 静息显像:患者检查前30 min口服过氯酸钾封闭脉络丛,静脉埋三通管,视听封闭10 min后静脉注入 99 mTc-ECD 740~1 110 MBq(20~30 mCi)。平卧,头部固定于探头旋转中心,30~40 min后开始采集图像,采用平行孔LEGP/LEHR准直器采集SPECT图像。采集参数为3°~6°/帧,15~20 s/帧,矩阵64×64,能峰140 keV。
1.4.3 负荷成像:静息状态与尼莫地平药物负荷SPECT成像时间间隔1 d,操作步骤:①250 mL生理盐水中加入1.5 mg尼莫地平;②静滴速度控制在172 m L/h(约 2.9 mL/min);③静脉滴注约20 min后停止输液,之后立即静脉注射99m T-ECDc显像剂20~30 mCi;④注射99m Tc-ECD示踪剂后30~40 min按静息成像条件行脑SPECT成像。静脉滴注尼莫地平期间需监测患者生命体征,在静脉滴注0、5、10、15、20和30 min时间点分别测量患者的血压和心率。提前终止静脉滴注标准:①出现过敏反应;②血压明显降低 (收缩压较用药前降低 20 mm Hg以上或<85 mmHg)伴头晕、恶心、大汗等;③其他未列出的无法耐受的反应。
提前终止标准:①出现皮疹及过敏反应;②血压明显降低(收缩压较用药前降低20 mmHg以上或<85 mmHg)伴头晕、恶心、大汗等;③其他不能耐受的反应。
1.5图像分析应用半定量方法对脑血流灌注成像进行对比分析 35 例患者的负荷和静息脑血流灌注差异,同时与相应的 MRI结果对比分析。由两位放射科医师判读影像资料。
1.5.1 阳性标准:MRI阳性,局灶性神经功能缺失对应部位上呈高DWI、低ADC 信号,且责任灶符合血管区域分布。SPECT 阳性,在静息、负荷脑血流灌注横断面图像上,应用感兴趣区(ROI)技术,选择双侧小脑、额、顶、枕、颞叶、基底节和脑干的最大层面/病变最大层面勾画各部位感兴趣区(ROI),应用镜像自动生成对称部位 ROI。由软件计算 ROI的平均放射性计数并用来反应 rCBF,两侧比值法(病灶侧/镜像侧)计算病灶区/镜像区>1.1 或<0.9。
1.5.2 局部脑血流量的测定与CVR评估:局部脑血流量(rCBF)参考OGASAWARA制定的标准用放射性计数来反映[7],静息与负荷像均选择同一层面,且 ROI大小相同,若负荷与静息rCBF差值>0为CVR正常,差值≤0为 CVR 下降。
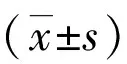
2 结果
2.1MRI与尼莫地平负荷前后SPECT脑血流灌注显像对急性非致残性脑血管病责任病灶的检出阳性率比较本组35例患者MRI、尼莫地平负荷前后SPECT显像检查结果见表1。MRI诊断阳性率为45.7%(16/35),SPECT静息及尼莫地平负荷显像诊断阳性率分别为71.4%(25/35)、91.4%(32/35)。与静息显像相比,尼莫地平负荷SPECT脑血管灌注显像可增加急性非致残性脑血管病病灶检出阳性率(P<0.05)。见图1。
2.2尼莫地平药物负荷前后的SPECT图像变化比较双侧对比各ROI负荷前后rCBF变化的四种情况:A:CVR减低:静息时rCBF 正常,负荷后减低,共5例;B:CVR减低:静息时rCBF 减低,负荷后降低无明显改善,共11 例;C 型:CVR减低:静息时rCBF 减低,负荷后降低更明显,共8例;D 型:CVR正常:静息时rCBF 降低,负荷后改善,共 11 例。对于患者的CVR正常或减低与性别、年龄、血压、血糖、吸烟史、BMI、LDL-C、CHO、HCY采用Logistic回归分析。见表2。2组在高血压、LDL-C、CHO上差异有统计学意义(P<0.05)。见图2、3。
2.3交叉性小脑失联络35例患者中6例新发脑梗死者脑血流灌注显像可见对侧小脑血流灌注减低,但MRI小脑未见明显异常。见图4。
2.4尼莫地平不良反应发生率35例患者中2例发生不良反应,均表现为血压下降,经减慢输注速度数分钟后血压逐渐平稳。

图1男性,72岁,短暂性脑缺血发作A、B(静息):右额颞顶、基底节放射性分布较对侧低;C、D(尼莫地平负荷后):缺损区范围及程度缩小;E、F(MRI):未见明显缺血灶(标注处为SPECT成像异常病灶)。
Figure1Male,72years old,transient ischemic attack A,B (resting):right frontotemporal parietal and basal ganglia have lower radioactive distribution than the contralateral side;C,D (after nimodipine load):extent of defect area the degree is reduced;E,F (MRI):no obvious ischemic focus is seen(The marked areas are abnormal lesions of SPECT imaging).

图2 男性,47岁,轻型卒中 A、B(静息显像):左额颞顶叶放射性分布较对侧低;C、D(尼莫地平负荷后):缺损区程度及范围缩小;E、F(MRI):左颞叶急性脑梗死
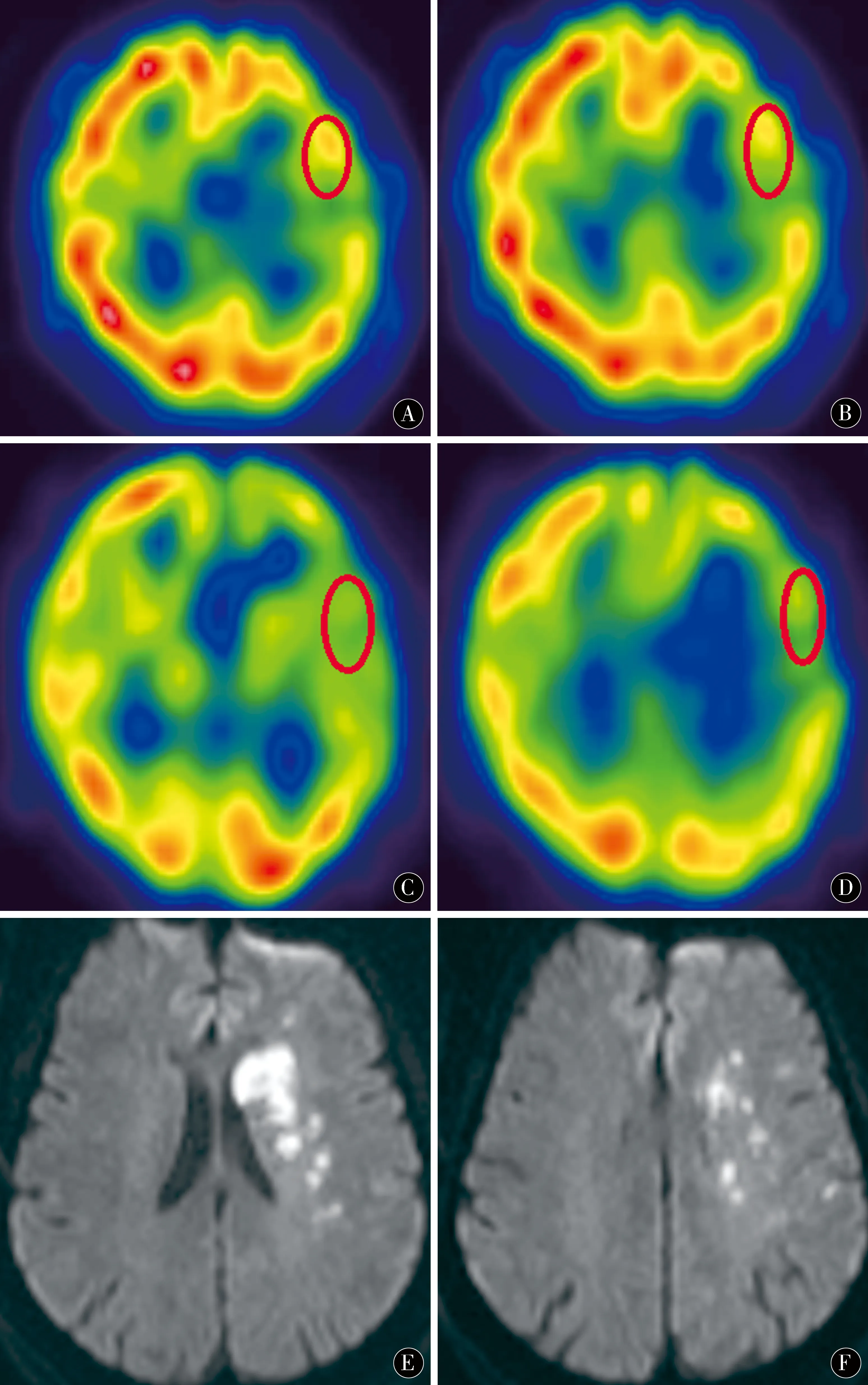
图3 男性,45岁,轻型卒中 A、B(静息显像):左额颞顶、基底节放射性分布较对侧低;C、D(尼莫地平负荷后):缺损区明显扩大;E、F(MRI):左侧放射冠急性脑梗死

图4 男性,64岁,轻型卒中 A、B:左额颞顶、基底节放射性分布较对侧低;C、D:右侧小脑灌注减低;E、F:MRI小脑未见明显异常

表1 MRI、负荷显像前后检查结果阳性率
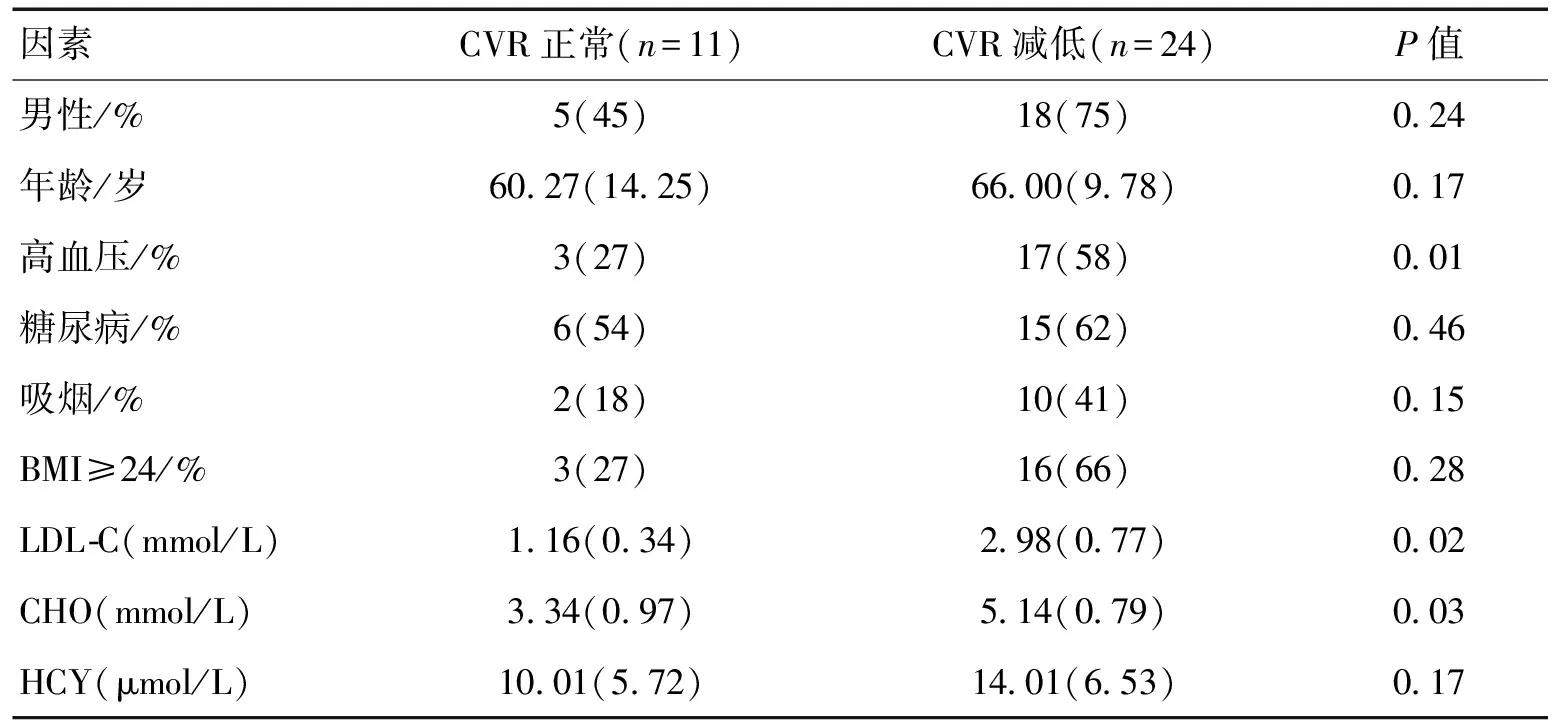
表2 CVR正常组与CVR减低组卒中危险因素比较
3 讨论
急性非致残性脑血管病因早期不稳定和复发率高等特征[8],早期规范治疗对降低致残率、减轻经济负担,改善预后有着重要作用[9]。TIA、轻型卒中发病90 d内的复发卒中风险是10%~13%,其中约50%在发病2 d内发生[10]。急性非致残性脑血管病中,SPECT 脑血流灌注显像对其治疗和预测复发都具有重要指导意义。SPECT 分析方法[11]有定量、半定量和定性分析。OKU等[12]研究证明,与定量分析方法相比,半定量分析方法的小脑比值法、对侧比值法也可以很好的显示病灶及脑血管储备功能。本研究采用半定量分析。
研究表明TIA发作间期仍存在脑血流灌注异常[13]。脑血流灌注SPECT显像提示患者的临床神经功能损害程度、TIA 发作次数与低灌注区范围呈明显正相关[14]。OKU等[12]的研究表明SPECT 灌注成像对腔隙性脑梗死和短暂性脑缺血发作的检出率高于MRI。本研究显示,MRI发现急性非致残性脑血管病病灶阳性率45.7%,低于静息与尼莫地平负荷脑血流灌注显像,SPECT灌注成像静息时阳性率为71.4%,负荷后提高至91.4%,证明负荷前后SPECT脑血流灌注成像显著提高了急性非致残性脑血管病的诊断阳性率。本研究中有1例基底节区梗死和2 例脑干梗死患者行MRI检查证实局部新发梗死灶,而SPECT 灌注成像未发现相应区域明显放射性计数减低,这与Wang等的研究结果相符[15-16]。原因可能为:大脑灰质、小脑的神经核团血流丰富、脑功能活跃,脑血流显像剂分布较多,而在以神经纤维束为主的白质中脑血流显像剂分布很少,脑干及双侧脑室旁白质区可能是SPECT脑血流灌注显像的盲区。
药物负荷SPECT试验中,乙酰唑胺负荷试验在国外应用已成熟[17],因国内无乙酰唑胺针剂,国内常用的有腺苷、潘生丁药物负荷SPECT脑血流灌注试验,各有优缺点。LIU等[18]用腺苷负荷发现联合静息及腺苷负荷试验后的SPECT评价脑血流灌注特征,能够发现腺苷负荷脑血流灌注成像(99m)Tc-ECD SPET可以识别出更多的异常rCBF脑区。既往有研究[19]将双密达莫与乙酰唑胺对比发现,双嘧达莫负荷脑SPECT可以很好的评价脑血流储备。尼莫地平负荷试验中,不良反应主要表现为颜面潮红、头晕、恶心呕吐,发生率约 4.17 %,不良事件发生概率较低。这表明尼莫地平药物负荷SPECT脑血流灌注成像具有重要的临床应用价值。本研究35例患者中仅2例患者出现不良反应,发生率约为5.71%,表现为血压下降,且症状较轻,减慢输液速度数分钟后血压平稳,无因明显不良反应而终止试验者,说明尼莫地平负荷试验安全性高。
本研究利用尼莫地平的扩张脑血管作用研究脑血管储备功能,出现了4种类型:A型,静息态血液供应尚可,但CVR差;B型,负荷态较静息态相比rCBF减低无明显改善,提示CVR差;C型,提示静息态血液供应及CVR均减低;D型,静息态脑血流供应减少,但CVR尚可。本研究发现高血压、LDL-C、CHO与脑血管储备功能下降影响较大。脑内各组织对药物负荷试验的不同反应提示CVR下降的患者预后较差[20]。研究表明[21],CVR下降者发生卒中或TIA的可能性约为正常人的4倍。LIU等[22]研究发现,CVR 受损与颅内外大动脉狭窄程度相比,能够更好的预测脑梗死的发生。有研究[23]提示,颈动脉CVR损伤与颈动脉狭窄或闭塞的缺血性事件风险增加密切相关,可能能指导卒中风险分层。TOMURA等[24]认为,静息rCBF与颈内动脉狭窄程度无明显关系,而CVR与颈内动脉狭窄程度明显相关。CVR下降可以早期预测缺血性脑血管病风险,发现脑梗死高危人群,及早进行干预[25]。
本研究中6例患者SPECT显像出现交叉性小脑失联络现象(CCD)。CCD 指的是大脑半球脑组织一侧损伤后,其对侧的小脑半球出现葡萄糖代谢或血流灌注减低的现象。目前尚不明确其确切发生机制,其在脑梗死患者中最常见,发生率为50%~70%[26]。皮质-脑桥-小脑(cortical-ponts-cerebellum CPC)纤维束目前被认为与CCD的发生有关[27]。CPC 传导通路由大脑额顶叶皮层下传至同侧脑桥,后从脑桥传导至对侧小脑半球。CPC的中断可导致相应的对侧小脑血流灌注量的减低[28]。CHEN等[29]研究表明CPC的中断导致对侧小脑功能障碍。CT及MRI上无法揭示此种现象[30],这也体现了脑血流灌注SPECT显像的又一优势。
综合分析说明,联合尼莫地平负荷前后脑血流灌注SPECT显像可提高急性非致残性脑血管病诊断阳性率,评估脑血管储备力,尼莫地平负荷脑血流灌注显像安全有效。
