碳酸钙复合载药纳米粒的制备与表征
2019-12-24谷峙樾赵健辉刘占军
谷峙樾 雷 宇 赵健辉 刘占军
华北理工大学药学院,河北唐山 063000
纳米载药系统作为一种新兴的给药方式,纳米粒吸附或静电力接合药物在缓控释药物应用上更有利[1]。无机空腔纳米球作为药用载体有很多好处,它们容易制成确定大小的纳米粒[2],另外在合成上,无机空腔纳米球比聚合物空腔纳米粒易于合成且具有更高稳定性,不易形成塌陷[3]。尤其是空腔结构的碳酸钙可以用作药用载体和诊断标记物,如其它的空腔纳米球一样,它除了具有优越的生物相容性外,还可生物降解,在体内具有很好的酸度响应性,不至于发生反应和降解[4-6]。主要研究如何制备出更适宜载药的碳酸钙空腔纳米球并进行载药。海藻酸钠是一种生物相容性很好的天然高分子。海藻酸钠溶液可以与二价以上金属离子形成盐而凝固[7-9]。因此我们选择海藻酸的钠盐来修饰碳酸钙空腔纳米粒来提高空腔纳米粒的稳定性。制备出的复合纳米粒用激光粒度分析仪、TEM 对其进行表征测定纳米粒径[10-11]。
1 实验部分
1.1 实验材料
十六烷基三甲基溴化铵(分析纯,天津市福晨化学试剂厂);碳酸钠(分析纯,天津河西工业气体有限公司);氯化钙(分析纯,天津市江天化工技术有限公司);盐酸阿霉素(分析纯,天津市福晨化学试剂厂);高速离心机3K30(德国Sigma 公司);不锈钢加热磁力搅拌器RET[艾卡(广州)仪器设备有限公司];电热恒温鼓风干燥箱DHG-9101.2(金坛市荣华仪器制造有限公司);UPWS 超纯水器UPWS-I-10T(杭州永洁达净化科技有限公司);真空干燥箱DZ-1BC(天津泰斯特仪器公司);透射电子显微镜H-7650(日本HITACHI 公司)。
1.2 碳酸钙空腔纳米球的制备
(1)精确称取0.1g 的十六烷基三甲基溴化铵加入到盛有100mL 去离子水的500mL 的烧杯中,将烧杯置于恒温磁力搅拌器上恒温30℃,600r/min,溶解20min,不断搅拌加速溶解,搅拌使十六烷基三甲基溴化铵完全溶解至溶液无色。(2)取制备好的0.1mol/L Na2CO3溶液50mL,加入到上步所得的溶液中,继续搅拌20min,维持反应温度和转速均不变。(3)取制备好的0.1mol/L CaCl2溶液50mL,加入到上步所得溶液中,将温度降至0,转速缓慢升高到1200r/min,将氯化钙溶液逐滴从旋转中心至边缘中间部位加入(若在旋涡中心处加入则转速过低,会形成较大且不规则的碳酸钙纳米粒;若在边缘处滴加则转速过快容易附着在玻璃容器内壁上降低了纳米粒的均一性),滴加时间在30min 左右,滴加完成后继续搅拌5min,反应温度一直维持在5℃以内。(4)用离心机4000r/min 离心20min,得到沉淀,沉淀用50%乙醇洗涤3 次洗涤后继续用离心机4000r/min 离心,放入干燥箱80℃干燥12h,在放入马沸炉中150℃煅烧4h,收集[12]。(5)在固定十六烷基三甲基溴化铵的量,且碳酸钠和氯化钙的投料比为1 ∶1 后,探究了碳酸钠浓度分别为0.005、0.01、0.02、0.04、0.08mol/L 五组不同浓度实验;在固定十六烷基三甲基溴化铵的量,投料比和浓度后进行了300、500、700、1000、1500r/min 五组不同转速实验;在固定十六烷基三甲基溴化铵的量,投料比,浓度和转速后进行了0、10、20、40、60℃五组不同温度的实验,目的是探究碳酸钙空腔纳米粒的最佳制备条件。
1.3 透射电镜观察
将最佳条件下制备得到的碳酸空腔纳米粒置于透射电镜下观察形态结构。并观察不同温度条件下碳酸钙空腔纳米粒的结构。
1.4 碳酸钙空腔纳米球的修饰及电位
选取纳米粒形态较好的且分散性和均一性均不错的进行载药后,测量其载药量。精密称取0.1mg CaCO3空腔纳米球冻干干燥粉,将其用超声仪超声分散于10mL 去离子水中,精密称取0.1mg 海藻酸钠,将其用超声仪超声分散于10mL 去离子水中,充分搅拌,使海藻酸钠完全溶解。将纳米球溶液滴加到海藻酸钠溶液中,搅拌30min,300r/min,25℃,反应结束之后4000r/min 离心20min,用去离子水洗涤两次,采用冷冻干燥零下20℃干燥12h,收集[13]。分别取0.1mg 的碳酸钙空腔纳米粒、ALG-CaCO3-P53、ALG-CaCO3-DOX-P53、ALG-CaCO3-DOX 四 种 纳米粒的Zeta 电位。
2 结果
2.1 激光粒度分析仪检测结果及分析
2.1.1 不同浓度的粒径 在十六烷基三甲基溴化铵的量和其他反应条件不变情况下,碳酸钠和氯化钙的浓度分别在0.020mol/L 时所得到的碳酸钙空腔纳米球粒径最小。见表1。
碳酸钙空腔纳米粒的粒径在0.020mol/L 时相对较小。本研究开始已经进行了碳酸钠浓度和氯化钙浓度浓度梯度从0.001 ~ 0.2mol/L 的测定,结构发现浓度高于0.1mol/L 则粒径过大,会产生团聚现象而且会持续不断生成碳酸钙沉淀而导致粒径过大。
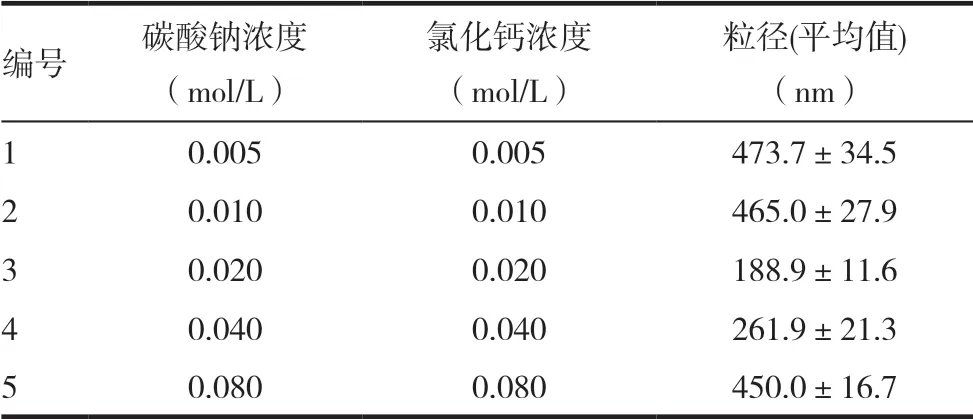
表1 不同浓度的粒径
2.1.2 不同反应转速的粒径 在十六烷基三甲基溴化铵的量和其他反应条件不变情况下,反应转速在1000r/min 时所得到的碳酸钙空腔纳米球粒径最小,之后还会在1000r/min 周围进行研究探究出转速最佳条件。见表2。
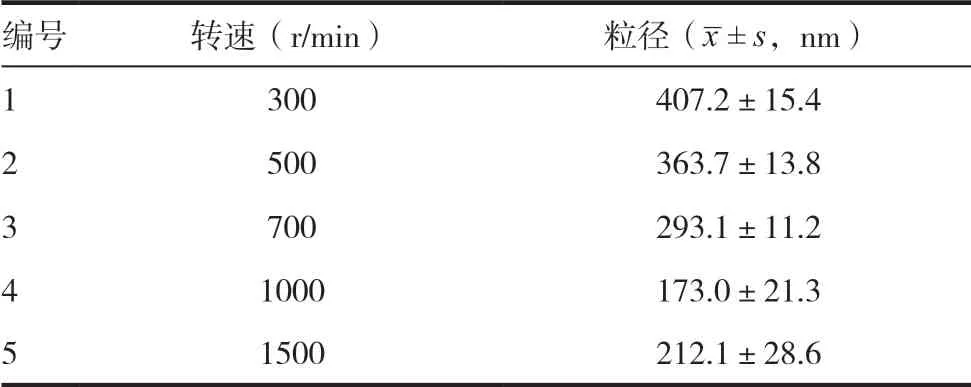
表2 不同反应转速的粒径
2.1.3 不同反应温度的粒径 碳酸钙空腔纳米粒的粒径在20℃时相对较小。在十六烷基三甲基溴化铵的量和其他反应条件不变情况下,反应温度在20℃时空腔纳米球粒径最小。见表3。
2.2 透射电镜结果及分析
制得的碳酸钙空腔纳米粒其外观圆整,呈球形或类球形颗粒状分布,中间有明显空腔,粒径大致分布在(196±2)nm 左右,均一性良好且分散性良好。见图1。
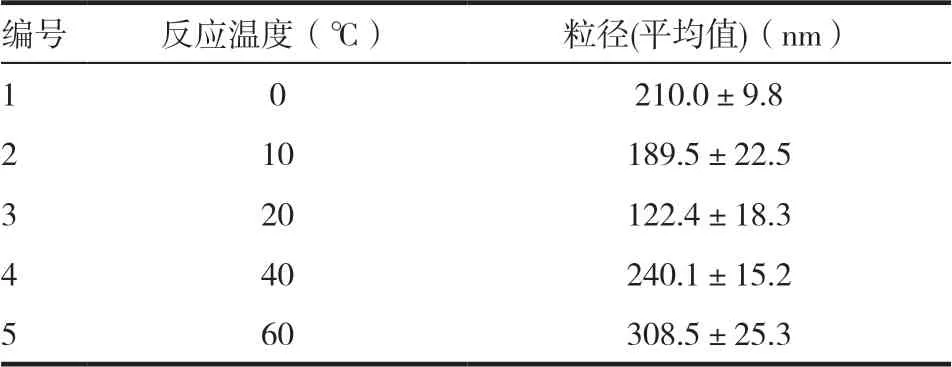
表3 不同反应温度的粒径
在10、20、40℃均出现明显的空腔结构,在0、60℃时无明显的空腔结构,因为温度较低时直接形成了碳酸钙结晶,温度较高时反应过于剧烈,形成的碳酸钙多为片状结构。见图2。
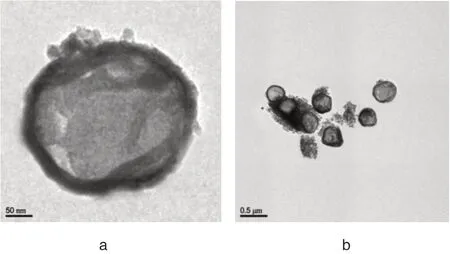
图1 透射电镜照片

图2 不同温度下透射电镜照片
2.3 碳酸钙空腔纳米球修饰后的粒径及电位
相对于碳酸钙空腔纳米粒电位为(-10.08±0.17)mV,表面带负电荷的海藻酸钠修饰后的CaCO3-ALG-P53 和CaCO3-ALG-DOX-P53 纳 米 粒 子 电位分别为(-27.20±0.75)mV 和(-21.53±0.24)mV,经海藻酸钠修饰后电位明显降低,稳定性更好。P53 作为带负电的质粒其也增加了复合纳米粒的负电从而使其更稳定,但P53 所带电荷相对较少因此对整体电位的影响并不多。见表4 ~ 5。

表4 纳米粒载药后的粒径

表5 不同载药种类的电位
3 讨论
本研究开始进行了碳酸钠浓度和氯化钙浓度浓度梯度从0.001 ~ 0.2mol/L 的测定,结构发现浓度高于0.1mol/L 则粒径过大,在超过0.1mol/L 浓度之后因为浓度过大因此快速生成碳酸钙结晶沉淀,同时会产生团聚现象而且会持续不断生成碳酸钙沉淀,因此产生的碳酸钙纳米粒壁过厚再加上多个碳酸钙纳米粒团聚在一起由碳酸钙结晶粘附在一起,而导致粒径过大。当浓度低于0.01mol/L 时,其在十六烷基三甲基溴化铵表面结晶不完全,在表面无法形成完整的碳酸钙空腔纳米球,大多呈现长条状或半圆状,因此其粒径测量平均值虽然为465.0nm,但测量值是由布朗运动等效而来的,其真实粒径值并没有如此大,但是足以证明其形成的结晶沉淀不规则且均一性不好,因此最佳浓度为0.020mol/L。通过探究了反应转速500、1000、1500r/min 三组不同转速实验,对其最佳的反应转速进行了研究,由表2 可知碳酸钙空腔纳米粒在1000r/min 的时候纳米粒粒径相对较小,当反应转速为500r/min 较低时其粒径平均值为363.7nm,溶液滴入到十六烷基三甲基溴化铵溶液后其反应是不完全的,溶液中离子浓度分布不均,因此导致形成的碳酸钙纳米粒的均一性不好而且容易形成颗粒较大的碳酸钙纳米粒。当反应转速为1500r/min 过高时其纳米粒径平均值为212.1nm,由于包裹物十六烷基三甲基溴化铵在去离子水中转速过高是会产生泡沫,因此当转速过高时加入的氯化钙溶液会残存于表层,导致反应不完全,而且表面形成的碳酸钙纳米粒过大不合标准。探究了0、10、20、40、60℃五组不同温度的实验,对其最佳的反应温度进行了研究,由表3和图2 可知碳酸钙空腔纳米粒的粒径在20℃的时候相对较小。当温度为0 时其纳米粒径平均值为210.0nm,虽然其纳米粒径不大但是其透射电镜下观察发现其形成的纳米粒不规则,多见单独存在的碳酸钙结晶沉淀,围绕在较大纳米粒周围会有诸多小的结晶晶体结构;当温度为60℃时其纳米粒径为308.5nm,由于反应快速进行,因此所形成的的碳酸钙纳米粒壁薄厚不一,其物理稳定性不稳定高温过程中易出现破碎的现象,纳米粒碳酸钙结晶壁较厚载药量也相对较低,因此20℃为最佳的制备温度,此温度下制备的碳酸钙空腔纳米粒物理性质稳定,空腔壁薄厚适中载药量相对较大,纳米粒径相对较小有助于其在体内的代谢。
由表4 可以看出相对于碳酸钙空腔纳米粒,CaCO3-ALG-P53 和CaCO3-ALG-DOX-P53 的复合纳米粒粒径变大,负载了盐酸阿霉素之后其粒径会较之前变大。由表5 可以看出Zeta 电位,相对于碳酸钙空腔纳米粒,表面带负电荷的CaCO3-ALG-P53和CaCO3-ALG-DOX-P53 纳米粒子电位明显降低,稳定性更好。加入盐酸阿霉素后,相比CaCO3-ALG-P53 纳米粒子,CaCO3-ALG-DOX-P53 纳米粒子粒径变大,由于阿霉素带正电,使得整个纳米粒子的电位稍微升高一些,但负电荷依旧较高对其稳定性影响不大。因此海藻酸钠的引入增加了碳酸钙空腔纳米粒的稳定性使其能够负载药物而且稳定存在。
盐酸阿霉素可以插入碱基对之间形成一种较为稳定的结构,从而使癌细胞停止转录而死亡从而达到杀死癌细胞的目的,加入盐酸阿霉素后,相比CaCO3-ALG-P53 纳米粒子,CaCO3-ALGDOX-P53 纳米粒子粒径变大,由于阿霉素带正电,使得整个纳米粒子的电位稍微升高一些,但负电荷依旧相对较高对其稳定性影响不大。因为碳酸钙纳米粒在高温条件下可以去除有机物残留,同时会让碳酸钙纳米粒表面形成多孔结构,大量的纳米孔径可以使得基因药物P53 通过毛细管力更好的负载进入到碳酸钙空腔纳米粒内部[14-15]。同时海藻酸钠与钙的交联作用粘附在纳米粒表面,所带负电荷可以对带正电的盐酸阿霉素进行吸附,其对带正电的吸附力可以保证复合纳米粒在机体内持续稳定的释放。
