放疗联合阿帕替尼、多西他赛治疗晚期肺癌的临床疗效研究
2019-12-23牛东升孙丽敏
牛东升 孙丽敏
肺癌是目前全球发病率最高的实体恶性肿瘤[1],血管内皮生长因子(VEGF)是肺癌比较重要的靶点[2],阿帕替尼是VEGF靶点的抑制剂,联合其他治疗手段时,疗效较好,与化疗药物合用可增强疗效[3-4]。目前,对放疗联合VEGF靶点抑制剂、多西他赛化疗治疗晚期肺癌的报道较少[5-6],本研究应用阿帕替尼、多西他赛联合放疗对晚期肺癌进行疗效观察,对我院探讨放疗联合VEGF靶点抑制剂、化疗药物治疗的疗效,探讨1种更为有效的治疗方法,以期为临床工作提供参考,报告如下。
1 资料与方法
1.1 一般资料
选择69例2015年8月至2017年7月于我院呼吸内科及肿瘤科就诊的晚期肺癌患者。将69例患者分为对照组和治疗组。对照组32例,男性15例,女性17例,年龄51~81岁,平均(71.5±7.7)岁,病理类型:小细胞肺癌5例,鳞癌11例,腺癌8例,腺鳞癌8例;按国际抗癌联盟分期标准Ⅲa期5例,Ⅲb期12例,Ⅳ期15例;治疗组37例,男性18例,女性19例,年龄50~79岁,平均(65.5±7.9)岁,病理类型:腺癌10例,鳞癌13例,腺鳞癌7例,小细胞肺癌7例;临床分期:Ⅲa期8例,Ⅲb期16例,Ⅳ期13例。统计分析发现,2组患者年龄、性别、肺癌分期及病理分型无差异(P>0.05),各项资料均具有可比性。纳入标准:①病理及细胞学等临床检查符合晚期肺癌标准,影像学检查结果显示存在1个及以上可测量病灶;②年龄≥18岁;③预期生存时间>3个月;④卡氏(KPS)评分≥60分;⑤化疗前基本血生化、血常规及心电图等检查无异常;⑥充分了解实验内容,自愿参与并签署知情同意书,符合医学伦理学要求。排除标准:①有放疗禁忌症或对实验药物过敏;②依从性差,放疗照射野区皮肤病或过敏肤质者;③存在严重肝肾功能与凝血功能障碍、有严重高血压及糖尿病未控;④有传染或感染性疾病或精神障碍患者。本研究方案由我院医学伦理委员会审查批准,所有患者治疗前了解治疗方案及替代治疗方案并签署知情同意书。
1.2 治疗方法
对照组进行放疗和阿帕替尼单一靶点抑制剂治疗,治疗组进行放疗和阿帕替尼加多西他赛治疗。对照组:①放疗采用医科达precise直线加速器对胸部患区实施全程三维适形放疗(threedimensionalconformalradiationtherapy,3DCRT),射线能量6MV-X线,precise计划系统,常规分割放疗,采用患者仰位,并用真空体模翼板固定,CT扫描定位,层厚5 mm,用MOSAIQ系统进行网络数据传输和处理,5次/周,连续放疗6周;②靶向药物治疗:采用阿帕替尼(江苏恒瑞医药股份有限公司,规格250 mg,国药准字H20140103)500 mg/次,每天一次,餐后半小时口服治疗。阿帕替尼剂量在治疗期间可因不良反应进行适当调整。治疗组:在对照组的基础上给予多西他赛(江苏恒瑞制药有限公司,国药准字H20020543,20 mg×1支)60 mg/m2/次,静脉滴注,滴注时间大于60 min,每三周重复一次,重复两个周期。所有患者靶向治疗均监测用药6周,定期观察病情进展,密切关注患者出现不能耐受或其他异常情况,对于出现Ⅳ级骨髓抑制者,或出现阿帕替尼或多西他赛Ⅲ~Ⅳ级相关不良事件,则相应的靶向治疗药物阿帕替尼或多西他赛使用剂量降低25%,至不良反应好转。期间观察中位生存时间、中位无进展生存时间(progression-freesurvival,PFS)以及不良反应的发生情况,同时2组患者均给予常规的血常规、尿常规、心电图和胸片检查。
1.3 观察指标
本研究的主要观察指标:①功能状态(karnofsky,KPS)评分[5]:采用KPS量表进行评分,得分越高,功能状态越好;②疗效评价:用实体瘤的疗效评价标准(RECIST)1.1版[7]对疗效进行评价,其中疗效评价包括完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。每三周化疗后复查头部MRI和颈、胸、腹部CT进行疗效评价,客观缓解率ORR=(CR+PR)/总例数×100%,疾病控制率DCR=(CR+PR+SD)/总例数×100%;③不良反应参照WHO抗肿瘤药物不良反应事件评价分度标准,不良反应Ⅲ、Ⅳ度者作为观察指标。对患者数据根据科室登记随访系统进行统计,所有患者采用返院复查或电话方式随访。
1.4 统计学分析

2 结果
2.1 KPS功能评分比较
患者接受不同方式的治疗后,KPS评分两组均明显升高,与放疗加靶点抑制剂对照组比较,放疗加多西他赛加靶点抑制剂治疗组KPS评分高于对照组,有差异但无统计学意义(P<0.05),见表1。
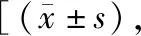
表1 2组患者治疗前后KPS评分情况分]
2.2 临床疗效分析
放疗加靶点抑制剂加多西他赛治疗组和放疗单加靶点抑制剂对照组的DCR分别为81.08%和56.25%(P=0.0254);治疗组和对照组的ORR分别为48.65%和25.00%(P=0.0432)。两组差异有统计学意义,P<0.05,见表2。

表2 2组患者疗效比较(例,%)
2.3 不良反应情况分析
治疗过程中,Ⅲ、Ⅳ度不良反应两组均有出现,骨髓抑制和消化道反应两组差异不大,无统计学意义(P>0.05);与对照组相比,治疗组在皮疹脱发不良反应方面要重些,尤其是皮疹。但可以耐受,差异有统计学意义(P<0.05),见表3。
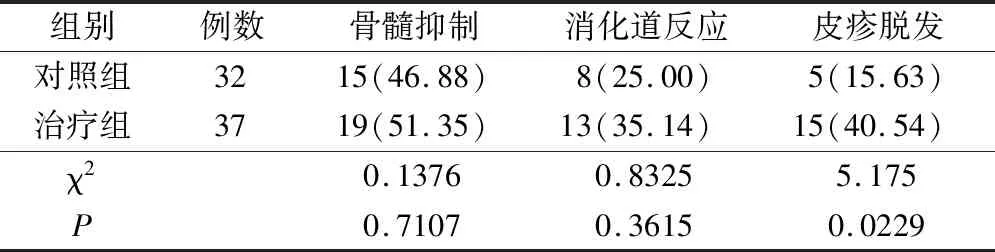
表3 两组患者不良反应情况(例,%)
3 讨论
肺癌的发病率和死亡率均高居各种肿瘤首位,作为第一常见癌症,严重威胁着人们的健康。对于晚期的肺癌,化疗和放疗是标准的治疗方案,是缓解病情,提高生活质量,延长生存时间的主要方法,然而,也有文献报道其疗效不佳[8],大多数患者经历放射治疗后6个月内会出现PD。在放疗过程中,肿瘤细胞出现抵抗的现象,比如,在实体瘤中会产生对放射线抵抗的低氧细胞,临床资料表明[9-10],Ⅲ期肺癌单纯放疗后的局部未控率和复发率可高达60%~80%,研究中还发现若放射治疗剂量增加,虽然肿瘤控制率有所升高,但周围正常组织器官的急慢性毒副作用却大幅增加。因此,如何在提升放疗疗效的同时减少正常组织损伤,减少毒副作用,一直是医生及科研工作者关注的焦点。
有研究[11-12]指出晚期肺癌细胞向周围侵犯并向远处转移是导致晚期肺癌疗效低下的重要原因,其病理基础就是肿瘤血管的不断生成,因此,抑制肿瘤血管生成具有直接抑制肿瘤生长及转移的作用,抗新生血管治疗已成为当今肺癌治疗的1个重要方面[13-14]。血管生长因子(VEGF)是血管新生的关键因素,是目前所知作用最强、特异性最高的因子之一[14],目前临床应用VEGF抑制剂较多的是阿帕替尼[15],阿帕替尼是1种TKI,1种重组人单克隆抗体[16],其以VEGF为靶点,其在低的浓度即能有效抑制VEGFR-2酪氨酸激酶活性[17],与VEGF结合后能选择性抑制VEGFR2介导的内皮细胞的迁移和增殖,发挥其生物学拮抗其作用,从而阻断或减缓肿瘤血管的生长以及肿瘤细胞侵袭和迁移。近来研究表明[18],放疗联用抗血管生成类药物时疗效显著,因此,对于放疗耐受性差的患者,可联用抗血管生成类药物,在不改变疗效情况下,降低放射剂量,减少放疗副作用,从而提高患者对放疗的依从性和生活质量。既往的多中心随机对照试验表明阿帕替尼是晚期肺癌标准的二线治疗方案,另有研究显示[19-20],VEGF基因突变能够上调肿瘤细胞程序性凋亡因子1(programmed death-1,PD-1)受体及其配体(PD-L1)的表达,通过VEGF基因抑制剂间接使PD-L1表达水平明显下降。晚期肺癌患者接受血管内皮生长因子受体-酪氨酸激酶抑制剂(VEGFR-tyrosine kinase inhibitor,VEGFR-TKI)治疗后,PD-L1表达水平明显下降。众所周知,阻断PD-L1/PD-1通路可达到治疗肿瘤的效果。研究显示[21],同步放化疗后中位PFS时间为8~10个月,在同步放化疗的基础上进行VEGF靶点的抑制剂的巩固治疗,PFS可达16.8个月,时间延长了11.2个月,多西他赛是临床常用治疗晚期肺癌的药物[22],与放疗联合应用可以提高放疗敏感性和患者生存率[23],联合VEGF靶点的抑制剂可以提高患者的中位生存时间和五年生存率。
目前,国内外已经将阿帕替尼和多西他赛广泛应用于治疗肺癌,本研究旨在评估放疗联合阿帕替尼和多西他赛对晚期非小细胞肺癌患者的疗效、安全性。本研究结果显示,放疗联合阿帕替尼、多西他赛治疗晚期肺癌显示出良好疗效,其中治疗组DCR值81.08%明显高于对照组56.25%,差异显著。治疗组常见的不良反应包括骨髓抑制、消化道反应比对照组略高,与对照组相比治疗组在皮疹脱发不良反应方面要重些,尤其是皮疹,但可以耐受。治疗的不良反应总体可控,但在临床应用阿帕替尼和多西他赛联合用药时,需要严密监测患者血常规及凝血功能,密切观察患者病情变化,以避免严重不良反应导致危及患者生命。因此,在进行联合用药时,要特别注意给药方式、剂量、疗效,同时,不良反应监测都尤为重要。目前,放疗联合抗血管生成及化疗治疗方法尚未成熟,用药还需大样本临床数据的支持。期待放疗联合VEGF靶点抑制剂和多西他赛化疗的应用在治疗晚期肺癌辅助治疗能有进一步推进,丰富肺癌的巩固和维持治疗的手段,使得获益人群覆盖各个阶段和分期的肺癌患者。本研究运用放疗联合VEGF靶点抑制剂与多西他赛化疗治疗晚期肺癌为肺癌综合治疗带来诸多思考与启示,同时也存在不足之处,病例数也较少,随访时间较短,未统计患者的长期生存率,作为新辅助治疗和辅助治疗的患者是否能够长期获益仍需更长时间的随访来验证,另外,放疗联合VEGF和化疗用药方式的选择(同时给药或序贯给药)仍需要更大样本的前瞻性研究来验证。因此,需要在后续的研究中增加病例数,延长随访时间,使研究的数据更加完善。综上所述,放疗联合阿帕替尼(VEGF靶点抑制剂)和多西他赛可显著提高晚期肺癌治疗的DCR和ORR而且不良反应可控,值得临床推广。
