溶剂热法制备SrWO4:Dy3+荧光粉及其发光性质研究
2019-12-18李琳琳吴天娇张冬洋
李琳琳,吴天娇,张冬洋
稀土离子具有丰富的4f、4f5d电子组态能级结构,当电子在这些不同能级之间跃迁时会产生非常多的激发谱线和发射谱线.与其他荧光材料相比,稀土发光具有一系列优点:吸收能力强、转换效率高、色纯度高、发射光谱范围广,可发射从紫外到红外的光谱,特别在可见光区有很强的发射能力[1-2].因此稀土发光材料已经广泛应用于显示显像、光电子器件、照明光源以及医学监测等方面[3].其中的稀土离子 Dy3+发射光谱主要由4F9/2→6H15/2跃迁对应的蓝光发射带和4F9/2→6H13/2跃迁对应的黄光发射带组成[4].其中,4F9/2→6H13/2为超敏跃迁,发光强度受Dy3+周围的晶体场影响,相反,4F9/2→6H15/2为磁偶级跃迁,很难受到周围环境的影响[5].由于适当比例的蓝光和黄光可以复合成白光,所以在适合的晶格点阵中,Dy3+能够实现白色发光.
钨酸盐多用作功能材料,其中单钨酸盐CaWO4、SrWO4以及BaWO4具有四方晶系白钨矿结构,空间群为I41/a.在单钨酸盐中,每个W6+离子中心格位与四个O2-配位,形成了一个WO42-四面体,使其相对稳定.碱土金属离子与相邻的四个WO42-中的八个O2-配位,具有S4对称性,没有反演中心[6].钨酸根基团可以很好地吸收紫外光区域的能量,而且吸收后的能量可以从钨酸根传递到稀土离子,从而大大提高稀土离子掺杂荧光粉的外部量子效率[7].因此,单钨酸盐将会是稀土离子掺杂适宜的材料.
溶剂热合成法可称为热液法,是液相化学法的一种.在密闭压力容器中,用水或有机物作为溶剂,原料在高温高压条件下进行化学反应.溶剂热合成法能够以单一反应步骤完成.此体系对原材料的要求比高温固相反应的要求低,原材料范围广;而且溶剂热合成法制备的样品纯度高,粒径小[8].
本研究采用溶剂热合成法制备了Dy3+掺杂的SrWO4荧光粉,并对其结构、形貌、激发光谱和发射光谱进行了研究.
1 实验部分
1.1 仪器和试剂
(1)仪器.电子分析天平、磁力搅拌器、不锈钢反应釜、电热鼓风干燥箱、离心机以及数控超声波清洗器.
(2)试剂.Na2WO4·2H2O(分析纯);Sr(NO3)2(分析纯);Dy2O3(纯度99.99%);硝酸(分析纯);无水乙醇(分析纯);乙二醇(分析纯);去离子水.
1.2 样品制备
以纯水溶剂中制备0.002 mol SrWO4:0.05 Dy3+为例,具体实验步骤如下:在不断搅拌的条件下将0.018 7 g的Dy2O3溶解于稀硝酸,通过加热将过量的HNO3除去.称取0.540 7 g的Sr(NO3)2以及20 mL去离子水加入到上述溶液中,形成无色的混合溶液,记作 Sr(NO3)2:Dy3+.同时,将0.659 7 g的Na2WO4·2H2O溶解于15 mL去离子水中.然后在剧烈搅拌下缓慢将 Sr(NO3)2:Dy3+混合溶液滴入Na2WO4溶液中,在玻璃烧杯中立即会观察到白色沉淀.最后,将前驱体溶液转移到50 mL聚四氟乙烯内衬的不锈钢高压反应釜中,120oC下反应12 h,将反应釜自然冷却至室温.通过离心分离,用去离子水和无水乙醇洗涤几次,在70°C真空烘箱中进行干燥,得到最终的SrWO4:0.05Dy3+样品.
分别在以下溶剂:14 mL乙二醇+21 mL H2O、7 mL乙醇+28 mL H2O、35 mL H2O中按以上步骤制备样品,研究溶剂对形貌和发光性质的影响.
1.3 样品的测试与表征
采用日本理学D/max-II B X射线粉末衍射分析仪对样品的结构进行了测试,扫描速度为10°/min、扫描角度为 10°~80°、辐射源为 Cu 靶(λ=0.154 06 nm).采用场发射扫描电子显微镜(SEM,S-4800)测试所合成产物的形貌,加速电压为10 kV.采用日本日立F-7000分光光度计测试了样品的激发光谱和发射光谱,其中激发光源为150 W Xe灯.所有测试均在室温下进行.
2 结果与讨论
2.1 物相及形貌分析
图1为不同溶剂组成情况下制备的SrWO4:0.05Dy3+典型样品的X射线衍射(XRD)图,通过与SrWO4标准卡片对比发现,样品的XRD图与白钨矿结构SrWO4的标准卡片基本一致(JCPDS No:08-0490),没有其他杂质峰的出现,表明所得的荧光粉均为纯相的白钨矿结构,掺杂的Dy3+在合成过程中没有引起任何明显的相变.由于Dy3+离子半径与Sr2+的离子半径比较接近,所以在四方相白钨矿结构的SrWO4基质中,Dy3+离子将占据Sr2+的格位[9].从图 1中也可以看出,稀土离子成功地掺杂进SrWO4基质晶格中,没有明显改变其晶体结构.
另外,对比图1中衍射峰的宽度可以发现,随着有机物分子量以及加入体积的增加,衍射峰逐渐变宽.这表明加入有机物越多将越不利于SrWO4晶体结构的结晶,可能归因于乙醇和乙二醇中的羟基有较强的螯合能力[10].
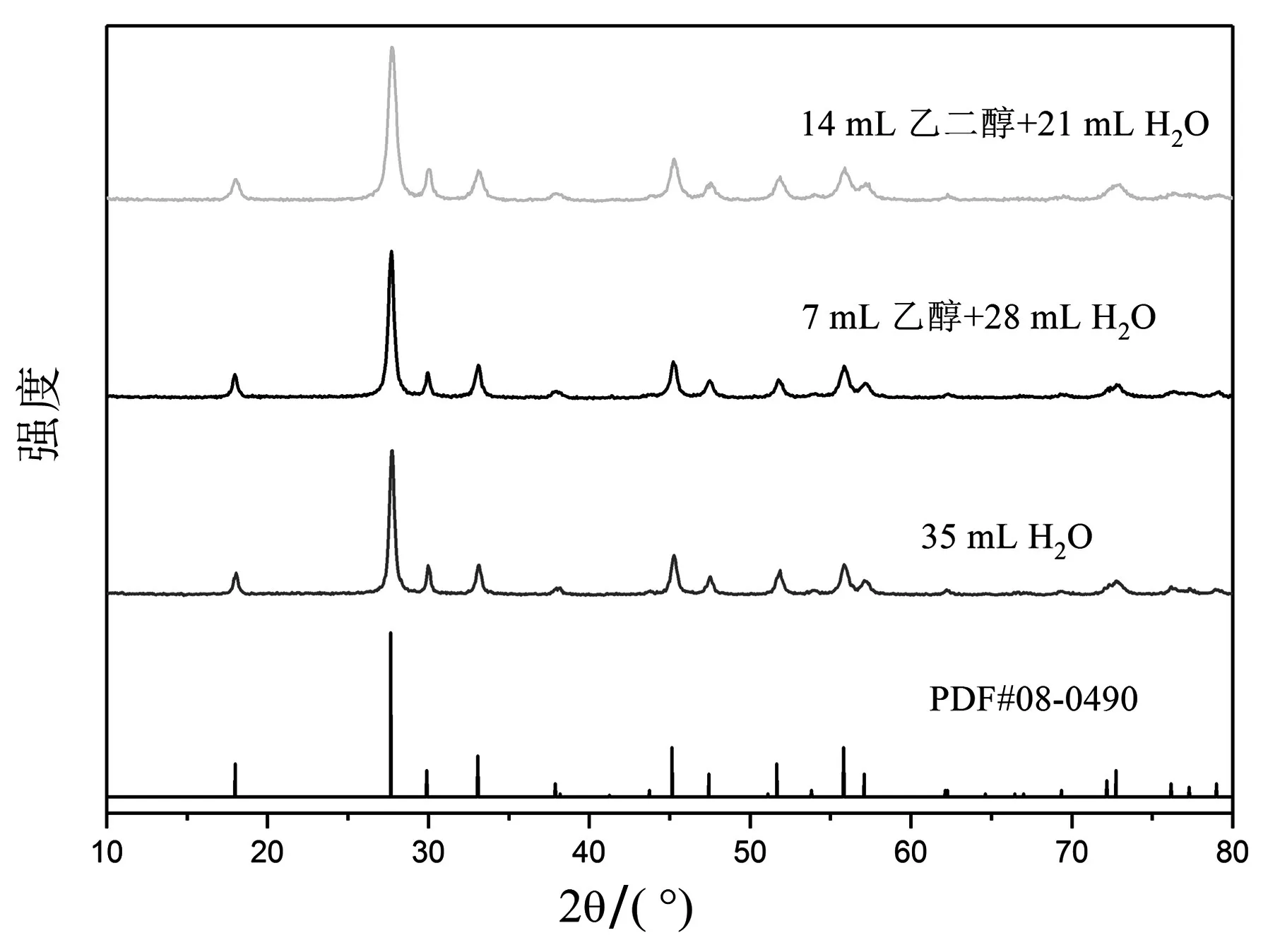
图1 不同溶剂下合成样品SrWO4:0.05Dy3+的X射线衍射图谱
图2为在不同溶剂条件下制备样品的扫描电镜(SEM)照片.如图2a所示,在纯水条件下制备的SrWO4样品是由汉堡状结构组成.这些微米汉堡的直径大约是6 μm,而且每一个微米汉堡状SrWO4颗粒都有一个分界线,将其划分为两个半球或四分球,这一现象是由于孪晶和晶体劈裂造成的.此外,所制备的SrWO4微米结构由许多小颗粒组成,有粗糙的表面.加入7 mL乙醇之后,样品的形貌发生很大的变化,从图2b可以看出,此时的样品由大小均一单分散的爆米花形貌组成,直径大约为1 μm,而且表面变得更加粗糙.图2c为14 mL乙二醇和21 mL H2O的混合溶剂下制备的样品,从图2c可以清晰地看出球状的SrWO4:0.05Dy3+平均直径约为2 μm.
在此实验中,样品的形貌随溶剂的组成而变化.根据实验现象和结果,这些形貌可能是通过以下三个阶段形成的.首先,快速成核阶段.在初始阶段,两种分别含Sr(NO3)2和 Na2WO4的溶液直接混合,形成微小的SrWO4核.其次,溶解、重结晶阶段.当沉淀转移到反应釜中,在溶剂热条件下,SrWO4核开始溶解并逐渐释放出Sr2+和WO42-离子.最后,进一步增长阶段.通过静电相互作用以及在使系统的总自由能最小化的驱动下,每个粒子在反应过程中相互聚集,最终导致上述不同形貌的形成.三种溶剂中的水、乙醇和乙二醇对金属离子具有不同的络合能力,从而使其中的SrWO4核生长和溶解的速度不同,最终使得到的样品形貌随溶剂的不同发生改变[11].

图2 不同溶剂下合成SrWO4:0.05Dy3+样品的扫描电镜图
2.2 荧光粉SrWO4:Dy3+的发光特性
图3为Dy3+离子单掺SrWO4荧光粉的激发光谱和发射光谱.左侧为在573 nm光的监测下,SrWO4:0.05Dy3+的激发光谱.从图3中可以看出,激发光谱由两部分组成.从220 nm到320 nm的宽峰是由于O2-→W6+以及O2-→Dy3+的电荷迁移带引起的.另一部分包括一些位于354 nm、369 nm、390 nm、429 nm、455 nm和477 nm尖锐的激发峰.这些激发峰归属于Dy3+离子从基态6H15/2到各激发态6P7/2、6P5/2、4F7/2+4I13/2、4G11/2、4I15/2、4F9/2的跃迁[12].最强的激发峰位于351 nm处.
在351 nm光的激发下相应的发射光谱主要包括位于蓝光和黄光区域的两个发射峰.位于478 nm和485 nm的蓝光发射对应于4F9/2→6H15/2跃迁,而位于约573 nm的黄光发射属于4F9/2→6H13/2跃迁[13].众所周知,4F9/2→6H15/2跃迁属于磁偶极跃迁,受Dy3+离子周围晶体场的影响很小.而4F9/2→6H13/2跃迁属于电偶极跃迁(ΔJ=2),易受Dy3+周围化学环境的影响[14].当Dy3+占据低对称性(没有反演中心)的格位时,4F9/2→6H13/2的跃迁发射将在发射光谱中占主导.在四方相白钨矿结构的SrWO4基质中,Dy3+离子将占据Sr2+的格位(无对称中心),因此,对应于4F9/2→6H13/2跃迁的573 nm发射峰比其他峰强得多,这与上面的结构分析相一致.
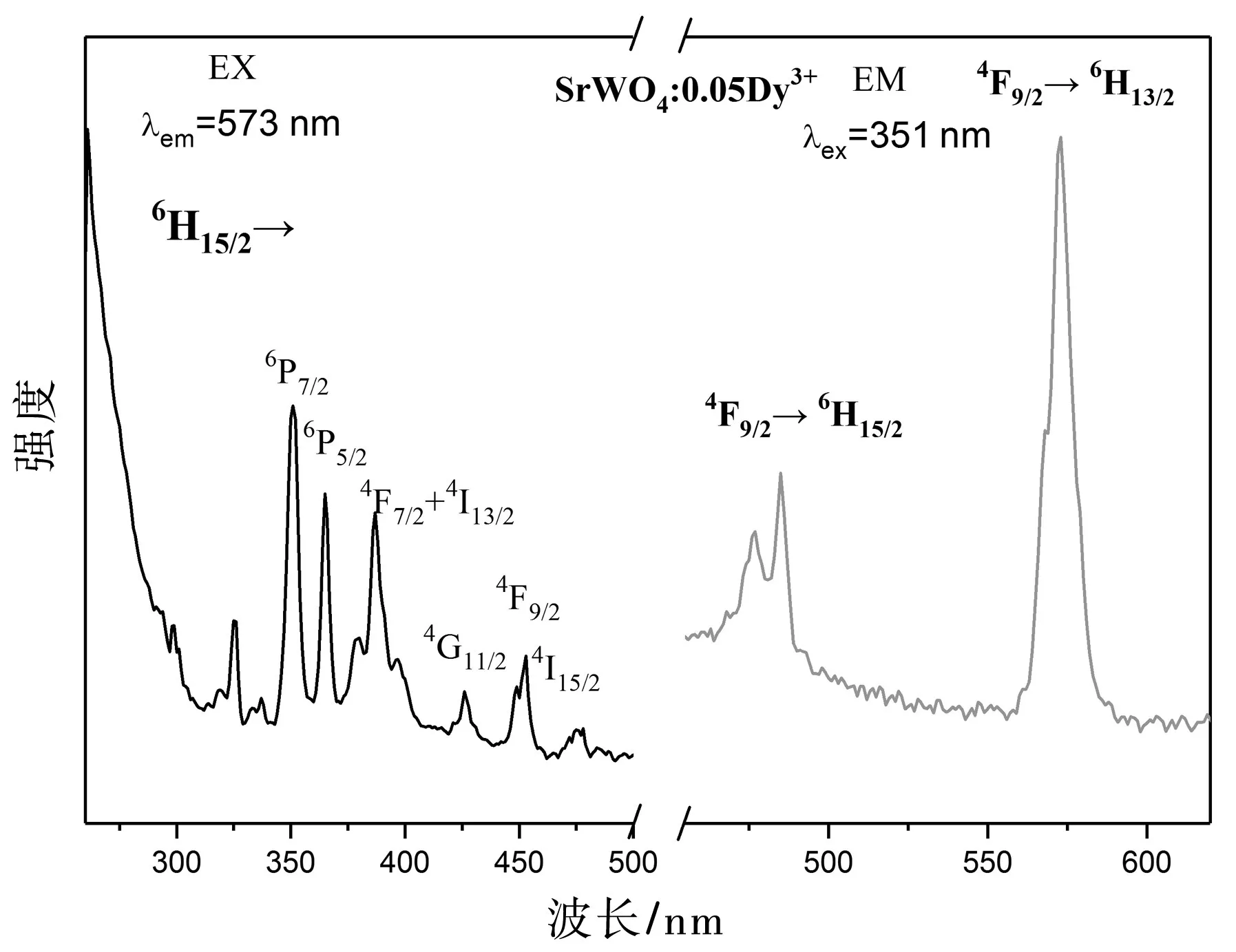
图3 纯水溶剂中制备样品SrWO4:0.05Dy3+的激发光谱(左)和发射光谱(右)
SrWO4基质中Dy3+离子的能级排布如图4所示.首先Dy3+离子吸收能量,电子从基态6H15/2跃迁到各个激发态:6P7/2、4F7/2+4I13/2和4I15/2等.激发态是不稳定的,可通过非辐射跃迁到较低的激发态4F9/2,然而这样的激发态电子仍然是不稳定的,最终返回6H13/2和6H15/2得以稳定.使得能量以黄光和蓝光的形式释放出来.另外,基质吸收能量之后也可以传递给Dy3+离子,所以激发光谱中存在O2-→W6+以及O2→Dy3+电荷迁移带.具体过程如下:处于基质的电子吸收紫外光后从1A1基态跃迁到1T2激发态.随后,当Dy3+离子掺入SrWO4基质中,将会发生WO42-到稀土离子有效的能量传递.然后通过多声子弛豫,能量从较高激发态非辐射弛豫到低激发态.多声子弛豫可以增加亚稳态能级上稀土离子的累积,进而影响其发光效率.
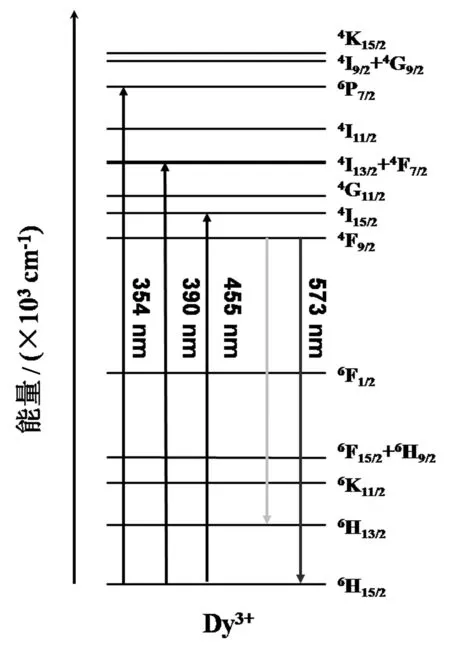
图4 SrWO4基质中Dy3+离子的能级示意图
图5为在三种溶剂中合成SrWO4:0.05Dy3+样品的发射光谱.a、b、c溶剂条件分别为35 mL H2O、7 mL乙醇+28 mL H2O、14 mL乙二醇+21 mL H2O.从图中对比发光强度可知,纯水的时候发光强度最高,其次是溶剂为14 mL乙二醇+21 mL H2O时制备的样品,添加乙醇的溶剂中制备的样品发光强度最低.可能是由以下原因引起的:一般来说,接近球形、表面光滑、尺寸较大的样品发光强度较高,因为球形时样品结晶度比较高,而且球形发光具有高密度和低散射的特点;另外,表面光滑以及尺寸较大的样品比表面积比较小,避免部分Dy3+离子因表面缺陷引起的发光猝灭[15-16].
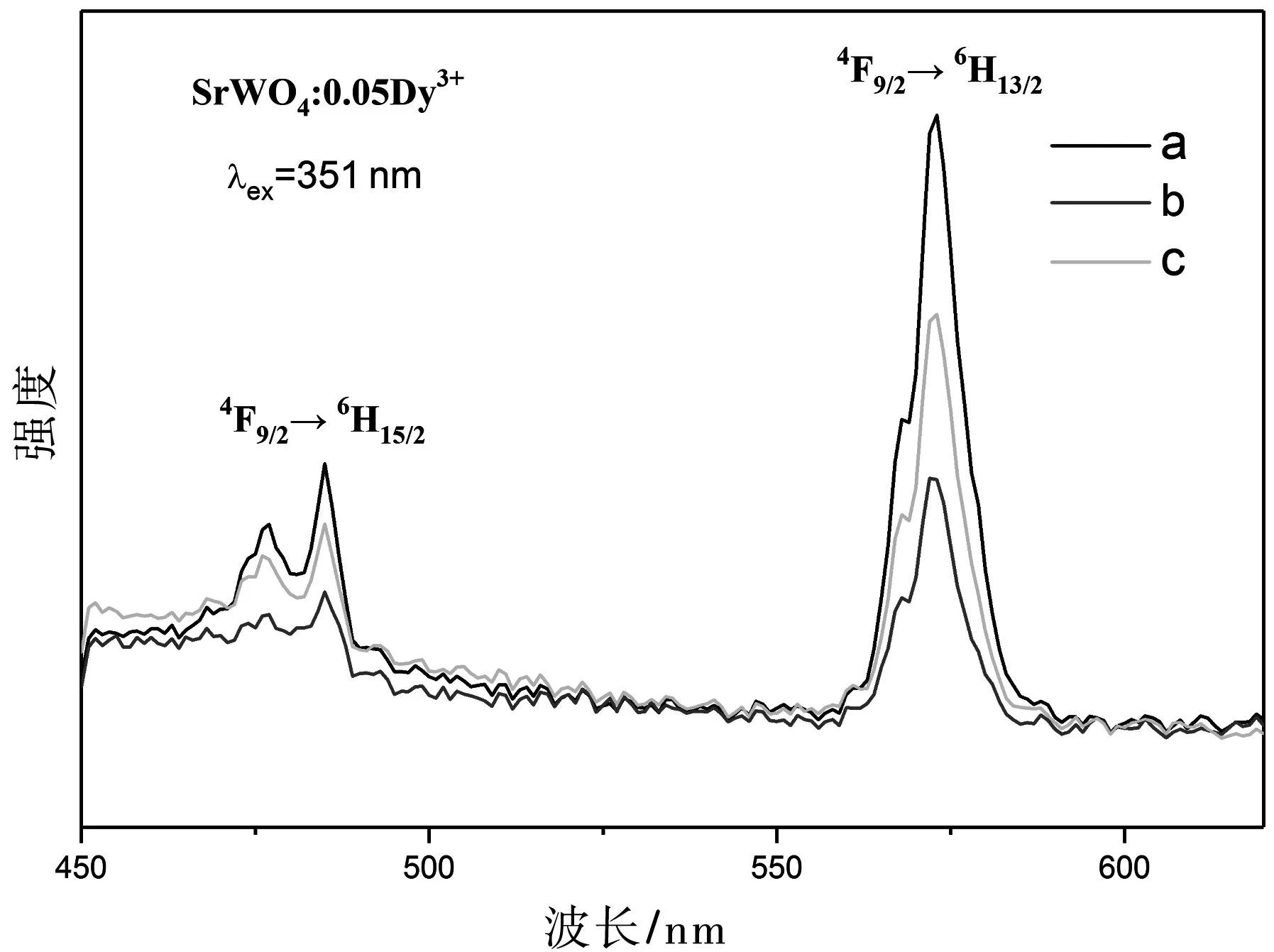
图5 不同溶剂下合成SrWO4:0.05Dy3+样品的发射光谱
3 结论
本研究利用溶剂热法成功制备了Dy3+荧光粉掺杂的SrWO4荧光粉,确定了晶体的结构及其最佳合成条件.取得了以下创新成果和结论.
(1)在比较简单和环保的溶剂热条件下制备的所有样品均为纯相物质,但是加入的有机溶剂不利于晶体的结晶.
(2)溶剂不同时,制备样品的微观形貌不同,溶剂中的水、乙醇和乙二醇对金属离子具有不同的络合能力,从而使其中的SrWO4核生长和溶解的速度不同,最终使得到的样品形貌随溶剂的不同发生改变.
(3)制备的荧光粉能够表现出Dy3+离子的特征激发和发射.最强的激发峰位于351 nm,对应于Dy3+离子的6H15/2→6P7/2跃迁.最强的发射位于573 nm处,对应于Dy3+离子的4F9/2→6H13/2跃迁.
(4)溶剂为纯水时制备的样品发光强度最高,因为纯水溶剂制备的样品接近球形、表面相对光滑、尺寸较大.
