利妥昔单抗治疗儿童抗NMADR脑炎疗效分析
2019-12-06于春梅屈晓张洪伟刘勇
于春梅 屈晓 张洪伟 刘勇
抗N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor,NMDAR)脑炎是一种儿童常见的自身免疫性脑炎,其临床表现多样,易漏诊及误诊,如不尽早诊断并给予及时的免疫治疗,其病残率及复发率都很高。我们对32 例患儿同时行血清与脑脊液抗NMDAR 抗体测定,给予早期诊断及治疗,根据疾病症状轻重、头颅影像、脑电图、对一线药物治疗反应,探讨进行二线免疫抑制治疗时机。利妥昔单抗(Rituximab,RTX)是一种B 细胞表面CD20 抗原的嵌合式单克隆抗体,具有杀伤B 细胞,从而使B 细胞分泌抗体的作用减弱。RTX 在儿科的长期疗效、副作用等仍有待阐明。我们通过长期随访,对12 例使用利妥昔单抗患儿的疗效、安全性进行了阐述,以期为临床应用提供有力证据。
1 资料与方法
1.1 一般资料
回顾性分析2016 年10 月—2018 年6 月于本院确诊为抗NMADR脑炎的32 例患儿,平均年龄(8.2±2.7)岁,男女比为1:3。所有患儿诊断标准均符合Graus 与Dalmau 标准(2016 年)[1],确诊抗NMADR 脑炎需符合以下3 个标准:(1)下列6 项症状中的1 项或者多项:①精神行为异常或者认知障碍;②癫痫发作;③言语障碍;④识水平下降;⑤意运动障碍/不自主运动;⑥自主神经功能障碍或者中枢性低通气。(2)抗NMDAR 抗体阳性。(3)合理排除其他病因。所有32 例患儿均给予免疫球蛋白及甲泼尼龙治疗后,其中12 例一线免疫治疗无效,加用利妥昔单抗的为治疗组,余20 例为观察组,对其临床表现、辅助检查、治疗恢复及随访情况进行观察研究。
1.2 临床表现
入组的32 例患儿均有精神行为异常及不自主运动;部分患儿有语言障碍、睡眠障碍、运动障碍、记忆力下降;出现频繁癫痫发作12 例,其中4 例出现癫痫持续状态;2 例患者有昏迷史。
1.3 影像学及脑电图
全部患者行头颅MRI 检查,其中3 例MRI 平扫提示颅内多发病灶,1 例MRI 提示脑萎缩,2 例颞叶有异常信号,余头颅MRI检查未见异常。脑电图:32例患儿均行脑电图检查,12例发现δ刷,6 例弥漫性慢波,10 例癫痫样放电(5 例为局灶性),4 例前头部有阵发性慢波。女性患儿均行腹膜后及子宫双附件超声检查,男性均行腹膜后及睾丸B 超检查,均未发现肿瘤。
1.4 腰椎穿刺结果
本研究中8 例脑脊液压力增高,其中6 例白细胞计数轻度升高(最高为38×106/L),3 例蛋白质浓度轻度增高(最高为750 mg/L),3 例脑脊液寡克隆区带弱阳性。抗NMDA 受体IgG 抗体:32 例患儿同时行血清及脑脊液抗体检测,22 例脑脊液抗NMDAR 抗体阳性,18 例血清抗NMDAR 抗体阳性,其中有8 例血清及脑脊液均阳性。抗体检测采用纯化抗原转染细胞系CBA 法(Cell Based Assay),采用欧蒙试剂。同时对患儿的配对的脑脊液与血清标本进行检测。
1.5 治疗方案
早期予以静脉免疫球蛋白1 g/(kg·d),共使用2 d,予甲泼尼龙20 mg/(kg·d)连用3 d 后,口服泼尼松2 mg/(kg·d)共4 d,共3 个疗程,后给予泼尼松口服序贯治疗。所有患儿均在给予免疫球蛋白,予甲泼尼龙冲击治疗3 疗程后,总治疗时间3 周左右,其中12 例治疗效果差,仍有精神行为异常、烦躁、不自主运动、癫痫发作、意识障碍等,需给予二线药物利妥昔单抗治疗,签署知情同意书。按利妥昔单抗375 mg/m2静脉滴注,每周1 次,连用4 周。首次静滴速度为50 mg/h,30 min 后观察无不良反应,后逐渐增大剂量,每30 min 增加50 mg,最大剂量不超过400 mg/h。每次用药前30 min予布洛芬、氯雷他定口服,氢化可的松静脉输注。RTX 输注期间给予心电监护检测呼吸、心率、血压观察并记录不良反应情况,患儿均按计划接受治疗并进行随访,定期检查血常规和血生化、T 淋巴细胞亚群、B 细胞计数。于RTX 治疗前及治疗1 周后需检测血清CD4+T 淋巴细胞计数,如果治疗1 周其计数小于200 个/ul 或CD4/CD8 的值小于0.5,则停止RTX 重复给药,经密切观察直至CD4+T 细胞大于200 个/μL 可重复给药。
1.6 统计学方法
该研究采取统计学SPSS19.0 软件进行数据分析和处理,计数资料用率(n,%)表示,计量资料用()表示,组间比较应用秩和检验。P<0.05 为差异具有统计学意义。
2 结果
2.1 临床症状
两组一般情况对比,对照组癫痫发作4 例(20%),治疗组8例(66.7%),意识水平下降对照组6 例(30%),治疗组12(100%),病情高峰期mRS 评分≥4 分对照组5 例(25%),治疗组12 例(100%)。脑电图δ 刷改变,对照组4 例(20%),治疗组8 例(66.7%),均提示利妥昔治疗组病情较危重。
2.2 临床疗效
治疗组给予利妥昔单抗治疗4 个疗程,行改良Rankin 量表(modified Rankin scale,mRS )评分,本次选取患儿病情高峰期、治疗第1 月后及第3 个月后mRS 评分分析短期疗效评价指标,以及免疫治疗半年后的mRS 评分分析长期疗效评价指标。给予对照组及治疗组两组患儿的疗效进行对比观察。病情高峰期出现临床症状总数:对照组(1~4 个),平均(1.75±0.40)个,治疗组(4~6 个),平均(4.50±1.25)个,P<0.05 差异有统计学意义。发病高峰期mRS 评分:对照组(3.26±0.87)分,治疗组(4.33±0.78)分,P<0.05,差异有统计学意义。两组治疗1 月、3 月及半年mRS 评分对比,P<0.05,差异有统计学意义。随访1 年,对照组的患儿有5 例复发,而治疗组患儿均无临床复发。见表1。
2.3 不良反应
治疗组12 例患儿共接受4 个疗程RTX 治疗,其中5 例患儿疗程中发生粒细胞减少症或口腔霉菌感染或呼吸道感染。经对症积极处理后均较快获得改善。
3 讨论
抗N-甲基-D-天冬氨酸受体脑炎,系抗NMDAR 抗体介导的突触功能障碍相关的自身免疫性脑炎,还是儿童自身免疫性脑炎中发病率最高的一种脑炎[2]。本文所有患儿均出现精神行为异常及不自主运动(包括肢体及口咽部异常运动),治疗组12 例均有意识障碍,提示症状较重。脑电图12 例发现δ 刷,6 例弥漫性慢波,10 例癫痫样放电(5 例为局灶性)。有研究报道少数抗NMDAR 脑炎患儿脑电图呈极度δ 刷状波,提示病程迁延、反复及预后不良[3-4]。血清及脑脊液抗NMDAR 抗体阳性是确诊该病依据,本文中的32 例患儿均符合诊断标准。该病脑脊液及血清抗NMDAR 抗体可同时阳性,或者其中之一阳性。其中脑脊液中抗NMDAR 抗体阳性与疾病相关性更密切[5-6]。NMDAR 抗体检测在脑脊液(CSF)中较血清中更具有特异性,且灵敏度高,提示其鞘内有生成[7]。我们所选32 例患儿同时行血清及脑脊液抗体检测,22 例脑脊液抗NMDAR 抗体阳性,18 例血清抗NMDAR 抗体阳性,本研究显示脑脊液抗体阳性率略高于血清抗体阳性率。怀疑自身免疫性脑炎的患儿尽量同时检测血清及脑脊液抗NMDAR 抗体,尽早明确诊断。本文研究显示病情高峰期出现临床症状总数,对照组与治疗组比较差异有统计学意义,病情高峰期mRS 评分2 组对比差异有统计学意义,提示高峰期mRS 评分较高者及病程中出现多个临床症候群(≥4 个)患儿,是对一线免疫治疗效果不佳的高危因素,应及时加用利妥昔单抗治疗。有报道意识障碍是抗NMDAR 脑炎病程迁延、遗留致残的高危因素之一,尽早开始二线治疗能显著缓解症状及改善预后。
表1 治疗组与对照组疗效对比()
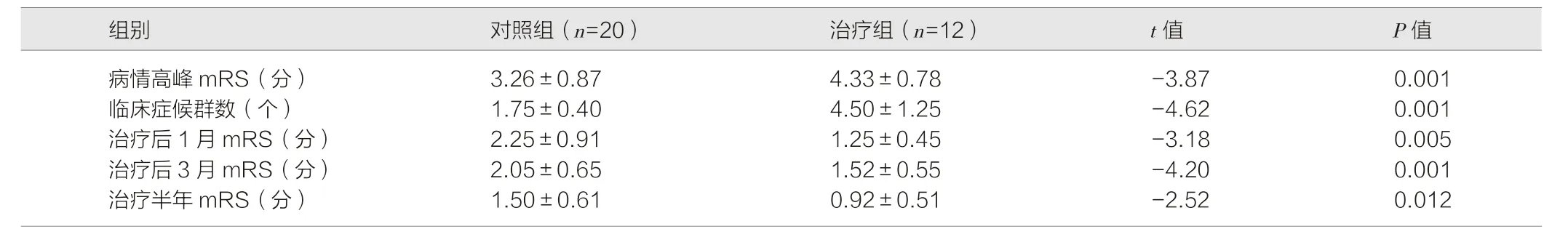
表1 治疗组与对照组疗效对比()
注:改良Rankin 量表(modified Rankin scale,mRS)评分。轻度:mRS 评分≤3 分(没有丧失独立行走功能);重度:疾病高峰期评分≥4 分(丧失独立行走功能);部分恢复组(mRS 评分2~3 分);痊愈:(mRS 评分0~1 分)。
目前指南推荐一线免疫治疗药物包括免疫球蛋白、糖皮质激素和血浆置换等,单独和联合应用均可起效。当一线免疫药物治疗无效时,或者应用一线药物治疗10 天后病情仍未改善,应尽早采用二线免疫治疗,主要包括利妥昔单抗、巯唑嘌呤、环磷酰胺、吗替麦考酚酯等[8-9]。临床研究证实联合应用效果优于单独治疗[10]。利妥昔单抗(RTX),系抗靶向B 细胞治疗,主要是免疫球蛋白IgG1,通过特异性结合B 淋巴细胞表面CD20 抗原引起B 细胞耗竭而发挥免疫抑制作用,并且具有免疫调节活性[11]。现有报道,利妥昔单抗可清除血清中100%及脑脊液中90% 的CD 20+B 细胞,而CD 20+细胞的再生与疾病的迁延及复发相关[12]。本研究给予利妥昔单抗治疗组其1 月、3 月、半年mRS评分均较前逐渐下降,症状改善明显。治疗组与对照组1 月、3 月及半年mRS 评分比较差异有统计学意义。表明给予利妥昔单抗治疗的患儿获得较好治疗方法,治疗顺利,远期治疗效果明显。Dalmau[13]随访2 年的病人报道为复发率12%,复发2 次以上的占4%。对照组患儿应用一线免疫治疗的1 年内有5 例(15.62%)复发,治疗组患儿无复发,与既往报道复发率接近。Byrne 等[14]研究结果显示,AE 患者早期接受利妥昔单抗治疗,可以减少复发。近年来有研究发现RTX 治疗能有效减少复发、减缓残疾的进展,大部分患儿可完全恢复,约25%可遗留认知、运动障碍等。
利妥昔单抗其副作用多为轻度至中度,绝大部分患儿多可耐受或对症治疗后可缓解。有研究表明绝大多数患儿基本上能耐受二线免疫治疗药物,其发生严重不良反应的较少,且均为可逆性[15-16]。目前关于RTX 治疗儿童抗NMADR 脑炎尚无严重不良反应的报道。其短期治疗的副作用通常具有较好的耐受性且容易管理。且给予通过减慢输液速度等措施,多数不良反应都是可以避免的。我们治疗组给予利妥昔单抗治疗的12 例患儿,其中5 例患儿治疗过程中发生粒细胞减少症或口腔霉菌感染或呼吸道感染,给予对症处理均缓解。
儿童抗NMDA 脑炎复发率较高,其复发的原因可能与病毒感染、肿瘤等有关。故临床症状、抗体检测、脑电图及头颅影像改变等是诊断和评估复发的重要手段。有疑似该病的患儿应早期进行血清及脑脊液抗体检测,以便早期确诊,早期有效治疗,改善预后,预防复发,并长期随访并注意排查肿瘤。
总之,利妥昔单抗治疗重症儿童抗NMADR 脑炎能够使症状基本缓解,安全性较高,无严重不良反应,是抗NMADR 脑炎患儿的有效治疗方案。并且能明现降低残疾程度,及早进行二线免疫治疗有利于降低复发率。
