嗅觉异常首发的抗LGI1抗体相关边缘性脑炎1例报告
2019-12-06石书娜路永刚
石书娜,路永刚
边缘性脑炎主要临床表现有近期记忆障碍、精神行为异常、癫痫发作,起病形式为急性或亚急性,呈渐进性发展,主要责任病灶为边缘结构,如海马、岛叶、杏仁核等。其相关的抗体有3种,除外最常见的LGⅡ抗体外,还有抗γ-氨基丁酸β受体抗体(GABABR)和抗α-氨基-3羟基-5甲基-4-异唑丙酸受体抗体(AMPAR),富亮氨酸胶质瘤失活1蛋白抗体(LGI1)属于电压门控钾离子通道(VGKC)复合物抗体,作为一种分泌性蛋白质,其主要表达部位是新皮质及海马,通过控制突触前的钾通道及突触后的-氨基羟甲基恶唑丙酸受体AMPAR来影响突触的传递[1],进而调节神经元的应激。边缘性脑炎在神经科并非少见疾病,而LGIl抗体相关边缘性脑炎确并不多见,现将我院神经内科所诊治的以嗅觉异常为首发的LGIl抗体相关边缘性脑炎的临床资料进行分析、讨论,以期为临床提供借鉴。
患者,男性,38岁。2018年2月28日主因“头晕伴嗅觉异常半年,加重伴乏力1 m。”入住我院神经内科三病区。半年前无明显诱因出现头晕,头蒙,转颈加重,嗅觉异常,记忆力减退,发作性失神,诉间断闻到汽油味、消毒水味(实际周围无汽油味、消毒水味),流涕,打喷嚏,自行口服复方氨酚烷胺胶囊,流涕、打喷嚏症状减轻,仍头晕、嗅觉异常,未予重视;1 m前上述症状加重,并出现乏力、心慌、全身汗出,表现为行走即大汗淋漓,无意识障碍,无肢体无力及感觉障碍,无发热,按照“过敏性鼻炎”治疗,口服抗过敏药物(氯雷他定片),效差,3 d前在我院门诊做头部MRI平扫+增强(见图1):双侧海马区及海马旁回区异常信号,多考虑炎性病变,肺部CT:双侧胸膜局限性增厚,为求系统治疗,门诊以“颅内感染”为诊断收入我科。发病来神志清,精神差,乏力,多汗,记忆力下降,饮食睡眠可,二便正常,体重未见明显变化。既往体健,吸烟10 y,1包/d,对酒精、花粉过敏,过敏时出现面部潮红,数小时后可自行缓解。入院后查体:体温36.6 ℃,脉搏90次/min, 呼吸19次/min,血压141/96 mmHg,心、胸、腹部无异常,双侧额纹无变浅,双侧瞳孔等大等圆,直径约3 mm,对光反射灵敏,双侧鼻唇沟无变浅,嗅觉粗测异常,诉闻到汽油味、消毒水味(实际周围没有汽油或消毒水)。软腭上抬力尚可,咽反射正常,伸舌不偏,构音无障碍,四肢肢体肌力5级,四肢深感觉、浅感觉正常,四肢腱反射正常。四肢肌张力正常。闭目难立征阴性,脑膜刺激征阴性,双侧病理征阴性。自主神经功能检查:多汗(全身),动则满头汗珠,卧立位血压无明显差别。入院后完善检查:肝功能、血糖、血脂、心肌酶、肾功能、电解质、CRP、凝血四项+D二聚体、血常规、尿常规、大便常规未见明显异常。甲功五项:总甲状腺素T4:179.78 nmol/L(66.97~152.52);血管炎三项、ANA(自身免疫抗体)13项阴性,肿瘤标志物套餐全套(男性):癌胚抗原5.12 ng/ml(0~5);脑脊液清亮透明,颅压70 mmH2O,细胞数、生化无异常,抗酸染色、墨汁染色均阴性;脑脊液病毒全套:巨细胞病毒抗体IgG(CMV IgG )阳性;副肿瘤综合征抗体谱10项均为阴性,自身免疫性脑炎抗体(血清):抗富亮氨酸胶质瘤失活蛋白1抗体IgG ++ 1∶100;抗谷氨酸受体(NMDA)抗体IgG阴性,抗谷氨酸受体(AMPA1)抗体IgG阴性,抗谷氨酸受体(AMPA2)抗体IgG阴性,抗接触蛋白关联蛋白2(CASPR2)抗体IgG阴性,抗GABA受体抗体IgG阴性。自身免疫性脑炎抗体(脑脊液):抗富亮氨酸胶质瘤失活蛋白1抗体IgG++ 1∶10,余阴性;脑电图:双侧枕部以9~10.5 Hz,30~60 μV,a波为背景节律,少量散在为5~6 Hz,40~80 μV θ波,左顶可见少量100~150 μV棘波、尖波,双侧顶波幅较低;闪光刺激同背景节律,睁眼闭眼抑制完全,过度换气同背景节律,两侧点活动大致对称;结果提示局灶性异常脑电图。四肢及双侧面部肌电图未见明显异常。头部MRA:双侧大脑前动脉管壁稍毛糙。诊断抗LGI1抗体相关边缘性性脑炎,患者拒绝免疫球蛋白治疗,给予注射用甲泼尼龙琥珀酸500 mg qd×4 d,240 mg ivgtt qd×3 d,120 mg qd×4 d,80 mg qd×3 d,醋酸泼尼松片(5 mg/片) 60 mg po qd。妥吡酯50 mg qn 4 d,50 mg bid 7 d,50 mg tid 3 d,后改为50 mg qd,100 mg qn,治疗27 d后头晕好转,发作性失神、嗅觉异常消失,乏力好转,多汗好转,患者各项辅助检查未发现占位性病变,患者家属拒绝行全身PET检查及进一步肿瘤筛查,办理出院,出院后激素每月减1片托吡酯50 mg bid,3 m后于我院复查自身免疫性脑炎抗体(血清+脑脊液)均阴性。
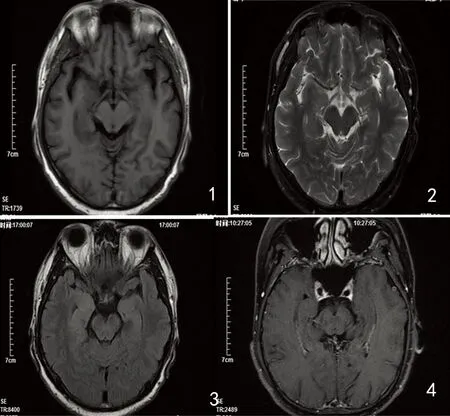
1~3分别为T1序列、T2序列、FLAIR序列,提示双侧海马区及海马旁回异常信号;4为增强
图1 头部MRI
讨 论边缘性脑炎主要表现为精神行为异常、癫痫发作(起源于颞叶)和近记忆力障碍,脑电图与神经影像学符合边缘系统受累,脑脊液检查提示炎性改变。常见的有抗LGll抗体、抗GABABR抗体与抗AMPAR抗体相关的脑炎[2],2010年LGⅡ抗体相关脑炎首次被认识,是一种新型自身免疫性边缘性脑炎[3],2013年国内报道首例[4],随着医疗条件的提升,越来越多的LGⅡ抗体相关脑炎被发现。LGⅡ抗体主要分布在颞叶皮质及海马[5],其相关脑炎主要表现为面臂肌张力障碍、记忆力下降、低钠血症,合并肿瘤罕见,免疫治疗效果好[6]。具有诊断意义的典型临床表现为面臂肌张力障碍,而本例报道患者提示无面臂肌张力障碍患者亦不能排除LGll抗体相关边缘性脑炎的可能,需要进一步完善血清、脑脊液相关抗体的检测。本例报道患者抗LGⅡ抗体相关脑炎颞叶内侧T2WI和FLAIR高信号与既往报道一致[7]。对于磁共振影像学上显示一侧颞叶异常信号,尤其是那些伴海马萎缩的患者,需要与伴海马硬化的内侧颞叶癫痫进行鉴别,抗LGⅡ抗体相关脑炎起病形式多是急性、亚急性,发作频繁,每日发作可达数次,而后者多慢性起病,发作频率相对较少[8]。关于本病诊断的的实验室检测,血液及脑脊液LGⅡ抗体阳性的诊断意义特殊,目前尚未在健康人群中发现抗LGⅡ抗体阳性的报道[9]。
Van等[10]研究结果显示诊断为LGI1抗体相关脑炎病例中,癫痫发作为首发表现的比例为53%,在疾病发展过程中,90%左右患者出现一种或超过一种的癫痫发作。LGI1抗体相关脑炎其他症状有自主神经功能障碍、睡眠障碍,自主神经功能障碍包含多汗、心动过缓和括约肌功能障碍[11]。本患者以嗅觉异常为主要症状,嗅觉异常为颞叶癫痫表现,逐渐加重,并出现自主神经功能异常表现:多汗,符合报道,结合记忆障碍及脑脊液、血液LGⅡ抗体阳性,且血清LGⅡ抗体滴度高于脑脊液LGⅡ抗体滴度,诊断明确。有研究发现NMDA抗体脑炎患者其抗体主要为IgG1,脑脊液抗体滴度高于同期外周血清,与NMDA抗体脑炎不同,LGI1抗体相关脑炎患者抗体主要为IgG4,其脑脊液抗体检测阳性率低于外周血,即使为阳性,其滴度仅为血清的1%~10%[12],本例报道中的脑脊液LGll抗体滴度1∶10,低于血清LGll滴度1∶100,与研究相符。
在临床诊断中,本病需与副肿瘤相关边缘性脑炎、病毒性脑炎、神经梅毒、克雅病、莫忘综合征相鉴别[13],本患者副肿瘤综合征抗体谱阴性,相关检查无肿瘤表现,不支持副肿瘤相关边缘性脑炎;无头痛、发热、脑膜刺激征表现,结合脑脊液常规、生化,不支持病毒性脑炎;传染病检查梅毒抗体阴性,不支持梅毒;与克雅病的脑脊液抗体为NMDA或VGKC不同;与莫忘综合征的脑脊液抗体为复合物抗体亦可区别。
本病的治疗一线药物有类固醇激素、静脉注射免疫球蛋白、血浆置换等,大多预后良好,本例报道患者给予激素治疗,联合妥吡酯对症治疗,效果较好,随访3个月无复发情况。但后期是否会合并肿瘤及潜在肿瘤,需待进一步随访、复查肿瘤相关方面的检查。
综上,在临床上遇到急性或亚急性起病,表现记忆障碍、精神症状、癫痫发作、自主神经功能障碍患者,需考虑抗LGⅡ抗体相关边缘性脑炎,并尽早完善脑脊液自身免疫性脑炎相关抗体检测、副肿瘤综合征抗体谱检查,尽早明确诊断,及时治疗。
