ZnFe2O4的制备及光催化性能研究
2019-11-25田志茗
田志茗,常 悦
(齐齐哈尔大学化学与化工学院,齐齐哈尔 161006)
1 引 言
光催化氧化技术是一种新型的高级氧化技术,因其具有高效、彻底、成本低廉以及不会产生二次污染等优势,在降解有机污染物方面具有广泛的应用[1]。ZnFe2O4是一种具有尖晶石晶体结构的半导体功能材料,被广泛应用于医学,高频变压器,磁记录介质等领域[2-4];由于ZnFe2O4的带隙窄 (约1.9 eV),成本低,稳定性好,具有磁性能,近年来在光催化领域引起了人们的广泛关注[5-6]。一般来说,ZnFe2O4的光催化活性会受到晶体尺寸和形貌影响,因此可以根据改变合成方法和控制反应条件进行性能的调控。
ZnFe2O4的制备方法主要有机械球磨法、化学共沉淀法、溶胶凝胶法等。徐明等[7]对分析纯的ZnO和Fe2O3粉末进行超声波分散及高能球磨预处理后恒温焙烧制备ZnFe2O4材料结果表明,700 ℃时即可制得纯ZnFe2O4,且温度升高有利于结晶、扩散,晶粒固熔范围扩大,铁酸锌随温度的升高其溶解速率加快。马孝瑜等[8]以硝酸铁、硝酸锌为原料,柠檬酸为络合剂,采用溶胶-凝胶法制备了尖晶石型 ZnFe2O4材料,结果表明在900 ℃制备的ZnFe2O4粉体晶型发育完整,相同条件下,适当延长保温时间有助于ZnFe2O4粉体的合成。Yadav等[9]通过共沉淀法合成纳米ZnFe2O4,并研究了其对亚甲基蓝光催化活性,研究结果表明,纳米铁酸锌材料具有良好的光催化活性。但上述方法都有局限性,如机械球磨法制备的产品纯度低、分散性差、粒径分布不均匀,溶胶-凝胶法需要高温高压的苛刻反应条件,共沉淀法操作繁琐、费时。溶剂热/水热法反应条件温和、反应过程容易控制、反应体系均匀而备受研究者关注[10], Jessyamma等[11]采用水热法和溶剂热法,在相同的温度和加热时间条件下,在高压釜中制备纳米铜铁氧体(CuFe2O4)、镁铁氧体(MgFe2O4)和锌铁氧体(ZnFe2O4),研究表明溶剂热法制备的晶体在光学和磁性等方面优于水热法。吕玉珍等[12]采用溶剂热法在两种不同反应体系中制备TiO2纳米棒,结果表明表面修饰和结晶过程是影响TiO2纳米棒形貌的主要因素。Shao[13]等以无水乙醇为反应介质,通过NaOH调节反应溶剂pH,采用溶剂热法制备了磁性铁酸锌纳米颗粒,并研究了其对苯酚的光催化降解性能。
本文以乙二醇作为溶剂,采用溶剂热法制备ZnFe2O4,通过控制煅烧温度获得具有不同粒径尺寸的铁酸锌。对样品进行X射线粉末衍射、紫外可见漫反射吸收光谱、扫描电镜的表征,研究了反应温度对铁酸锌催化剂形貌的影响。通过光催化降解有机染料亚甲基蓝,研究了样品的光催化性能。
2 实 验
2.1 铁酸锌的制备
分别称取0.88 g乙酸锌、2.16 g氯化铁和3.0 g结晶乙酸钠,加入到含有60 mL乙二醇的烧杯中,搅拌溶解60 min后,将溶液转移到聚四氟乙烯衬里的晶化釜(100 mL)中,在180 ℃下保温24 h。反应结束后过滤,用去离子水洗涤沉淀物至无氯离子,在室温下干燥24 h,得到黑色粉末,记为ZnFe2O4。将ZnFe2O4在不同温度下煅烧3 h制备ZnFe2O4,研究煅烧温度对ZnFe2O4晶相的影响。不同温度下制备的ZnFe2O4样品记为ZnFe2O4(T),T代表煅烧的温度,如300 ℃煅烧制备的ZnFe2O4记为ZnFe2O4(300 ℃)。
2.2 催化剂的表征
采用D/Max-ⅢC 型 X 射线衍射仪测定样品的晶相结构;利用S-4300 扫描电子显微镜分析催化剂形貌特征;利用TU-1901双光束紫外可见分光光度计测试UV-Vis 漫反射光谱分析催化剂的光学性质。采用TG-DSC,德国耐驰STA449F3热重-热差综合分析仪记录样品的热失重和差热曲线。
2.3 光催化降解实验
光催化降解实验在光化学反应器中进行。将10 mg催化剂加入到50 mL亚甲基蓝(浓度为5/10/15/20/25 mg/L)中,用0.1 mol/L HCl溶液和0.1 mol/L NaOH溶液调节pH值。用300 W汞灯照射,每隔15 min取样,离心后测上清液的吸光度。根据测得的吸光度计算降解率。用E(%)表示:
(1)
其中C0为染料溶液初始浓度mg/L,A0为测得的染料初始吸光度;Ct为染料溶液在t时刻的浓度mg/L,At为染料溶液在t时刻的吸光度。
3 结果与讨论
3.1 物相分析及形貌分析
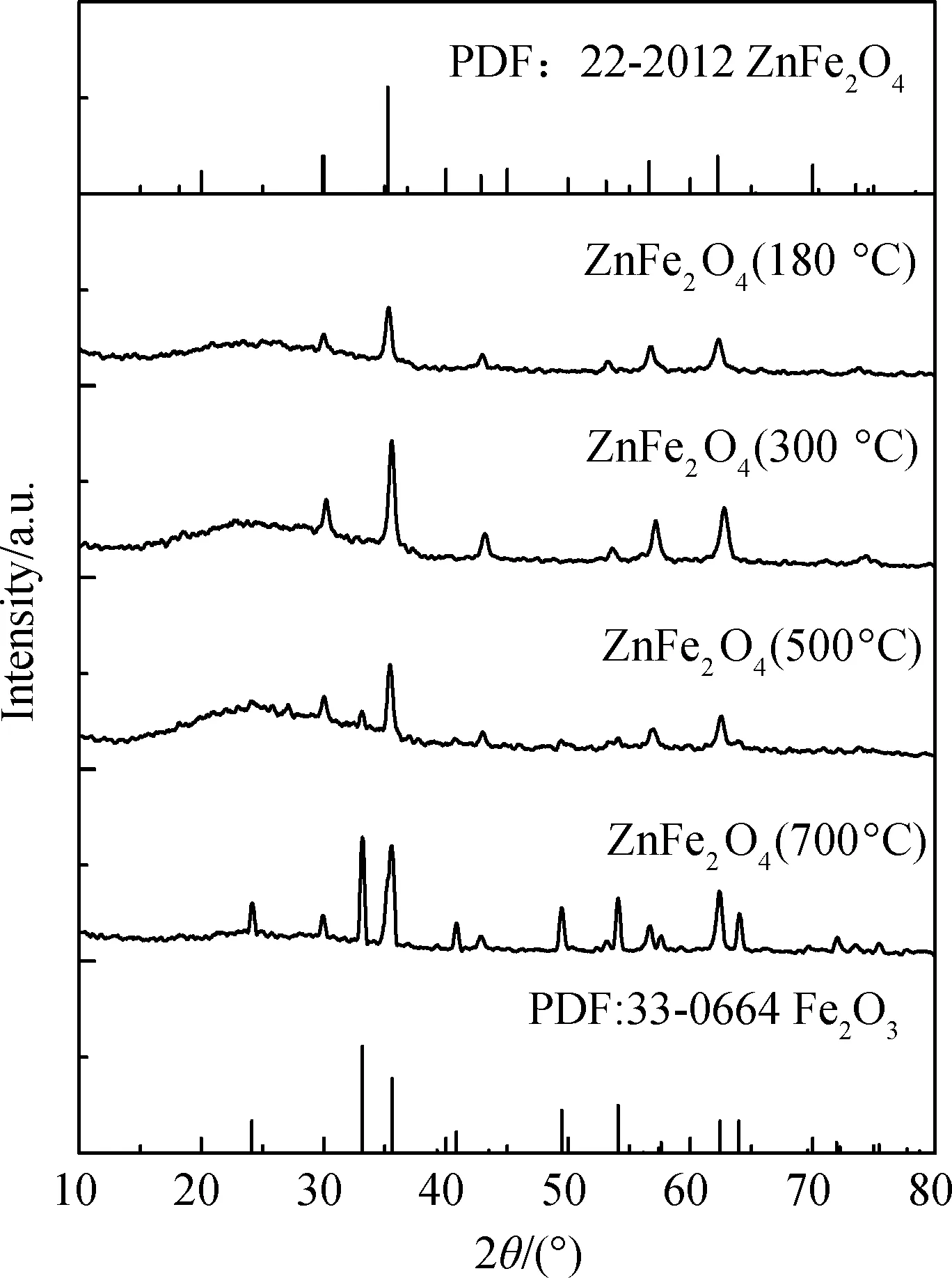
图1 ZnFe2O4样品的XRD图谱Fig.1 XRD patterns of the ZnFe2O4 samples
图1为不同温度条件下制得的ZnFe2O4的XRD图谱,对照PDF标准卡片(22-1012)可以看出,样品的XRD谱图在2θ=30.26°,35.62°,43.20°,53.78°,57.10°,62.82°处均出现了与PDF标准卡片对应的(220),(311),(400),(422),(511),(440)晶面的特征衍射峰。180 ℃晶化的样品中出现衍射峰较宽,说明在晶化条件下已有ZnFe2O4晶粒产生;300 ℃煅烧的样品XRD图谱中峰型尖锐,说明在300 ℃高温煅烧下所制备的ZnFe2O4结晶度较高,而在500 ℃煅烧制备的样品衍射角在57.10°,62.82°处的(511),(440)晶面的特征衍射峰明显减弱,出现了晶格缺陷。700 ℃煅烧制备的样品XRD图谱中晶面的衍射峰与ZnFe2O4的特征衍射峰比较有新的衍射峰出现,与标准图谱Fe2O3的PDF(33-0664)对照这些衍射峰与Fe2O3的特征衍射峰完全一致,说明ZnFe2O4在700 ℃高温煅烧下有Fe2O3晶相。根据Scherrer公式:
(2)
(D为晶粒尺寸(nm),K为常数,λ为X射线波长,θ为衍射角,β为XRD衍射峰的半高峰宽),得出不同温度煅烧下制得的晶粒尺寸和晶格参数,如表1所示。由此可见,不同煅烧温度制得ZnFe2O4颗粒均为纳米尺寸。
图2(a)为ZnFe2O4(300 ℃)样品的SEM图。从图2(a)和局部放大的图(b)中可以观察到样品的微球大小约为200 nm,结合XRD数据对晶粒尺寸的计算可知,微球是由尺寸约20 nm的ZnFe2O4微晶组装而成。微球颗粒形状均匀,边界清晰[14]。

表1 样品的晶粒尺寸和晶格参数

图2 ZnFe2O4(300 ℃)的SEM照片及局部放大图Fig.2 SEM images and partial enlargement of ZnFe2O4(300 ℃)
3.2 UV-vis 漫反射分析
图3是ZnFe2O4样品的紫外-可见漫反射光谱图及其带隙图。由UV-vis 吸收关谱曲线可以看出ZnFe2O4样品在紫外和可见光波长范围内都有很比较强的吸收,说明ZnFe2O4能够很好利用太阳光中的可见光。400 nm以下的吸收谱带是铁酸盐纳米材料中Zn-O 键电荷跃迁和 Fe-O键电荷跃迁的共同作用结果。半导体的带隙能量可以通过Tauc plot方程:
(3)
(4)


图3 ZnFe2O4样品的UV-vis 光谱及带隙图Fig.3 UV-vis DRS and band gaps energy analysis of ZnFe2O4 samples
3.3 光催化活性研究
图4为不同煅烧温度的ZnFe2O4对亚甲基蓝的降解率影响及ZnFe2O4前躯体的TG-DSC曲线。由图4(a)可以看出,煅烧温度条件对催化剂的催化活性影响很大,不同催化剂催化活性顺序为:ZnFe2O4(500 ℃)﹥ZnFe2O4(300 ℃)﹥ZnFe2O4(700 ℃)﹥ZnFe2O4,当煅烧温度为500 ℃制备ZnFe2O4催化活性最高。分析图4(b)DSC和TG 曲线可以看出,0~112 ℃是样品吸热脱水的过程,在112~160 ℃之间是残留溶剂乙二醇吸热挥发的过程;在160~350 ℃内出现类似晶粒生长的放热变化,对应的 TG 曲线有一个明显的失重,结合ZnFe2O4(300 ℃) 样品的XRD可以说明晶格已趋于完善,350~702 ℃出现一个大的吸热峰,结合ZnFe2O4(500 ℃)样品的XRD可以说明此时晶格开始出现缺陷。由于ZnFe2O4(500 ℃)晶体中晶体缺陷提供了更多的活性位点,从而增强了其催化活性[17]。

图4 不同煅烧温度的ZnFe2O4对亚甲基蓝的降解率的影响及ZnFe2O4前躯体的TG-DSC曲线Fig.4 Degradation rate of methylene blue by ZnFe2O4 with different calcination temperatures and TG-DSC curves of the catalyst of ZnFe2O4
3.4 初始pH值对降解效果的影响
溶液的pH值可以影响催化剂和有机染料之间的吸附性能。实验研究pH范围在3~11,实验结果如图5所示。结果表明,随着溶液的初始pH(3~11)不断增大,染料的降解率逐渐提高。这是因为一方面ZnFe2O4的零电荷(pzc)值为9.3,ZnFe2O4的表面电荷在pH值低于pzc时为正,在pzc时为中性,在pH值高于pzc时为负。在pH为9.3以下,ZnFe2O4纳米光催化剂表面带正电荷,由于ZnFe2O4和染料溶液的电荷相同,带电物质相互排斥,因此很难分解染料分子;在pH>9.3时,ZnFe2O4的表面带负电,因此ZnFe2O4和阳离子染料溶液的相反电荷相互吸引[18],从而使催化剂和有机染料之间的吸附性能增强。另一方面,从光降解机理分析,水分子和OH-与价带上的空穴反应产生·OH活性基团,当溶液为碱性溶液时,溶液中OH-与该反应中H+结合生成H2O,从而促进·OH的生成;碱性条件下较高浓度OH-促进了反应的进行,从而影响了ZnFe2O4催化剂的降解速率。所以ZnFe2O4的光催化活性应该在碱性介质中进行。

图5 溶液的初始pH值对光催化降解的影响Fig.5 Effect of pH value on the photocatalytic degradation

图6 不同初始浓度对降解率的影响Fig.6 Effect of different initial concentrations on degradation rate

图7 ZnFe2O4催化降解动力学模型Fig.7 Kinetic model of ZnFe2O4 catalytic degradation

图8 ZnFe2O4降解亚甲基蓝重复使用性Fig.8 Reuse of ZnFe2O4 for degradation of methylene blue
3.5 初始染料浓度的影响及动力学研究
在光降解过程中,染料的初始浓度是研究ZnFe2O4光催化活性的重要参数。图6为不同亚甲基蓝溶液初始浓度的降解率。由图6可知,不同初始浓度的催化活性顺序为:10 mg/L>5 mg/L>15 mg/L>20 mg/L>25 mg/L。当亚甲基蓝溶液的初始浓度为10 mg/L时,催化剂的催化活性最高,达96.8%。随着染料浓度的增大,光催化活性降低。一是因为随着染料浓度的增大,催化剂表面吸附更多的染料,染料可以吸收入射光,光子不能到达催化剂表面产生反应自由基,所以催化性能降低;另一个可能的原因是染料本身的可见光屏蔽效果,导致部分可见光可以被染料吸收[19]。
3.6 ZnFe2O4的重复用性
ZnFe2O4光催化剂的重要特征是其可重复使用性和进一步光催化应用的回收率。在这项实验中,通过外加磁场可以高效的回收催化剂,重复三次实验后ZnFe2O4光催化剂仍然表现出很高的光催化活性,并且在第三次循环后仍能有效地进行83.3%的降解,如图8所示。亚甲基蓝降解的轻微衰减可归因于催化剂表面上活性位点的浸出或多次光催化测试期间样品的损失。
4 光降解机理
由文献[18]可知当催化剂ZnFe2O4在紫外光照射下,吸收的光子能量(hv)大于或等于ZnFe2O4光催化剂的带隙能时,其基态价带上的电子(e-)吸收光子能量后跃迁到激发态的导带上,价带会产生空穴(h+)形成光生电子-空穴对(1),价带上产生的光生空穴直接迁移到ZnFe2O4晶体表面与表面吸附的有机污染物直接反应,或者与ZnFe2O4晶体表面吸附的水分子作用生成羟基自由基·OH活性基团(6)。这些生成的超氧自由基和羟基自由基等强氧化性物质能够有效分解水溶液中有机污染物,将其降解成无毒、无污染的CO2和H2O等物质(7~9)。
(1)
(2)
(3)
2·O2H → H2O2+ O2
(4)
H2O2→ 2·OH
(5)
(6)
(7)
(8)
(9)
根据 UV-Vis 的表征结果,按照下式计算了 ZnFe2O4(500 ℃)半导体光催化剂的能带结构,即导带与价带的相对位置。
ECB=X-Ec-Eg/2
EVB=ECB+Eg

5 结 论
采用溶剂热法,通过控制煅烧温度制备了不同纳米尺寸具有尖晶石结构的ZnFe2O4催化剂。煅烧温度为300 ℃条件下制备的ZnFe2O4样品由铁酸锌纳米微晶构成,呈现球状,表面粗糙,形貌规则;当煅烧温度为500 ℃时制备的ZnFe2O4样品在紫外光和可见光范围均有响应,带隙为1.60 eV,具有磁性和较高的光催化活性;当亚甲基蓝浓度为10 mg/L时,在300 W汞灯照射2 h,催化剂用量为0.04 g/L,亚甲基蓝降解率达到96.8%,三次重复使用降解率达到83.3%。
