超声引导联合腔内心电图定位在中心静脉置管中的应用
2019-11-19薛薇薇奚艳朱志韬
薛薇薇 奚艳朱志韬
中心静脉导管(CVC)广泛应用于临床以解决各类静脉通路问题。传统CVC置管多依靠体表解剖标志定位进行穿刺,即盲穿。由于个体解剖差异、术者经验等因素限制,常出现动脉损伤、穿刺区血肿、气胸、置管失败、导管头端异位等并发症,而导管头端异位可进一步引起感染、血栓、化学性静脉炎、导管闭塞、心律失常、心肌损伤等[1]。目前,常用的导管头端定位方法为置管后行胸部X线检查,但存在部分导管X线透光度较高难于观察、X线检查存在辐射、术后导管位置调管易导致感染等弊端。我院采用超声引导联合腔内心电图应用于颈内静脉置管,可降低并发症发生率、提高穿刺成功率及导管头端到位率,取得了较满意效果,报告如下。
资料与方法
一、临床资料
选取2016年1月至2018年6月在我院行超声引导下颈内静脉穿刺并经腔内心电图定位植入CVC的患者52例,男27例,女25例,平均年龄(59.5±8.5)岁;均是短期内使用化疗药物/高渗性药物,不适于或拒绝经外周静脉置入中心静脉导管(PICC)置管的患者;置管原因:恶性肿瘤行周期性静脉化疗37例、外科术后行静脉营养支持12例、外周血管条件极差3例。排除标准:凝血机制障碍、上腔静脉综合征、颈部肿瘤放疗或颈部术后、颈部皮肤感染、破损、心脏外科术后或起搏器置入术后。所有患者均于术前签署中心静脉置管知情同意书。
二、仪器和材料
GE Logiq7便携式彩色多普勒超声诊断仪、迈瑞床旁心电监护仪、福尼亚中心静脉导管包(16G,单腔)、中心静脉置管心电转换器、心电引导导线、可莱福正压接头、3M敷贴(10 cm×12 cm)、生理盐水、10 U/ml肝素钠、2%盐酸利多卡因等。
三、操作方法
本操作均由取得相应资质的主管护师施行。患者取去枕平卧位,肩部垫枕稍抬高,头稍后仰15°~20°[2],穿刺点选取右侧颈部,头偏向穿刺点对侧。探头先探查颈内静、动脉走行及位置关系,确定穿刺点并作体表标记,确定穿刺角度和深度。常规消毒、铺无菌洞巾,2%利多卡因局部浸润麻醉满意后,先以局麻针试穿颈内静脉,进一步明确穿刺角度及深度。超声探头用无菌薄膜紧密包裹,涂适量无菌耦合剂,再次定位穿刺血管,左手固定探头,右手持注射器接穿刺针在定位图像引导下负压进针,缓慢进针至回抽出暗红色血液,并经超声图像观察、确认穿刺针位于颈内静脉内,代表穿刺成功。依次引入导丝、撤注射器和穿刺针,引入扩张器行皮肤扩开,后拔出扩张器,导丝引导下置入中心静脉导管,导丝末端接心电导线并连接心电转换器,助手将心电转换器与心电监护仪(标准域导联右上肢电极)相连,转动转换器开关,将腔内心电图导出,边送管边观察监护仪屏幕上导丝“J”形端拾取的腔内心电波形,通过观察P波振幅的高低和形态调整导管置入的深度。
前期缓慢送管过程中,腔内心电图P波振幅与体表心电图无明显差异,后P波振幅呈进行性高尖变化(图1);继续送管,P波回落继而出现负向或双向P波(图2),此时立即停止送管,询问患者有无不适,并将导管缓慢回撤2~3 cm,观察至P波振幅为R波振幅的1/2~3/4(图3),此作为最佳置管深度[3],撤导线并固定导管。随即将患者转运至影像科行胸部X线摄片或行床边胸部X线检查,以进一步证实导管尖端位置。
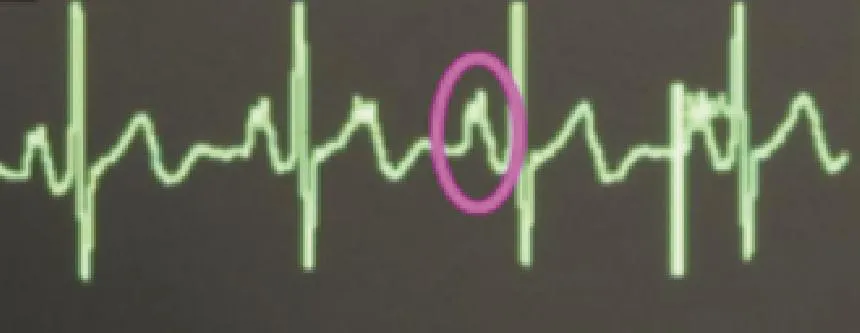
图1 P波开始呈高尖改变
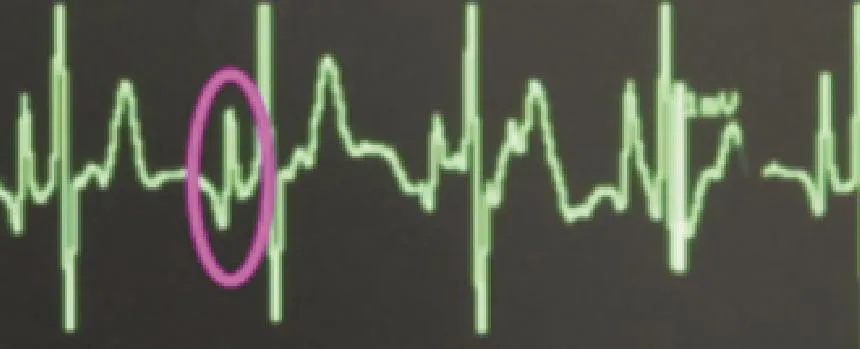
图2 出现双向P波

图3 P波振幅为R波1/2~3/4
结 果
52例患者行超声引导下颈内静脉穿刺均获得成功,其中首次穿刺即成功置入导管50例,首次穿刺成功率为96.2%;首次穿刺失败需2次穿刺并置管成功2例。所有患者穿刺过程未出现颈动脉误穿及损伤、血气胸及空气栓塞等并发症。
52例患者经腔内心电图定位置管达最佳深度后行胸部X线检查,均证实导管头端位于上腔静脉下1/3段,置管深度一次性到位率100%。2例(3.8%)在调整最佳置管深度过程中出现心前区不适感,心电监护显示一过性心律失常,及时纠正导管位置并对症处理后患者症状消失。而后经进一步超声证实,该2例患者颈内静脉管径小于邻近动脉,静/动脉管径比值分别为5.5/9.8、5.1/12.7。
讨 论
CVC置管传统盲穿依靠体表解剖标志定位,穿刺成功率多取决于置管者操作经验及水平[4];同时,颈内静脉的变异也是影响穿刺成功率的重要因素,Samy等[5]报道约有18%的患者右颈内静脉直径小于5 mm。Gordon等[6]报道约有5.5%的患者颈内静脉与颈总动脉存在易位关系,即颈内静脉在颈总动脉内侧。以上因素导致传统盲穿易出现误穿颈动脉导致血肿甚至大出血、误伤胸膜导致血气胸、误伤神经或淋巴管等并发症,严重时甚至危及生命。而超声引导下行CVC置管可直观了解颈动、静脉关系、走行、管径等,及时发现变异,同时可实时监测穿刺针的位置、走向并做及时调整,避免了传统穿刺的盲目性,可有效提高穿刺成功率及减少并发症[7]。而本研究中52例患者在超声引导下均取得穿刺成功,其中首次穿刺失败的2例患者即存在颈内静脉细小的情况,静/动脉管径比值分别为5.5/9.8、5.1/12.7,在超声引导下反复定位进行第2次穿刺均取得成功。
腔内心电图用于中心静脉置管定位的主要原理是利用导丝和血液的导电性,以导丝作为探测电极经上腔静脉探入近心端拾取右心房P波,依据P波振幅变化指导导管尖端定位[8]。目前多用于PICC头端定位[3,8]。当导管头端位于颈内静脉及上腔静脉上段时,腔内心电图P波振幅与体表心电图无明显差异;当导管尖端进入上腔静脉下1/3段时,P波振幅明显高尖变化,到达右心房上部时,可出现双向或负向P波,缓慢后退2~3 cm,观察P波振幅降为R波振幅的1/2~3/4,此作为最佳置管深度[3],而这也是目前国际上公认CVC头端的理想位置[9-10]。导管置入过深进入右心房甚至更深处,易出现心律失常,严重者损伤心肌或瓣膜,导致心脏穿孔甚至心包填塞等并发症[11],危及患者生命。若导管置入过浅,头端贴附于上腔静脉侧壁,心脏大血管搏动、患者日常活动可引起导管头端的摆动,对血管壁造成持续损伤,增加血栓形成的发生率;甚至导管可能漂浮进入血流量相对较小的外周静脉,更易导致血流不畅,从而引发血栓形成、静脉炎甚至导管阻塞等并发症[12]。
本组52例患者置管后行胸部X线检查均证实导管头端位于上腔静脉下端近右心房处,导管头端一次性到位率100%,与李建国等[13]的研究结果一致。而术中调整导管位置过程中出现2例患者一过性心律失常,亦证实了导管位置过深可导致并发症。
综上,相对于传统盲穿,超声引导下颈内静脉穿刺可直观了解穿刺区域血管走行、管径等状况,明确有无变异,避免误穿动脉,从而准确引导穿刺,减少并发症,提高置管成功率。同时,腔内心电图用于导管头端定位可实时提示置管深度,术中可及时、满意调整导管头端位置,临床推广可减少患者暴露于X线辐射的机会,同时可减少二次调整导管可能带来的感染等风险。
