阻塞性睡眠呼吸暂停低通气综合征对成人听力影响研究
2019-11-05邢宇轩乔月华
吴 扬 仝 悦 邢宇轩 蒋 雯 刘 稳 乔月华
阻塞性睡眠呼吸暂停低通气综合征(OSAHS)是一种睡眠期间的呼吸节律紊乱,频繁发生完全或不完全的上气道塌陷阻塞所致的呼吸暂停和通气不足,反复发作易引起机体的低氧血症、高碳酸血症以及机体代谢障碍,对人体内代谢旺盛且需氧量大的器官功能易造成影响[1]。由于耳蜗的解剖和生理特点,当微循环发生缺血时,其无法在短时间内建立有效的侧支循环,容易受到缺血、缺氧的直接和间接损伤导致听功能障碍[2]。笔者的研究采取纯音测听、宽频声导抗(WAI)及畸变产物耳声发射(DPOAE)对OSAHS患者进行测试,将结果与正常对照组比较,以了解患者听力情况以及听觉传导系统各部分功能是否正常。
资料与方法
1.病例选择:(1)临床资料:选取主诉长期睡眠打鼾来门诊就诊的患者,收集其完整临床资料且筛选符合研究标准的OSAHS患者共30例,男性23例,女性7例,患者年龄20~57岁,平均年龄43.40±11.99岁,病史4~20年。对照组12例,其中,男性8例,女性4例,患者年龄25~54岁,平均年龄39.75±10.31岁。(2)入选标准:OSAHS组:①符合OSAHS诊断标准,且呼吸暂停低通气指数(apnea hypopnea index,AHI)≥15次/小时,男性女性不限;②无高血糖、高血脂,血压控制在140/90mmHg以内(包括药物治疗);③既往无耳科相关疾病史,无长期噪声接触史,无耳毒性药品应用史,无颅脑疾病或外伤史;④患者未诉双耳闷胀感等特殊不适,行耳内镜检查见双侧外耳道通畅,鼓膜完整,标志清。双耳226Hz鼓室导抗图为A型。对照组:均由家人以及本人证实无打鼾症状,男女不限;其余入选条件同OSAHS组第②③④项。
2.仪器及方法:(1)多导睡眠监测(polysomnography,PSG):采用美国安波澜公司生产的Embletta X100睡眠呼吸监测系统,记录整夜睡眠≥7h,记录呼吸暂停低通气指数(AHI)、最长呼吸暂停时间和经皮血氧饱和度等指标,用Remlogic软件进行分析。(2)宽频声导抗:采用美国米莫萨声学公司生产的HearID听觉诊断系统,于标准隔声室,本底噪声<20dB,频率范围200~6000Hz,将数据处理后得出正常环境压力下声能吸收率值和吸收率曲线。(3)纯音听力测试:采用丹麦尔听美公司Aurical Aud纯音听力仪,隔声室中噪声<20dB SPL,测试频率范围为0.125kHz~8kHz。(4)耳声发射检测:采用美国米莫萨声学公司生产的 HearID听觉诊断系统,于隔声室内测试。DPOAE测试时两个初始刺激信号L1-L2=10dB SPL,两者频率之比f2/fl=1.2,f1、f2的几何均数范围位于1kHz~16kHz,读取2f1-f2的强度。所有耳声发射的测定都重复两次,两次的信号较稳定时为有效值,DPOAE反应幅值以高于本底噪声6dB为引出。
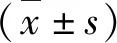
结 果
1.PSG监测结果:OSAHS组中30例成人患者,其AHI介于15.8~80.7,平均血氧饱和度78.6%~95.6%,最低血氧饱和度50%~80%。
2.纯音测听结果:OSAHS组60耳和对照组24耳,在4kHz、6kHz、8kHz的平均听阈值OSAHS组明显高于对照组,其余频率比较差异无统计学意义(表1)。

表1 OSAHS组与对照组纯音听阈各频率比较
3.WAI测试结果:在所分析的200~6000Hz范围内的7个频率中,OSAHS患者与对照组其声能吸收率值比较,差异无统计学意义(P>0.05,表2)。

表2 OSAHS组与对照组各频率WAI曲线吸收率均值比较
4.DPOAE检查结果:在1kHz~16kHz频率范围内所选取的各频率,DPOAE幅值OSAHS组均低于对照组,除16kHz外其余频率比较差异有统计学意义(P<0.05,表3、表4)。
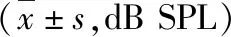
表3 OSAHS组与对照组1kHz~6kHz频率DPOAE幅值变化
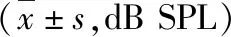
表4 OSAHS组与对照组8~16kHz频率DPOAE幅值变化
讨 论
依照最新指南OSAHS定义为每夜7h睡眠过程中呼吸暂停及低通气反复发作达30次以上,或AHI≥5次/h,呼吸暂停事件以阻塞性为主,伴打鼾、睡眠结构紊乱、频繁出现血氧饱和度下降、白天嗜睡等病征[3]。OSAHS患者大脑或脑干的神经功能及末梢器官等可因长期处于慢性缺氧状态而受到损害,同时耳蜗微血管属于终末血管,缺少侧支循环,且为高能量依赖器官,因而对缺血、缺氧十分敏感,机体长期处于缺氧状态可代偿性地引起促红细胞生成素的增加致血液流变学改变,全血比黏度增加,加上血氧饱和度下降,从而影响脑干部位和耳蜗的氧及能量供应,导致听觉系统兴奋传递的延迟及内耳功能的下降[4]。
因单一频率的声导抗检测在反映中耳微小病变中存在不足,且中耳疾患中不同病变相互影响可能因增高降低的声顺值彼此抵消而使鼓室图表现为正常波形[5]。所以在本研究中,采用宽频声导抗测试0.2kHz~6kHz频率范围,获取中耳鼓室图的同时测得各频率的声能吸收率及反射率,将所选取频率OSAHS组与对照组WAI吸收率值进行比较,发现两组结果差异无统计学意义,表明OSAHS组受试者不存在中耳内细微或复杂病变,这与Matsumura等[6]对38例OSAHS患者的研究结果相吻合。
阅读近年来相关文献资料发现,在多数研究者的研究中,均采取纯音测听、耳声发射及听觉脑干诱发电位等方式检测患者的听觉功能,然而研究中虽然采取同样的测试手段评估患者听力情况,其所得结果及结论并非完全一致。纯音听力测试中,研究结果显示OSAHS组较对照组在4kHz、6kHz及8kHz频率段存在明显的听阈值升高,而在4kHz以下差异无统计学意义。在Martine等[7]研究中,对100例OSAHS患者进行测试,按照病情轻重程度分组后,纯音测听示在0.25kHz~3kHz所有分组听阈均正常,而在6kHz以上听阈值则随病情程度加重而呈上升趋势。同样Ekin等[8]选取了27例OSAHS患者,纯音测听结果显示OSAHS组较对照组听阈值常频比较,差异无统计学意义,而在扩展高频(10kHz~16kHz)则显著增高。有研究观察发现不同频率的声波在基膜产生最大振幅其部位不同,高频声波所引起基膜最大振幅的部位靠近前庭窗。由于蜗底的血液供应丰富,代谢旺盛,且耗氧量大,当机体长期受OSAHS影响时,其相对耳蜗顶部对缺血、缺氧更加敏感[9]。因此,OSAHS患者的听功能受损早期可表现为高频听力的下降。
DPOAE由不同频率的诱发源引发,反映的是各频率耳蜗节段外毛细胞的功能,各频率的特异性和稳定性可提示所受累的基膜节段[10]。DPOAE幅值明显下降,表明耳蜗外毛细胞可能已有结构或功能的改变。本研究中1kHz~16kHz频率范围内测定DPOAE的幅值,OSAHS组均明显低于对照组,提示OSAHS患者耳蜗功能已受到不同程度损害。在佘万东及韩浩伦等研究中,分别选取20例及24例重度OSAHS患者,DPOAE检测幅值在0.5kHz~8kHz同样较对照组存在明显降低[4,11],而华娜等[12]及Erika等[6]研究也得出相似的数据结果。有动物试验发现耳声发射比ABR能更早地显示出缺血、缺氧对耳蜗功能损害,同时,DPOAE也比纯音测听检测更加敏感,因此即使纯音听力测试正常的OSAHS患者,其DPOAE振幅的减低也提示缺氧等因素可能已经对患者的听觉功能造成一定程度损害。
长期慢性缺氧引起的机体代谢障碍及血液流变学改变,继而导致耳蜗功能损害,为OSAHS患者听功能下降的主要原因。长期受OSAHS困扰的患者,其清醒状态下的基础脑血流速度较正常人低,尤其大脑中动脉及椎-基底动脉[13]。在Fischer等[14]研究中发现,睡眠状态下呼吸暂停阶段,右侧大脑中动脉的血流较正常明显减慢,血液流变学变化为全血比黏度增高,红细胞聚集指数增高,加上机体缺氧,将影响脑干部位及耳蜗的氧和能量供应,从而造成听觉系统的兴奋传递延迟以及内耳功能的下降。同样Mom等[15]实验发现,当阻断内听动脉血供时间不超过7s时所引起的DPOAE改变和耳蜗血流的下降可以完全恢复正常,但若是持续部分阻断或多次间歇性中断内听动脉的血流,DPOAE改变和耳蜗血流下降则难以完全恢复。因而OSAHS患者DPOAE检测的异常可能为睡眠状态下频繁发生呼吸暂停,造成耳蜗的慢性间断性缺氧而导致的不可逆结果。但同时笔者还考虑是否有打鼾产生的噪声因素同样参与其中。噪声对听力的损害是一个复杂的多因素机制,噪声可损害耳蜗内的微循环,导致耳蜗缺血、缺氧,造成毛细胞和螺旋器的退行性变[16]。另外噪声可引起毛细胞、支持细胞酶系统严重紊乱,导致氧和能量代谢障碍,致细胞变性、死亡。噪声所引起听力曲线变化最明显的特征是早期出现4kHz处的“V”字型切迹,随着病变发展,3kHz、6kHz的听力也出现下降,听力曲线呈“U”型[16]。而笔者的纯音测听结果也显示OSAHS患者组在4kHz处其听阈值较对照组升高最明显,具有一定相似性,提示鼾声可能同样为致OSAHS患者听功能受损的潜在因素。因而在以后的研究中还应扩大所纳入研究对象数量,设计更完善的对照实验,来获取详尽数据以明确解释其机制。
