颈内动脉与椎动脉夹层的血管超声评估及管腔再通的差异性分析
2019-10-29李兆强华扬贾凌云杨洁
李兆强 华扬 贾凌云 杨洁
颈部动脉夹层(cervical artery dissection,CAD)是中青年人缺血性卒中发病的重要原因[1],根据病变累及血管可分为颈内动脉夹层(internal carotid artery dissection,ICAD)与椎动脉夹层(vetebral artery dissection,VAD)。影像学检查是诊断CAD的重要手段[2],既往研究CAD主要通过MRI、CT血管成像(CTA)等诊断[3-4],而超声对CAD的诊断及随访报道较少。此外,既往研究多将ICAD与VAD统一分析,而Debette等[5]与von Babo等[6]研究结果表明,ICAD与VAD在发病年龄、临床表现等方面存在差异。本研究通过彩色多普勒血流显像(CDFI)对ICAD与CAD进行诊断及随访检查,比较二者在发病原因、临床症状、超声表现、管腔再通等方面的差异性,探讨CDFI对CAD的诊断及随访价值。
1 对象与方法
1.1 对象
回顾性连续纳入2014年1月至2018年12月于首都医科大学宣武医院就诊的CAD患者136例,男80例(58.8%),女56例(41.2%);年龄15~72岁,平均(41±11)岁;伴高血压病35例,高脂血症23例,糖尿病15例,吸烟46例;临床症状:脑缺血症状119例[其中脑梗死78例,短暂性脑缺血发作(TIA)41例],头颈部疼痛70例;发病原因:自发性夹层46例,继发性夹层90例(主动性运动60例,被动性运动30例)。136例患者夹层病变血管共160支,其中ICAD 75支(46.9%),VAD 85支(53.1%);CAD单支病变者116例(85.3%),双支病变者17例(12.5%),三支病变者2例(1.5%),四支病变者1例(0.7%);单纯ICAD患者62例(45.6%),单纯VAD患者69例(50.7%),ICAD与VAD共病患者5例(3.7%)。本研究方案经本院伦理委员会审核批准。
1.2 纳入与排除标准
纳入标准:(1)突发脑缺血和(或)头颈部疼痛等临床症状患者;(2)CDFI明确壁内血肿型CAD征象;(3)CDFI与高分辨率MR和(或) CTA诊断结果一致。排除标准:(1)非壁内血肿型CAD;(2)合并严重动脉粥样硬化性病变者;(3)临床或其他影像学资料不完整者。
1.3 资料收集
收集所有患者的人口统计学资料(性别、年龄)、病史如(高血压病、糖尿病、高脂血症)、吸烟史等,以及临床资料如CAD患者发病原因、临床症状、影像学检查结果及随访结果等。
脑血管病相关危险因素的判断依照中国国家卒中登记研究中使用的方法[7]。高血压病:既往高血压病史,或入院后相隔1周重复测量血压≥140/90 mmHg)。糖尿病:既往糖尿病病史,或入院测定快速血糖浓度>7.8 mmol/L。高脂血症:既往高脂血症病史,或存在如下情况中1项及以上,即血清低密度脂蛋白胆固醇≥3.12 mmol/L,总胆固醇≥5.80 mmol/L,三酰甘油≥2.25 mmol/L。吸烟:当前或既往吸烟≥1支/d。
CAD患者发病原因分类[1]:根据发病前活动状态,分为自发性夹层及继发性夹层。自发性夹层:安静状态下发病;继发性夹层:继发于相关危险活动,如颈部剧烈运动、过度转颈、按摩、外伤、医源性损伤等,并进一步分为主动性运动(包括颈部剧烈运动、过度转颈等)与被动性运动(包括按摩、外伤、医源性损伤等)。
CAD患者脑缺血症状按照中华医学会脑血管疾病分类标准分为脑梗死和TIA[8]。脑梗死:患者出现持续性、24 h内不能缓解的肢体无力、言语不清、头晕等症状,MRI检查可见新发梗死灶;TIA:患者出现上述症状但可于24 h内消失,MRI检查无异常。
1.4 研究方法
1.4.1超声仪器及检查方法:颈内动脉及椎动脉CDFI检查采用荷兰PHILIPS公司生产的E-PIQ5和日本HITACHI-ALOKA公司生产的Ascendus超声诊断仪,分别使用12-3 MHz线阵、8-4 MHz微凸和5-1 MHz凸阵探头联合检查。常规检查模式包括二维灰阶、彩色血流成像、频谱多普勒。对颈内动脉起始段、中段、远段(入颅前段)及椎动脉起始段(V1段)、椎间隙段(V2段)和枕段(V3段)分别进行检查评估。
CDFI诊断CAD标准[3,9-10]:(1)病变管腔增宽;(2)可见低回声壁内血肿和(或)撕裂的内膜;(3)血流信号不规则变细或消失;(4)狭窄处血流速度升高,闭塞段无血流信号。见图1。
CAD狭窄程度:参照既往诊断标准[11-13],测量CAD病变处原始血管内径及残余真腔内径、联合病变处血流速度参数,包括收缩期峰值流速(PSV)、舒张期末流速(EDV),评估血管狭窄程度,分为狭窄<70%、狭窄≥70%或闭塞。
1.4.2高分辨率MRI与CTA检查:高分辨率MRI检查采用德国西门子公司生产的3.0 T超导MRI仪,CAD影像特征为管腔增宽,可见新月形壁内血肿高信号[14]。 CTA检查采用德国西门子公司生产的第3代双源CT血管成像仪,CAD影像特征为颈内动脉或椎动脉管腔长段或局限性不规则变细,或管腔呈“火焰状”或“锥形”闭塞[4]。见图2。
1.5 分组
将所有研究对象分为ICAD组与VAD组,其中ICAD组66例,VAD组70例(5例ICAD与VAD共病者,4例以前循环症状发病,纳入ICAD组;1例以后循环症状发病,纳入VAD组);按病变血管支数分组,分为ICAD组75支和VAD组85支。
1.6 CAD随访检查
患者首次检查确诊后,均进行抗凝或抗血小板聚集治疗,并于发病后3、6、12个月复查CDFI,检查模式与初诊相同。完全再通为管壁结构恢复正常,内径均匀一致,血流充盈良好,血流速度正常(图3);不全再通为仍可探及壁内血肿,管腔局限性狭窄,血流充盈不全,血流速度升高,并将管腔残余狭窄分为狭窄<70%、狭窄≥70%或闭塞(图4)。
1.7 统计学分析
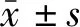
2 结果
2.1 两组患者临床资料比较
ICAD组与VAD组患者平均年龄及高血压病所占比例差异均有统计学意义(均P<0.05),其余因素组间差异均无统计学意义(均P>0.05)。见表1。
2.2 两组患者病变血管侧别及狭窄程度比较
两组患者病变侧别差异无统计学意义(P>0.05);病变血管狭窄程度差异有统计学意义(P<0.01), ICAD组狭窄程度≥70%或闭塞血管较VAD组明显增多。见表2。
2.3 两组患者病变血管再通结果比较
发病后3、6个月随访时,ICAD组病变血管管腔完全再通率分别为21.7%(10/46)、37.3%(19/51),VAD组分别为46.6%(27/58)、58.7%(37/63),VAD组病变血管管腔完全再通率明显高于ICAD组,差异均有统计学意义(χ2值分别为6.891、5.201,P值分别为0.009、0.023)。
发病后12个月随访结束时,共随访105例126支病变血管,其中ICAD 58支,VAD 68支,ICAD组与VAD组病变血管完全再通率差异无统计学意义(P>0.05)。见表3。ICAD组与VAD组不全再通血管中,管腔狭窄<70%与狭窄≥70%或管腔闭塞比例分别为55.6%(15/27)、44.4%(12/27)和48.1%(13/27)、51.9%(14/27),差异无统计学意义(χ2=0.297,P=0.586)。
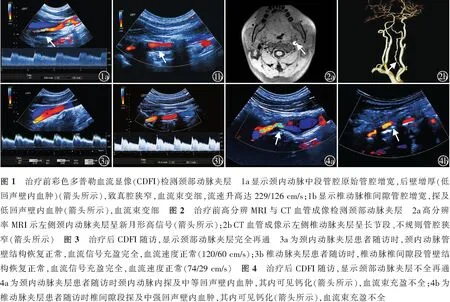

表1 ICAD组与VAD组患者临床资料比较

组别例数发病原因[例(%)]自发性夹层主动性运动被动性运动临床症状[例(%)]脑缺血症状脑梗死TIA头颈部疼痛ICAD组6626(39.4)28(42.4)12(18.2)60(90.9)43(65.2)17(25.8)30(45.5)VAD组7020(28.6)32(45.7)18(25.7)59(84.3)35(50.0)24(34.3)40(57.1)检验值2.889a1.918a3.188a1.173a1.858aP值0.092a0.166a0.074a0.279a0.173a
注:ICAD为颈内动脉夹层,VAD为椎动脉夹层,TIA为短暂性脑缺血发作;a为χ2值,b为t值
3 讨论
CAD好发于中青年人,多无动脉粥样硬化危险因素[1-2];但Pezzini等[15]、Yaghi等[16]研究报道,高血压病患者由于血管壁弹力纤维受损、血管平滑肌细胞增生,造成动脉血管僵硬度增加及顺应性下降,其机械特性发生改变,该机械损伤作用于椎动脉可能更为明显;同时,血压升高、血流剪切力增加使得管壁内膜更容易撕裂而引起CAD。Debette等[5]与von Babo等[6]报道,ICAD与VAD患者的高血压病比例无明显差异。本研究中,VAD组高血压病患者比例高于ICAD组,这可能与VAD组患者年龄大有关。

表2 ICAD组与VAD组患者病变血管的彩色多普勒血流显像特点比较[支(%)]
注:ICAD为颈内动脉夹层,VAD为椎动脉夹层

表3 ICAD组与VAD组患者发病后12个月病变血管再通率随访比较[支(%)]
注:ICAD为颈内动脉夹层,VAD为椎动脉夹层
2005年,一项纳入31项对比研究的荟萃分析结果显示,颈部创伤是导致CAD的独立危险因素[17]。多项研究指出,颈部压迫、过度旋转、按摩等创伤性因素能够导致CAD[2,18],其中,Engelter等[18]报道,约40%的CAD患者有颈部创伤史。Debette等[5]报道,VAD患者发病前出现颈部创伤的比例高于ICAD患者,而von Babo等[6]研究则认为两组差异无统计学意义。本研究结果显示,自发性夹层与继发性夹层患者所占比例两组间差异无统计学意义,但均以继发性夹层较多,说明ICAD和VAD与颈部不恰当运动的相关性更大,在长时间低头、颈部劳损或按摩时易发生CAD,年轻患者应尤为注意。
本研究两组均有超过80%的患者出现脑缺血症状,这与Debette等[5]与von Babo等[6]研究报道相同,说明ICAD与VAD均易导致脑缺血;但上述研究中,VAD患者较ICAD患者出现脑梗死的比例较高,而本研究中ICAD与VAD患者脑梗死或TIA的比例差异无统计学意义。CAD导致脑梗死是基于动脉-动脉栓塞机制,即壁内血肿微栓子脱落导致脑缺血的发生[19-20]。因此,我们认为ICAD及VAD患者是否发生缺血性脑梗死与壁内血肿型夹层微栓子脱落、动脉狭窄导致的血流灌注异常相关。
CDFI能够准确检测ICAD或VAD,具有良好的敏感度与特异度[21],但少有文献对ICAD与VAD的CDFI表现进行分析比较。本研究结果显示,ICAD较VAD更易造成血管狭窄≥70%或闭塞,与Dittrich等[22]报道一致。其原因为椎动脉相对颈内动脉管径细,且走行于横突孔中,骨性结构使病变扩展相对受限;而颈内动脉管腔较粗,血流量较高,血流对管壁压力较大,当动脉内膜撕裂时,血流在高压力作用下进入假腔,造成内膜撕裂更严重,壁内血肿形成更大,易致颈内动脉管腔重度狭窄或闭塞。
有学者认为,CAD患者预后良好,管腔再通率较高[23]。Nedeltchev等[24]报道ICAD的再通率约为60%,Wessels等[25]随访VAD的再通率为63%。Baracchini等[26]报道105支ICAD及VAD的再通率分别为55%与46.5%(P>0.05)。本研究发病后12个月随访结束时,ICAD与VAD的病变血管完全再通率分别为53.4%、60.3%(P>0.05),与上述研究一致。然而,既往研究较少报道CAD不全再通管腔的残余狭窄程度。本研究病变血管不全再通者中,ICAD组与VAD组均存在狭窄<70%与狭窄≥70%或闭塞者,组间差异无统计学意义。
既往研究报道,CAD管腔再通主要发生在6个月内,6个月后很少出现管腔通畅性改变[23-24]。Sengelhoff等[27]报道,CAD在发病6个月后仍可见管腔通畅率变化(改善率为19%),Baracchini等[26]研究结果表明,发病1年后仍可见ICAD与VAD管腔再通。本研究ICAD与VAD组发病后12个月均有管腔通畅性改善,与上述观点一致。既往未见针对于ICAD与VAD各时间段管腔再通率差异的报道,本研究结果显示,VAD在发病3、6个月的血管完全再通率均高于ICAD,说明VAD的管腔再通早于ICAD,而发病后12个月两组完全再通率差异无统计学意义。因此,与VAD相比,ICAD短期内管腔完全再通率较低,可能与ICAD壁内血肿大、管腔狭窄程度更高,ICAD壁内血肿的吸收需更长时间相关。
本研究报道了ICAD与VAD发病年龄、危险因素、血管狭窄程度及血管再通的差异性,提出ICAD与VAD同期比较的必要性,明确了CDFI对于CAD临床治疗及预后评估具有重要价值。本研究小组所在医院以脑血管病为特色,所纳入病例较少,但相对多于其他中心,与文献中CDFI诊断CAD的病例数相比具有一定优势。本研究为单中心结果,未来需进行多中心研究,以更准确地探索ICAD与VAD的CDFI表现及管腔再通的血管结构与血流动力学特征,对CAD的早期筛查与治疗提供更加客观精准的评估。
综上所述,ICAD与VAD患者在高血压病史、管腔狭窄程度及不同随访时间血管再通率等方面具有差异性。CDFI作为简便、无创、无放射性的检查方法,能够有效诊断ICAD与VAD,并及时进行随访检查,对其管腔再通性评价、评估临床治疗的有效性具有较高的应用价值。