超声引导美兰染色切除不可触及乳腺病变临床研究
2019-10-22沈海滨刘小金
沈海滨 刘小金 吕 昊
不可触及乳腺病变(nonpalpable breast lesion,NPBL)是指通过超声、X 线、MRI 等影像学检查发现而临床查体不可触及的乳腺病变,其中约27%的NPBL 为高危病变甚至不可扪及的乳腺癌(nonpalpable breast cancer,NPBC)[1]。由于NPBL 在原位局麻后不易找到,导致手术困难,因此,能及时发现、准确诊断并进行合理的治疗对于NPBL 甚至NPBC 的早期诊断和治疗具有重要意义。本文比较超声引导美兰染色手术方案与超声引导细针穿刺定位、微创旋切手术方案切除NPBL 的优势和不足,综合评估超声引导美兰染色切除NPBL 的临床应用价值。
1 资料与方法
1.1 一般资料 选择2016 年7 月—2017 年6 月杭州市第三人民医院收治的NPBL 患者120 例,均为女性,年龄18~62 岁。按随机数字表分为超声引导细针穿刺组(定位针组)、微创旋切组(旋切组)以及超声引导美兰染色组(美兰组),每组40 例。本研究经医院伦理委员会审核通过,且患者签署知情同意书。
1.2 纳入、排除标准 纳入标准:(1)结节经影像学检查,评定为BI-RADS(breast imaging reporting and data system)3-4 类的病灶[2];(2)结节长径≤20mm,体检确实不能扪及;(3)无出凝血功能障碍;(4)单侧肿块数量不超过3 个;(5)年龄18~70 岁;(6)无严重心、肺、肝、肾功能障碍。排除标准:(1)导管内肿瘤;(2)肿块位于乳头下方;(3)年龄>70 岁;(4)假体植入术后。剔除标准:(1)在入组后,患者入院完善检查后考虑恶性肿瘤,且伴有腋下淋巴结转移可能性大者;(2)患者因其他疾病或者原因延长住院或治疗的。
1.3 治疗方法(1)定位针组:术前B 超引导下细针穿刺定位,局部浸润麻醉后,根据定位针路径,寻至定位针所定位的组织,行手术切除。(2)旋切组:患者仰卧位,患侧上肢置于头上,常规消毒铺巾。皮肤局部麻醉,在超声引导下避开周围的血管,确定最佳进针点,注射隔离液后,进针对病灶进行旋切、抽吸,直至超声显示目标病灶旋切干净,确定无任何残留后,拔出旋切刀头,压迫止血。标本送快速冰冻,若结果良性肿瘤,在病灶局部的体表部位垫以纱布方加压,然后包扎弹力绷带48h。(3)美兰组:患者取仰卧位,患侧上肢外展,B 超定位肿块位置,常规消毒铺巾,超声引导下在肿块表面选好穿刺点,用7 号注射器垂直声束,在超声下见针尖进入肿块表面后注入美兰0.1mL。采用局部浸润麻醉后,于肿块正上方采用弧形或放射状切口切开皮肤和皮下组织,垂直探查腺体组织,寻找到美兰染色组织后,根据染色指引予以完整切除肿块。
1.4 观察指标(1)临床指标:各手术方式组手术时间,出血量,切口长度,疼痛评分,术后并发症,住院费用,住院天数,肿块病理等数据结果[1]。(2)随访指标:术后随访1 年,观察伤口愈合情况,有无局部残留、复发。(3)病理为恶性的患者,本研究仅统计病理是否符合、肿瘤局部有无残留。
1.5 统计学方法 应用SPSS 22.0 统计软件,组间均数比较采用独立样本t 检验或单因素方差分析,不服从正态分布的数据采用Mann-Whitney’s U 检验;计数资料采用率表示,组间比较采用卡方检验;所有P 值均为双侧检验,P<0.05 为差异有统计学意义。
2 结果
2.1 三组患者一般资料比较 三组患者年龄、肿块直径等比较差异无统计学意义(P>0.05)。术后病理结果:(1)定位针组:纤维腺瘤25 例,乳腺腺病8 例,导管内癌1 例,浸润性癌6 例;(2)旋切组:纤维腺瘤27 例,乳腺腺病7 例,导管内癌2 例,浸润性癌4 例;(3)美兰组:纤维腺瘤22 例,乳腺腺病10 例,导管内癌3 例,浸润性癌5 例。
2.2 三组手术切口比较 旋切组具有最小的手术切口(P<0.01),定位针组与美兰组无明显差异(P>0.05),见表1。
2.3 三组术后疼痛评分比较 旋切组术后疼痛评分最低(P<0.01),定位针组与美兰组无明显差异(P>0.05)。
2.4 三组手术时间、快速冰冻病理时间比较 美兰组手术时间最短(P<0.05)。旋切组术中快速冰冻病理耗时最长(P<0.05),见表1。
2.5 三组手术出血量比较 三组患者手术平均出血量无明显差异(P>0.05),但旋切组有个别患者出血较多,最多一例出血30mL。
2.6 三组治疗费用比较 美兰组治疗费用明显低于旋切组(P<0.01),美兰组与定位针组相比无统计学差异(P>0.05),见表1。
2.7 三组术后并发症情况 定位针组中针脱落者导致定位失败者5 例,术后切口感染1 例。旋切组中术后复发1 例,冰冻病理与石蜡病理不符1 例,手术部位血肿2 例。美兰组术后无切口感染、血肿等并发症发生,术后无复发。
3 讨论
乳腺癌是女性最常见的恶性肿瘤,随着乳腺体检的普及以及乳腺彩超、X 线、MRI 等影像技术的发展,越来越多的不可触及的NPBL 被检出。研究发现,约27%的NPBL 为高危病变甚至不可扪及的乳腺癌(NPBC)[1]。多数NPBC 病灶直径<10mm,质地与正常腺体组织类似,距离体表较远,致使其手术难度较大,传统的开放切除术由于定位识别困难往往盲目扩大手术范围,对乳房外形造成极大破坏,影响美容效果,有时甚至可能漏切而导致误诊[10]。因此对于NPBL 尤其是NPBC,选择合适的定位方式,及时精准切除送检至关重要。
目前NPBL 的切除方法主要有两种:B 超引导定位针固定后切除术、超声引导下微创旋切术[4]。B 超引导定位针固定后切除术在面对纤维瘤或致密腺体时,由于纤维瘤质地光化位置不固定导致金属丝不易刺入结节,致密腺体也会影响进针路径;此外,术中操作如果拔出或移动定位针将直接影响定位效果[4]。本课题组对40 例NPBL 患者开展超声引导细针穿刺定位后切除手术,术中定位针脱落导致定位失败者多达5 例,占该组患者总数的12.5%,且该术式从手术切口、疼痛评分、手术时间及术中出血量等方面与超声引导美兰染色手术方案相比无明显优势,住院费用较美兰术式高,不建议向基层医院推广。
表1 三组不可触及乳腺病变患者术后资料比较(±s)
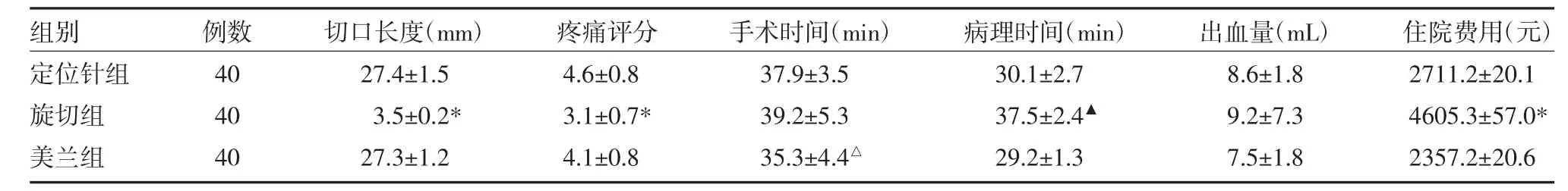
表1 三组不可触及乳腺病变患者术后资料比较(±s)
注:与定位针组、美兰组比较,*P<0.05;与旋切组、定位针组比较,△P<0.05;与定位针组、美兰组比较,▲P<0.05
超声引导下微创旋切术因其在术中动态超声引导下进行,可准确定位并精确切除肿块,而且具有切口小、美容效果好的优点,被认为是目前获得NPBL病理诊断的理想方法[4]。但是,该术式对乳腺腺体内部创伤较大,且存在微小病灶残留问题、癌细胞的针道播散及血行转移问题、假阴性和组织学低估问题、不适用凝血功能异常患者、价格昂贵等缺点,中远期效果仍不明确[4]。本课题组对40 例NPBL 患者开展微创旋切手术,其手术切口3.5mm,远小于另外两种术式,且术后第一天疼痛评分最低,证明该术式术后美容效果和手术耐受度最好。但是微创旋切术所取标本为碎片,对于组织切缘及有无残留判断较困难,造成术中冰冻耗时久,手术时间长的缺点。并且在本课题组纳入的120 例患者术后1 年的随访中,有1例患者术后复发、1 例冰冻与病理不符,均出自微创旋切组。微创旋切术还由于其不能直视下止血致使发生术中术后出血的概率增大,我们的研究中40 例行旋切术的患者有2 例发生术后局部血肿形成,占该组所有患者的5%。同时,微创旋切术需要专用器械,需要外科医师接受专业培训才能开展,治疗均费为4604.7 元,远高于另外两种手术方案,因此基层医院难以普及。
超声引导美兰染色定位切除术式的优点:(1)手术时间短,该方法定位准确性高,不需反复探查,也避免对隧道不必要的广泛分离,减少损伤;(2)住院费用低,美兰成本低廉,良性病例均费只有1480 元;(3)近期远期并发症少,入组的40 例患者无切口感染、血肿、定位失败等并发症发生,术后随访1 年无复发、转移;(4)操作简单。但是也要注意:(1)美兰弥散较快,需要在定位后尽快手术,手术时间尽量控制在30min 之内;(2)要在超声引导下确保美兰注射在病灶内;(3)注射0.05-0.1mL 美兰已足够染色,注射过多反而影响操作视野和准确性;(4)可循染色针道寻找肿块。超声引导美兰染色对于性质不确定的NPBL 是一种安全有效的手术方式,操作简单方便,有较高的经济学价值。
