结肠癌急诊全结肠系膜切除术的临床疗效
2019-09-25刘发强王重周迈常迎彬
刘发强 王重 周迈 常迎彬
结直肠癌全球发病率逐年增高,2015年中国新增病例37.63 万例[1],其中伴发肠梗阻、肠穿孔、出血等需急诊处理病例占30%以上,以肠梗阻为最常见(达70%)。由于急诊手术患者无法完善肠道准备,术中情况复杂多变,术后患病率较高,可采取传统的姑息治疗,争取机会或完善准备行择期手术。但部分患者情况危急,常需急诊手术以挽救生命[2-4]。2009年,德国的Hohenberger 等[5]首先提出全结肠系膜切除术(complete mesocolic excision,CME)概念,并逐渐在临床上推广使用。CME 具有视野清晰,根治效果好,无病生存时间较长等优点[6]。目前,尚缺乏CME在结肠癌急诊手术中的应用报道。民航总医院自2014年5月起开展CME 术式,根据患者入院时间和手术方式,本研究回顾性对比分析了结肠癌患者急诊手术中采取传统根治术和CME的短期临床效果和安全性。
1 材料与方法
1.1 病例资料
回顾性分析民航总医院于2011年1月至2017年12月因肠梗阻、穿孔、出血等原因行急诊开腹手术的84 例结肠癌患者临床资料。纳入标准:1)年龄≥18岁;2)伴发肠梗阻、出血或穿孔等,保守治疗无效;3)术前无重要脏器功能障碍。排除标准:1)合并智力障碍或精神疾患;2)依从性差者;3)术前伴随重要脏器功能障碍等严重内科疾患,无法耐受手术者;4)术前影像学检查不除外cTNM 分期Ⅳ期者。本研究通过民航总医院伦理委员会审核,所有患者及其家属术前均告知手术方式,全部手术均由同一团队共同完成,入组患者均接受肿瘤Ⅰ期切除吻合术。根据上述条件,共入组53例患者,以民航总医院开展CME术式起始时间为界限,按照手术方式方法的异同,分为传统手术组28例,CME组25例。
1.2 方法
1.2.1 术中结肠肿瘤远近端灌洗 所有患者急诊开腹术中均行大量生理盐水结肠灌洗[7-8]。具体方法如下:首先距肿瘤近端至少10 cm 处结扎离断肠管,近端肠管置入清洁袋内,自Treize韧带由头端逐渐挤压排出肠内容物,距阑尾根部2 cm处切除阑尾,经阑尾开口置入双腔单囊标准型导尿管并固定,自导尿管内注入5 000~10 000 mL 生理盐水灌洗结肠。待肿瘤切除后,自远端肠管断端注入适量生理盐水灌洗远端结肠,自肛门流出灌洗液。均灌洗至流出液清洁透亮为止。
1.2.2 手术方式 CME组:患者急诊入院后均行胃肠减压、禁食水、营养支持、抗休克等保守治疗,疾病均无明显缓解,进而行急诊开腹手术治疗。患者全身麻醉后,取仰卧分腿位,消毒铺巾,取纵行经腹直肌探查切口或腹部正中切口逐层进腹,腹腔探查后按下述步骤手术:1)按上述方法行结肠近端灌洗;2)全结肠系膜切除:行右半结肠切除术时,首先锐性游离胰头、十二指肠至肠系膜上动脉根部(Kocher手法),再按逆时针方向逐步游离升结肠、回盲部及回肠末端,将升结肠及其系膜充分游离、掀起,再从内侧入路,充分显露肠系膜上静脉和动脉,在右结肠及回结肠血管根部离断结扎。结肠肝曲肿瘤则需游离结扎中结肠及胃网膜右血管根部,清扫其周围淋巴结。行左半结肠切除术时,需按顺时针方向,将结肠脾曲、降结肠、乙状结肠外侧腹膜入路,将肠管及其系膜充分游离掀起,注意保留肾前脂肪、左侧输尿管及生殖血管等结构。横结肠及结肠脾曲肿瘤按“动脉弓原则”切除距离肿瘤10 cm范围的胃网膜动脉弓和幽门下淋巴结,即从胃网膜右血管根部离断结扎,之后锐性分离大网膜与横结肠系膜,于胰腺下缘分离结扎中结肠血管,彻底清扫其周围淋巴结;3)依照上述方法行结肠远端灌洗;4)肠道重建Ⅰ期吻合,大量温热生理盐水冲洗腹腔,留置引流管,逐层关腹。
传统手术组:患者急诊入院后的术前处理同CME 组。术中处理:1)依照上述方法行结肠近端灌洗;2)切除肿瘤近端、远端肠管至少10 cm,之后完成结肠周围区域淋巴结清扫,切除包括肿瘤在内的局部肠管及部分系膜;3)依照上述方法行结肠远端灌洗;4)肠道重建Ⅰ期吻合,大量温热生理盐水冲洗腹腔,留置引流管,逐层关腹。
1.2.3 观察指标 一般资料:年龄、性别、术前Karnofsky活动功能状态评分、麻醉评分(ASA)、肿瘤大小、肿瘤部位等。临床数据:手术时间、手术出血量、淋巴结清扫数目、病理分期、住院时间、副损伤、术后首次肛门排气时间、术后并发症、术后30天死亡率等。
由于本研究纳入患者均为急诊入院,因急诊检验条件所限,术前缺乏CEA 等肿瘤标记物的实验室化验结果。全部患者在首次肛门排气后,即开始进水及流食。
1.3 统计学分析
采用SPSS 24软件进行统计学分析。计数资料采用χ2检验。计量资料先行单样本K-S检验验证正态分布,服从正态分布者,在F检验基础上(齐/异方差)进行两个独立样本单尾t检验;不服从正态分布者,进行两个独立样本非参数Mann-Whitney U检验。以P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者一般资料
两组患者术前就诊原因各有不同。CME组中术前有肠梗阻者19 例(76%);消化道出血引起失血性贫血者4 例(16%);表现为急性阑尾炎特征,术中发现为盲肠部肿物,术后病理证实为盲肠部肿瘤者2例(8%)。传统手术组中术前有肠梗阻者21 例(75%);消化道出血引起失血性贫血者6 例(21.4%);术前肿瘤性穿孔1例(3.6%)。
所有入组患者的中位年龄为67(44~92)岁。两组患者的年龄、性别、术前Karnofsky活动功能状态评分、ASA评分、肿瘤大小、肿瘤部位等指标差异均无统计学意义(P>0.05,表1)。
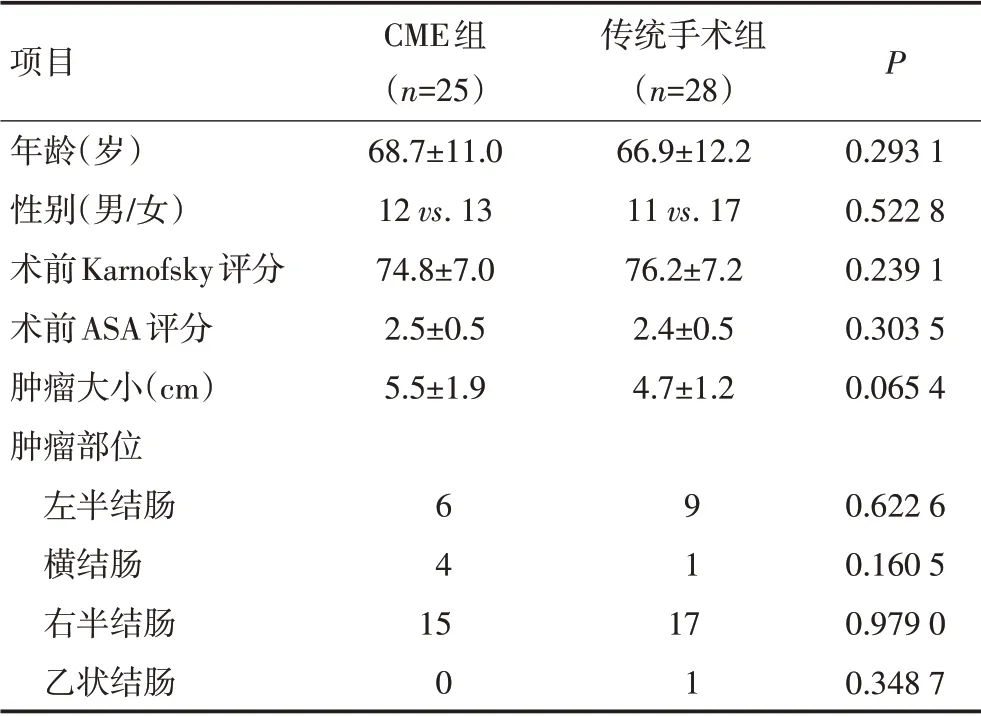
表1 两组患者一般资料
2.2 两组患者术中情况与术后短期临床效果的比较
全部患者均顺利完成手术,均未发生术中副损伤。两组的手术时间、手术出血量、病理分期、住院时间、首次肛门排气时间等指标差异均无统计学意义;CME组淋巴结清扫数目显著增加(P>0.05,表2)。
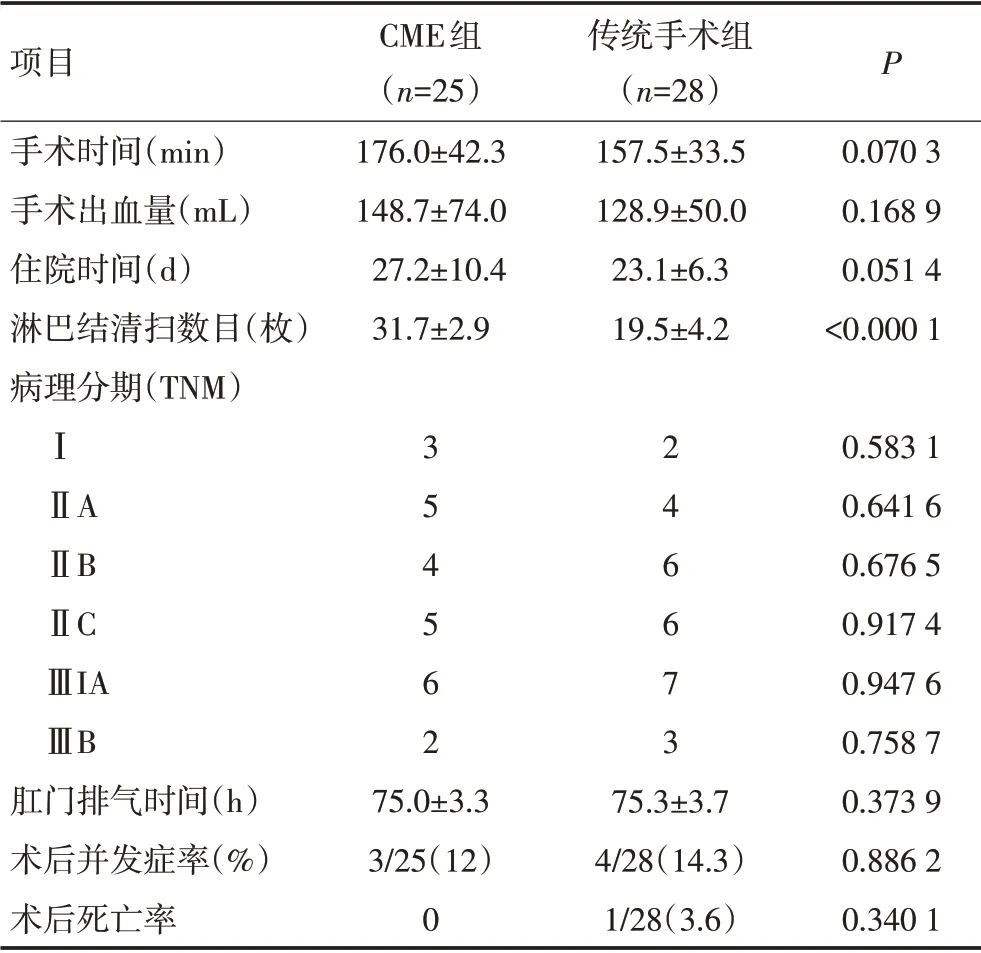
表2 两组病例术中情况与术后短期临床效果和预后的比较
2.3 两组患者术后短期预后比较
两组的术后并发症率、术后死亡率等指标差异均无统计学意义(P>0.05,表2)。
CME 组术后并发症率为12.0%(3/25):1 例术后肠梗阻,1 例肺部感染并切口感染,另1 例切口感染。传统手术组术后并发症率为14.3%(4/28):1 例切口感染,2 例发热,明确为中心静脉导管感染,1 例术后吻合口瘘,伴发心衰、肾衰,于术后第26天死亡。
其中术后发热(中心静脉导管感染)、肠梗阻、肺部感染等属于术后并发症Clavein 系统分级Ⅰ级,切口感染经局部换药后逐渐痊愈,属于Ⅲa 级并发症。本研究入组患者无Ⅲb级以上并发症发生。
3 讨论
结肠癌急诊患者围手术期病情复杂,需手术者多数存在急腹症或消耗性表现,如发热、腹痛、贫血和低蛋白血症等[9]。本研究入组患者均行结肠癌急诊根治性切除并Ⅰ期吻合术,传统手术组有1例术后发生吻合口瘘,同时伴发心衰、肾衰,于术后30 天内死亡。有研究认为结肠癌急诊Ⅰ期切除吻合手术具有一定安全性[7,10-11]。临床实践表明,预防性肠造瘘可降低吻合口瘘发生后的死亡率,本研究建议临床上应结合患者全身情况及局部肠管血运情况,实时性预防性肠造瘘,避免更严重后果。
急诊结肠癌患者多属中晚期,以Ⅱ~Ⅲ期为主,预后较差[12-13]。本研究入组患者符合这一规律。对于此类患者,既往为了缩短手术时间、降低损伤,多数采取相对保守的处理方法[3,7,10-11]。在充分考虑安全的基础上,本研究结合CME 在民航总医院的开展情况,探索了CME 在此类患者中的临床应用。结果提示,虽然此类患者多数合并肠梗阻导致的肠壁水肿或肠管严重扩张,经过充分准备,如术中肿瘤远近端的结肠灌洗,CME亦能顺利实施,并未明显延长手术时间,两组患者的术中出血量与术后的肛门排气时间接近,提示CME并未增加副损伤;在解剖层面的游离,术后肠道功能的恢复也相应得以保障;CME虽然扩大了术中游离和切除范围,但术后并发症率与传统手术组相当。因此,本研究认为,CME可安全地应用于结肠癌急诊患者中。
与传统的根治手术方式相比,CME 具有较多优点[5-6,14-15]:1)肿瘤学优势:沿胚胎解剖学间隙锐性游离至系膜血管起始部,从根部结扎肿瘤的供养血管,达到彻底清扫淋巴结的效果。结肠癌淋巴结转移的第1站位于肠管周围,第2站位于结肠系膜,第3站位于系膜血管根部。从根部结扎供养血管,则有利于清扫更多数量的淋巴结,达到更彻底的D3 根治效果。2)手术标准化优势:2008年,英国的West等[16]提出的结肠系膜平面手术,与CME具有相同的优势,即可以通过规范化培训,使专业外科医生的手术理念和技术进一步标准化、强化,进而使结肠癌手术过程更加规范化,尤其Ⅲ期以上的结肠癌,能够获得更好的淋巴结清除率和5年生存率。
近年来部分系统评价提示[6,17-18],CME 能够达到更好的根治效果,但并未明显改善患者的远期生存质量和生存率。对于普遍高龄的结肠癌急诊患者而言,全身情况更为复杂,预后的负面影响因素更多,因此亟需进一步研究揭示CME 对此类患者远期预后的影响。
综上所述,本研究表明,对于需急诊手术处理的结肠癌患者,CME 能够获得与传统根治手术相当的短期临床效果和预期,并未增加手术危险性,值得临床推广应用。
