乳腺原发性腺样囊性癌的影像学表现
2019-09-25张淑平青春韩敏刘芳芳刘佩芳
张淑平 青春 韩敏 刘芳芳 刘佩芳
乳腺原发性腺样囊性癌(adenoid cystic carcinoma,ACC)是一种临床罕见的特殊亚型乳腺癌,约占所有乳腺恶性肿瘤的0.1%[1]。该病预后较好,极少发生区域淋巴结和远处转移,5年和10年生存率分别可达95%和90%以上[1-2]。术前通过乳腺影像学检查诊断或提示临床,对治疗和预后具有重要意义,而目前关于其影像学表现的报道较少且多为个案报道,认识尚不充分。本研究旨在通过分析乳腺原发性ACC 的X 线和超声检查表现,探讨其影像学特征,提高对其认识和术前诊断准确性。
1 材料与方法
1.1 一般资料
收集2012年1月至2018年9月天津医科大学肿瘤医院临床、病理和影像学检查完整的31 例乳腺原发性ACC 患者的资料,均为女性,年龄32~75 岁,平均57.5 岁,其中年龄<50 岁为4 例、50~60 岁为15例、年龄>60岁为12例。31例患者中除1例宫颈癌和1例对侧乳腺非特殊型浸润性导管癌曾治疗外,其余患者均无肿瘤相关病史和乳腺癌家族史。
1.2 方法
1.2.1 乳腺X 线检查 使用LORAD Selenia 全数字化乳腺X 线机(美国HOLOGIC 公司),选用AUTOTIME 曝光模式,常规行双乳头尾位(craniocaudal,CC)和内外斜位(mediolateral oblique,MLO)摄影,必要时加行病变局部加压摄影。
1.2.2 乳腺超声检查 使用LOGIQ E9 彩色多普勒超声诊断仪(美国GE公司)和6~15 MHz变频线阵探头。患者仰卧位,充分暴露乳房,常规行二维超声检查,从边缘向乳头方向反放射状和旋转扫查,发现病变后行多切面扫查及彩色多普勒血流成像(color doppler flow imaging,CDFI)、弹性成像检查。
1.2.3 影像分析 根据美国放射学院乳腺影像报告与数据系统(breast imaging reporting and data system,BI-RADS)标准(2013年),由2 名经验丰富的乳腺影像诊断医师对病变表现进行分析。乳腺X 线检查分析内容包括病变基本类型、是否伴钙化及具体表现。乳腺超声检查分析内容包括病变类型、大小/范围和具体特征、周围组织表现、是否伴钙化、CDFI 及改良5分法的弹性成像评分[3]。
1.2.4 组织病理学检查 手术标本以4%甲醛固定,常规石蜡包埋,蜡块连续切片,切片厚度4 μm。所有病变均行H&E 染色及免疫组织化学法检测雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)及人表皮生长因子受体-2(human epidermal growth factor receptor-2,HER-2)等表达。
1.3 随访
共21例患者随访资料完整,随访时间为2~58个月,中位随访时间为32个月。随访期间1例患者于根治术后22个月发现胸壁复发(切检病理为ACC),其余20例均未发现复发或转移。
2 结果
2.1 影像学表现特征
31例患者的乳腺X线检查表现及BI-RADS诊断情况见表1,将圆形、卵圆形和分叶形归为形态规则类。31例患者中25例表现为肿物,其中16例高或稍高密度肿物多数符合乳腺癌的典型X 线表现(图1A)、7例等密度肿物中多表现为边缘模糊(图1B)、2例混杂密度肿物包括1 例含脂肪样密度和1 例呈中等-稍低混杂密度,6 例表现为局限不对称致密(图1C)。所有病例均无钙化。
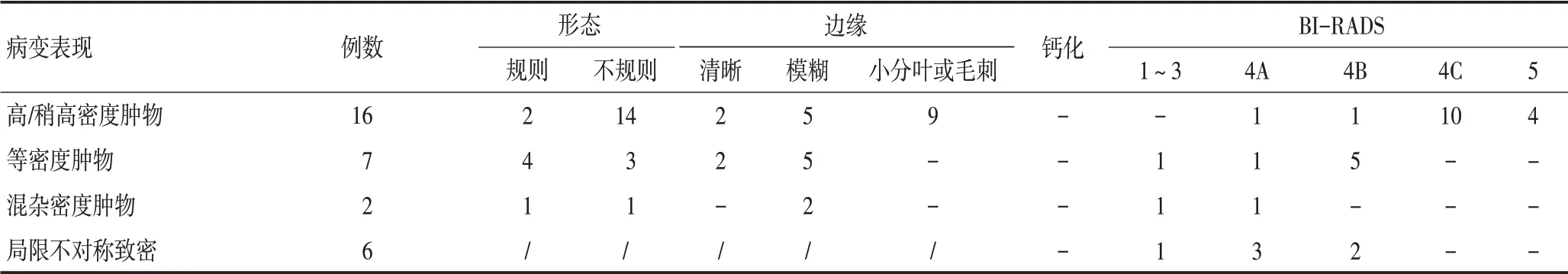
表1 31例乳腺原发性ACC患者的乳腺X线表现及BI-RADS诊断情况
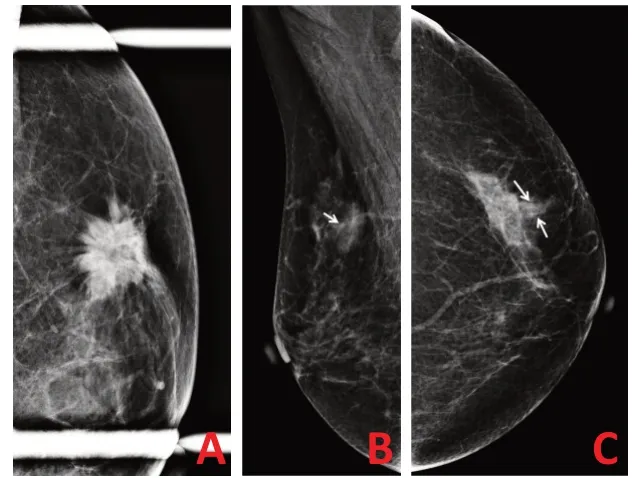
图1 乳腺原发性ACC的X线表现
31例患者的乳腺超声检查中25例表现为低回声(22例)和混合回声(3例)肿物,6例表现为低回声或混合回声区的非肿块样病变(表2)。22例低回声肿物中14例符合乳腺癌的典型超声表现(图2A)、BI-RADS分类为4C或5类、弹性成像评分包括3分3例、4分8例、5分3例,其余8例均有若干征象不符合乳腺癌的典型超声表现、BI-RADS分类包括4A类3例和4B类5例。3例混合回声肿物的BI-RADS分类均为4B,其中2例表现为高回声为主(图2B)、1例表现为囊实性混合回声并呈多发肿物融合堆积状。6例非肿块样病变中3例表现为以偏高回声为主的混合回声区(图2C)、BI-RADS分类为4A类2例、4B类1例,3例表现为不均匀低回声区患者中2例伴周围组织回声增强、BI-RADS分类4B类2例和4C类1例。非肿块样病变均无沿导管走行方向分布的趋势。
2.2 临床病理特征
31例乳腺原发性ACC患者均无腋窝淋巴结转移,免疫组织化学法检测显示ER、PR及HER-2均阴性为23例,ER和PR阳性、HER-2阴性为3例,ER阳性、PR阴性、HER-2阴性为5例。典型病例的病理表现见图3。

表2 31例乳腺原发性ACC患者的超声检查表现

图2 乳腺原发性ACC的超声表现

图3 乳腺原发性ACC的病理表现(H&E×40)
3 讨论
乳腺原发性ACC 多发生于30~90 岁女性,以50岁以上较为常见,偶见男性病例报道[4-5],确诊的平均年龄为63岁[6]。本研究的年龄分布特点与文献报道基本一致,但平均发病年龄小于国外的研究[2,6],符合中国女性乳腺癌发病年龄早于欧美国家的特点。在临床上,常可触及边界清、质地韧、活动度较好的肿块,多见于乳晕区,少有乳头溢液[1-2]。大体病理上肿瘤界限清晰,镜下由腺上皮和肌上皮细胞排列成经典的管状或筛状结构,真、假腺腔均可见到,也可见实性结构,具有显著基底样特征,联合多种免疫组织化学检测有助于病理诊断与鉴别[7-8]。关于其临床治疗方案尚存争议,多数研究[6-9]发现乳腺原发性ACC 的ER、PR 和HER-2表达常为阴性,但不同于传统意义的三阴性乳腺癌,预后良好,很少发生区域淋巴结和远处转移,单纯乳腺切除即可治愈,分期较晚时需行根治性手术,局部复发可能与肿瘤切除不完全有关。辅助放化疗的临床获益尚待进一步研究。
乳腺原发性ACC 的影像学表现报道较少,且多为个案分析[5,10-12]。乳腺X线上可表现为不规则形或分叶形肿块,密度较高,边界不清或部分清晰,也可表现为局限不对称致密,钙化罕见,仅Santamaría等[10]研究中有1 例表现为局限不对称致密伴细小钙化。本研究16 例高或稍高密度肿物中14 例符合乳腺癌的典型X线表现,另2例结合患者近期触及肿物明显增大的病史,考虑叶状肿瘤而误诊。2例混杂密度肿物中1例含脂肪样密度,一般认为X线上含脂肪样密度肿物多数为良性,该患者术后组织病理学检查显示肿物内含错构瘤成分,分析其X线表现发现肿物内除含脂肪样密度外,其他密度明显高于邻近正常乳腺实质,且部分边缘模糊,具有一些恶性肿瘤征象,该患者超声表现为高回声为主的混合回声肿物,BI-RADS分类为4B类;另1例可见稍低密度区,边缘模糊不清,术后病理显示癌组织累及周围脂肪,相应超声表现为低回声肿物伴周围组织回声增强,以浅层皮下脂肪层回声增强为主,推测可能与邻近脂肪受累有关,以上特殊表现鲜见报道。乳腺X线表现为局限致密是诊断的难点,常需与既往X线片比较或结合局部加压摄影、断层合成图像等进一步分析,结合超声和MRI 检查综合分析有助于诊断与鉴别诊断。本研究6例乳腺X线表现为局限致密的患者,相应超声检查中4例表现为肿块型病变,其形态学及血流动力学相关表现为诊断提供了更多依据,因此,多种影像学检查相结合可为临床提供更多参考。本研究中患者的乳腺X线检查均无钙化表现。
本研究超声检查表现为低回声肿物的乳腺原发性ACC 大部分符合乳腺癌的典型超声表现,与其他研究相一致[5,11-14],但均无后方回声衰减,可能与组织病理学特征相关。组织病理学检查显示,镜下可见肿瘤的腺上皮和肌上皮细胞排列不如常见的浸润性导管癌致密,组织对超声波的吸收相对较弱,因此少有后方回声衰减表现。以高回声为主的混合回声肿物是乳腺原发性ACC 的少见超声表现,可能因癌组织向邻近脂肪组织浸润导致脂肪层回声增强,需与脂肪坏死及炎症性病变相鉴别。典型脂肪坏死多有外伤、手术等相关病史,常发生于皮下脂肪层,有随时间缩小的趋势,而炎症性病变的症状多数较明显,常伴触痛,结合临床并分析其影像学表现大部分尚可鉴别,必要时需行穿刺活检。此外,本研究6 例患者表现为非肿块样混合回声或不均匀低回声区,均无沿导管走行方向分布的趋势,与浸润性导管癌呈“导管样”或“段样”沿导管走行方向分布的特点不同,因此,超声检查发现此征象时,在排除炎症等病变后可考虑有腺样囊性癌的可能。超声CDFI表现无特异性,弹性成像评分对此病诊断意义不大。
综上所述,本研究为回顾性研究,存在一些局限性。因仅2例行乳腺MRI检查且表现差异较大(分别为不规则形肿物和非肿块样异常强化),未行具体分析。另外,乳腺X线和超声检查显示的一些少见征象因病例数较少未行统计学分析,仍需积累更多病例进一步研究。乳腺原发性ACC大部分具有恶性病变的典型影像学表现,但术前确诊困难。当发现病变在乳腺X 线表现为形态不规则且边缘模糊的高密度肿物内含稍低密度或脂肪样密度、乳腺超声表现为偏高回声为主且不沿导管走行方向分布的非肿块样病变时,可考虑有腺样囊性癌的可能,但确诊仍需依靠病理。
