江西吉安地区高尿酸血症患病情况及危险因素分析
2019-09-18孙俊明徐柳青蒋晓露聂正玉庄守纲
方 路,潘 星,孙俊明,徐柳青,陶 敏,蒋晓露,刘 娜,聂正玉,庄守纲
江西吉安地区高尿酸血症患病情况及危险因素分析
*方 路1,潘 星1,孙俊明1,徐柳青2,陶 敏2,蒋晓露2,刘 娜2,聂正玉1,庄守纲2
(1. 上海市东方医院吉安医院,江西,吉安 343000;2. 上海市东方医院,上海 200001)
了解江西省吉安市人群高尿酸血症患病特点及相关危险因素分析。在2018年1月1日至7月30日期间于吉安医院体检的人群中,随机抽取1000名16岁及以上吉安常住居民体检者作为研究样本,统计不同年龄段、不同性别者高尿酸血症的患病率,并应用Logistic回归模型进行高尿酸血症相关危险因素分析。1000名体检者中高尿酸血症患病率为23.3% (95%20.68%~25.92%),其中男性患病率28.08% (95%24.44%~31.73%)明显高于女性患病率16.59% (95%13.01%~20.16%),具有统计学意义(< 0.001)。多因素logistic回归分析显示收缩压(= 1.014, 95%= 1.005-1.023,= 0.002)、甘油三酯(=1.263, 95%= 1.106-1.443,= 0.001)、低密度脂蛋白(=1.376, 95%=1.026-1.845,= 0.033)升高,肾小球滤过率(=0.985, 95%= 0.977-0.993,<0.001)和高密度脂蛋白(= 0.612, 95%= 0.402-0.931,= 0.022)降低是高尿酸血症的独立危险因素。在江西省吉安地区人群中,收缩压、甘油三酯、低密度脂蛋白升高,肾小球滤过率和高密度脂蛋白降低是高尿酸血症的独立危险因素。积极控制血压、血脂,保护肾脏功能,对于预防和治疗高尿酸血症具有重要意义。
高尿酸血症;患病率;危险因素
尿酸作为嘌呤化合物在人体代谢的终末产物,其代谢过程受到环境或遗传因素影响,导致代谢失调后而引起血尿酸水平的升高。研究表明,伴随着人们生活质量的提高及饮食结构的改变,例如进食富含蛋白质及嘌呤的食物,高尿酸血症的患病率越来越高[1]。多项基础及流行病学研究均提示血尿酸水平的升高与动脉粥样硬化、冠心病、高血压等心血管疾病的发生显著相关[2-6]。Wheeler等人的一项meta分析结果显示,在患有高尿酸血症的人群当中,男性患心血管疾病的相对风险会增加1.12,女性会增加1.22[7]。同时另1项前瞻性队列研究meta分析结果也显示,血尿酸每升高1 mg/dL,心血管疾病的死亡率增加12%[8]。为了解高尿酸血症在江西省吉安地区患病情况及分布特征,并进一步探索影响血尿酸升高的相关危险因素,本研究对2018年1月1日至7月30日吉安地区16岁及以上常住城市户籍居民体检者的体检资料进行了统计分析。
1 资料与方法
1.1 一般资料
在2018年1月1日至7月30日期间上海市东方医院吉安医院体检的人群中,随机抽取1000名16岁及以上吉安常住居民体检者作为研究对象,并签署知情同意。研究对象年龄16~89岁,平均(48.12 ± 14.82)岁,中位年龄49岁,其中包括女性416名,男性584名。
1.2 方法
1.2.1 基本信息
基本信息包括患者年龄、性别、身高(m)、体重(kg)和血压(mmHg)。血压测量采用水银血压计,保持环境安静,检查者取坐位,保持右上肢与心脏、血压计持平状态,测量2次,间隔1 min,取平均值。体质指数(BMI)= 体重(kg)/身高^2(m)。
1.2.2 血液生化检测
所有体检者空腹抽取静脉血,静置待凝固后离心,取上层血清于迈瑞BS-300全自动生化分析仪上测定,检测指标包括肌酐、尿素、尿酸、白蛋白、总胆固醇、甘油三酯、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)、血糖及肾小球滤过率(GFR)。所有生化指标均在江西省吉安市的上海市东方医院吉安医院完成。
1.3 诊断标准
高尿酸血症诊断标准参照《内科学(第8版)》教材:血清尿酸男性≥ 420 μmol/L,女性≥ 360 μmol/L。肾小球滤过率(eGFR)的计算采用了 2012年改善全球肾脏病预后组织(KDIGO)指南推荐的 EPI公式[9]。
1.4 统计方法
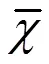
2 结果
2.1 不同性别、年龄,高尿酸血症分布特点
1000名体检者中,有233名体检者血尿酸水平超过正常范围,患病率为23.30%(95%20.68%~25.92%),其中男性164人,患病率为28.08% (95%24.44%~31.73%),女性69人,患病率为16.59% (95%13.01%~20.16%),男性的高尿酸血症患病率明显高于女性,差异有统计学意义(2= 17.97,< 0.001)。结果见表1。
表1 不同性别人群中尿酸症的患病情况

Table 1 Prevalence of hyperuricemia in different genders
女性人群血清尿酸水平随着年龄增加而升高,单因素方差分析显示差异具有统计学意义(0.027)。结果见表2。不同年龄段、不同性别下高尿酸血症患病情况,结果见图1。
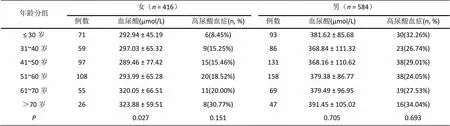
表2 不同年龄段、不同性别尿酸平分布情况
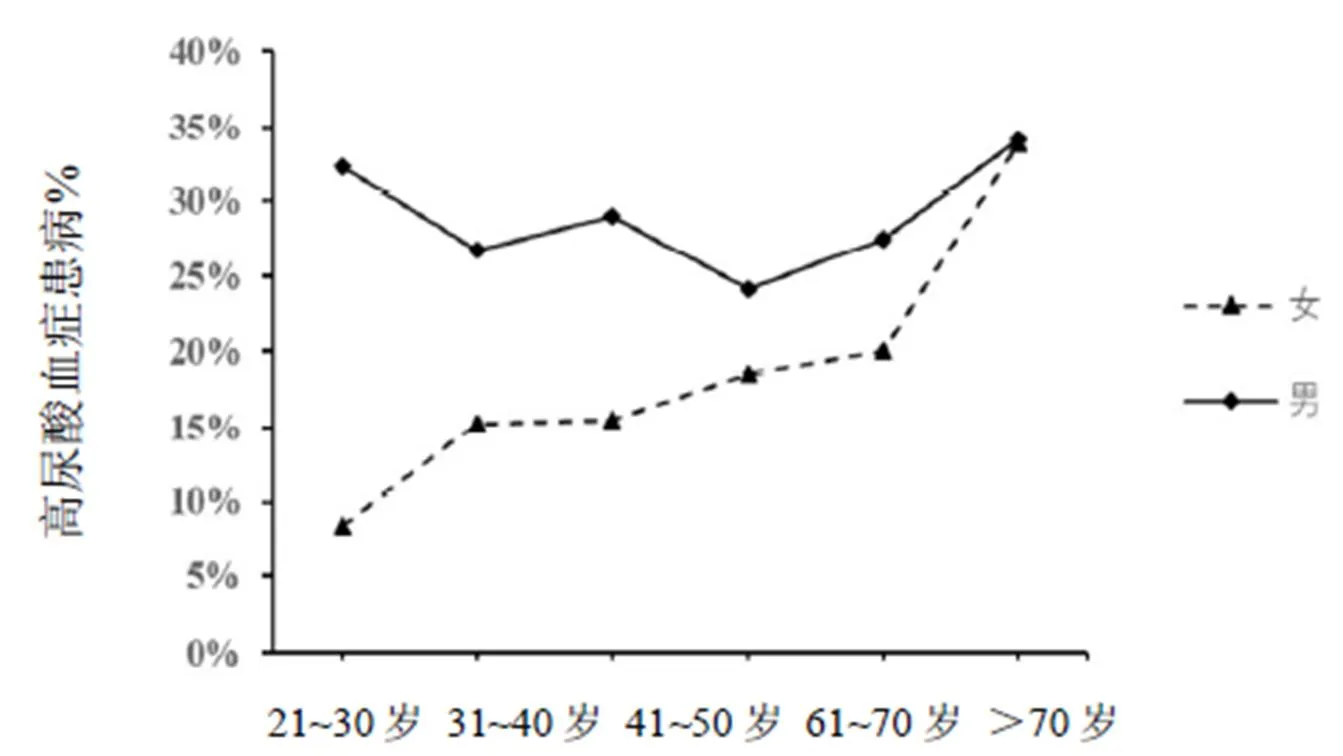
图1 不同年龄段、不同性别高尿酸血症的患病情况
与正常尿酸组相比,高尿酸人群组的BMI、收缩压、舒张压、空腹血糖、血清肌酐、总胆固醇、甘油三酯、低密度脂蛋白水平均偏高,高密度脂蛋白及肾小球滤过率均偏低,且具有统计学意义(< 0.05)。结果见表3。
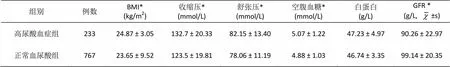
表3 正常血尿酸与尿酸症群的代谢相关指标的比较
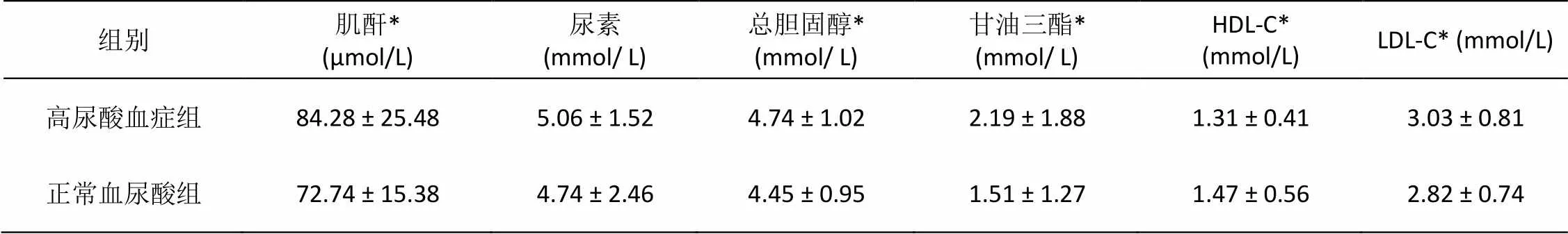
组别肌酐*(μmol/L)尿素(mmol/ L)总胆固醇* (mmol/ L)甘油三酯*(mmol/ L)HDL-C*(mmol/L)LDL-C* (mmol/L) 高尿酸血症组84.28 ± 25.485.06 ± 1.524.74 ± 1.022.19 ± 1.881.31 ± 0.413.03 ± 0.81 正常血尿酸组72.74 ± 15.384.74 ± 2.464.45 ± 0.951.51 ± 1.271.47 ± 0.562.82 ± 0.74
注:BMI:体重指数, GFR:肾球滤过率, HDL-C:高密度脂蛋白胆固醇,LDL-C:低密度脂蛋白胆固醇, *: 两组间比较,<0.05
2.3 高尿酸血症相关危险因素分析
以高尿酸血症为因变量,将性别作为二分类变量,年龄、BMI、收缩压、空腹血糖、血清白蛋白、总胆固醇、甘油三酯、高密度脂蛋白、低密度脂蛋白血症、肾小球率滤过率等因素作为连续性自变量,分别纳入模型进行单因素logistic回归分析。对单因素分析中< 0.05的变量,采用后退法进一步筛选自变量,进行多因素logistic回归分析,结果显示收缩压每升高1 mmHg,患高尿酸血症的优势比(自变量每变化一个单位,高尿酸血症的患病概率与不患病概率的比值是变化前相应比值的倍数)为1.014(= 1.014, 95%= 1.005-1.023,= 0.002);甘油三酯每升高1 mmol/L,患高尿酸血症的优势比为1.263(= 1.263, 95%= 1.106-1.443,= 0.001);高密度脂蛋白每升高1 mmol/L,患高尿酸血症的优势比为0.612(= 0.612, 95%= 0.402-0.931,= 0.022);低密度脂蛋白每增加1 mmol/L,患高尿酸血症的优势比为1.376(= 1.376, 95%= 1.026-1.845,= 0.033);肾小球滤过率每升高1 mL/(min*1.73 m2), 患高尿酸血症的优势比为0.985(= 0.985, 95%= 0.977-0.993,<0.001)。因此,收缩压、甘油三酯、低密度脂蛋白升高,肾小球滤过率和高密度脂蛋白降低是高尿酸血症的独立危险因素(结果见表4)。
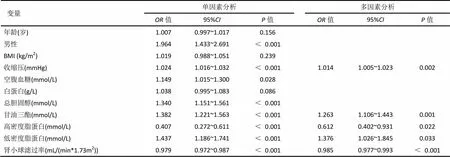
表4 尿酸症相关危险因素分析
3 讨论
人体尿酸生成主要来源于两大途径:一是内源性尿酸,主要依赖于体内核蛋白分解代谢;另外一条途径则是外源性尿酸,依赖于摄入食物当中富含的嘌呤分解代谢而来[10]。随着人们生活水平和生活方式的改变,摄入过多富含嘌呤的食物,引起外源性尿酸生成增多,破坏尿酸代谢平衡,这是高尿酸血症的一个重要发生机制。本研究发现,江西省吉安地区体检人群中高尿酸血症患病率为23.3% (95%20.68%~25.92%),明显高于陈涛等调查的我国9省市2005~2006年高尿酸血症患病率12.08%[11],也高于刘姝等成都地区2010年高尿酸血症患病率20.14%[12],且接近于李瑜鹏等齐齐哈尔地区2015~2016年高尿酸血症患病率23.2%[13],表明近年来高尿酸血症患病率呈明显上升的趋势。这可能是由于经济的快速发展,同时伴随而来的人口老年化现象加重,肥胖人群增多,高嘌呤的食物摄入增多以及人们喜欢熬夜、饮酒等不健康的生活习惯等因素,在不同程度上导致的高尿酸血症患病率的增加。
本研究发现,与男性人群相比,女性人群平均血尿酸水平随年龄增长呈上升趋势(< 0.05)。男性高尿酸血症患病率28.08% (95%24.44%~31.73%)明显高于女性16.59% (95%13.01%~20.16%)(< 0.05)。这与姜昌丽等在昆明地区的调查研究结果相一致[14]。有相关研究发现,人体尿酸转运体(human urate transporter,hUAT)作为肾尿酸分泌的关键物质,其基因表达受到人体内雌激素水平的调控,较高水平的雌激素可以上调hUAT基因表达,增加hUAT数量,促进肾脏排泄尿酸,最终降低人体内血尿酸水平[15]。
本研究对高尿酸血症相关危险因素分析时发现,升高的收缩压、甘油三酯、低密度脂蛋白,降低的高密度脂蛋白是高尿酸血症的独立危险因素。这与Choi等人的研究结果相一致,他们发现在美国成人中血尿酸水平升高的患者同时伴发代谢综合征(高血压、血脂异常、糖尿病等)的概率高达62.8%[16]。在过去的研究中发现,代谢综合征发生的主要机制为胰岛素抵抗,胰岛素的增加可以抑制肾脏分泌尿酸,同时通过促进人尿酸盐转运子(human urate transporter 1, URAT1)和近曲小管刷状缘上Na+离子通道对尿酸的重吸收使血尿酸水平上升[17-18]。代谢综合征中氧化磷酸化过程受到破坏是造成水钠及尿酸盐潴留的另一项重要机制[18]。
除此之外,该研究发现高尿酸血症与肾功能不全有着紧密的联系。血肌酐升高、GRF降低,肾脏滤过功能受损,直接影响肾脏对于尿酸的分泌,高浓度的尿酸盐离子转化为尿酸盐沉积于肾小管及肾间质中,诱发炎症反应,引起肾脏纤维化[19-20],进一步加速肾功能恶化,如此反复形成恶性循环,最终发展为慢性肾功能衰竭。因此加强对高血压、血脂异常和肾功能不全的筛查,合理使用药物调脂、降压、改善肾功能,对于预防和治疗高尿酸血症同样具有重要意义。
综上所述,高尿酸血症的发生,通常会伴有代谢异常及肾功能受损,并且会增加心血管疾病的患病率及死亡率。持续升高的血尿酸水平,会引起患者的尿酸盐沉积于关节及肾脏,最终引发痛风发作及慢性肾脏衰竭[10, 21-22]。因此加强对人群,尤其是健康无症状人群高尿酸血症的筛查,适当干预人群生活及饮食方式,鼓励低盐、低脂优质蛋白饮食,控制血压,对于高尿酸血症的治疗及疾病管理具有重要意义。
[1] Choi H K. A prescription for lifestyle change in patients with hyperuricemia and gout[J].Curr Opin Rheumatol, 2010,22(2):165-172.
[2] Egas-Izquierdo M, Wong-Achi X, Alvarado-Villa G, et al. Relation between serum uric acid levels with the degree of coronary artery disease: A prospective study from Ecuador[J]. Clin Investig Arterioscler, 2019,31(1):8-14.
[3] Wang J, Qin T, Chen J, et al. Hyperuricemia and risk of incident hypertension: a systematic review and meta-analysis of observational studies[J]. PLoS One,2014,9(12):e114259.
[4] Kang D H, Park S K, Lee I K, et al. Uric acid-induced C-reactive protein expression: implication on cell proliferation and nitric oxide production of human vascular cells[J].J Am Soc Nephrol,2005,16(12): 3553-3562.
[5] Lan M, Liu B, and He Q.Evaluation of the association between hyperuricemia and coronary artery disease: A STROBE-compliant article[J].Medicine (Baltimore),2018, 97(44):e12926.
[6] Gaubert M, Marlinge M, Alessandrini M, et al. Uric acid levels are associated with endothelial dysfunction and severity of coronary atherosclerosis during a first episode of acute coronary syndrome[J].Purinergic Signal,2018, 14(2):191-199.
[7] Wheeler J G, Juzwishin K D, Eiriksdottir G, et al. Serum uric acid and coronary heart disease in 9,458 incident cases and 155,084 controls: prospective study and meta-analysis[J].PLoS Med,2005,2(3):e76.
[8] Kim S Y, Guevara J P, Kim K M, et al. Hyperuricemia and coronary heart disease: a systematic review and meta-analysis[J].Arthritis Care Res (Hoboken),2010, 62(2):170-180.
[9] GROUP. KDIGOKCW. KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease[J]. Kidney Int Suppl, 2013, 3(1):1-150.
[10] 施映枫,王莉,徐柳青,等. 高尿酸血症肾脏损害的研究进展[J].中华肾脏病杂志,2014,30(10):794-798.
[11] 陈涛,李卫,王杨,等. 高尿酸血症的患病情况及相关因素分析[J].中华临床医师杂志,2012,6(13):49-52.
[12] 刘姝,徐开平,秦恳,等. 成都地区高尿酸血症的患病情况及相关因素分析[J].西部医学,2012,24(3):474-476.
[13] 李瑜鹏,康乐,石翯. 健康体检人群高尿酸血症患病情况及其相关因素分析[J].齐齐哈尔医学院学报,2017, 38(16):74-76.
[14] 姜昌丽,李雪梅,李云,等. 昆明市3885名体检人员血尿酸水平与性别、年龄相关性分析[J].国际检验医学杂志,2017,38(5):671-673.
[15] 卢彦敏,王霞,付正菊,等. 雌激素与人尿酸盐转运子(hUAT)基因表达的相关性研究[J].重庆医学, 2010,39(20):2739-2740.
[16] Choi H K, Ford E S, Li C Y, et al. Prevalence of the metabolic syndrome in patients with gout: The third national health and nutrition examination survey[J]. Arthritis & Rheumatism,2007,57(1):109-115.
[17] Enomoto A, Kimura H, Chairoungdua A, et al. Molecular identification of a renal urate anion exchanger that regulates blood urate levels[J].Nature,2002, 417(6887): 447-452.
[18] Choi H K, Mount D B, and Reginato A M. Pathogenesis of gout[J]. Ann Intern Med,2005,143(7):499-516.
[19] Gustafsson D and Unwin R. The pathophysiology of hyperuricaemia and its possible relationship to cardiovascular disease, morbidity and mortality[J].BMC Nephrol,2013,14:164.
[20] Na L, Wang L, Yang T, et al. EGF receptor inhibition alleviates hyperuricemia nephropathy[J].J Am Soc Nephrol,2015,26(11):2716-2729.
[21] Xu L, Shi Y, Zhuang S, et al. Recent advances on uric acid transporters[J].Oncotarget,2017,8(59):100852-100862.
[22] 郭建生,刘晓峰,郭一民. 湿热型痛风性关节炎的分期治疗[J]. 井冈山大学学报:自然科学版, 2018,39(1): 87-89.
PREVALENCE AND RISK FACTORS OF HYPERURICEMIA IN JI’AN OF JIANGXI PROVINCE
*FANG Lu1, PAN Xing1, SUN Jun-ming1, XU Liu-qing2, TAO Min2, JIANG Xiao-lu2, LIU Na2, NIE Zheng-yu1, ZHUANG Shou-gang2
(1. Jian Hospital of Shanghai East Hospital, Ji’an, Jiangxi 343000, China; 2. Shanghai East Hospital, Shanghai 200001, China)
:To survey the prevalence of hyperuricemia of residents in Ji’an City, Jiangxi Province and investigate the risk factors of hyperuricemia.: We collected 1000 samples from adult residents, who were
physical examination from 1 January to 30 July 2018 in Ji’an Hospital. Counting the prevalence in different ages and different genders, logistic regression model was used to find out the risk factors associated with hyperuricemia.: The prevalence of hyperuricemia was 23.3% (95%20.68% - 25.92%). And the prevalence of hyperuricemia in male (28.08%, 95%24.44% - 31.73%) was higher than that in female (16.59%, 95%13.01% - 20.16%) (< 0.001). After multivariate logistic regression analysis (multiple adjusted models), increased systolic pressure (=1.014, 95%= 1.005 - 1.023,= 0.002), triglyceride (= 1.263, 95%= 1.106 - 1.443,= 0.001), low density lipoprotein cholesterol (= 1.376, 95%= 1.026 - 1.845,= 0.033), decreased glomerular filtration rate (= 0.985, 95%= 0.977 - 0.993,< 0.001) and high density lipoprotein cholesterol (= 0.612, 95%= 0.402 - 0.931,= 0.022) were independent risk factors for hyperuricemia.: Increased systolic pressure,triglyceride, low density lipoprotein cholesterol and decreased glomerular filtration rate and high density lipoprotein cholesterol were independent risk factors for hyperuricemia in the residents of Ji’an City. Controlling blood pressure, blood lipids, and protecting kidney function are important for the prevention and treatment of hyperuricemia.
hyperuricemia; prevalence rate; risk factors
R589.7
A
10.3969/j.issn.1674-8085.2019.05.020
1674-8085(2019)05-0101-06
2019-05-16;
2019-06-17
国家自然科学基金项目(81670690, 81470991, 81200492, 81270778, 81470920, 81670623, 81830021);江西省卫计委计划项目(20184077);浦东新区重点学科附带课题项目(PWZxk2017-05);科技部重大专项子课题项目(2018YFA0108802)
*方 路(1967-),女,上海人,副主任医师,硕士,主要从事肾脏病及血液净化研究(E-mail: fanglumail@sina.com);
潘 星(1992-),女,江西吉安人,住院医师,主要从事肾脏病及血液净化研究(E-mail: 1260993155@qq.com);
孙俊明(1990-),男,江西吉安人,住院医师,主要从事肾脏病及血液净化研究(E-mail: 1049682703@qq.com);
徐柳青(1990-),女,安徽芜湖人,住院医师,硕士,主要从事肾损伤机制及防治研究(E-mail: 465244682@qq.com);
陶 敏(1992-),女,安徽滁州人,硕士生,主要从事肾损伤发生机制及防治研究(E-mail: taominsunny@163.com);
蒋晓露(1992-),女,江苏徐州人,硕士生,主要从事肾损伤发生机制及防治研究(E-mail: 1947427387@qq.com);
刘 娜(1976-),女,黑龙江哈尔滨人,副教授,博士,博士生导师,主要从事急慢性肾损伤发生机制及防治研究(E-mail:naliubrown@163.com);
聂正玉(1986-),女,江西吉安人,主管护师,主要从事血液净化研究(E-mail: 1120294985@qq.com);
庄守纲(1960-),男,山东临沂人,教授,博士,博士生导师,主要从事急慢性肾损伤发生机制及防治研究(E-mail:gangzhuang@hotmail.com).
