蓝莓果汁贮藏中非酶褐变影响因素评价
2019-09-11马永强
王 鑫,魏 婧,2,马 蕊,马永强,*
(1.哈尔滨商业大学食品工程学院,省高校食品科学与工程重点实验室,黑龙江哈尔滨 150076;2.潍坊市皓远食品有限公司,山东潍坊 261000)
蓝莓(Blueberry)为杜鹃花科(Ericaceae)越橘属(Vacciniumspp.)常绿灌木,其果皮呈蓝色(或蓝黑色)故称蓝莓[1]。蓝莓果很小,但口感极佳,可直接食用,也可以加工成果汁饮料、果酱和果酒饮品等[2-3]。果汁褐变分为酶促褐变(Enzymatic browning)和非酶促褐变(Non-enzymatic browning),酶促褐变主要发生于果汁加工过程中,且反应机制已广泛研究,而非酶促褐变反应机制复杂,不仅在果汁加工和贮藏过程中常见,同时可促使果汁贮藏寿命减短。
多元酚氧化缩合反应、美拉德反应、焦糖化反应以及抗坏血酸氧化分解反应可引起果汁非酶褐变,并对不同果汁影响大小不同[4]。目前,很多学者对各类果汁贮藏过程中非酶褐变反应进行了研究,Roig等[5]通过桔汁储藏实验发现,由于抗坏血酸发生氧化降解导致储藏过程中美拉德反应对其发生非酶褐变作用不显著,同时氨基化合物可促进非酶褐变发生。Marti等[6]研究表明,向果汁中过多添加抗坏血酸会致使褐变程度加重。Paravisini等[7]发现苹果汁在35 ℃下储存时,非酶褐变主要与多元酚类化合物有关。Macdonald等[8]发现香蕉汁在杀菌过程中,颜色变化的主要原因是焦糖化反应。张添等[9]研究发现在芦荟制品加工和贮存过程中,多酚类物质的浓度是造成非酶褐变的主要原因。国内对蓝莓的研究起步较晚,目前主要集中于蓝莓的生物活性功能方面的研究,对蓝莓汁非酶促褐变反应方面尚未进行深入研究,对预防蓝莓汁非酶褐变的研究对于提高蓝莓汁品质具有重要意义。
本实验选用三氯乙酸(TCA)作为酶促褐变反应终止剂,对蓝莓汁分别在4、25 和37 ℃下进行贮藏,以总酚、褐变指数(BI)、5-羟甲基糠醛(5-Hydroxymethylfurfural,5-HMF)含量以及抗坏血酸含量为考查指标,对蓝莓汁贮藏过程中非酶因素进行评价,为抑制和降低褐变程度提供有力依据。
1 材料与方法
1.1 材料与仪器
蓝莓(-18 ℃下贮存) 大兴安岭百盛蓝莓科技开发有限公司;三氯乙酸(TCA) 天津永大化学实际有限公司;抗坏血酸 天津博迪化工股份有限公司;2,6-二氯靛酚、福林酚 国药集团化学试剂有限公司;亚硫酸氢钠、亚硫酸钠 湖北邦盛化工有限公司;邻苯二酚 郑州盛凯化工产品有限公司;乙酸锌 天津市巴斯夫化工有限公司;草酸 哈尔滨市新达化工厂;D001强酸大孔苯乙烯系阳离子交换树脂 上海维塔化学试剂有限公司。
BS 224S型分析天平 德国赛多利斯科学仪器有限公司;LG10-2.4A型高速离心机 北京京立离心机有限公司;R-205型旋转蒸发器 上海申胜生物技术有限公司;V-5000可见分光光度计 上海元析仪器有限公司;恒温摇床培养箱 上海智诚分析仪器制造有限公司;ZD-2型自动电位滴定仪 上海仪田精密仪器有限公司;UV1000单光束紫外-可见分光光度计 上海天美科学仪器有限公司;TU-1901双光束紫外分光光度计 北京普析通用仪器有限公司;PHS-3C型pH计 上海精密仪器有限公司。
1.2 实验方法
1.2.1 蓝莓果汁的制备 将蓝莓果室温下自然解冻,在榨汁机中破碎15 s,将得到的蓝莓汁在4000 r/min下离心15 min,过滤,取上清液分装于100 mL玻璃瓶中,即为蓝莓果汁样品。并存入4 ℃冰箱中备用。
1.2.2 非酶促褐变反应各体系的建立 按照表1进行体系的建立。

表1 不同体系的成分表Table 1 Composition table of different systems
1.2.2.1 体系1的建立 为研究抗坏血酸分解反应、美拉德反应、焦糖化反应及多元酚氧化缩合反应对蓝莓果汁非酶促褐变的影响建立体系1,且由于体系1只抑制了酶促反应可研究总酚含量的变化。参照田玉庭[10]的试验方法,取一定量的蓝莓果汁样品利用三氯乙酸来终止酶促反应,按1 mL多酚氧化酶粗酶液(两层纱布过滤,4 ℃,10000 r/min离心30 min)加等量TCA,其中TCA浓度逐步为0、2%、4%、6%、8%、10%、12%、14%八个浓度梯度直至令其反应终止,添加0.05 mol/L邻苯二酚2 mL,用分光光度计在410 nm下测定样品的OD值,每隔30 s读数,观察吸光值变化情况。算出所对应酶活(每分钟增加0.001吸光值即为1单位活力)并作图。
1.2.2.2 体系2的建立 根据1.2.2.1确定体系1中TCA浓度为12%后,用阳离子交换树脂处理体系1的蓝莓汁,去除氨基酸[11]。此体系的建立是为了研究焦糖化、抗坏血酸氧化分解及多元酚氧化缩合对非酶促褐变的影响。具体操作为:为去除氨基酸形式所存在的氮元素以去除氨基酸,进行D001大孔苯乙烯系强酸阳离子交换树脂对氨基态氮静态交换吸附实验,向蓝莓汁中添加不同含量的D001阳离子交换树脂(0、5%、10%、15%、20%),每30 min搅拌一次,在室温下放置15 h,原果汁作为未处理的空白组,每隔2小时测定20 h内原果汁和交换吸附后果汁的氨基态氮的浓度,筛选最佳阳离子交换树脂添加量。之后向蓝莓果汁中添加最适含量的D001阳离子交换树脂,步骤同上,求出表观交换吸附量,获得阳离子交换树脂交换吸附平衡时间。
式(1)
式中:Q-表观吸附量(mg/g);C0-起始浓度(mg/mL);Ct-某时间点的浓度(mg/mL);V-吸附溶液的体积(mL);W-树脂湿质量(g)。
1.2.2.3 体系3的建立 此体系的pH=2(抗坏血酸(VC)在pH=2时氧化反应缓慢而不明显)。体系3的建立是为了研究焦糖化反应和多酚氧化缩合反应对非酶促褐变的影响[12]。具体操作为:蓝莓样液加1 mL TCA经离心(4000 r/min 15 min)后,分别取10 g蓝莓汁于试管中按不同比例分别添加亚硫酸盐,以不添加亚硫酸盐为对照组,90 ℃水浴5 h,测定A420值并计算其非酶褐变抑制率。其中,添加亚硫酸钠和亚硫酸氢钠的浓度梯度均选用为50、100、150、200、250、300 μg/g。
即利用相减法可得,体系1-体系2间所发生的是美拉德反应,而体系2-体系3之间发生的是抗坏血酸氧化分解反应。
1.2.3 贮藏实验 各体系样液分别于4、25和37 ℃条件下贮藏50 d,每5 d测定褐变指数、5-HMF、VC、总酚等相关指标。
1.2.4 褐变指数的测定及抑制率计算 果汁的褐变度用420 nm波长处的吸光度(A420)表示。取适量待测果汁样品,于9000 r/min离心20 min,取上清液,测定A420值,以水为空白[13]。
式(2)
式中:T为抑制率,%;A0为420 nm处未加抑制剂的蓝莓汁的吸光度;Ai为420 nm处加入抑制剂的蓝莓汁的吸光度[14]。
1.2.5 VC含量测定 采用电位法测定[15-16]。
1.2.6 氨基态氮的测定 采用GB/T 5009.39-2003方法测定。
1.2.7 5-羟甲基糠醛含量测定 取蓝莓汁样品5 g,用25 mL蒸馏水稀释溶解后,移入50 mL容量瓶,加入0.5 mL澄清剂Ⅰ(15% 亚铁氰化钾)、摇匀;再加入0.5 mL澄清剂Ⅱ(30%乙酸锌),摇匀,用蒸馏水定容至刻度。于9000 r/min离心10 min,吸取上层清夜各5 mL于2个10 mL比色管中。在一个比色管中加入5 mL 0.20 g/100 mL NaHSO3溶液,混匀,为参比液;另一个比色管中5 mL蒸馏水,混匀,为待测液。用石英比色皿于284 nm和336 nm波长处测定待测样液的吸光度[17-18]。
式(3)
式中:X为蓝莓汁样品中5-HMF的含量,mg/100 g;m为样品质量,g;14.97为换算系数。
1.2.8 总酚含量的测定 福林-酚比色法测定[19],总酚标准曲线绘制:测定没食子酸浓度分别为0.1、0.2、0.3、0.4、0.5 mg/mL时吸光度,得到标准曲线方程为:y=1.9522x+0.0585,R2=0.981。
1.3 数据处理
采用DPS 9.50软件进行数据处理,数据用Mean±SD表示。图表采用Excel 2013和Origin 8.5完成。
2 结果与分析
2.1 各体系样品预处理条件筛选结果
2.1.1 体系1中三氯乙酸浓度的确定 由图1可知,随TCA添加浓度的上升,酶活性逐渐下降,当TCA添加浓度为14%时,酶活力为-0.0018 U/g,酶的活力只能为0或正值,负值并无意义。同时也可看出,各浓度下的三氯乙酸对酶促反应都起到了一定的抑制作用。经比较,最终选用添加TCA浓度为12%(处理后即为体系1样品)。
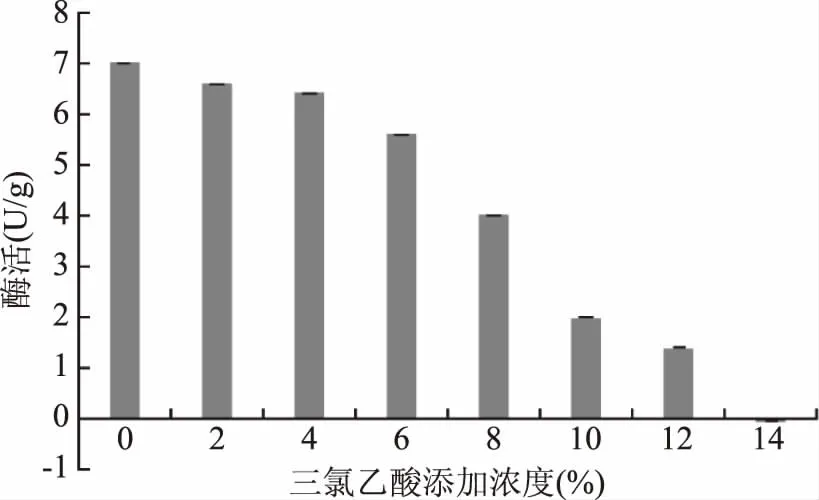
图1 三氯乙酸浓度对酶活力的影响Fig.1 Effects of trichloroacetic acid concentration on enzyme activity
2.1.2 体系2中D001阳离子交换树脂的筛选 由表2可得,不同含量的阳离子交换树脂对蓝莓果汁中氨基态氮含量的影响不同,体系2蓝莓汁样品中添加D001阳离子交换树脂含量为10%、15%时对氨基态氮含量的影响差异不明显,随着树脂添加量增加表观吸附量趋于平衡,且无明显差异。因此选择填加D001阳离子交换树脂含量为10%时吸附作用最适。

表2 不同含量树脂对果汁中氨基态氮的影响Table 2 Effects of different fruit juice contents on resin amino nitrogen
向蓝莓果汁中加入10%含量D001阳离子交换树脂,随着吸附时间的增加,氨基态氮含量逐渐降低,且吸附量逐渐增大,当超过16 h后,氨基态氮的表观交换吸附量趋于无显著差异的稳定状态(见表3),说明吸附作用达到平衡,因此D001阳离子交换树脂交换吸附平衡时间为16 h。
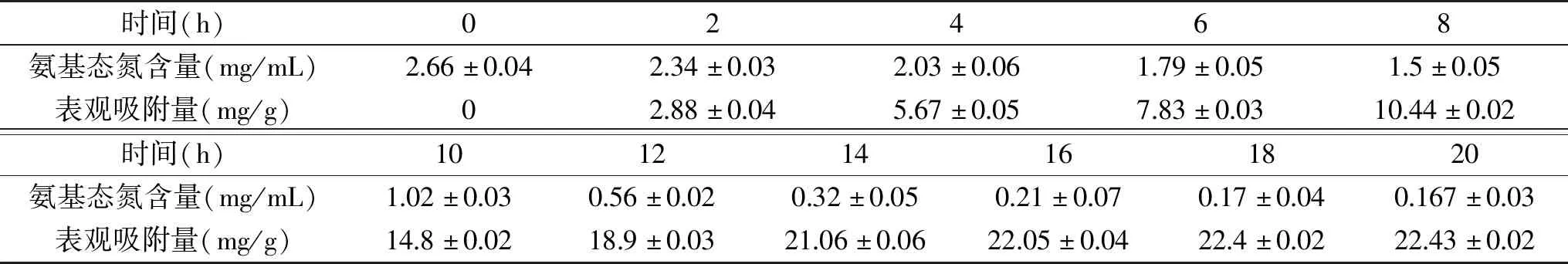
表3 10% D001阳离子交换树脂对氨基态氮的影响Table 3 Effects of 10% D001 cation exchange resin on of amino nitrogen
2.1.3 体系3中亚硫酸盐的筛选 如图2所示,无论是亚硫酸钠还是亚硫酸氢钠对蓝莓果汁褐变均有一定的抑制作用,随着浓度的提高,抑制率也相应增大,当浓度≥200 μg/g时,则趋于平衡状态,相对而言,亚硫酸氢钠的抑制效果更为明显,所以本试验选取浓度为200 μg/g的NaHSO3添加到蓝莓汁中,即构成体系3样品。
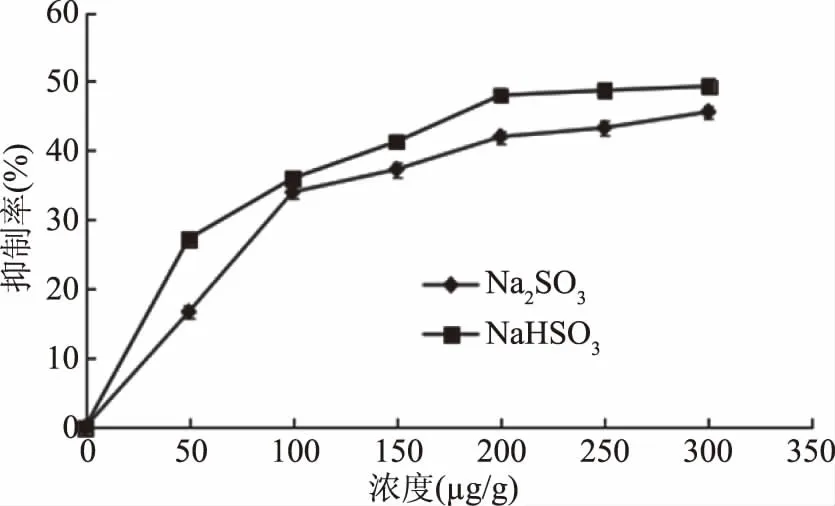
图2 亚硫酸盐对蓝莓果汁褐变的抑制Fig.2 Sulfite inhibition of blueberry juice browning
2.2 非酶褐变反应对蓝莓汁在贮藏过程中主要因素的影响
2.2.1 褐变指数的变化 在贮藏过程中,各体系蓝莓汁A420值均有上升趋势,但增加程度不同,如图3所示,贮藏50 d时,当温度为37 ℃时,体系1的A420值分别是体系2和体系3 A420值的1.03倍和1.76倍;当温度为25 ℃时,体系1的A420值分别是体系2和体系3 A420值的1.1倍和1.86倍;当温度为4 ℃时,体系1的A420值分别是体系2和体系3 A420值的1.37倍和1.71倍,褐变指数均呈现出体系1>体系2>体系3的规律,体系1-体系2间所发生的是美拉德反应,而体系2-体系3之间发生的是抗坏血酸氧化分解反应,且从图中体系1、2、3曲线相差幅度可看出抗坏血酸氧化分解反应褐变程度比美拉德反应严重。

图3 褐变指数的变化Fig.3 Changes browning index注:a为4 ℃贮藏下各体系A420的变化;b为25 ℃贮藏下各体系A420的变化;c为37 ℃贮藏下各体系A420的变化。
2.2.2 VC含量的变化 由于抗坏血酸极易氧化分解,并可与氨基酸发生反应生成红色素和黄色素,因此选取蓝莓汁+TCA的体系1可体现抗坏血酸含量的变化,图4中可以看出抗坏血酸随贮藏时间的延长有一定的降解,不同贮藏温度下,其降解程度不同,前5 d内急剧下降,随后贮藏期间VC降解的速率相对缓慢,这一现象与Rolga等[20]研究的柑橘汁和万鹏[21]研究的荔枝果汁中抗坏血酸的变化规律十分相似。
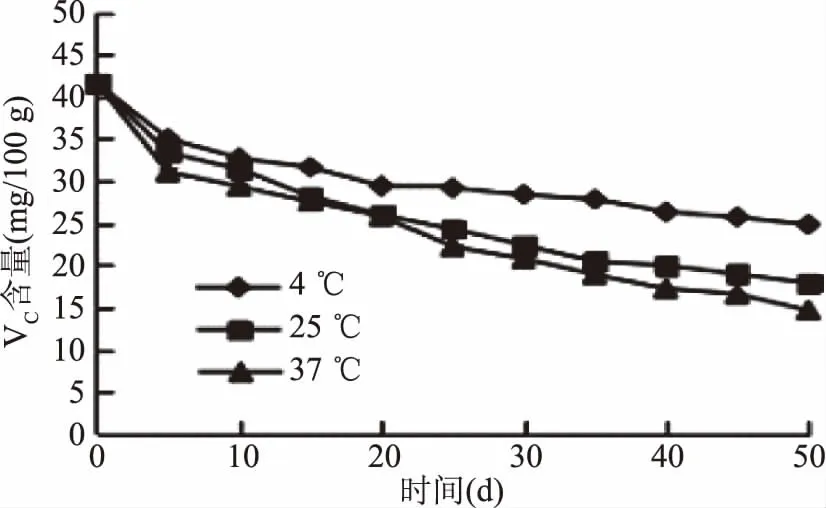
图4 贮藏过程中蓝莓汁抗坏血酸的变化(体系1)Fig.4 Changes during storage blueberry juice ascorbic acid(System 1)
2.2.3 总酚含量的变化 果汁中的多元酚不仅仅可以与蛋白质作用形成聚合物使其含量减少,导致果汁混浊,还可以自身进行氧化缩合、与果汁体系中其他物质发生共色作用,最终导致果汁非酶褐变,影响果汁品质[22-23]。如图5可知,没食子酸的浓度与吸光度呈现良好的线性关系,R2=0.981。将体系1蓝莓果汁样品分别置于4、25和37 ℃下贮藏,总酚含量随时间增加而逐渐下降(图6)。贮藏50 d后,各温度下总酚含量分别损失了2.1%、7.2%和9.4%,变化不是很明显,该结果表明,总酚含量的变化是引起蓝莓汁非酶褐变的原因之一,但不是主要原因。
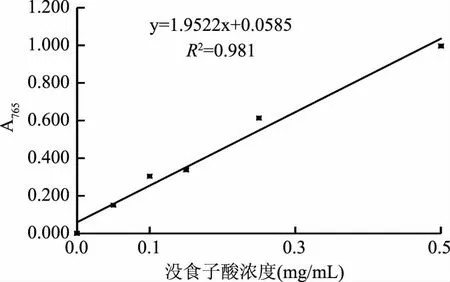
图5 总酚的标准曲线Fig.5 Standard curve of total phenols
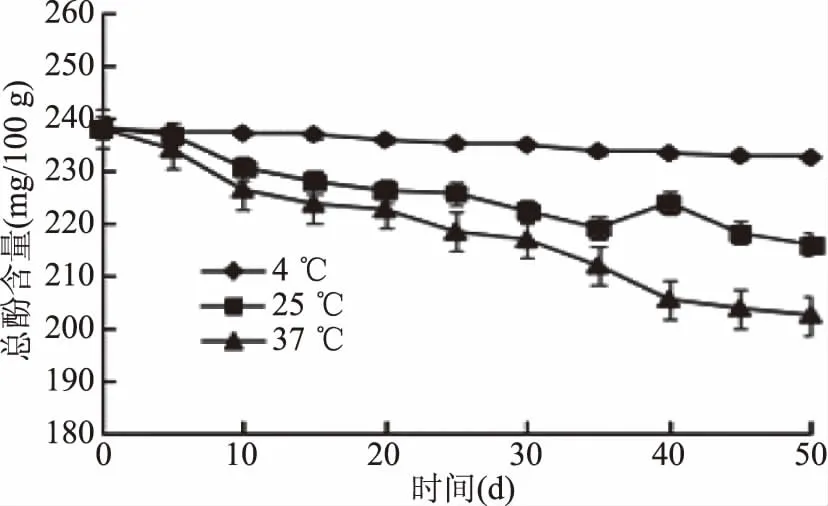
图6 贮藏过程中蓝莓汁总酚含量变化(体系1)Fig.6 Changes during storage blueberry juice total phenol content(System 1)
2.2.4 5-HMF含量的变化 体系1为研究抗坏血酸分解反应、美拉德反应、焦糖化反应及多元酚氧化缩合反应对蓝莓果汁非酶促褐变的影响,且5-HMF是衡量果汁褐变的重要指标之一,是美拉德反应、焦糖化反应以及抗坏血酸氧化分解反应的共同中间产物[24-25],因此选取体系1为研究对象,如图7所示,蓝莓汁贮藏50 d时,37 ℃下5-HMF总含量分别为25、4 ℃贮藏下的1.2倍和1.8倍,总体而言,贮藏温度不断提高,5-HMF含量也随之增加。因此可以5-HMF为重要测定指标来评价这三种反应分别对蓝莓汁在贮藏过程中的作用大小。
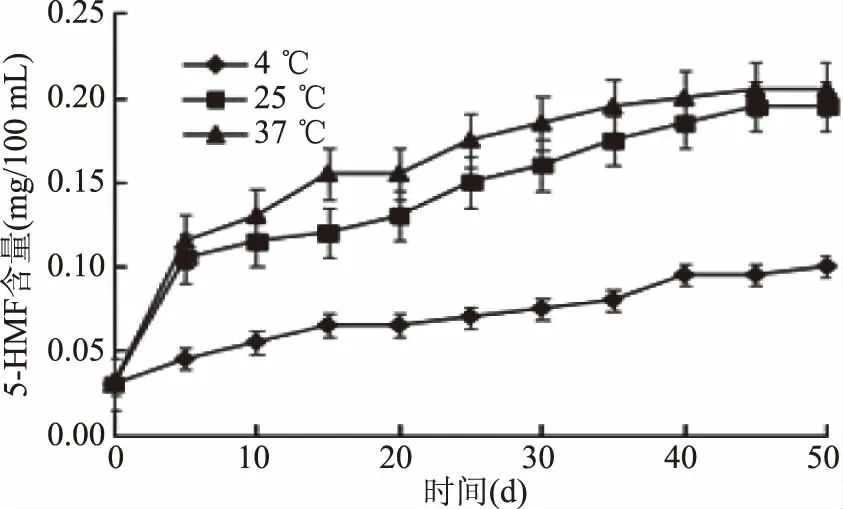
图7 贮藏过程中蓝莓汁非酶褐变5-HMF总量(体系1)Fig.7 Storage blueberry juice non-enzymatic browning 5-HMF total process(System 1)
2.2.5 焦糖化反应对蓝莓汁非酶褐变的影响 果汁中甜味的主要来源是糖,糖类除了与氨基化合物发生美拉德反应外,在加工或贮藏过程中高温、酸性及高糖浓度条件下,极易发生焦糖化反应。体系3在体系1的基础上经过添加200 μg/g NaHSO3来抑制美拉德反应的产生,以确定焦糖化反应对非酶褐变的影响,同时调节pH=2,使VC在整个贮藏期稳定不易分解(图8)。如图9所示,蓝莓汁贮藏前5 d时,4,25和37 ℃这三种贮藏条件下5-HMF均有所上升,其原因是贮藏时将蓝莓汁样品装入玻璃瓶中封盖时空隙中残留空气中的氧气与果汁中抗坏血酸有氧分解而导致的,耗完氧后,褐变指数不显著,无变化,这一结果表明,焦糖化反应几乎对其非酶促褐变无影响,相对于其他反应而言,可忽略不计。
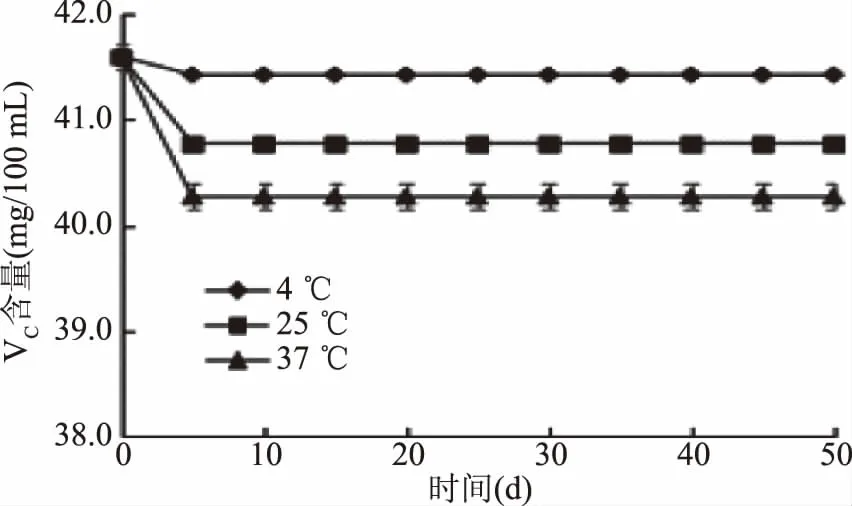
图8 贮藏过程中蓝莓汁抗坏血酸(VC)的变化(体系3)Fig.8 Ascorbic acid(VC)of blueberry juice changes during storage(System 3)
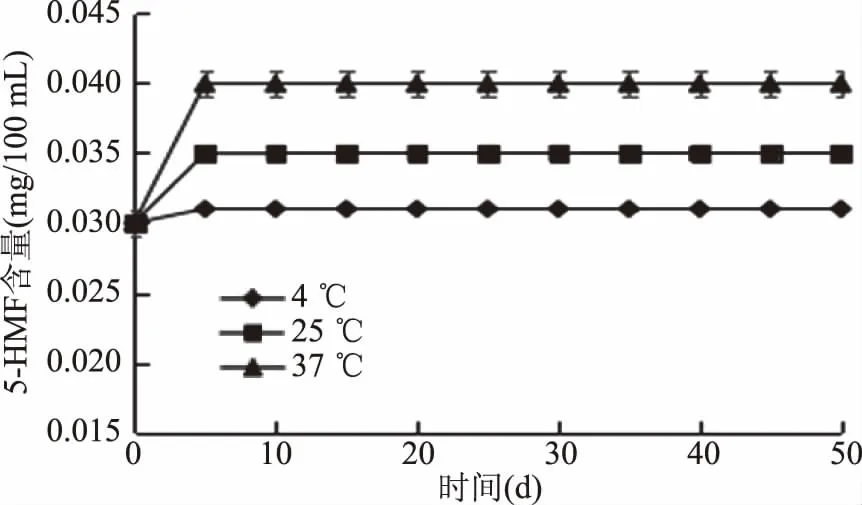
图9 贮藏过程中蓝莓汁5-HMF的变化(体系3)Fig.9 5-HMF changes of blueberry juice during storage(System 3)
2.2.6 抗坏血酸氧化分解对蓝莓汁非酶褐变的影响 利用相减法体系2-体系3即体现抗坏血酸氧化分解反应是蓝莓汁非酶促褐变的影响,由2.2.5结论可知,焦糖化反应对蓝莓汁非酶褐变的影响可忽略不计,即体系2所得数据结果主要是由抗坏血酸氧化分解反应所导致。如图10所示,所测得的5-HMF含量为抗坏血酸氧化分解与焦糖化反应所产生5-HMF之和,根据2.2.5分析结果表明,可视体系2所测5-HMF为抗坏血酸氧化分解而得。低温情况下,5-HMF生成量甚少,即VC分解缓慢,无明显特征。随贮藏温度上升,5-HMF生成量逐渐增加,25 ℃和37 ℃下贮藏前5 d,5-HMF生成速率极快,随后5~45 d,逐渐增长,当贮藏50 d时,4、25和37 ℃条件下产生的5-HMF含量分别为0.075、0.165、0.19 mg/100 mg。由此可得,抗坏血酸氧化分解对非酶褐变反应有一定程度的影响。

图10 贮藏过程中蓝莓汁5-HMF的变化(体系2)Fig.10 5-HMF changes of blueberry juice druing storage(System 2)
2.2.7 美拉德反应对蓝莓汁非酶褐变的影响 以5-HMF这一理化指标为基准,利用相减法(体系1-体系2)所得到的5-HMF含量,即由美拉德反应所生成。从图11可以观察到各个温度下,体系2产生的5-HMF含量远远大于体系1-2的值,经数据分析可得,各贮藏温度下抗坏血酸氧化分解反应产生5-HMF的含量分别是美拉德反应产生5-HMF含量的3、5.5、5.4倍。结果表明,美拉德反应在蓝莓汁贮藏过程中的作用仅占一小部分,相对而言,影响蓝莓汁非酶褐变程度大小为:抗坏血酸氧化分解反应>美拉德反应>焦糖化反应。
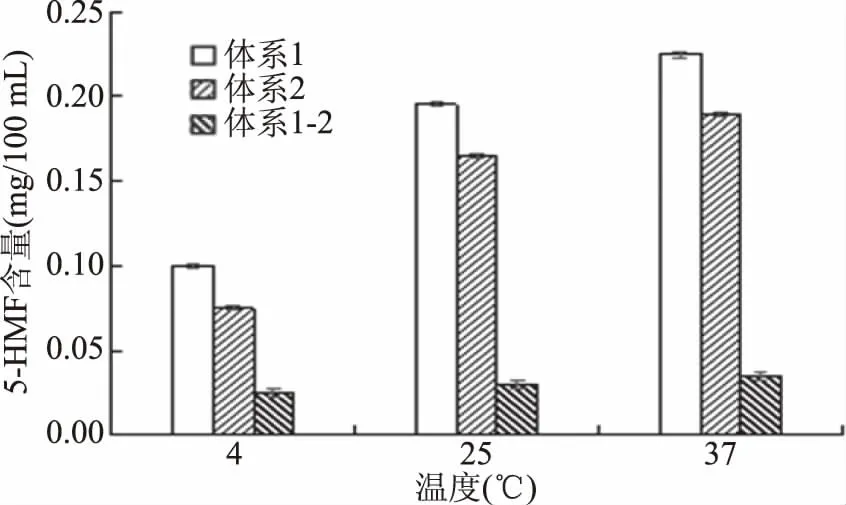
图11 模拟体系在贮藏50d后产生的5-HMF含量比较Fig.11 Compare of 5-HMF contents in simulation system after 50 d storage
3 结论
实验构建三个不同蓝莓汁体系,分别置于4、25和37 ℃条件下贮藏50 d,随时间和温度的变化,蓝莓汁呈现出不同程度非酶褐变,其中总酚含量在整个贮藏过程中变化不大,因此总酚对于蓝莓汁非酶褐变的影响较小。利用相减法分析得出各反应分别产生5-HMF大小排列为抗坏血酸氧化分解反应>美拉德反应>焦糖化反应,可见抗坏血酸对其影响最大,从而揭示蓝莓汁在贮藏过程中非酶褐变机制对褐变指数、总酚、抗坏血酸和5-羟甲基糠醛各指标影响大小,对后续的非酶褐变机理深入研究有着重要的意义。
