甘草多糖的提取及其抗氧化活性研究
2019-09-10乌兰其其格宋学军段雪琴
乌兰其其格 宋学军 段雪琴
摘要:本文利用水提醇沉法从甘草中提取甘草粗多糖,用沉淀法对提取的甘草粗多糖进行分离纯化后,得到三种多糖,即水提一级、二级、三级多糖,并对粗多糖和三种分级多糖进行了光谱性能分析.紫外光谱结果显示,四种多糖在260-280nm处均有吸收,表明含有蛋白质或核酸;红外光谱结果表明,四种多糖都具有多糖的特征吸收峰.另外,根据芬顿反的原理研究了所制备的甘草多糖清除羟自由基的能力,并研究了甘草多糖对酱油中羟基自由基清除能力的影响,结果表明,加入甘草多糖的酱油试样对羟基的清除能力有明显的增强.
关键词:甘草多糖;提取;分级;抗氧化性
中图分类号:S567.2;O657 文献标识码:A 文章编号:1673-260X(2019)06-0036-03
1 前言
甘草别名还有乌拉尔甘草,国老,甜根,甜草,属豆科,是著名的传统药用植物[1],主要生长在内蒙古,新疆,宁夏等地.随着科学的发展,在1860-1869年学者们开始对甘草进行化学方面有关的研究[2],研究表明,甘草中含有许多药用成分.多糖是生物体的重要组成部分,可以从植物,微生物和动物等生物中提取.在体内,有许多重要的生物功能,如防御功能、结构支持和储能,同时,多糖在细胞和细胞之间,细胞与外界之间的能量和物质转化中起重要作用.作为甘草的重要活性成分之一,许多研究表明甘草多糖具有抗肿瘤,抗炎,抗病毒[3-5],免疫调节,抗氧化和抗菌等生理活性[6,7],常用的提取法主要有超声辅助提取法、溶剂浸提法等[8-12].
本研究利用水提醇沉法从甘草中提取甘草粗多糖,进行分离纯化并对提取的粗多糖和三种分级多糖进行了光谱性能分析,根据芬顿反应原理研究了所制备的甘草多糖清除羟自由基的能力,并研究了加入甘草多糖对酱油试样的羟基的清除能力的影响.
2 实验部分
2.1 仪器和材料
红外光谱仪(Nicilet iS5),紫外光谱仪(普析),SHD-(III)循环真空泵(河南予华),可见光度计(菁华科技);双氧水(30%,沈阳华东试剂),抗坏血酸(红岩试剂,硫酸亚铁铵(双船化学试剂),甲醇(国药),无水乙醇(国药),磷酸氢二钠(国药),二甲亚砜(沈阳华东试剂),正丁醇(恒兴化学试剂),三氯化铁(泉瑞试剂),其他试剂(KH2PO4,乙二胺四乙酸二钠,三氯甲烷,茚三酮等)均购于国药集团.
2.2 试剂配制
(1)0.2mol/L的PBS溶液(pH=7.4):准确称量35.8010gNa2HPO4·12H2O,溶于500ml蒸馏水中,标为液①;准确称量3.1120gKH2PO4·2H2O,溶于100ml蒸馏水,标记为液②;适量混合①号溶液和②号溶液配制所需缓冲溶液.
(2)2.0mmol/L的EDTA-Fe(II)溶液:EDTANa2溶液(4.0mmol/L):EDTANa2 0.3721g溶于250ml超纯水,记为溶液①,精确称量硫酸亚铁铵0.3923g溶于250ml蒸馏水记为溶液②,将①、②两种溶液按1:1的体积比进行混合,得到2.0mmol/L的EDTANa2-Fe(II)溶液.
(3)0.52mg/mL的番红花红T溶液、6%的H2O2溶液、0.2%的水合茚三酮溶液的配制
准确称量藏红花红T0.0525g溶于超纯水中,转移至100ml容量瓶中,定容,备用.量取10ml30%的H2O2,并转移至50ml的容量瓶中后定容.在100ml容量瓶中准确称取0.2010g茚三酮,将其溶解在乙醇中,稀释至刻度并备用.
(4)配制5%的FeCl3溶液:在10ml容量瓶中准确称取0.5000gFeCl3,将其溶解在超纯水中,并稀释至刻度.
2.3 多糖的提取与分级
用粉碎机将天然甘草破碎过,分别脱脂、脱色,按一定比例加入溶剂搅拌均匀,静置后置于80℃的水浴锅中恒温6h,冷却至室温后离心分离,然后将残余物保持在烧杯中,重复上述步骤三次.将滤出四次的滤液合并,置于烧杯中,在60℃的水浴中浓缩至没有水层后冷却至室温.按体一定体积比加入乙醇密封静置36小时后过滤.将沉淀物用少量甲醇洗涤三次,并将沉淀物置于干燥的容器中真空干燥后的产品即为甘草粗多糖.称取一定量的粗糖,加入蒸馏水,加热至60℃使多糖充分溶解后冷却至室温后过滤,然后加入无水乙醇,当醇的浓度达到20%时会产生大量的棕色沉淀,静置、抽滤,干燥后所得物质即为“水提1级多糖”.再将乙醇继续加入上述保留的滤液中,在溶液中得到浓度为40%的无水乙醇,得到沉淀物“水提2级多糖”,如上所述继续向母液中加入乙醇,使醇的浓度至60%,得到“水提3级多糖”,其他分级操作与1级糖的相同.
2.4 甘草多糖清除各样品羟自由基
分别在六个试管中,吸取三毫升上述配制的PBS缓冲液,再加1.5ml浓度为2.0mmol/L的EDTA二钠铁,0.45ml的浓度为0.51mg/mL的番红花红T溶液,然后加入2.0毫升不同浓度的多糖,加入0.9ml的6%H2O2溶液后稀释至10毫升.将混合溶液置于40℃的恒温水浴中半小时,在520nm的波长处测定样品吸光度.由测得的各空白和样品的吸光度值计算清除率E(%),计算公式如下:
E(%)=(A樣品-A空白)/(A对照-A空白)*100%
3 结果和讨论
3.1 甘草多糖的显色特性
本研究对提取的甘草多糖进行了三氯化铁和茚三酮实验,结果表明每种甘草多糖和三氯化铁(FeCl3)溶液样品反应溶液均变黄,表明不存在烯醇、酚羟基.在茚三酮显色实验中,发现部分多糖溶液变成紫色,表明含有氨,此结果与UV的结论一致.
3.2 紫外光谱研究
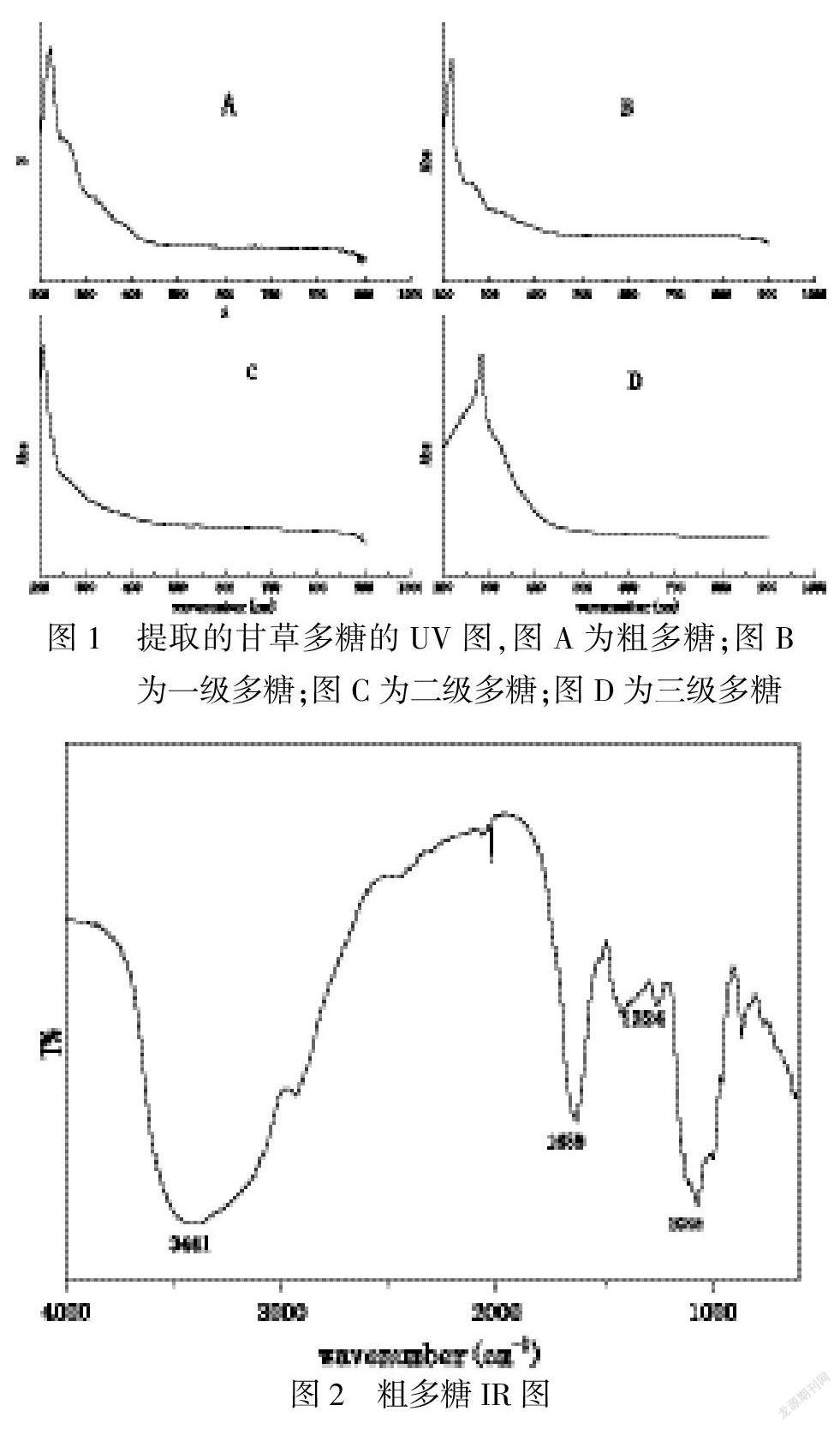
对所提取各多糖试样进行了紫外吸收测试,实验在200-900nm波长范围内进行.从紫外光谱测试结果可以看出,粗多糖,水提取物一级,二级和三级多糖均有吸收峰,表明粗多糖和每种分级的多糖含有蛋白质或核酸.
3.3 红外光谱
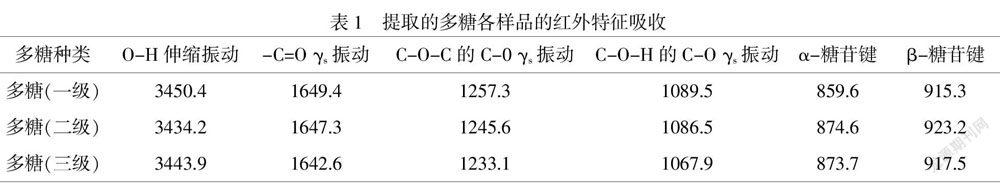
设定红外光谱仪的试验条件,用溴化钾压片法制备粗多糖和各分级水提多糖红外试样,在4000-600cm-1之间依次扫描压制样品,获得相应多糖样品的红外光谱,红外特征峰的数据示于表1.
以图2粗多糖为例,从红外光谱可以看出,在3450.4cm-1處有一个强而宽的吸收峰.这是多糖中的O-H伸缩振动吸收峰;在1635.4cm-1处是C=O的伸缩振动吸收峰;1257.3cm-1处的吸收峰是由糖环中醚环C-O-C的C-O伸缩振动引起的吸收峰;在1089.5cm-1处的强吸收峰是由糖环C-O-H的C-O伸缩振动引起的吸收峰;915.3在cm-1处是β-糖苷键的特殊吸收峰;α-糖苷键在859.6cm-1处具有特定的吸收峰,表明在水提粗多糖中存在β-糖苷键和α-糖苷键.
3.4 甘草多糖对羟自由基清除能力的活性研究
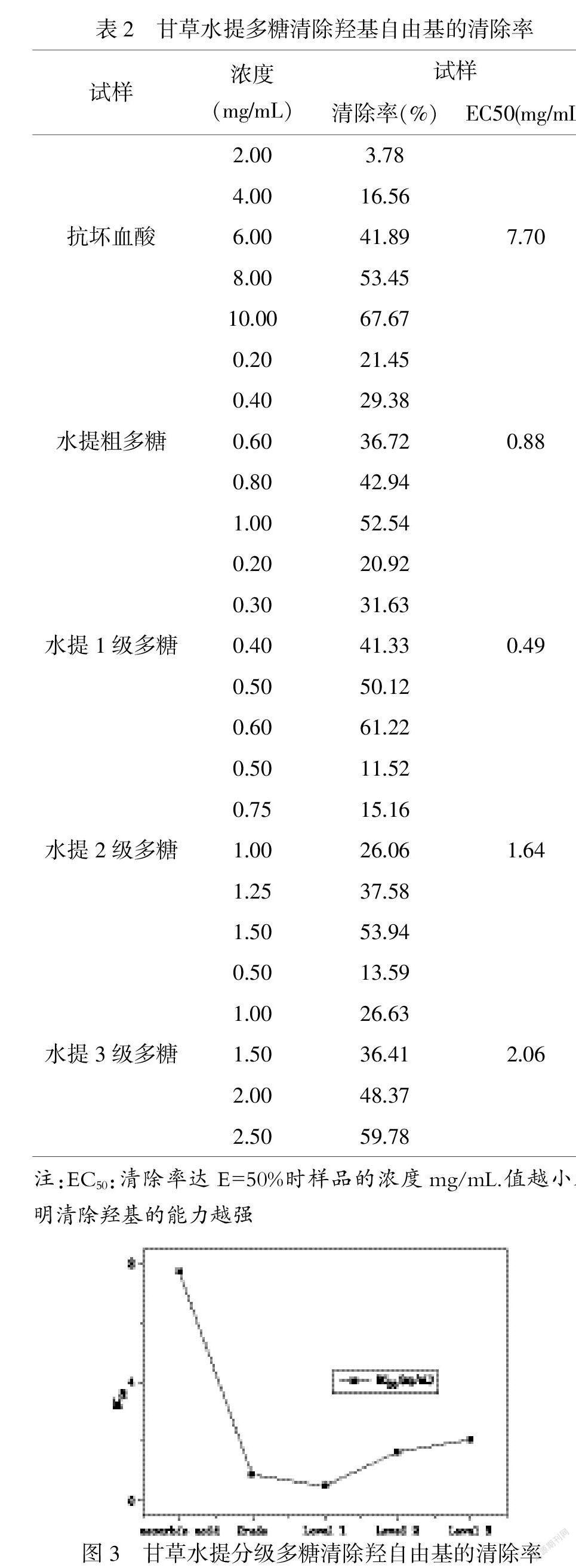
我们探讨了甘草多糖对羟自由基的清除能力,原理为在Fe2+存在时,与H2O2可生成·OH的同时还生成Fe3+,反应方式如下:H2O2+Fe2+→·OH+OH-+Fe3+,而·OH又可使翻红花红T褪色,基于以上原理可通过分光光度计法来检测甘草多糖对羟自由基清除能力.本研究提取的四种甘草多糖各试样的清除羟自由基能力见表2,对应EC50值的大小见图3.
由以上实验结果可知,EC50由小到大排列依次为1级多糖>粗多糖>2级多糖(EC50)>3级多糖(EC50)>抗坏血酸(EC50),由上述结果可知提取的多糖的羟自由基清除能力强于对照品(抗坏血酸).同时,也表明随着甘草水提分级的增加,羟自由基的清除能力降低.
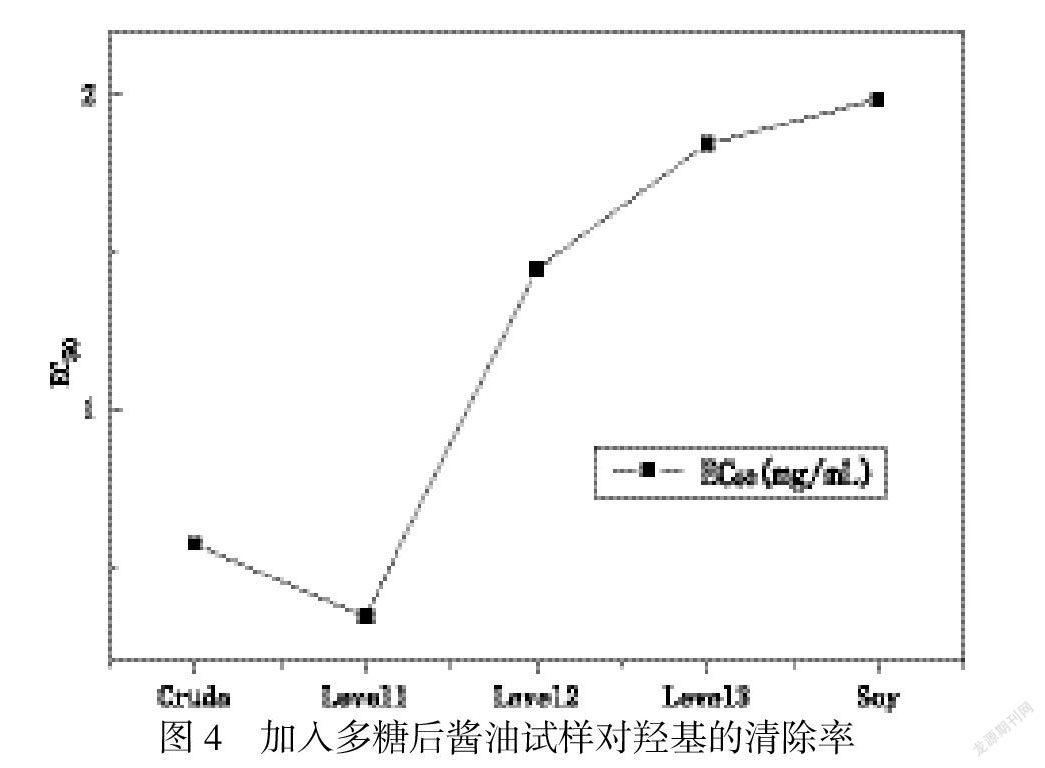
本研究也探讨了加入甘草多糖对酱油试样的羟基自由基清除能力的影响,结果表明,加入甘草多糖后酱油试样对羟基的清除能力明显的增强.
4 结论
本文是以甘草为原料,采用水提醇沉法提取了甘草多糖后对甘草多糖进行分级,分别得到水提一级、二级,三级糖.用紫外、红外等方法对提取的多糖进行了表征,根据芬顿反的原理研究了所制备的甘草多糖清除羟自由基的能力,并在酱油试样中添加提取的多糖后,研究了其羟基自由基清除能力,结果表明,加入甘草多糖的酱油试样对羟基的清除能力有明显的增强.
参考文献:
〔1〕陈橙,帕丽达.阿不力孜,米仁沙.亚库甫,胀果甘草酸性多糖的分离纯化、结构分析及免疫活性测定[J].2017,21(10):1110-1112.
〔2〕贺敏,吕慧英,梁逸曾.甘草化学成分分析(英文)[J].湘潭化工学院化学工程与制药系,2014,27(4):290-295.
〔3〕Ikegami N.Prophylactic effect of long-term oral administration of glycyrrhizin on AIDS development of a symptomatic patients.PO-825-0596 IX International Conference on AIDS,Berlin,1993.
〔4〕Chen M,Christensen S.B,Theander T.G,Kharazami A.Antileishmanial Activity of Licochalcone A in mice infected with Leishmania major and in hamsters infected with Leishmania donovani. Antimicrobial Agents and Chemotheraphy,1994,38:1339-1344.
〔5〕张泽生,史珅,杨超慧,等.甘草多糖免疫调节作用的研究[J],现代生物医学进展,2008,8(10):1855-1837.
〔6〕王忱.甘草多糖抑瘤的体内实验及其分子机制的研究[D].天津医科大学,2002.1213-1215.
〔7〕魏炜.甘草药用成分的萃取、分离、纯化方法研究[D].大连:大连理工大学,2005.
〔8〕刘树兴,唐孟忠.“米邦塔”食用仙人掌多糖分级新方法的研究[J].食品工业科技,2006(4):108-109.
〔9〕郭立山.郁金中水溶性多糖的梯度分离和含量测定[J].中医药学报,1996(4):48-49.
〔10〕蔡亚平,韩学忠.五味子多糖分级注射剂的含量和性质测定研究[J].中草药,2010,32(7):228-230.
〔11〕刘湘,汪秋安.天然产物化学[M].北京:化学工业出版社,2010.
