1,2,4-苯三甲酸与 2,2-联吡啶构筑的银(Ⅰ)和镉(Ⅱ)配合物的合成、晶体结构、热稳定性及荧光性质
2019-09-09杨洪利张秀清
杨洪利 陈 芳 张 丹 贺 雄 张秀清
(桂林理工大学化学与生物工程学院,广西电磁化学功能重点实验室,桂林 541004)
过渡金属配合物可以在光、电、磁、气体吸附与储存以及生物医药等方面发挥重大的作用[1-10],因此它一直受到众多科学研究者的关注。羧基是构筑过渡金属配合物的重要官能团之一,其可以通过单齿、螯合和桥联等多种配位方式来构筑多种结构,因此羧酸配体是重要的过渡金属配合物构筑单元,也受到了研究者们的高度重视。此外,有机羧酸配体的构象灵活性对最终结构的维数和拓扑结构的确定也起着决定性的作用。
具有多种配位模式的有机多羧酸配体是构建配合物的优良选择,因为它们可以用于设计与合成从零维到多维等多种空间结构类型的晶体,其结构的复杂性与多样性受到了广泛关注[11-12]。之前我们曾报道了使用 1,2,4-苯三甲酸(H3btc)作为主配体,通过pH调控的水热合成法合成出了一种一维链状结构Mn(Ⅱ)配合物,并探讨了它的荧光与磁性性质[13]。作为工作的延续,我们又陆续合成出了2种新颖的基于 H3btc的配合物[Ag(H2btc)(bpy)](1)和[Cd(Hbtc)(bpy)(H2O)2]n(2)(bpy=2,2′-联吡啶),并用 X 射线单晶衍射仪测定了晶体结构,对其进行了红外光谱、热重分析以及荧光性质的研究。
1 实验部分
1.1 试剂与仪器
试剂包括H3btc(AR,郑州阿尔法化工有限公司),bpy、八水合硫酸镉(AR,成都市科龙化工试剂厂),硝酸银(AR,广州市金珠江化学有限公司立新化工厂),三乙胺(AR,西陇化工股份有限公司)。
所用仪器有Agilent G8910A CCD单晶衍射仪,美国安捷伦公司;Spectrum One FT-IR Spectrometer傅里叶变换红外光谱仪,KBr压片,美国PerkinElmer公司;TGA Q600热重分析仪,日本TA公司;F-4600荧光光谱仪,日本Hitachi公司。
1.2 配合物的合成
1.2.1 配合物[Ag(H2btc)(bpy)](1)的合成
称取 H3btc(0.2 mmol,0.042 0 g)、bpy(0.2 mmol,0.031 2 g)、 硝 酸 银(0.2 mmol,0.033 9 g)加 入 到 25 mL的带有聚四氟乙烯衬底的水热反应釜中,并加入15 mL蒸馏水,以及滴加2滴三乙胺,将反应釜放入393 K烘箱中反应72 h。自然降温,冷却后开釜,得到白色粒状晶体。产率为38%(以金属原子Ag为基准)。 元素分析按 C19H13AgN2O6计算值(%):C 48.18,N 5.92,H 2.75;实验值(%):C 48.27,N 5.86,H 2.71。IR(KBr,cm-1):3 441(b),1 707(s),1 660(w),1 585(m),1 547(m),1 468(s),1 370(s),1 234(m),1 180(m),905(w)。
1.2.2 配合物[Cd(Hbtc)(bpy)(H2O)2]n(2)的合成
称取 H3btc(0.2 mmol,0.042 0 g)、bpy(0.2 mmol,0.031 2 g)、八水合硫酸镉(0.2 mmol,0.153 8 g)加入到25 mL的带有聚四氟乙烯衬底的水热反应釜中,并加入15 mL蒸馏水,以及滴加3滴三乙胺,将反应釜放入393 K烘箱中反应72 h。自然降温,冷却后开釜,过滤静置1个月后得到无色针状晶体。产率为31%(以H3btc为基准)。元素分析按C19H16CdN2O8计算值(%):C 44.47,N 5.46,H 3.12;实验值(%):C 44.39,N 5.49,H 3.17。IR(KBr,cm-1):3 417(b),3 159(b),1 588(m),1 479(w),1 436(w),1 370(m),1 120(s),768(m),650(w),618(w)。
1.3 配合物的晶体结构测定
晶体的X射线衍射数据收集采用美国Agilent Technologies公司的G8910A CCD面探单晶衍射仪。在常温情况下,用 Mo Kα 辐射(λ=0.071 073 nm),以ω扫描的方式来收集所有衍射点数据,使用CryAlis pro程序还原原始数据,全部数据均进行Lp因子校正和经验吸收校正[14-15]。先用SHELXS[16a]中的直接法解出粗结构,再用SHELXL程序[16b]对非氢原子坐标及其各向异性温度因子进行全矩阵最小二乘法精修[16c]。所有氢原子坐标均由理论加氢而得。整个结构修正过程在OLEX2[17]平台上完成。配合物1和2的晶体参数表见表1,主要的键长键角见表2。
CCDC:1872165,1;1872166,2。

表1 配合物1和2的晶体学和结构修正数据Table 1 Crystallography and structure parameters of complexes 1 and 2
2 结果与讨论
2.1 配合物的晶体结构描述
2.1.1 配合物1的晶体结构描述
配合物1的分子结构如图1所示。晶体结构解析表明,其最小结构单元包含1个Ag(Ⅰ)离子,1个H2btc-和1个bpy中性分子。仅脱去1个质子的H2btc-通过1个羧基氧原子单齿配位,中性bpy配体通过2个氮原子双齿螯合配位。Ag1分别与来自H2btc-的1个氧原子(O1)和1个bpy中性分子的2个氮原子(N1,N2)配位,3个配位原子在Ag1周围形成了平面三角形构型。
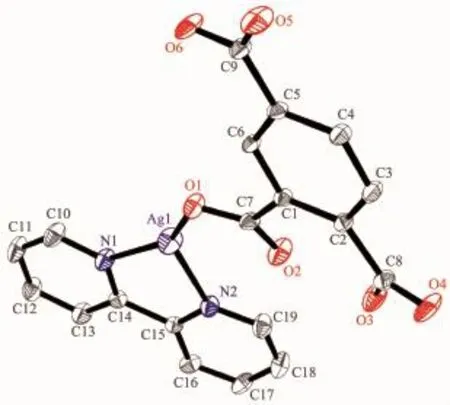
图1 配合物1的结构图Fig.1 Crystal structure of complex 1
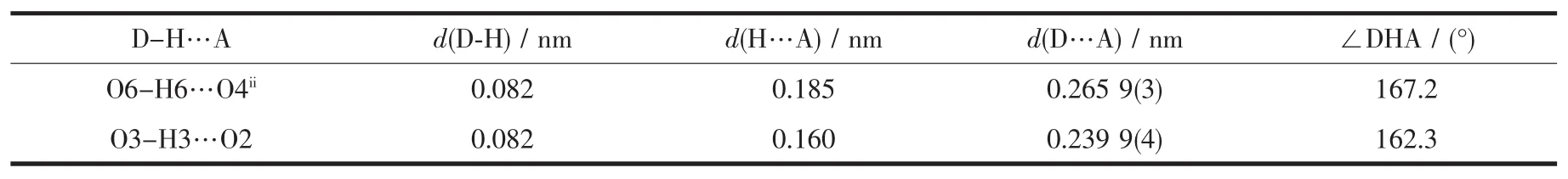
表3 配合物1的氢键键长和键角Table 3 Hydrogen bond parameters of complex 1
由图2所示,在三维空间结构中,分子与分子之间存在一定程度的π…π堆积作用,由相互平行的Cg(1)环(由C1-C2-C3-C4-C5-C6组成的苯环)与Cg(2)环(由C1i-C2i-C3i-C4i-C5i-C6i组成的苯环)之间形成(Symmetry code:i-x,1-y,2-z)。 其中,Cg(1)环的质心坐标为:-0.069 00,0.634 7,0.917 0,Cg(2)环的质心坐标为:0.069 00,0.365 3,1.083 0,环中心之间的距离为0.375 5 nm,二面角为0°。另外,如图3所示,配合物1分子之间还存在着大量的氢键作用,氢键键长键角如表3所示。这些相互作用构筑了该配合物的三维空间结构。赤道平面平均偏离0.014 0 nm。
如图5所示,通过Hbtc2-的双齿桥联的作用,配合物2形成了一维链状结构,链内邻近Cd…Cd之间的距离为0.759 2 nm。另外,链与链之间通过未脱去质子的羧基以及配位水分子等形成弱的氢键作用,和范德华力等相互作用力构建了配合物2的三维空间结构(图6),氢键的键长键角表如表4所示。
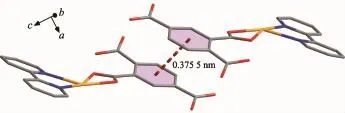
图2 配合物1分子间的π…π堆积相互作用Fig.2 π…π stacking interaction between molecules of complex 1
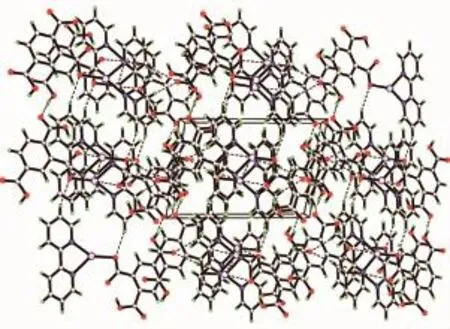
图3 配合物1的三维堆积图Fig.3 Three-dimensional packing diagram of complex 1
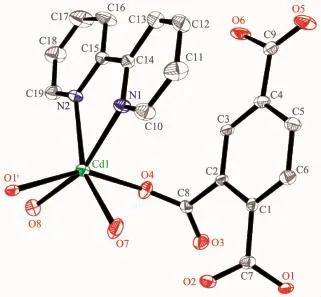
图4 配合物2的结构图Fig.4 Crystal structure of complex 2
2.1.2 配合物2的晶体结构描述
配合物2的分子结构如图4所示。晶体结构解析表明,其最小结构单元包含1个Cd(Ⅱ)离子,1个Hbtc2-,1个bpy中性分子和2个配位水分子。脱去2个质子的Hbtc2-的羧基采用单齿配位的方式,中性bpy配体通过2个氮原子双齿螯合配位。Cd1分别与Hbtc2-羧基的2个氧原子 (O1i,O4),1个 bpy中性分子的 2个氮原子(N1,N2)和 2个水分子(O7,O8)配位,6个配位原子构成了畸变的八面体构型,O7,O8,N1,N2组成赤道平面,O1A和O4呈轴向分布,
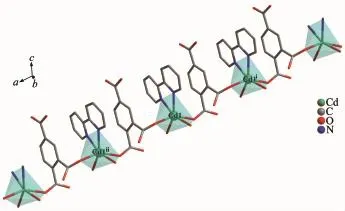
图5 配合物2的一维链状结构Fig.5 One-dimensional chain structure of complex 2
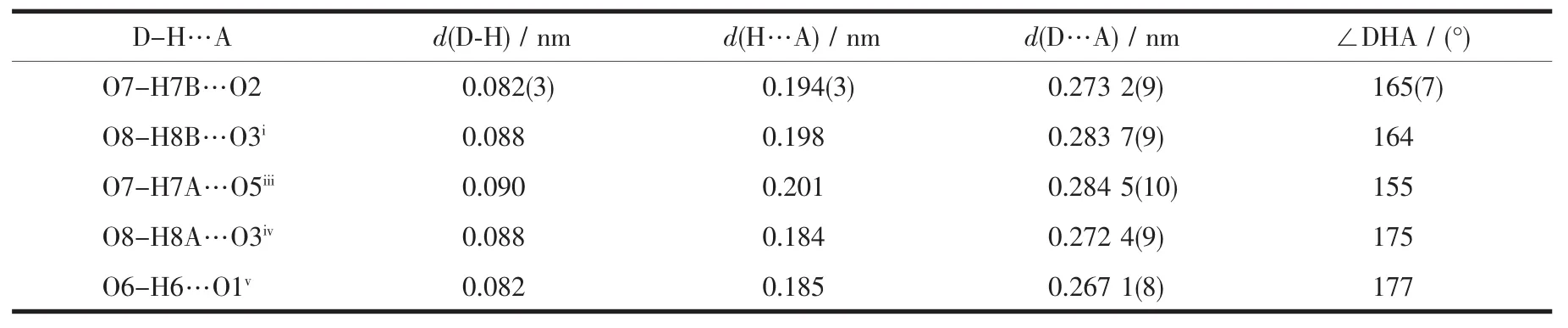
表4 配合物2的氢键键长和键角Table 4 Hydrogen bond lengths(nm)and bond angles(°)of complex 2
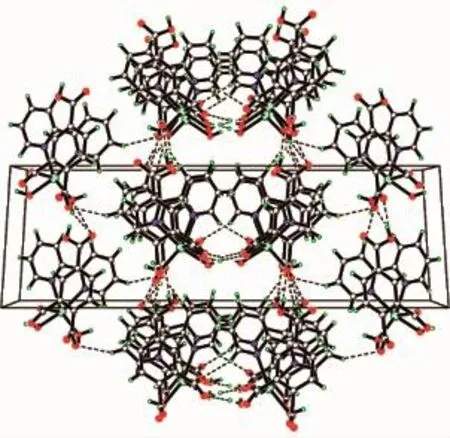
图6 配合物2的三维堆积图Fig.6 Three-dimensional packing diagram of complex 2
2.2 红外光谱
根据有机羧酸类配合物的红外光谱可以对其羧基的配位方式进行判断[18-19]。结果如图7所示。对于1和2,在3 441、3 448 cm-1均有一个非常宽的吸收带,这是形成氢键而缔合的-OH伸缩振动。配合物1 的-COOH 特 征 峰 νas(OCO)、νs(OCO)分 别 出 现 在1 585、1 370 cm-1处,其中 Δν(νas(OCO)-νs(OCO))=215 cm-1,说明配合物1中的羧基存在单齿配位的方式[20]。苯环的伸缩振动出现在1 468 cm-1,-C=O的伸缩振动、-C-O的伸缩振动分别出现在1 707和1 234 cm-1[21]。配合物2的-COOH特征峰νas(OCO)和νs(OCO)分别出现在1 588和1 370 cm-1处,其中Δν(νas(OCO)-νs(OCO))=218 cm-1,说明配合物 2 中的羧基也存在单齿配位的方式。3 159 cm-1处的峰为C-H的伸缩振动,而-C-O的伸缩振动出现在1 120 cm-1处。
2.3 配合物1和2的热稳定性分析
为了测定配合物1和2的热稳定性,在流速为10 mL·min-1的N2保护下对其进行热重测试,升温速率为10 K·min-1,测试温度范围从293~1 173 K。从图8可以看出,配合物1从460 K左右开始,晶体骨架开始分解坍塌,一直到646 K时失重曲线才开始趋于平坦,总失重率为77.64%(理论值为77.58%,残余产物推测为Ag)。而从图9得知,配合物2在428 K之前,失重率为7.84%(理论值为7.02%),是由于配位水分子的失去造成的。该配合物在温度达到428 K之后,骨架发生坍塌,H3btc开始分解。在576~720 K温度范围内,失重率为31.92%(理论值为30.46%),是由于bpy的分解造成。直至温度达到1 173 K时,配体仍未完全分解。
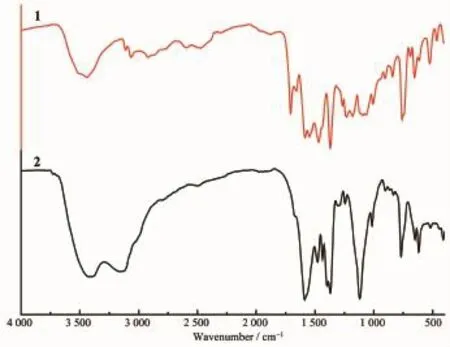
图7 配合物1和2的红外光谱Fig.7 IR spectra of complexes 1 and 2
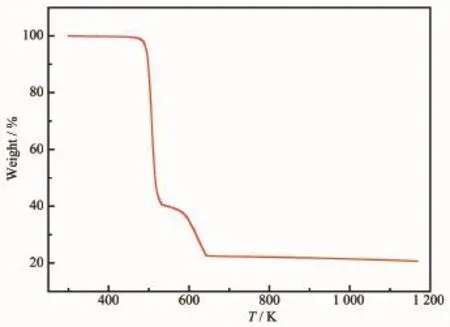
图8 配合物1的热重曲线图Fig.8 Thermal behavior of complex 1
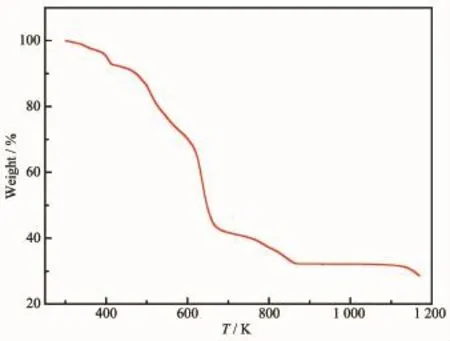
图9 配合物2的热重曲线图Fig.9 Thermal behavior of complex 2
2.4 配合物1和2的荧光性能
近年来,高效发光材料特别是含d10金属配合物发光材料得到科研工作者的重视,一方面其结构存在着一定的刚性,使其分子结构的辐射跃迁得到了较大地增强;另一方面,由于配合物分子结构的稳定性,使得该类化合物为功能型材料的应用提供了一定的保证,因此含d10金属配合物是一类有广泛应用领域的光致发光材料[22-24]。
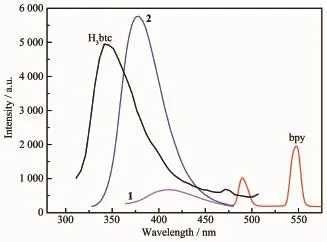
图10 配体、配合物1和2的荧光光谱Fig.10 Solid-state luminescent spectra of ligands,complex 1 and 2
本文对常温下以固态形式存在的2种配体以及配合物1和2的荧光性能进行了研究,结果见图10。荧光光谱表明,H3btc 在 331 nm(λex=260 nm)处出现了较强的荧光发射峰,主要是由于H3btc配体内部的π*→π电荷跃迁所致。bpy在489和546 nm(λex=331 nm)处出现2个较弱的荧光发射峰。而配合物1和2的最大发射峰的峰形与配体H3btc相似,且均发生了明显的红移,其最大发射峰分别出现在410 nm(λex=330 nm)和 377 nm(λex=279 nm)处,这可能是由于Ag+/Cd2+的核外电子构型是d10构型,不易发生氧化还原反应,因此配合物的荧光光谱既不是源于配体到金属的电荷转移,也不是源于金属到配体的电荷转移,配合物的荧光可能来自于配体H3btc配体内部的π*→π跃迁。但荧光强度均发生了明显的变化,配合物1的荧光强度明显降低,而2的荧光强度却显著增强,这可能是由于金属离子与配体H3btc结合后使得结构刚性发生变化,1和2的非辐射跃迁相对升高和降低造成的[25]。
3 结 论
通过水热合成法,以H3btc为第一配体,bpy为第二配体,在过渡金属Ag(Ⅰ)和Cd(Ⅱ)的作用下合成了新的金属有机配合物[Ag(H2btc)(bpy)](1)和[Cd(Hbtc)(bpy)(H2O)2]n(2),用X射线单晶衍射仪测定了配合物的单晶结构,并对它们进行了红外光谱、热重分析和荧光性质的表征。配合物1和2均具有良好的热稳定性。荧光测试结果表明,1和2均具有荧光性,为荧光材料的研究提供了一定的基础。
