直接Z型Zn2SnO4-x N x/ZnO1-y N y异质结光催化剂的制备及机理
2019-09-09谈国强颖党明月任慧君傲刘
王 敏 谈国强*, 张 丹 李 斌 王 颖党明月 任慧君 夏 傲刘 运
(1陕西科技大学材料科学与工程学院无机材料绿色制备与功能化陕西省重点实验室,西安 710021)
(2陕西科技大学文理学院,西安 710021)
(3陕西科技大学电子信息与人工智能学院,西安 710021)
0 引 言
近几年来,随着世界范围内经济的快速发展和工业化步伐的加快,能源短缺和环境污染两大问题日益突出,严重限制了人类社会的可持续发展。光催化技术作为一种环境友好、可持续发展的技术,可利用清洁可再生的太阳能和半导体基光催化剂同时解决以上2个问题[1-2]。在众多传统光催化剂中,TiO2因具有高热稳定性、化学稳定性、高反应活性、低价等优点被广泛研究[3]。但是,TiO2的禁带宽度较大(~3.2 eV),仅能被占太阳能4%~5%的紫外光激发,并且光生电子-空穴对易复合,导致其量子产率较低,限制了其在光催化领域的进一步发展[4]。Zn2SnO4(ZTO)作为一种新型的三元氧化物半导体材料,具有高电子迁移率(10~15 cm2·V-1·s-1)、高电导率(104S·cm-1)和高热稳定性等特点[5-6],在紫外光范围内具有强光吸收特性,且在紫外光照射下可以降解甲基橙、亚甲基蓝、罗丹明B、苯酚、甲醛和一氧化碳等多种有毒物质。但是,与TiO2类似,ZTO也是一种宽禁带半导体,其禁带宽度约为3.7 eV,对太阳光的利用率极低。
金属元素掺杂可应用于ZTO基光催化剂的改性研究[7],杂质元素的存在可以通过调控其电子结构和光学性质从而提高其光催化活性。但是金属元素掺杂会降低半导体的稳定性,并且光腐蚀现象的存在会使金属元素溶出,从而造成二次污染[8]。因此,非金属元素掺杂成为半导体基光催化剂改性的首选方法之一。向光催化剂中引入非金属杂质元素可以通过形成杂质能级拓宽其光响应范围,从而提高其光催化性能[9-10]。但是,非金属掺杂同时会向半导体中引入大量的缺陷和表面态,成为光生电子-空穴对的复合中心,对其光催化性能的提高起反作用[11-12]。此外,与能带结构相匹配的半导体复合,例如SnO2[13]、BiOI[14]、BiOBr[15]、V2O5[16]、g-C3N4[17]等 , 构 筑 异质结,可以通过提高光生载流子的分离效率从而提高ZTO的光催化性能。但是,对于传统的异质结,载流子在界面处分离的同时会导致光生电子和空穴的氧化还原能力削弱,反应活性降低。构筑新型的Z型异质结可以解决这一问题[18-19]。
结合以上2种改性方法的优缺点,采用微波溶剂热法一步合成N掺杂Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂,通过在紫外光照射下降解罗丹明B(RhB)、亚甲基蓝(MB),甲基橙(MO)和水杨酸(SA)等污染物表征其光催化活性,并通过活性物种捕获实验验证异质结构的类型,为制备新型Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂提供研究思路。
1 实验部分
1.1 Zn2SnO4-x N x/ZnO1-y N y光催化剂的制备
称取0.595 g Zn(NO3)2·6H2O加入到20 mL乙二醇中,磁力搅拌20 min后得到浓度为0.1 mol·L-1的硝酸锌溶液;称取0.351 g SnCl4·5H2O加入到20 mL去离子水中,磁力搅拌20 min后得到浓度为0.05 mol·L-1的氯化锡溶液;然后将氯化锡水溶液缓慢加入到硝酸锌的乙二醇溶液中,磁力搅拌20 min将溶液混合均匀;再向上述混合溶液中加入一定量0.6 mol·L-1的 N2H4·H2O 溶液,磁力搅拌 30 min 后得到乳白色的前驱液。将所得前驱液转移到内衬为聚四氟乙烯的微波水热反应釜中,200℃下反应60 min后自然冷却至室温。收集产物,用去离子水和无水乙醇分别洗涤3次后,70℃下恒温干燥12 h即得Zn2SnO4-xNx和Zn2SnO4-xNx/ZnO1-yNy复合光催化剂。当前驱液中0.6 mol·L-1N2H4·H2O溶液的加入量分别为 14、15、16、17、18、19 和 20 mL 时,所得前驱液中 N2H4·H2O 的 浓 度 分 别 为 0.156、0.164、0.171、0.179、0.186、0.193 和 0.200 mol·L-1, 结合后文表征结果,将所得产物分别命名为ZTN1、ZTN2、ZTN/ZN1、ZTN/ZN2、ZTN/ZN3、ZTN/ZN4 和 ZTN/ZN5。
ZnO1-yNy的 制 备 过 程 如 下 :0.595 g Zn(NO3)2·6H2O溶解到20 mL乙二醇和20 mL去离子水的混合溶液中,混合均匀后加入18 mL 0.6 mol·L-1的水合肼溶液,200℃下反应60 min后冷却、洗涤、干燥,得到ZnO1-yNy粉体。
1.2 Zn2SnO4-x N x/ZnO1-y N y光催化剂表征
采用 X射线衍射仪(XRD,D/max-2200 PC,Rigaku,Cu Kα,λ=0.154 06 nm,40 kV,40 mA) 对样品的物相组成和晶体结构进行表征,扫描速率为7°·min-1,扫描范围为 10°~70°。 样品的光吸收特性通过紫外-可见漫反射图(UV-Vis DRS,Cray 5000,Agilent,U.S.A.)反映,测试范围为 200~600 nm。 使用透射电子显微镜(TEM,FEI-Tecnai G2 F20)观察样品的表面形貌、组成和微观结构,其工作电压为300 kV。
1.3 Zn2SnO4-x N x/ZnO1-y N y光催化实验
通过在紫外光照射下降解RhB评估样品的光催化活性,300 W汞灯被用作紫外光光源。0.05 g光催化剂加入到50 mL初始浓度为5 mg·L-1的RhB水溶液中,置于XPA-7光化学反应仪(南京胥江机电厂)中,在磁力搅拌作用下暗反应30 min,待光催化剂粉体与染料分子间达到吸附-脱附平衡后开始光照,每隔一定时间取5 mL悬浊液,离心分离(3 500 r·min-1)取上清液,用紫外-可见分光光度计(SP-756P)测试其在554 nm处的吸光度(A)的变化。根据吸光度的改变计算RhB的降解率η:
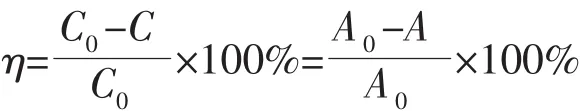
式中:C0为RhB溶液的初始浓度,C为光催化反应过程中某一时刻RhB溶液的浓度;A0为初始的RhB溶液在554 nm处的吸光度,A为光催化反应过程中某一时刻RhB溶液在554 nm处的吸光度。MB、MO和SA的降解反应与RhB类似,不同的是,以上3种污染物水溶液的初始浓度为10 mg·L-1。
1.4 Zn2SnO4-x N x/ZnO1-y N y光催化剂光电化学测试
使用CHI-660E电化学工作站对样品的光电化学性能进行表征。测试系统为标准三电极体系:Pt片作为对电极,饱和Ag/AgCl电极为参比电极,涂覆有样品的氟掺杂氧化锡(FTO)导电玻璃为工作电极,0.1 mol·L-1的Na2SO4溶液为电解液。工作电极的制备过程如下:称取0.02 g光催化剂粉体分散到1 mL无水乙醇和0.2 mL乙酰丙酮的混合溶液中,超声处理30 min后得到分散均匀的悬浊液。将该悬浊液旋涂到1.5 cm×2 cm的FTO玻璃基板上,在马弗炉内200℃退火2 h后随炉冷却至室温即得工作电极。在紫外光照射下测试样品的瞬态光电流响应(I-t曲线),测试时间为400 s,无外加偏压,开关灯间隔均为2 s;在紫外光照射下测试样品的电化学阻抗图谱(EIS),所选频率范围为 0.01~1×105Hz。 300 W 汞灯被用作紫外光光源。Mott-Schottky测试在暗光条件下进行,测试范围为-1~1 V。使用ZSimpWin软件对样品的Nyquist点图进行拟合。
2 结果与讨论
2.1 Zn2SnO4-x N x/ZnO1-y N y的组成与晶体结构分析
图 1a为样品的 XRD 图。 在 2θ=17.86°、29.15°、34.33°、41.70°、55.07°和 60.44°处的衍射峰分别对应立方相反尖晶石结构Zn2SnO4(PDF No.24-1470)的(111)、(220)、(311)、(400)、(511)和(440)晶面,而 2θ=31.77°、36.25°和 56.59°处的衍射峰则分别对应六方相 ZnO(PDF No.36-1451)的(100)、(101)和(110)晶面,说明 ZTN/ZN1、ZTN/ZN2、ZTN/ZN3、ZTN/ZN4 和 ZTN/ZN5样品中包含Zn2SnO4和ZnO两种物相。当前驱液中N2H4·H2O浓度较低时,样品ZTN1和ZTN2未出现ZnO相。随着N2H4·H2O浓度的增大,样品的结晶度先增大后减小,但其他样品的结晶度均大于ZTN1和ZTN2,说明碱性条件有利于ZnO的生成和样品结晶度的提高。较低结晶度的样品,意味着其具有较大的表面缺陷浓度和表面能。图1b是样品的XRD 图在 30°~40°范围内的放大图。 ZTN/ZN1、ZTN/ZN2、ZTN/ZN3、ZTN/ZN4 和 ZTN/ZN5 中 的 Zn2SnO4(311)晶面的衍射峰发生了不同程度的偏移,说明Zn2SnO4与ZnO之间存在相互作用力,即形成了异质结[20]。此外,与标准卡片相比,Zn2SnO4的(311)晶面以及ZnO的(101)晶面的衍射峰产生的明显偏移是由N掺杂所引起的晶格畸变导致的,说明N元素被成功的引入到了Zn2SnO4和ZnO的晶格中,形成了Zn2SnO4-xNx/ZnO1-yNy晶体。
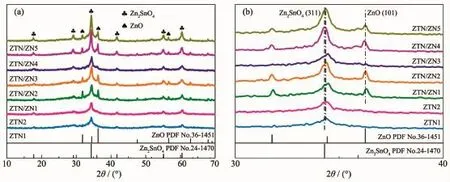
图1 (a)样品的XRD图;(b)XRD放大图Fig.1 (a)XRD patterns of samples;(b)Magnified XRD patterns
2.2 Zn2SnO4-x N x/ZnO1-y N y的形貌和元素组成分析
图 2(a,b)分别是 ZTN1和 ZTN/ZN3号样品的TEM图。图2a表明制备的Zn2SnO4由不规则纳米颗粒组成,颗粒尺寸较小,并且表现出明显的团聚现象。从图2b可以看出,ZTN/ZN3号样品由2种不同的形貌组成,Zn2SnO4为不规则纳米颗粒,而ZnO则表现为纳米棒形貌。Zn2SnO4纳米颗粒紧密地附着在ZnO纳米棒上,形成类核壳结构的界面异质结。图2c是ZTN/ZN3号样品的高分辨率透射电子电镜(HRTEM)图,晶面间距 0.310、0.264和 0.291 nm 分别对应于立方相反尖晶石结构 Zn2SnO4的(220)、(311)晶面和六方相ZnO的(100)晶面,证明Zn2SnO4和ZnO两相在复合材料中共存。图2d为选区电子衍射(SAED)图,环形的衍射斑点说明Zn2SnO4为多晶结构,ZnO为单晶结构。图2(e~h)为ZTN/ZN3的元素分布图,除了Zn、Sn、O元素之外,N元素同样可以被探测到,说明N元素被成功地引入到了Zn2SnO4和ZnO的晶格中,形成了Zn2SnO4-xNx和ZnO1-yNy结构单元,表明以N2H4·H2O为N源,采用微波溶剂热法成功制备了N掺杂Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂。
基于以上分析和相关文献报道[21-25]得出Zn2SnO4-xNx/ZnO1-yNy异质结构的形成机理。Zn(NO3)2·6H2O和SnCl4·5H2O在乙二醇和去离子水中解离成相应的离子,形成 2个透明溶液(反应式(1~3),图 3a)。将SnCl4·5H2O的水溶液分散到Zn(NO3)2·6H2O的乙二醇溶液后形成ZnSn(OH)6和Zn(OH)42-胶核(反应式(4,5))。加入水合肼溶液,搅拌均匀得到反应前驱液(图3(b,c))。 由于N2H4·H2O在去离子水中解离形成N2H5+和OH-(反应式(6))。在静电引力作用下,溶液中的 N2H5+离子吸附在 ZnSn(OH)6和Zn(OH)42-胶核表面,形成 ZnSn(OH)6·N2H5+和 Zn(OH)4(N2H5)2胶粒(反应式(7))。水热反应后,N杂质原子分别进入Zn2SnO4和ZnO的晶格中,形成Zn2SnO4-xNx和ZnO1-yNy(反应式(8),图 3d)。 N 原子在 Zn2SnO4-xNx和 ZnO1-yNy的价带顶部形成杂质能级,增大了Zn2SnO4和ZnO表面电荷密度,从而导致晶格畸变和界面变化。
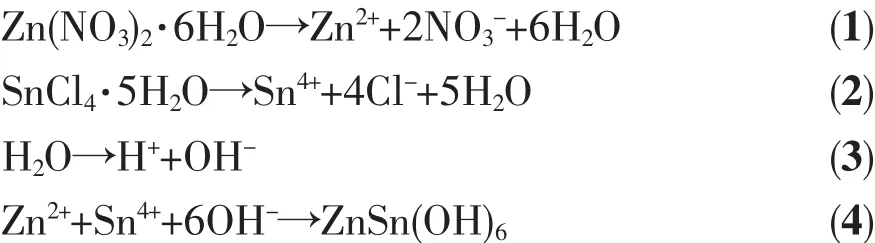

图2 (a)ZTN1和(b)ZTN/ZN3的TEM图;ZTN/ZN3的(c)HRTEM图和(d)SAED图;ZTN/ZN3 中(e)Zn、(f)Sn、(g)O 和(h)N 的 TEM mapping图Fig.2 TEM images of(a)ZTN1 and(b)ZTN/ZN3;(c)HRTEM and(d)SAED images of ZTN/ZN3;TEM mapping images of(e)Zn,(f)Sn,(g)O and(h)N in ZTN/ZN3
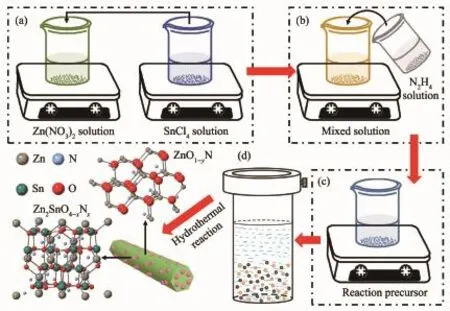
图3 Zn2SnO4-x N x/ZnO1-y N y异质结的形成机理Fig.3 Formation mechanism of Zn2SnO4-x N x/ZnO1-y N y heterojunction
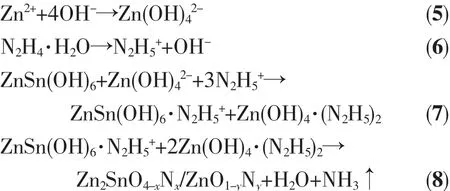
2.3 Zn2SnO4-x N x/ZnO1-y N y的紫外-可见漫反射光谱分析
图4是光催化剂的紫外-可见漫反射(UV-Vis DRS)光谱,ZTN1和ZTN2在200~300 nm范围光吸收明显大于其他光催化剂,是因为ZnO1-yNy的存在降低了其他样品在紫外光范围内的光吸收强度。另外两者在350~400 nm范围内微弱的吸收肩源于异质元素掺杂[26-27],进一步说明N原子取代O原子在Zn2SnO4价带顶部形成N杂质能级。对于ZTN/ZN1、ZTN/ZN2、ZTN/ZN3、ZTN/ZN4 和 ZTN/ZN5, 在 280~320 nm范围内的光吸收边带归属于Zn2SnO4-xNx,而400 nm左右的光吸收边带的出现则归因于ZnO1-yNy的存在。这进一步证明Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂被成功合成。
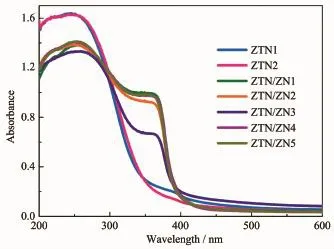
图4 样品的紫外-可见漫反射光谱Fig.4 UV-Vis DRS of samples
2.4 Zn2SnO4-x N x/ZnO1-y N y的光催化活性和稳定性分析
图5 a为光催化剂在紫外光照射下对RhB的降解曲线。ZTN1和ZTN2在紫外光照射30 min后对RhB的降解率分别为90.63%和86.05%。而ZTN/ZN3在30 min内对RhB的降解率为94.56%,说明Zn2SnO4-xNx与ZnO1-yNy形成异质结之后,有效地提高了Zn2SnO4-xNx的光催化活性。而其他异质结光催化剂样品光催化性能略低于ZTN1和ZTN2样品,这是由ZnO1-yNy的光腐蚀现象导致的[28-29]。当异质结中ZnO1-yNy的含量较大时,暴露在外的ZnO1-yNy增多,光腐蚀现象的增强导致光催化性能降低,而适量匹配的ZTN/ZN3样品形成Zn2SnO4-xNx纳米颗粒紧密地附着在ZnO1-yNy纳米棒上的ZnO@Zn2SnO4核壳结构的界面异质结,弱化了ZnO1-yNy的光腐蚀现象。根据Langmuir-Hinshelwood模型,RhB的光催化降解过程为伪一级反应。其表观速率常数可以根据经验动力学方程(9)计算[30]:

式中,C0′、C、kapp和 t分别代表暗反应吸附平衡之后RhB溶液的浓度、光催化过程中某一时刻RhB的浓度、表观速率常数(min-1)和光照时间(min)。根据上述公式计算得到所有样品的表观速率常数如图5b所示。ZTN/ZN3具有最大的表观速率常数(0.097 0 min-1),分别为 ZTN1(0.069 2 min-1)和 ZTN2(0.067 6 min-1)的1.40倍和1.43倍。该结果表明Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂在紫外光照射下的光催化活性较纯相Zn2SnO4-xNx有所提高。其性能提高的原因是ZnO1-yNy@Zn2SnO4-xNx核壳结构的界面异质结及双N杂质能级的效应拓宽了光响应范围。
为考察Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂的循环稳定性,以ZTN/ZN3作为光催化剂,经过5次循环实验之后(图6a),样品的光催化活性并没有明显降低,在第5次循环降解实验中,紫外光照射40 min后,RhB的降解率仍可达96.03%;图6b为反应前后ZTN/ZN3的XRD图,反应前后样品的物相结构没有明显改变,其衍射峰强度的降低可以归因于在水相条件下,部分小分子吸附在样品表面,导致其XRD衍射峰强度降低。以上结果表明Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂具有良好的循环稳定性。
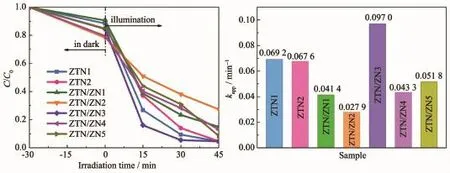
图5 (a)样品对RhB的光催化降解曲线;(b)表观速率常数Fig.5 (a)Photocatalytic degradation curves of RhB over samples;(b)Apparent rate constants
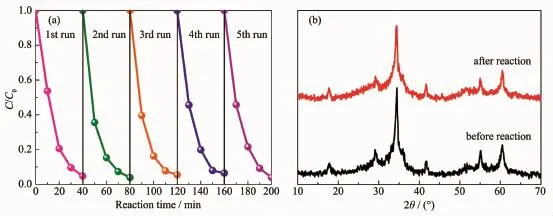
图6 (a)ZTN/ZN3在紫外光照射下对RhB的循环降解实验;(b)循环反应前后ZTN/ZN3的XRD图Fig.6 Recycle degradation experiments of RhB over ZTN/ZN3 under UV light irradiation;(b)XRD patterns of ZTN/ZN3 before and after cyclic reactions
为了验证明异质结光催化剂的对有机染料普适性,测试了ZTN/ZN3对MB、MO和SA的降解实验(图7(a~c))。 紫外光照射 60 min 后,ZTN/ZN3 对 MB、MO和SA的降解率分别为87.67%,91.29%和58.55%。其表观速率常数分别为0.032 27、0.037 31和0.018 1 min-1(图7d)。结果表明Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂对污染物的降解是非光敏化作用,具有普适性和较强的矿化能力。
2.5 光电化学性能分析
瞬态光电流的大小可以直接反映光催化剂光生电子-空穴对的分离和迁移情况。图8是不同样品在紫外光照射下数个开关灯循环间的瞬态光电流响应曲线。光照瞬间样品的光电流增大,暗光瞬间其光电流又减小为0,说明样品均具有快速稳定的光电流响应。样品的光电流大小与光催化活性基本相符。ZTN/ZN3具有最大的瞬态光电流值(5.090 μA),分别为 ZTN1(4.483 μA)和 ZTN2(3.407 μA)瞬态光电流的1.135倍和1.49倍。说明Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂与Zn2SnO4-xNx相比具有更高的光生电子-空穴对的分离效率。ZTN/ZN1、ZTN/ZN2、ZTN/ZN4 和ZTN/ZN5的光电流值明显低于ZTN1和ZTN2,源于ZnO1-yNy的光腐蚀特性。此外,当N掺杂量较小时,表现出基体的光电特性;当N杂质元素的含量过高时,成为光生电子-空穴对的复合中心,抑制光生载流子的分离,因而ZTN/ZN4和ZTN/ZN5的光电流较小。ZTN/ZN3最大的光电流值源于其适中的N掺杂量和ZnO1-yNy含量有利于构筑界面异质结和双杂质能级效应,提高了光催化活性。
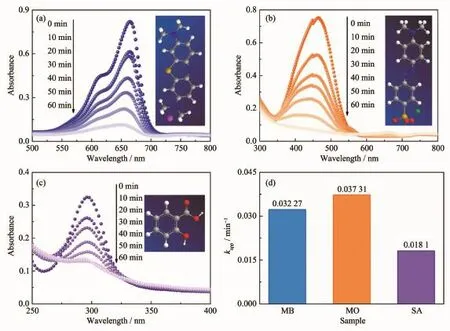
图7 ZTN/ZN3在紫外光照射下对(a)MB、(b)MO和(c)SA的降解曲线及(d)表观速率常数Fig.7 Degradation curves of(a)MB,(b)MO and(c)SA over ZTN/ZN3 under UV light irradiation and(d)corresponding apparent rate constants
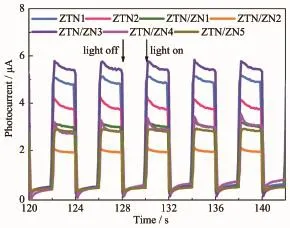
图8 样品在紫外光照射下的瞬态光电流响应Fig.8 Transient photocurrent response of samples under UV light irradiation
图9 是不同样品在紫外光照射下的电化学阻抗图谱(EIS)。曲线的圆弧半径越小,样品光生电子-空穴对的迁移阻力越小,载流子在界面的迁移速率越快[31]。EIS测试结果与瞬态光电流测试结果基本相符。ZTN/ZN3的阻抗图具有最小的圆弧半径(图9),即ZTN/ZN3具有最小的光生载流子迁移阻力。使用ZSimpWin软件对样品的Nyquist点图进行拟合,所选拟合电路为 Rs(QRct),其中 Rs、Q、Rct分别代表溶液电阻、常相位角元件和电荷转移电阻。拟合结果如表1所示。表中n值与Q元件的特性有关(n=1,代表理想电容;n=0,代表纯电阻;n=-1,代表电感;n=1/2,代表Warburg扩散阻抗;0<n<1,则为常相位角原件Q)。ZTN1、ZTN2和ZTN/ZN3的电荷转移电阻分别为75.89、97.57和 40.07 kΩ,ZTN/ZN3号样品的电荷转移电阻最小,表明Zn2SnO4-xNx和ZnO1-yNy间界面异质结的形成可以减小光生载流子的迁移阻力,加快界面电荷转移,从而提高光生电子-空穴对的分离效率,达到改善其光催化性能的目的。
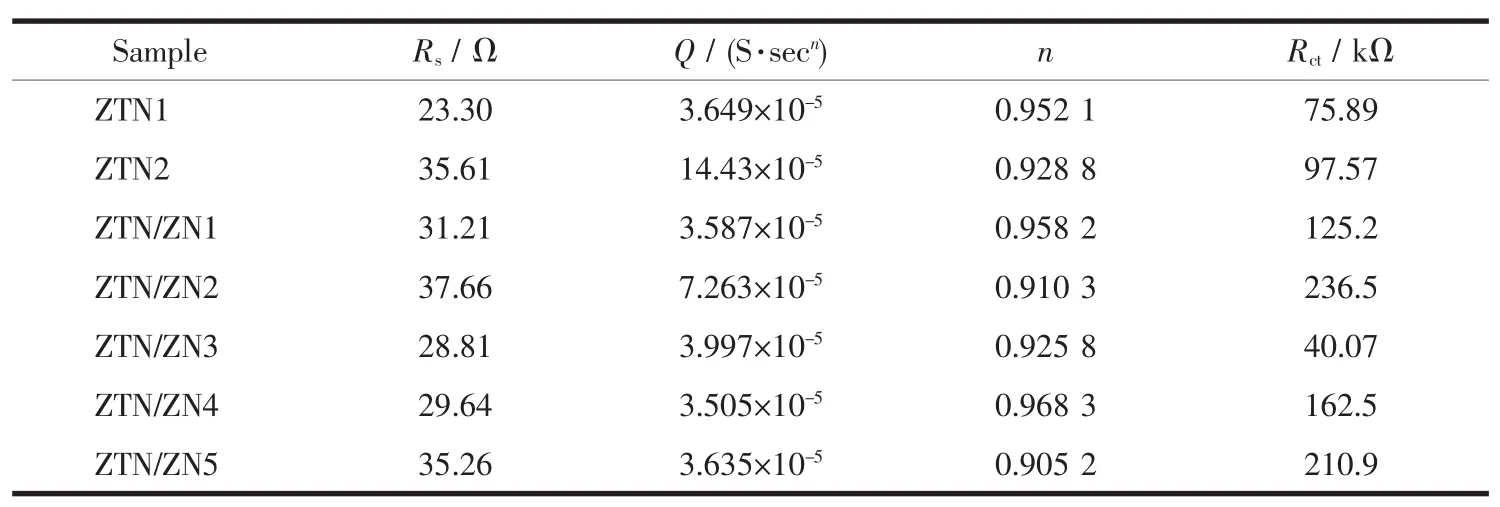
表1 所有样品Nyquist点图的拟合结果Table 1 Fitting results of Nyquist plots of all samples
2.6 Zn2SnO4-x N x/ZnO1-y N y的光催化反应机理分析
为了进一步分析Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂的光催化反应机理,并了解各种活性物种在光催化反应过程中所起的作用,以ZTN/ZN3作为光催化剂,向光催化系统中分别加入对苯醌(BQ,0.001 g)、乙二胺四乙酸二钠(EDTA-2Na,0.37 g)和叔丁醇(tBuOH,1 mL)作为超氧基(·O2-)、空穴(h+)和羟基自由基(·OH)的捕获剂,进行活性物种捕获实验。紫外光照射40 min后,加入3种捕获剂后对RhB的降解率由95.19%分别减小到34.00%、41.45%和50.37%,说明·O2-、h+和·OH 均为光催化反应期间起主要作用的活性物种。
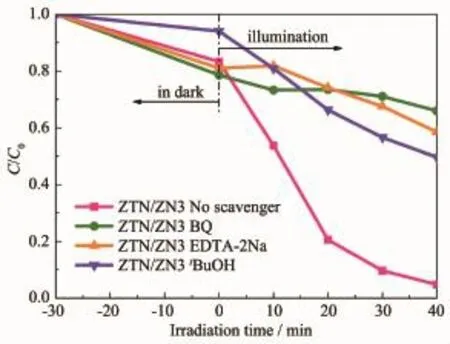
图10 不同捕获基对Zn2SnO4-x N x/ZnO1-y N y光降解RhB的影响Fig.10 Effect of different trapping agents on the photodegradation of RhB over Zn2SnO4-x N x/ZnO1-y N y photocatalyst
半导体的禁带宽度可以通过Kubelka-Munk公式(10)估算:

式中,α、h、ν、Eg分别代表样品的光吸收系数、 入射光频率、普朗克常数和禁带宽度。A为常数,n与半导体类型有关。Zn2SnO4-xNx和ZnO1-yNy均为直接带隙半导体,其n值为1[32-33]。根据公式(10),计算得到Zn2SnO4-xNx(ZTN1)和ZnO1-yNy(采用同样的方法制备得到的纯相ZnO1-yNy)的禁带宽度分别为3.82和3.19 eV。 图11b为Zn2SnO4-xNx和ZnO1-yNy的Mott-Schottky点图,正的斜率表明Zn2SnO4-xNx和ZnO1-yNy均为n型半导体。对于n型半导体而言导带电势约等于平带电势。根据Mott-Schottky点图中的直线部分在x轴上的截距可知Zn2SnO4-xNx和ZnO1-yNy的导带电势约为-0.73和-0.25 eV。根据公式(11):

式中,EV、Eg和EC分别为半导体的价带电势、禁带宽度和导带电势,计算得到Zn2SnO4-xNx和ZnO1-yNy的价带电势分别为3.09和2.94 eV。
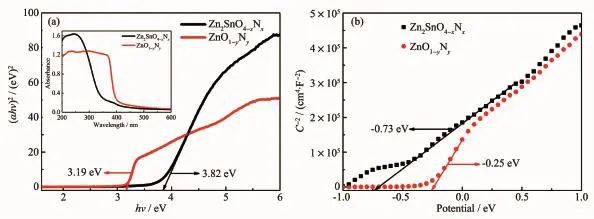
图 11 Zn2SnO4-x N x和 ZnO1-y N y的(a)(αhν)2-hν图和(b)Mott-Schottky 点图Fig.11 (a)Plots of the(αhν)2 vs hν and(b)Mott-Schottky plots of Zn2SnO4-x N x and ZnO1-y N y
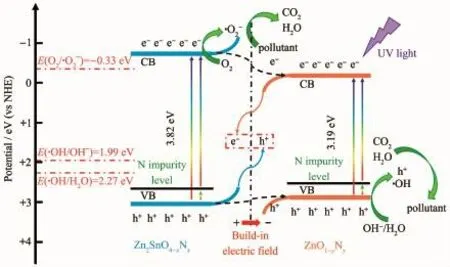
图12 Zn2SnO4-x N x/ZnO1-y N y异质结光催化剂的光催化机理图Fig.12 Photocatalytic mechanism of Zn2SnO4-x N x/ZnO1-y N y heterojunction photocatalyst
图12 是Zn2SnO4-xNx/ZnO1-yNy异质结的光催化机理图。在紫外光照射下,宽禁带的Zn2SnO4-xNx和ZnO1-yNy均可以被激发,价带电子吸收光子能量,跃迁到导带位置,同时在价带留下空穴。同时,N杂质能级可以作为电子跃迁的跳板,光生电子可以先跃迁到N杂质能级,再由杂质能级跃迁至导带位置,两步跃迁过程可以有效提高半导体的光响应范围和光生载流子的分离效率;此外,由于N原子是一个良好的电子供体,其电荷可直接被激发到导带位置参与光催化反应。根据传统的异质结理论,由于Zn2SnO4-xNx(-0.73 eV)的导带电势比ZnO1-yNy(-0.25 eV)的导带电势更负,价带电势(Zn2SnO4-xNx:3.09 eV)比ZnO1-yNy(2.94 eV)的价带电势更正,Zn2SnO4-xNx的光生电子和空穴倾向于迁移到ZnO1-yNy的导带和价带位置,如图12黑色虚线箭头所示,形成传统的Ⅰ型异质结。根据活性物种捕获实验结果,·O2-物种在光催化降解RhB过程中起到了很关键的作用。但是,在这种情况下,由于·O2-/O2(-0.33 eV vs NHE)[34]的电势比ZnO1-yNy的导带电势更负,氧气分子无法与ZnO1-yNy的导带电子反应生成·O2-物种,与活性物种捕获实验结果不符。基于以上分析,Zn2SnO4-xNx/ZnO1-yNy复合光催化剂并不是遵循传统的Ⅰ型异质结。根据之前的报道[35-36],Zn2SnO4和ZnO的功函分别为4.81和5.10 eV,Zn2SnO4的电子逸出功较小,因而,Zn2SnO4-xNx的表面电子将会向ZnO1-yNy转移,导致ZnO1-yNy的表面电荷密度增大,而Zn2SnO4-xNx的表面电荷密度减小,由此在界面处形成一个由Zn2SnO4-xNx指向ZnO1-yNy的内建电场,如图12红色箭头所示,并且这一电荷转移过程使Zn2SnO4-xNx的能带向上弯曲,ZnO1-yNy的能带向下弯曲,在两者的界面处,Ⅰ型异质结转变为Ⅱ型异质结。在内建电场作用下,ZnO1-yNy的光生电子很容易与Zn2SnO4-xNx的光生空穴复合,如图12中金黄色和蓝色实线箭头所示,Ⅱ型异质结再进一步转变为Z型异质结,留下具有更高还原电势的光生电子参与之后的反应。Zn2SnO4-xNx的导带电子将与氧气分子反应生成·O2-物种,而ZnO1-yNy的价带空穴则与水分子或者OH-反应生成·OH 物种。在·O2-、·OH和h+三者的共同作用下将有机污染物降解成为水和二氧化碳或者其他无毒性的小分子。因此,Zn2SnO4-xNx/ZnO1-yNy增强的光催化活性可归因于双杂质能级和Z型异质结的协同作用。
3 结 论
通过控制反应前驱液中水合肼的浓度,采用微波溶剂热法一步合成具有不同ZnO含量的核壳结构Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂,其在紫外光照射下对有机污染物的降解具有较强的矿化能力、普适性、良好的循环稳定性和非光敏化作用。由于不同功函所导致的界面电荷转移和能带弯曲使两者由传统的Ⅰ型异质结转变为Ⅱ型异质结,再由界面处内建电场的作用使其由Ⅱ型异质结转变为Z型异质结。N原子进入Zn2SnO4和ZnO的晶格中形成双杂质能级,拓宽了其光响应范围;Zn2SnO4-xNx颗粒附着在ZnO1-yNy纳米棒表面形成的核壳结构可缓解ZnO1-yNy的光腐蚀现象。Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂降解RhB的速率和瞬态光电流值分别为纯相Zn2SnO4-xNx的1.40~1.43倍和1.14~1.49倍,光催化性能的提高主要归因于Z型异质结和双杂质能级的协同作用。这种新型的直接Z型Zn2SnO4-xNx/ZnO1-yNy异质结光催化剂在环境净化领域具有潜在的应用前景。
