水貂犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)安全性评价
2019-09-06冯二凯易立罗国良王振军郭利陈立志程世鹏程悦宁
冯二凯,易立,罗国良,王振军,郭利,陈立志,程世鹏,程悦宁*
(1.中国农业科学院特产研究所,长春 130112; 2.吉林特研生物技术有限责任公司,长春 130122)
犬瘟热(canine distemper,CD)是犬瘟热病毒(Canine distemper virus,CDV)感染引起的、可导致多种食肉动物患病的一种急性、接触性传染病[1],可感染所有的犬科、鼬科以及水生哺乳动物,且感染宿主范围正在不断扩大[2-3]。不同动物对CDV的易感性和致死率各不相同,从30%~80%不等,对我国的养犬业,毛皮动物养殖业和野生珍稀动物保护造成了很大危害。
犬瘟热临床防治没有治疗药物,只能通过疫苗接种免疫预防。中国农业科学院特产研究所先后研究了我国第一代和第二代水貂犬瘟热活疫苗,疫苗的成功研制为有效控制我国毛皮动物犬瘟热疫情的发生和流行奠定了基础。为了适应毛皮动物饲养业对高品质生物制品的需求,提升企业产品的市场竞争力,中国农业科学院特产研究所又开展了水貂犬瘟Vero细胞活疫苗(CDV3-CL株,悬浮培养)的悬浮培养工艺的开发工作。
本研究在前期建立犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)悬浮培养生产工艺的基础上[4-6],利用建立的疫苗悬浮制备工艺生产3批疫苗半成品,实验室根据《新兽药研制管理办法》、《兽用生物制品注册分类及注册资料要求》的有关规定,制备了三批水貂犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养),在疫苗检验合格的基础上对疫苗的安全性进行了系统评价。
1 材料与方法
1.1 材料
1.1.1 种毒与细胞 非洲绿猴肾细胞(Vero),由中国农业科学院特产研究所保存;犬瘟热CDV3-CL毒株第15代(基础毒种),由中国农业科学院特产研究所鉴定和保存。
1.1.2 试验用疫苗 安全性试验用3批犬瘟热Vero活疫苗(CDV3-CL株,悬浮培养)冻干品(批号:201701、201702、201703),由吉林特研生物技术有限责任公司生产,规格为15头份/瓶,2017年1月份制备,疫苗在-20 ℃以下条件下保存。
1.1.3 微载体混悬液(5 g/L) 取已硅化蓝盖瓶,称5 g微载体,按照100 mL/g微载体的比例加入无Ca2+、Mg2+的PBS,于4 ℃浸泡过夜;次日弃PBS和漂浮微载体,按200 mL/g微载体的比例加入无Ca2+、Mg2+的PBS,120 ℃高压灭菌30 min,冷却至室温备用。
1.1.4 细胞维持液 含有2%小牛血清的DMEM培养基,用于接毒后病毒增殖。
1.1.5 试验动物 品系:美国短毛黑;2~4月龄和8~10月龄水貂以及妊娠30~35 d水貂(中和抗体SN≤1∶4),由吉林中特农业科技有限公司异兽路分公司提供。安全试验动物选择健康,未接种任何疫苗的水貂。
1.2 方法
1.2.1 疫苗检验 参照农业部第2215号公告[7]要求,对3批疫苗进行质量检验,质量检验由吉林特研生物技术有限责任公司质量管理部完成。
1.2.2 试验动物 本试验对2~4月龄水貂幼崽、8~10月龄育成水貂和妊娠30~35 d水貂进行安全性测试。试验动物管理按正常条件进行饲养管理;水貂均为单笼饲养,分组试验。
1.2.3 疫苗安全性评价指标 包括全身性和局部安全检查。全身性检查包括体温监测、精神状态、食欲变化、幼兽生长性能、妊娠水貂是否流产等;局部检查包括注射部位有无炎症或破溃、局部吸收情况等。
1.2.4 单剂量皮下接种安全性试验 3批疫苗分别接种2~4月龄和8~10月龄水貂,10只/组,后肢内侧皮下接种,1头份/只,接种后连续观察14 d,观察全身和接种局部变化;接种后10 d内每日记录体温变化。第15 d剖杀水貂,检查接种部位有无病理变化。
1.2.5 单剂量重复皮下接种安全性试验 3批疫苗分别接种2~4月龄水貂进行单剂量重复接种试验,10只/组,后肢内侧皮下接种,1头份/只,两次接种时间间隔14 d,二次接种后继续观察全身和接种局部变化;重复接种后10 d内,每日记录体温变化。
1.2.6 超剂量皮下接种安全性试验 3批疫苗分别接种2~4月龄水貂进行试验;10只/组,后肢内侧皮下接种,10头份/只,分四点注射,接种后连续观察14 d,观察全身和接种局部变化,接种后10 d内,每日记录体温变化。第15天剖杀水貂,检查接种部位有无病理变化。
1.2.7 微载体安全性试验 将制备的微载体混悬液(5 g/L)接种水貂幼崽和育成水貂,考察微载体对水貂的安全性,5只/组,后肢内侧皮下接种,1.0mL/只,分两点注射,接种后连续观察14d,观察全身和接种局部变化,并在接种后10 d内,每日记录体温变化。第15天剖杀水貂,检查接种部位有无病理变化。
1.2.8 妊娠水貂安全性试验 3批疫苗分别接种妊娠30~35 d水貂进行安全性试验。每组试验接种水貂10只,后肢内侧皮下接种,1头份(毫升)/只,接种后观察至产仔后1个月,记录妊娠水貂是否出现流产。
1.2.9 对照组 每个实验组设置对照组,水貂注射细胞维持液,5只/组,注射剂量、方式与上述试验同步进行。
1.2.10 组织病理切片分析 在每组试验的末期(第15天),剖杀2只水貂,观察接种部位有无炎症或破溃;取接种部位肌肉,甲醛固定后,经HE染色后,观察各实验组动物接种部位组织病理变化。
2 结果与分析
2.1 犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)质量检验结果 三批犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)无菌检验、外源病毒检验均为阴性,表明3批疫苗质量均符合标准,可以用于临床安全性评价试验;疫苗冻干后每头份病毒含量为103.80~104.00TCID50/0.1 mL(表1)。

表1 三批犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)检验结果Tab 1 The inspection result of three batch of CDV vaccine(CDV3-CL strain,suspension)
“-”表示检测结果阴性
2.2 一次单剂量皮下接种安全性试验结果 3批疫苗接种水貂幼崽(2~4月龄)及育成水貂(8~10月龄),通过14 d观察,接种10 d内各组水貂平均体温变化正常(未连续2 d超过40.5 ℃)(图1和图2);水貂食欲、粪便及精神状态均正常,接种局部无肿胀和炎症,未出现局部和全身炎症反应(表2和表3)。
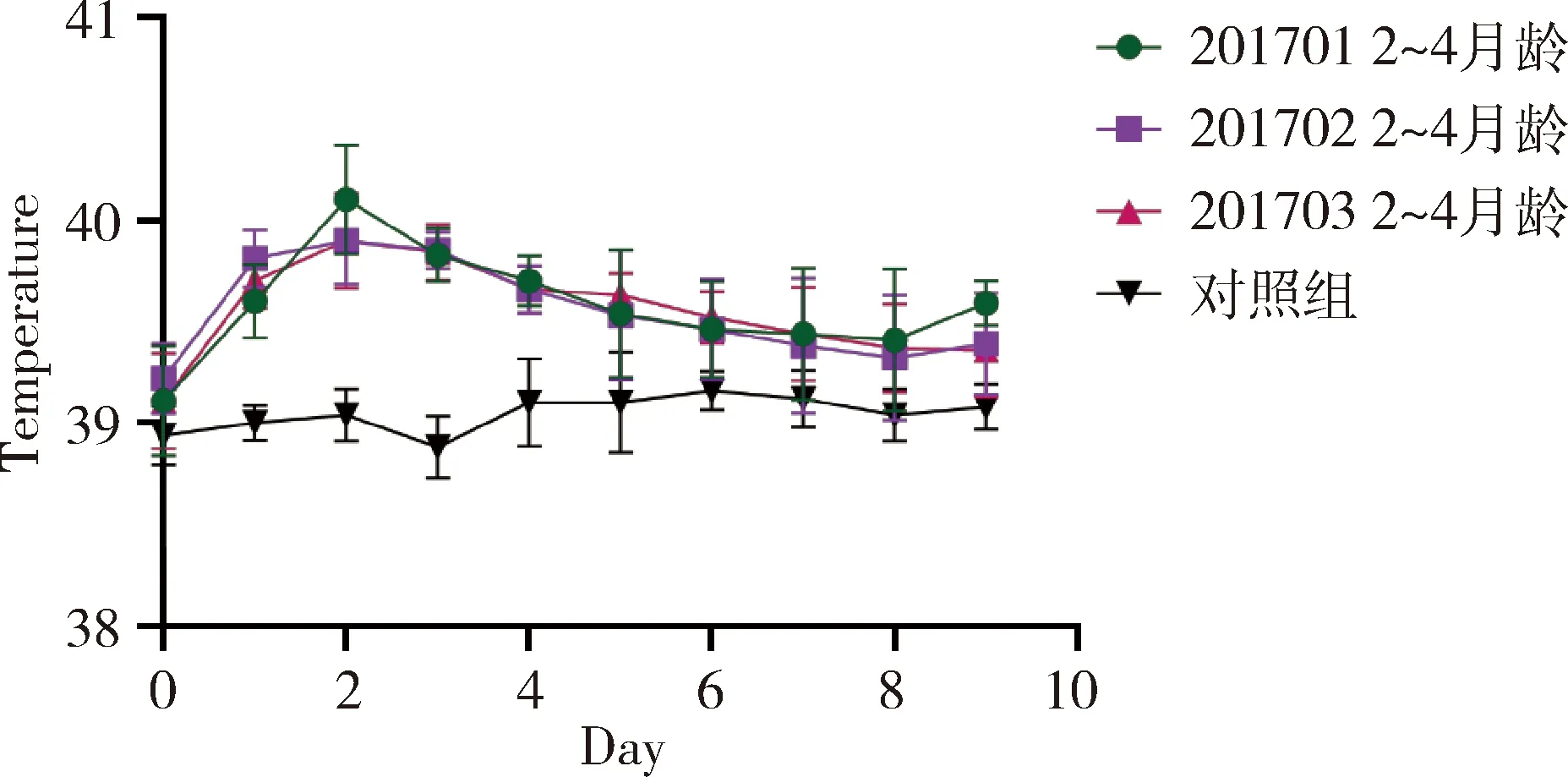
图1 疫苗对水貂一次单剂量接种后体温变化图(2~4月龄)Fig 1 The fluctuate curve of body temperature ofmink received one dose vaccine(2~4 month)
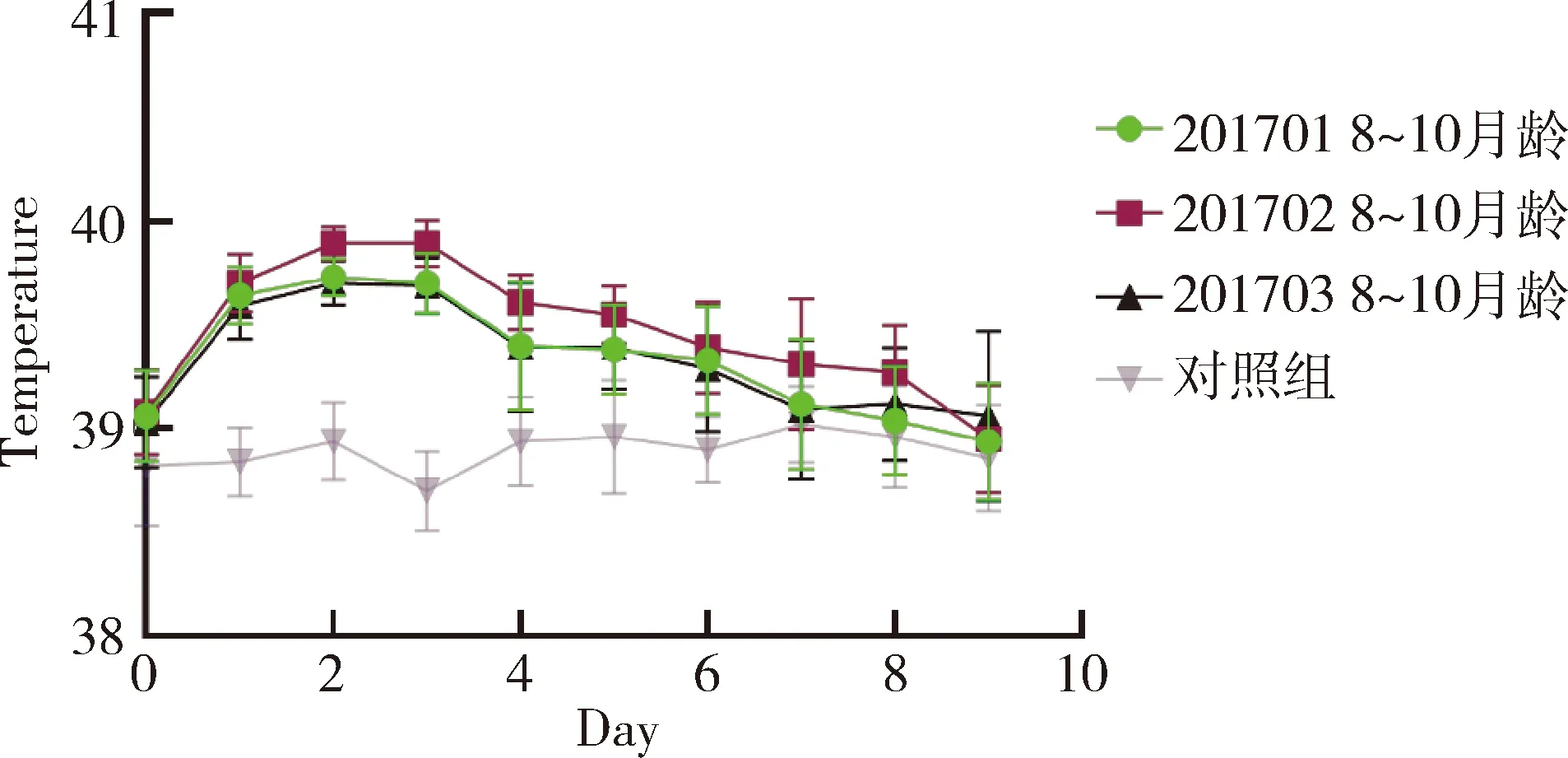
图2 疫苗对水貂一次单剂量接种后体温变化图(8~10月龄)Fig 2 The fluctuate curve of body temperature ofmink received one dose vaccine(8~10 month)
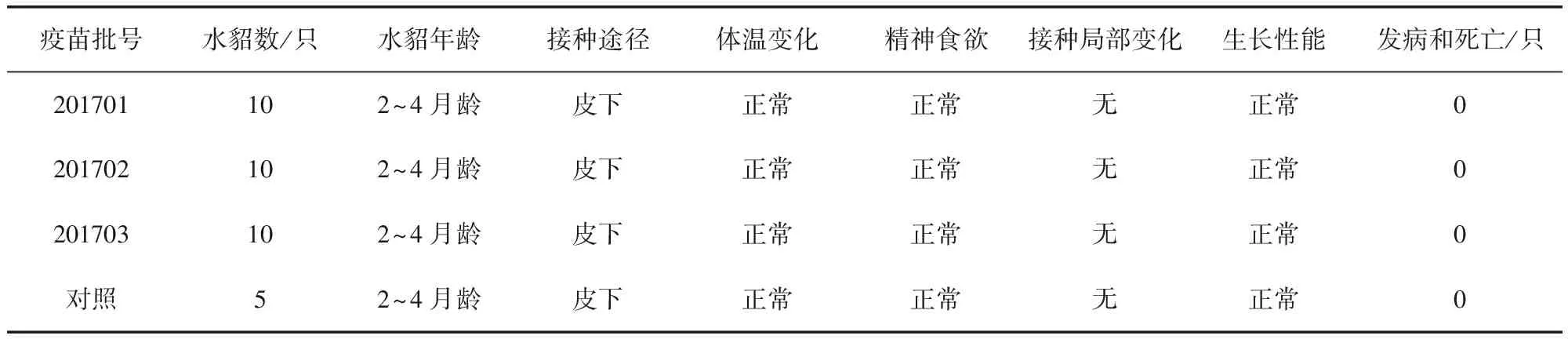
表2 疫苗对水貂一次单剂量接种安全性试验统计结果(2~4月龄)
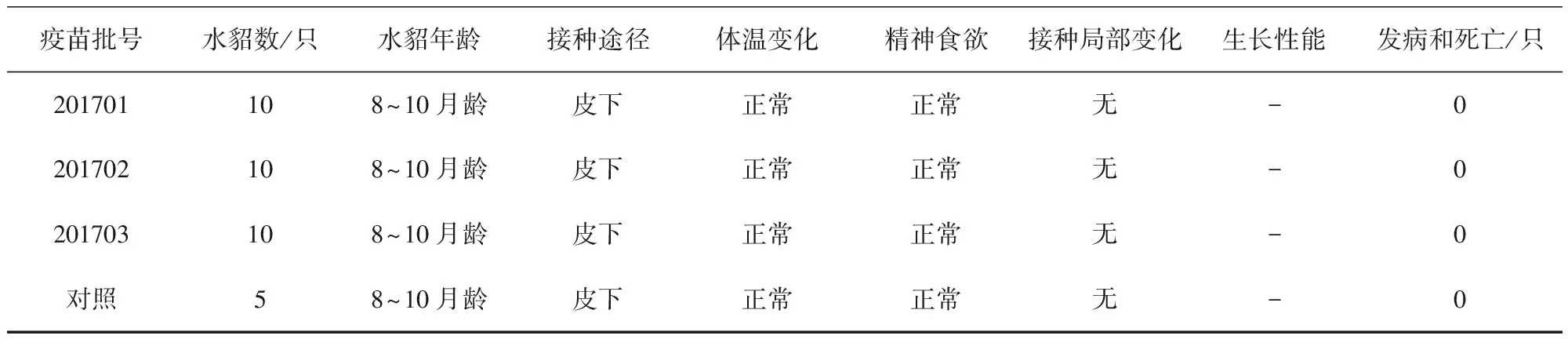
表3 疫苗对水貂一次单剂量接种安全性试验统计结果(8~10月龄)Tab 3 The security test record of one dose vaccine inoculation (8~10 month)
“-”代表水貂被打皮,未统计
2.3 单剂量重复皮下接种安全性试验结果 3批疫苗接种2~4月龄水貂幼崽,间隔14 d重复接种1次,通过14 d观察,接种水貂10 d内平均体温未超过40.5 ℃(图3);水貂食欲、粪便和精神状态均正常,接种局部无肿胀和炎症,未出现局部和全身反应(表4)。
2.4 超剂量皮下接种安全性试验结果 3批疫苗超剂量接种2~4月龄水貂幼崽,通过14 d观察,实验组水貂10 d内平均体温未超过40.5℃;3批疫苗接种后2~3 d内,水貂会出现体温短暂升高到40.5 ℃以上情况(图4);水貂粪便和精神正常,疫苗接种局部无肿胀和炎症,未出现局部和全身反应(表5)。
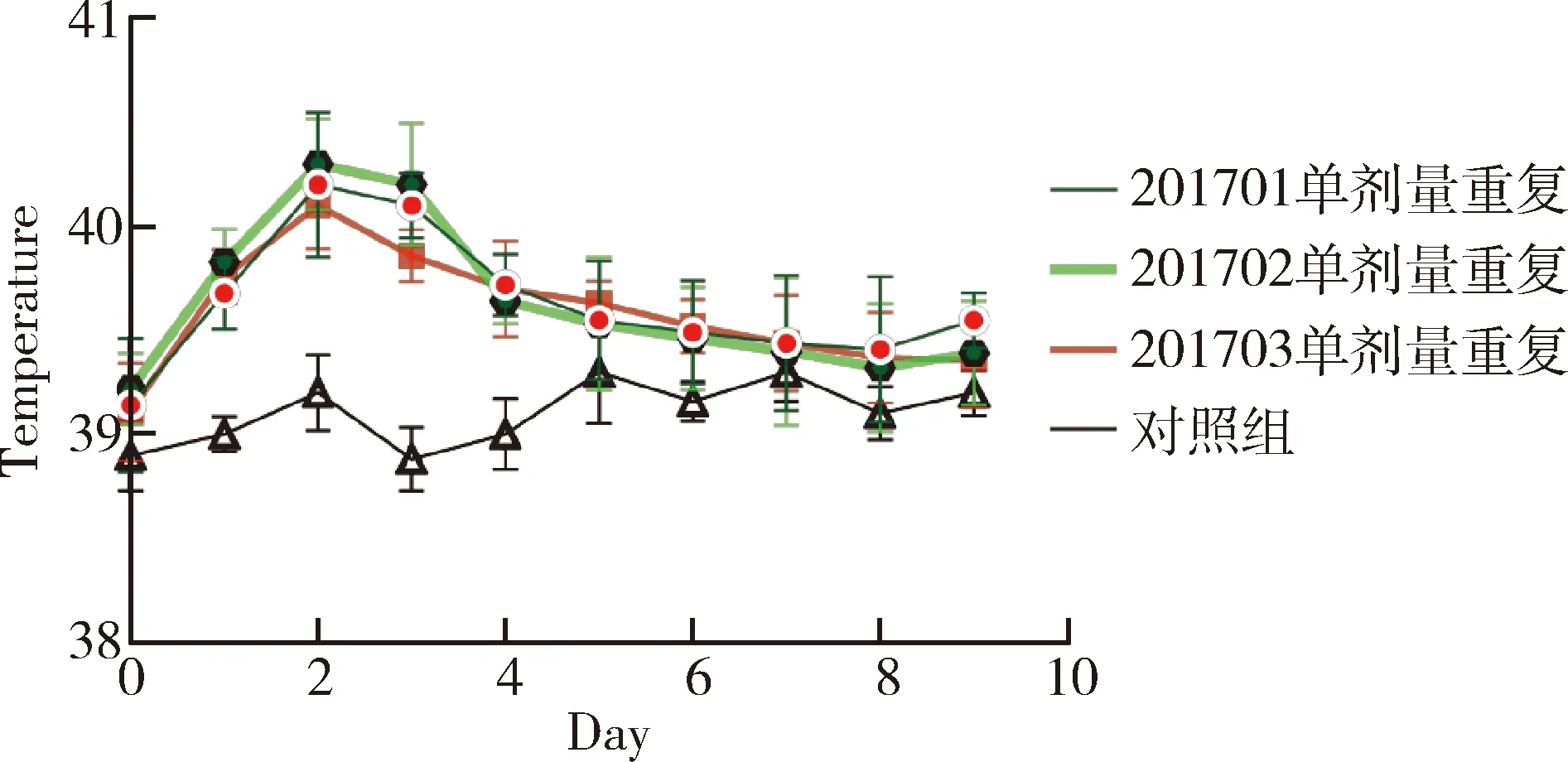
图3 疫苗单剂量重复接种水貂体温变化图Fig 3 The fluctuate curve of body temperature of minkreceived single dose repeat inoculation of vaccine
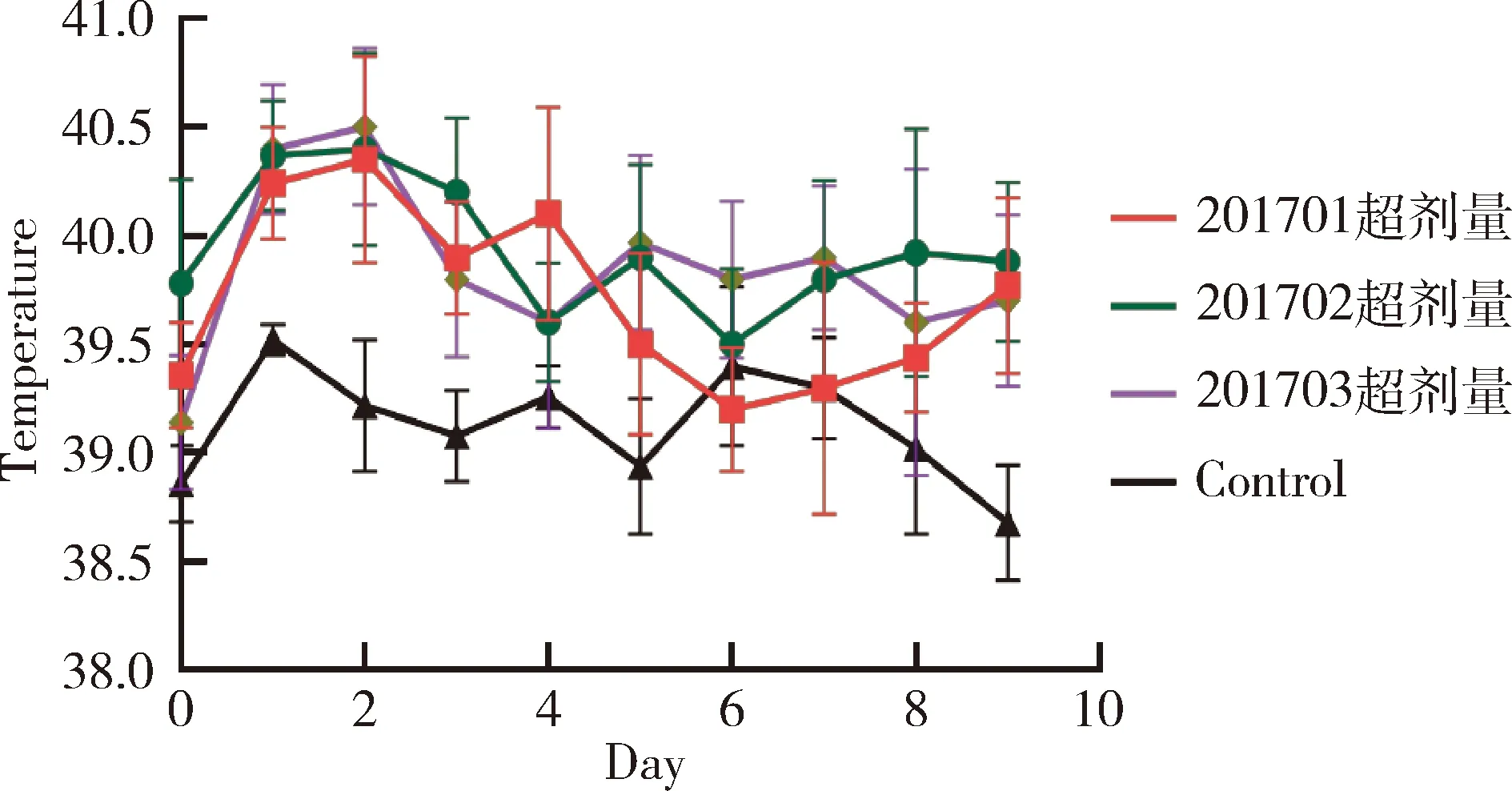
图4 疫苗超剂量接种水貂后体温测定结果Fig 4 The fluctuate curve of body temperature ofmink received overdose of vaccine

表4 疫苗单剂量重复接种安全性试验结果
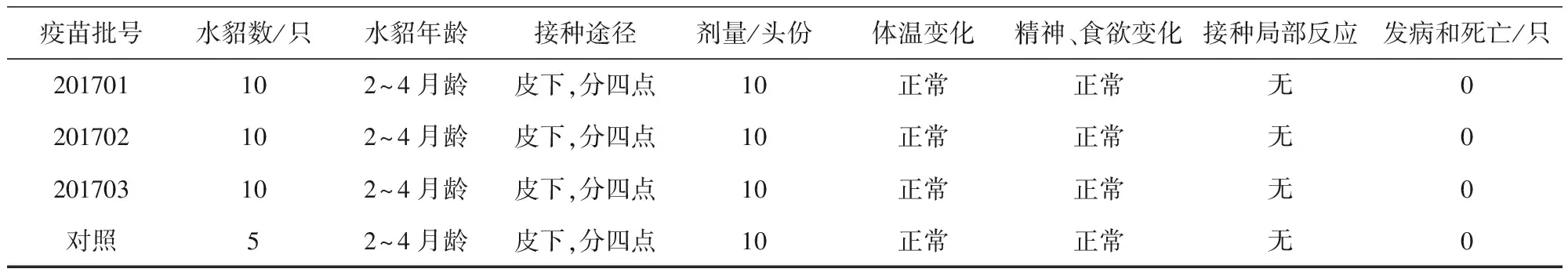
表5 疫苗超剂量接种水貂安全性试验结果
2.5 单剂量妊娠水貂安全性试验结果 3批试验疫苗皮下接种30~35日龄妊娠水貂,通过临床观察,接种水貂食欲、粪便和精神状态均正常,观察至产仔,未出现流产,产后胎儿发育未发现异常(表6),说明疫苗对妊娠水貂具有较好的安全性。
2.6 微载体安全性评价试验结果 微载体接种水貂幼崽(2~4月龄)后,接种10 d内各组水貂平均体温变化正常,与对照组没有显著区别(图5);水貂食欲、粪便及精神状态均正常,接种局部无肿胀和炎症,未出现局部和全身炎症反应(表7)。

表6 疫苗对妊娠水貂安全性试验结果Tab 6 The security test record of pregnancy mink received one dose of vaccine
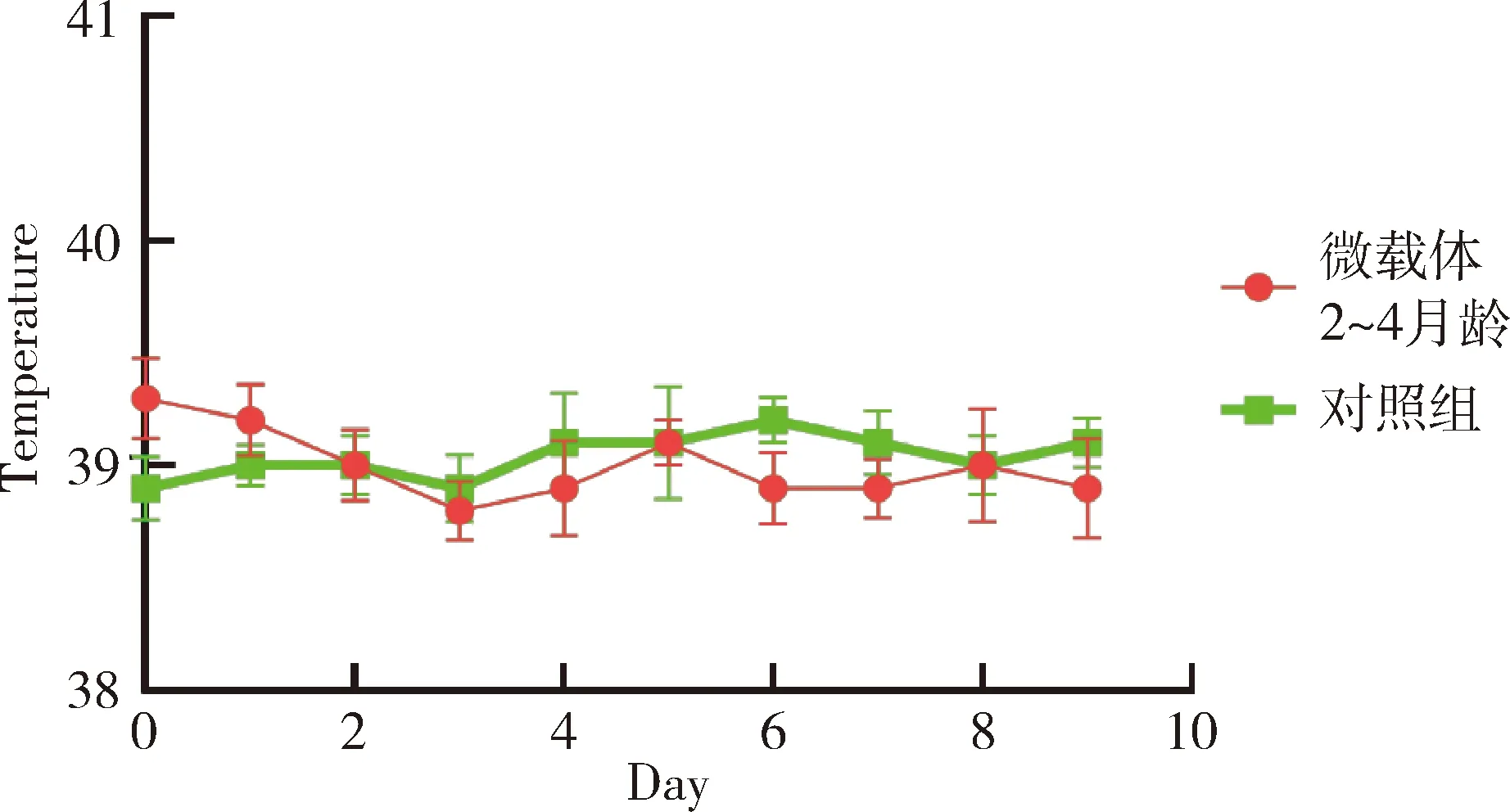
图5 微载体接种水貂后体温测定结果Fig 5 The fluctuate curve of body temperature of mink received of microcarrier
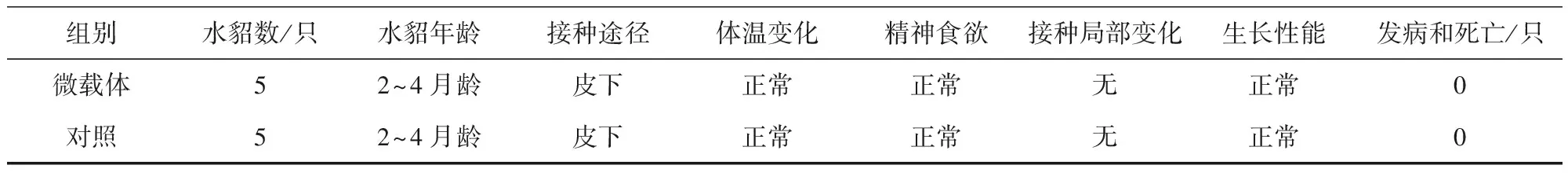
组别水貂数/只水貂年龄接种途径体温变化精神食欲接种局部变化生长性能发病和死亡/只微载体52~4月龄皮下正常正常无正常0对照52~4月龄皮下正常正常无正常0
2.7 疫苗接种部位组织病理切片观察 疫苗接种后,无论是对照组还是实验组,接种部位皮下均无异常变化,仅见颜色与周围皮肤略有不同,未见炎症反应。病理切片观察发现,接种部位的肌肉组织排列规整、肌纤维整齐、横纹肌明显,未见变性、坏死及炎性细胞浸润(图6)。
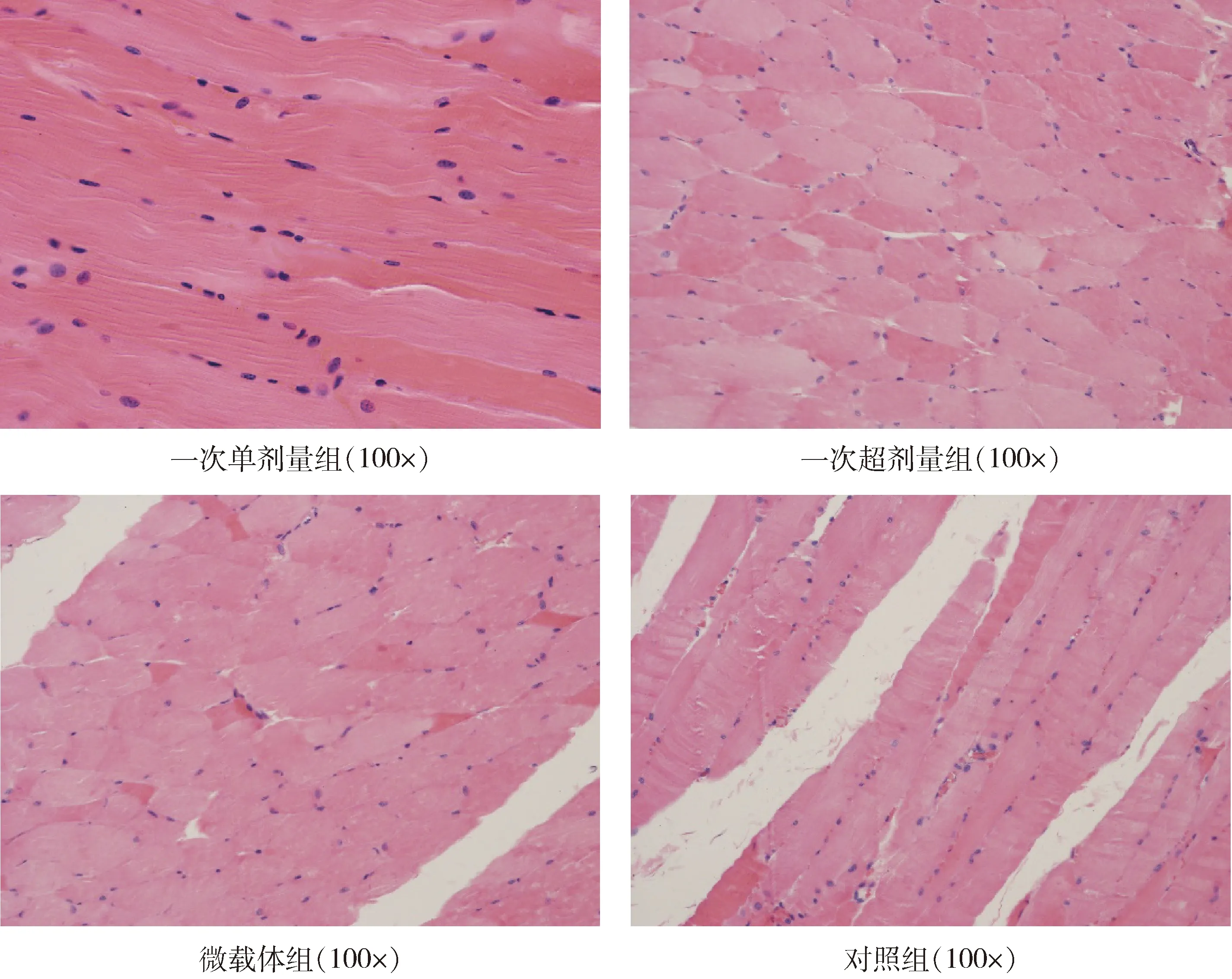
图6 接种部位组织病理切片观察Fig 6 The histopathology change of the inoculation site of mink
3 讨论与结论
无论是人用疫苗,还是兽用疫苗,安全和有效是其两大基本特性。因此,任何一个新疫苗在研发阶段或者推向市场之前,必须要开展疫苗的安全性评价。例如在我国发生小反刍兽疫(Peste destits ruminants virus,PRRV)疫情后,为了确保疫区外动物安全,我国批准利用PRR Nigerja 75/1疫苗株制造疫苗,并接种羊和豚鼠、小鼠进行了免疫接种,评价疫苗安全性[8-9]。崔艳丽等[10]在研制了鸡新城疫、传染性支气管炎、减蛋综合征、禽流感(H9亚型)四联灭活疫苗(LaSota株+HS25株+HZ株)后,也在本动物上开展了安全性评价。本研究为了尽快将利用悬浮培养工艺研制的水貂犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)推向市场,在本动物上(水貂)开展了疫苗的安全性评价。
根据农业部442号[11]公告中兽药变更注册事项及申报资料要求,改变兽药生产工艺,其生产工艺的改变不应导致药用物质基础的改变。因此需要对新工艺研发的疫苗临床试验。为了全面评价犬瘟热Vero细胞活疫苗(CDV3-CL株,悬浮培养)的安全性,参照农业部683号[12]公告中《兽用生物制品实验室安全试验技术指导原则》要求,本研究选择不同年龄的水貂(包括幼崽(2~4月龄)、育成水貂(8~10月龄)、妊娠水貂(30~35 d))进行安全性实验。实验分3组进行,每组10只水貂,采用单剂量(1头份)皮下接种、单剂量重复皮下接种(1头份)、超剂量(10头份)皮下接种动物进行安全性试验。结果表明,接种水貂全身和局部未见异常临床反应,对幼貂发育无不良影响,体温波动范围处于正常范围,说明疫苗具有较好的安全性。疫苗接种妊娠水貂未见有流产和死亡发生,进一步说明了疫苗的安全性。此外,为了验证培养介质(微载体)在动物体内的安全性,在单剂量安全性实验组中设置微载体安全性评价组,通过观察动物临床表现、监测体温变化,未发现异常,说明微载体对实验动物安全性无明显影响,这也是微载体悬浮培养技术被广泛应用于人和动物新工艺开发的重要原因[4,13-14]。
综上所述,基于悬浮工艺制备的水貂犬温热Vero细胞活疫苗(CDV3-CL株,悬浮培养)冻干品,具有很高的安全性,可以用于临床防治水貂犬瘟热疾病。
