原子荧光光谱法同时测定粮食中砷汞总量的条件选择及干扰控制
2019-08-30苏春燕汪海峰
姚 晶 任 蓉 樊 婷 苏春燕 汪海峰
(1 苏州市吴中区粮油质量监测中心,江苏 苏州 215156;2 南京财经大学食品科学与工程学院,南京 210003)
前言
目前,砷汞总量测定方法为现行国家标准方法GB 5009.17—2014和GB 5009.11—2014,均为原子荧光光谱法[1-2],其原理是在一级反应器中,被测金属元素与初生态氢H*反应生成气态的氢化物,在气液分离器内,气态氢化物逸出,在原子化器被检测器检测到产生信号[3],此方法操作简便、干扰少、检出限低、灵敏度高,已被广泛使用[4-6]。虽然仪器推荐的使用条件相似,但是,在实际测定过程中,针对不同的测定要求,应选择最适的工作条件,同时,还应充分考虑到干扰对仪器的稳定性和灵敏度的影响,特别是在检测过程中气相干扰和液相干扰因素带来的影响,而国内关于干扰因素的研究少有报道。因此,本文通过考察不同工作条件,对仪器工作条件进行优化,同时研究对仪器稳定性和灵敏度的影响,分析归纳相关规律,以期通过有效控制,获得更好的稳定性和灵敏度,保证测试结果的准确。
1 实验部分
1.1 仪器与试剂
6500型双通道原子荧光光度计(北京海光仪器有限公司),Topex微波消解平台(上海屹尧仪器科技发展有限公司),明澈超纯水机(美国默克密理博),FA2004电子天平(上海衡平仪器仪表厂),空调(广州美的集团),HTC-1型温湿度计(得力集团)。
盐酸(GR),硝酸(GR),氢氧化钾(GR),硼氢化钾(99%,天津南开允公合成技术有限公司)。
汞标准储备溶液(1 000 mg/mL,5%硝酸,GBW(E)083186)、BW30018-1000-N-50砷标准溶液(1 000 mg/mL,2%硝酸)均购自坛墨质检标准物质中心;高纯氩(ωAr≥99.99%,苏州金宏气体有限公司);其余试剂均为分析纯,所有试剂均现配现用,实验用水为二次去离子水。
检测样品为稻谷,由苏州市吴中区粮食购销总公司提供。
1.2 实验方法
1.2.1 检出限和重复性的测定

1.2.2 仪器条件的选择
分别考察原子荧光光谱仪的仪器条件原子化高度(8、9、10、11 mm),负高压(250、260、270、280、290、300 V),灯电流(As灯30、40、50、60、70 mA、Hg灯10、15、20、25、30 mA),载气流量(200、300、400、500、600 mL/min)等4个主要因素对仪器的影响,对同一标准溶液进行自动稀释,自动进样,延迟时间1 s,读数时间19 s,峰面积定量,稳定性和灵敏度测试方法同1.2.1,选择最佳仪器工作参数。
1.2.3 干扰因素的控制
环境温度干扰:在最佳的仪器工作条件下,考察不同环境温度对测定的影响。通过空调设定温度,以温度计数值为确定测试温度,待室温到达设定值后,恒温平衡30 min后开始测试,保持室温波动在设定值±0.5 ℃以内,依次设定不同温度(16、18、20、22、24、26 ℃)对稳定性和灵敏度的干扰,测试方法同1.2.1。
光源稳定性干扰:在最佳的仪器工作条件下,考察不同预热时间测定的影响,依次考察不同预热时间(10~50 min)对稳定性和灵敏度的干扰,测试方法同1.2.1。
试剂干扰:在最佳仪器工作条件下,相同环境最温度预热30 min后,依次考察5%(V/V)不同种类酸(HCl、HNO3、H2SO4、HAc)、不同浓度(V/V)酸(1%、3%、5%、7%、9%)、不同浓度KBH4(5、10、15、20、25、30 g/L)对稳定性和灵敏度的干扰,测试方法同1.2.1。
1.2.4 样品测试
样品经清理混匀后,经实验磨碎过筛后放入广口瓶备用。称取粉碎制样0.5 g(精确到0.001 g)至消解内管,加入5.0 mL硝酸后进行微波消解,微波消解条件为10 ℃/min升温至120 ℃,保温5 min;5 ℃/min升温至160 ℃,保持5 min;5 ℃/min升温至180 ℃,保持20 min,消解液冷却后加超纯水定容至10 mL,摇匀待测。加标试样在加入硝酸后加入一定体积标准溶液达到目标浓度,对样品按最佳仪器条件,控制干扰因素稳定情况下进行测定,同时做空白实验和平行实验,加标回收率实验的加标量如表1所示。

表1 加标回收实验的加标量
2 结果与讨论
2.1 仪器条件的选择
为了获得稳定可靠的测定结果,必须对仪器的测定条件进行优化选择。
2.1.1 原子化器高度
表2给出了不同的原子化器高度对测定元素的精密度和检出限的影响。
从表2数据可知,随着原子化器高度的增加,As的稳定性和灵敏度均渐下降,可知As的最佳原子化器高度为8 mm;Hg的稳定性先降后升,灵敏度均渐下降,当原子化器高度为10 mm时,Hg的稳定性和灵敏度最佳。在双通道同时测定时,仅可设置同一高度,因此,选择10 mm作为设定值,此时Hg已为最佳,As的稳定性和灵敏度较最佳时亦下降较小。
表2 原子化器高度的选择
Table 2 Selection of atomizer height
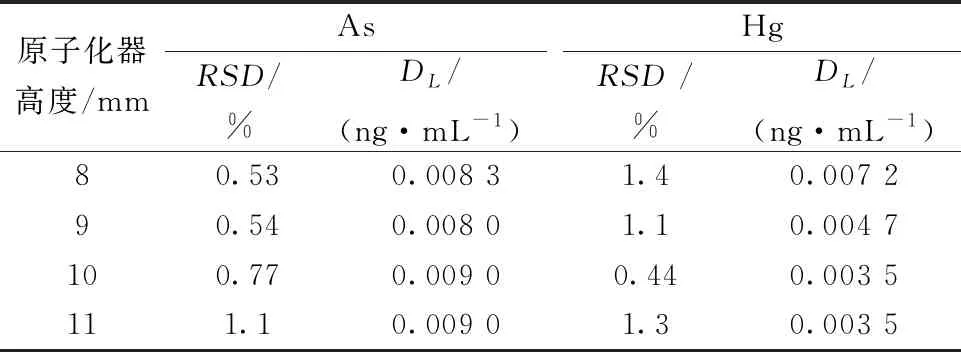
原子化器高度/mmAsRSD/%DL/(ng·mL-1)HgRSD /%DL/(ng·mL-1)80.530.008 31.40.007 290.540.008 01.10.004 7100.770.009 00.440.003 5111.10.009 01.30.003 5
2.1.2 负高压
负高压是施加在阳极和阴极间的电压,直接决定光电倍增管的放大倍数,负高压增大,灵敏度随之提高,但负高压增大的同时,信号噪声增大,稳定性降低,因此,测定时须选择最合适的负高压,见表3。
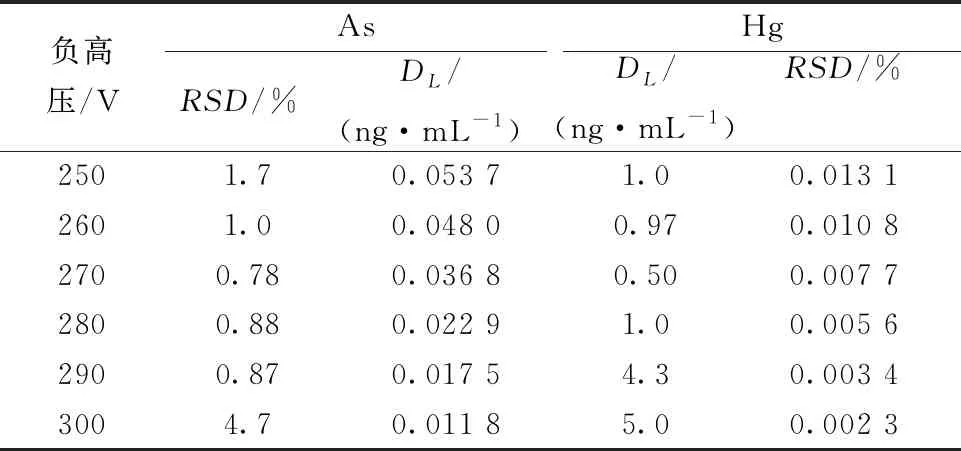
表3 负高压的选择
从表3可以得出,负高压由250至300 V时,As和Hg的稳定性均先升后降,灵敏度均随着电压增加,不断提高,每增加20 V,灵敏度约提高一倍。在双通道同时测定时,仅可设置同一负高压,实验选择270 V作为设定值,此时As、Hg稳定性均为最佳,灵敏度亦较好。
2.1.3 灯电流
灯电流在一定范围内与产生荧光强度存在线性关系,随着灯电流的增加,荧光强度逐渐增强,但电流增大,噪声增大,稳定性下降。因此要根据测定要求,选择合适的灯电流,见表4。
从表4可以得出,随着灯电流增大,As、Hg的检出限不断提高,但稳定性不断下降,当As灯电流60 mA,Hg灯电流15 mA时,灵敏度分别为0.010 9、0.002 6 ng/mL,已满足检测要求,且稳定性较好,灯电流继续提高,虽然灵敏度仍有所提高,但稳定性显著下降,在满足分析灵敏度的要求下,应尽量选择较小的灯电流作为工作电流,以延长灯的使用寿命,因此,As、Hg灯电流分别设置为60、15 mA。
2.1.4 载气流量
由于载气流量的大小直接影响Ar-H2火焰的形状、大小,对仪器的灵敏度和稳定性均有较大的影响,因此,在测定时应选择合适测定的载气流量,见表5。
从表5数据可知,载气从200 逐渐增大至600 mL/min时,稳定性和灵敏度均呈现先升后降的趋势,载气流量小时,火焰焰型圆矮,稳定性和灵敏度均较低,随着载气增大,火焰焰型逐渐变直变高,稳定性和灵敏度提高,在载气流速为300 mL/min,As、Hg的稳定性和灵敏度均为最佳,载气流量继续增大,稳定性和灵敏度又开始下降。

表4 灯电流的选择

表5 载气流量的选择
2.2 干扰因素的控制
2.2.1 环境温度的干扰控制
根据原子荧光光谱仪工作原理可知,环境温度在测定过程中,主要影响氢化物的发生效率,氢化物的逸出、传输及其热稳定性,会同时引起液相干扰和气相干扰,因此,测定时应对环境温度要严格控制,避免引起干扰,见表6。

表6 环境温度的干扰
从表6可知,当环境温度低于20 ℃时,反应不充分,氢化物发生效率偏低,稳定性较差,灵敏度不高,线性达不到测定要求;当环境温度达到20 ℃以上时,稳定性、灵敏度较好,且线性符合测定要求;当环境温度达到26 ℃时,空白荧光强度增高,噪声增大,灵敏度和标准曲线线性较好,但稳定性已有所下降,虽然目前国内仪器标识的工作环境温度范围较宽,在实际测定中,应控制在20~25 ℃为宜。
2.2.2 光源稳定性
光源的稳定性对原子荧光光谱会产生一定影响,这是原子光度光谱仪的光学结构所决定的,由于国产的仪器光路系统是无色散系统,一般采用日盲光电倍增管检测荧光信号,当光源不够稳定,荧光信号比发射和吸收信号更弱,此时检测器则容易受到散射光的干扰,因此,可通过提前预热,使工作灯稳定来避免干扰,见表7。

表7 光源稳定性的干扰
从表7可知,当预热时间不足时,稳定性较差,灵敏度不高,线性系数低,仪器达不到测定要求,经过30 min预热后,各项指标均得到了明显的改善,此时,稳定性、灵敏度、线性相关系数均较好,符合测定要求。因此,在操作时,为了保证光源稳定性,至少使仪器稳定30 min再开始测定,可以有效避免光源不稳定带来的干扰。
2.2.3 试剂的干扰
酸和硼氢化钾是反应体系重要的试剂,不同的试剂在反应过程中会影响还原态氢的生成速率、氢化物的逸出等,易造成气相干扰和液相干扰,因此,根据测定元素,应选择合适的试剂,并确定最佳的反应浓度。
2.2.3.1 酸种类的选择
不同酸种类对测定的影响见表8。
表8 酸种类的干扰
Table 8 Disturbance of acid types
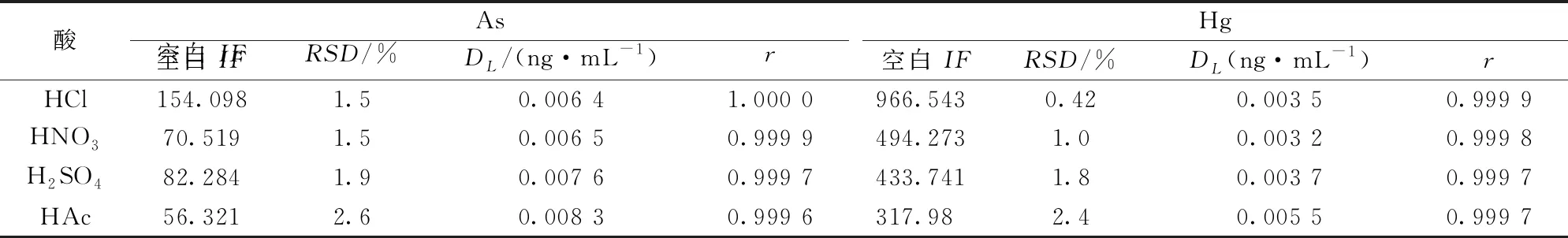
酸As空白 IFRSD/%DL/(ng·mL-1)r空白 IFHg空白 IFRSD/%DL(ng·mL-1)rHCl154.0981.50.006 41.000 0966.5430.420.003 50.999 9HNO370.5191.50.006 50.999 9494.2731.00.003 20.999 8H2SO482.2841.90.007 60.999 7433.7411.80.003 70.999 7HAc56.3212.60.008 30.999 6317.982.40.005 50.999 7

2.2.3.2 HCl浓度的选择
不同HCl浓度对测定的影响见表9。

表9 HCl浓度的干扰
从表9可知,不同HCl浓度对As、Hg测定的干扰不同。随着HCl浓度的增加,测As时,空白荧光强度、RSD、DL和线性相关系数r逐渐提高,在浓度达到5%(V/V)时开始趋于稳定;而测Hg时,各项指标并未有较大波动,可见HCl浓度变化对测Hg带来的干扰不大。因此,在反应时,浓度应不低于5%(V/V)的HCl浓度,此时As、Hg的稳定性、灵敏度和线性相关系数都较好,特别是当反应体系中存在过渡金属元素干扰时,可选用较高的酸浓度,以克服液相干扰。
2.2.3.3 KBH4浓度选择
不同浓度KBH4对测定的影响见表10。

表10 KBH4浓度的干扰
从表10可知,还原剂KBH4浓度对As的影响较Hg的影响大,当KBH4浓度为5.0 g/L时,As的稳定性、灵敏度和线性相关系数均无法测得,但Hg已可以稳定测得,且满足测定要求,随着KBH4浓度的增大至15~20 g/L范围内时,As、Hg的稳定性、灵敏度和线性相关系数为最佳,当还原剂浓度继续增大,灵敏度较为稳定,但稳定性和线性系数开始下降。还原剂的作用是与酸反应后提供初生态的H*和被测元素形成金属氢化物,还原剂的浓度过大会带来液相干扰,容易引起过渡元素的干扰,同时还原剂浓度过高,生成的大量氢,荧光强度变幅增大,导致稳定性下降,灵敏度变差,因此,还原剂KBH4浓度较低为宜,应控制在15~20 g /L。
2.3 样品精密度和加标回收实验
国家标准[7]中规定,双道仪器的线性相关系数不小于0.997,As、Hg的重复性指标小于2%,检出限分别为0.06、0.005 ng/mL[4],稻谷样品在最佳仪器条件、控制干扰因素稳定情况下进行测定,As的浓度为0.20 ng/mL,检出限为0.004 7 ng/mL,RSD为0.37%,线性相关系数r=0.999 9;Hg的浓度为0.023 ng/mL,检出限为0.001 5 ng/mL,RSD为0.44%,线性回归系数r=0.999 9,各项指标均优于标准规定,见表11。
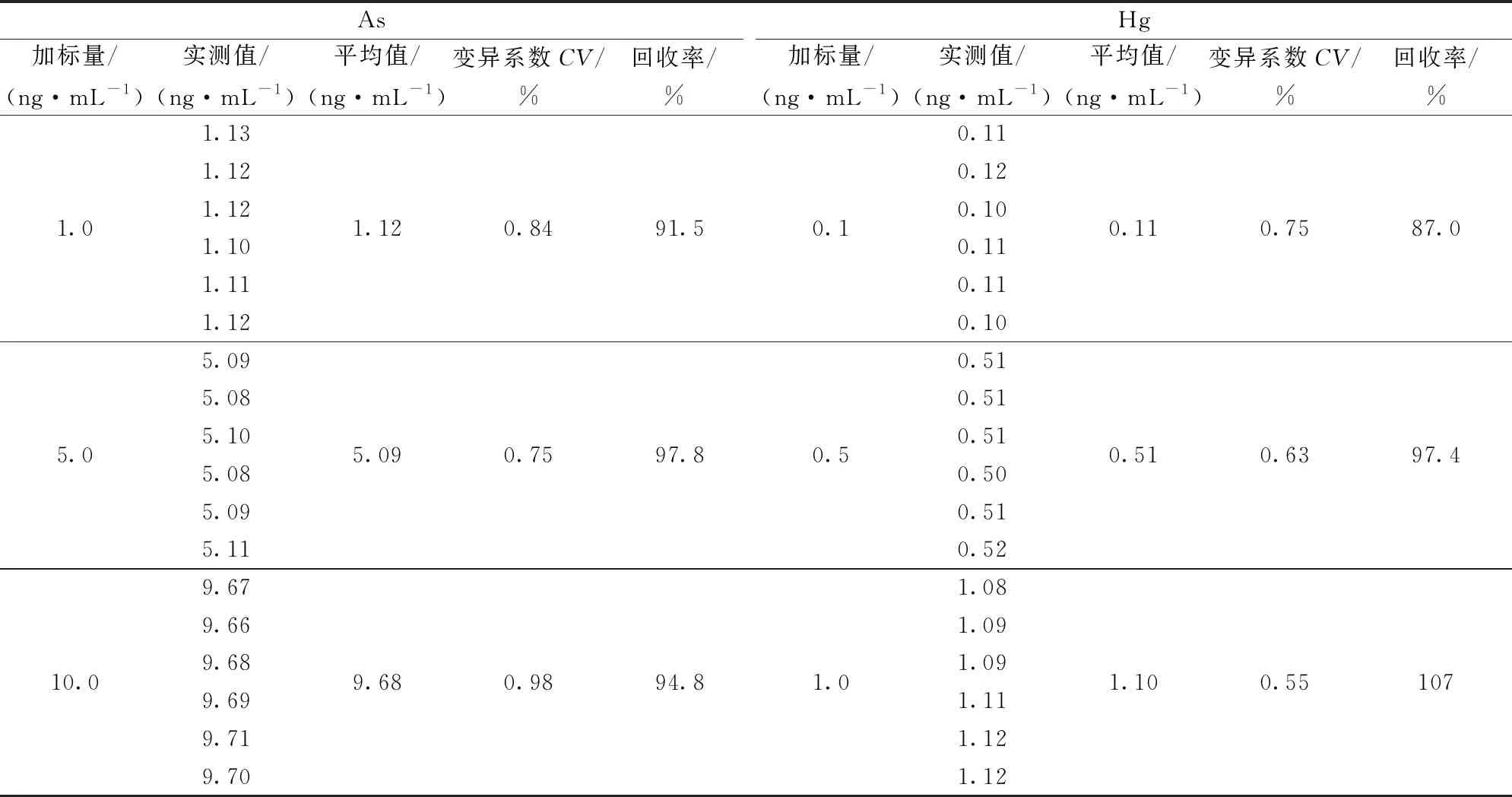
表11 精密度和加标回收实验结果
粮食中As、Hg的测定,属于痕量分析,一般情况下被测物质含量小于0.1 μg/kg,国家标准[8]规定,变异系数应小于43%,加标回收率范围满足60%~120%,如表11显示,三组实验的变异系数均小于1.00%,满足标准要求。As加标回收率为95%~105%,Hg的回收率为80%~110%,均高于标准规定。
3 结论
通过考察主要工作条件对仪器稳定性和灵敏度的影响,研究分析归纳相关规律,并进行了优化,得出最佳工作条件为:原子化高度10 mm,负高压270 V、As灯电流60 mA、Hg灯电流15 mA、载气流量300 mL/min。在此基础上对产生干扰因素进行了研究,研究结果表明:环境温度应控制在20~25 ℃、至少预热30 min、首选HCl作为反应用酸,浓度应不低于5%(V/V),还原剂浓度应控制在15~20 g/L,可获得更好的仪器测试效果;最后进行了三水平加标回收实验,结果显示,仪器经条件优化后,干扰因素在有效控制下,As的浓度为0.20 ng/mL,检出限为0.024 7 ng/mL,RSD为0.37%,线性相关系数r=0.999 9;Hg的浓度为0.023 ng/mL,检出限为0.001 5 ng/mL,RSD为0.44%,线性相关系数r=0.999 9,且稳定性好,灵敏度高,各项指标均优于标准规定。
