D301G大孔树脂吸附菊芋多糖色素机理探究
2019-08-28马海乐朱莉萍
陆 敏,马海乐,朱莉萍,洪 晨
(江苏大学食品与生物工程学院,江苏镇江 212013)
菊芋属于草本植物,又称鬼子姜、洋姜、五星草等[1],生长环境比较恶劣,全国各地都可以种植,联合国粮农组织称菊芋为“21世纪人畜共用作物”[2]。菊芋块茎含有丰富的多糖,其含量为菊芋湿重的15%~18%,干重的55%~80%左右,又称为菊糖或菊粉[3]。
菊芋多糖是由若干个D-果糖连接组成的链状多糖,末端常含有一个α-D-葡萄糖基[4]。其生理功能在西方国家被广为研究,它能够促进人体肠道益生菌的增长,稳定血脂、血糖含量,促进体内矿物元素的吸收[5-8]。日本、韩国、欧美等国家对菊芋多糖的研究、开发和应用已居于世界领先水平[9]。在早餐谷物、饮料、乳制品、烘培品和肉制品等产品中,菊芋多糖已是关键性配料,它不仅可以作为脂肪替代品,改善食品质构和风味,而且还能提供一定的营养物质[10],已被广泛应用于食品工业中。
我国菊芋多糖产业发展较晚,工艺水平不完善,产品质量落后,特别是菊芋多糖的色值和纯度无法达到高品质菊芋多糖的质量要求。脱色在菊芋多糖加工生产过程约占总成本的1/3,所以脱色过程的系统研究,对菊芋多糖的生产具有很大的应用价值[11]。目前常用的脱色方法有活性炭法、过氧化氢法、膜分离技术法、离子树脂法等。活性炭虽然使用方便、设备简单、吸附能力强,但是特异性较差,脱色的同时会吸附一定多糖[12];过氧化氢具有氧化性,会破坏多糖的生物活性[13];膜分离法对低分子量的有色物和无机物的去除率不高[14]。大孔树脂吸附量大、再生能力强、稳定性强、成本低、操作简单,而且菊芋多糖中色素分子呈电离状态,带负电荷,可与阴离子树脂发生交换,因此树脂应用于菊芋多糖的纯化过程得到越来越多的关注和重视[15-16]。但是目前的文献中较多地研究树脂对多糖的脱色工艺,关于吸附机理的研究较少。
本文选用6种对菊芋多糖色素吸附效果较好的大孔树脂,在相同条件下进行脱色比较,筛选出最好的树脂。并从热力学和动力学两方面研究筛选出的树脂对菊芋多糖色素的吸附机理,为菊芋多糖脱色过程提供一定的理论依据。
1 材料与方法
1.1 材料与仪器
菊芋干片 江苏徐州康芝源有限公司;S-8、D311、D280大孔树脂 河南郑州华溢新材料有限公司;D201大孔树脂 河北沧州宝恩化工有限公司;D296R、D301-G大孔树脂 天津南开合成有限科技公司;几种树脂的基本性质见表1。

表1 几种大孔树脂的基本性质
BS124S型电子天平 赛多利斯科学仪器有限公司;五频柱状逆流发散式超声设备 江苏大学食品与生物工程学院自主研发;T6新世纪紫外可见分光光度计 北京普析通用仪器有限责任公司;IS-RDD3台式恒温振荡器 上海珂淮仪器有限公司;HHS数显恒温水浴锅 江苏省金坛市医疗仪器厂;pHS-25型数显示pH计 上海精密科学仪器有限公司。
1.2 实验方法
1.2.1 菊芋多糖溶液的制备 菊芋干片烘干,粉碎并过60目筛。在超声工作模式为28/35 kHz,功率密度110 W/L、料液比1∶15 (m/v)、时间20 min和温度55 ℃下进行超声,然后4000 r/min离心20 min后过滤。过滤液放入60 ℃水浴锅加热15 min,加石灰乳调节过滤液的pH至11,再水浴20 min,经4000 r/min离心10 min去杂。再加入浓磷酸,调节pH至6,80 ℃水浴20 min,4000 r/min离心20 min去杂,得到菊芋多糖溶液(此时菊芋多糖含量43.45 mg/mL)。
1.2.2 菊芋多糖脱色率及保留率的测定
1.2.2.1 测定波长的确定 由于提取液中色素的成份较复杂,难以确定色素的种类,可以选择在可见光区的某一个波长的脱色率来表达总体的脱色率。本研究中选择波长380、400、420、450和500 nm,分别测定多糖溶液脱色前后的吸光度,确定测定波长。
1.2.2.2 脱色率的计算 在420 nm处测定溶液脱色前后的吸光度,并计算脱色率[17]。

式(1)
1.2.2.3 多糖保留率的计算 总糖含量测定采用苯酚硫酸法[18];还原糖含量的测定采用3,5-二硝基水杨酸法(DNS)法[19]。
菊芋多糖含量(mg/mL)=总糖含量-还原糖含量
式(2)
式(3)
式中:M0,M1分别是菊芋多糖溶液脱色前和脱色后的菊芋多糖含量,mg/mL。
1.2.3 六种树脂的筛选 取已滤干的S-8、D311、D280、D201、D296R、D301-G六种大孔树脂10 g,分别倒入实验室制备的菊芋多糖溶液100 mL,在恒温振荡器下以170 r/min振荡,在第2、6、12、20、30、45、65、95、135、185、245 min时各取样一次,测定并计算脱色率,第245 min时脱色液的多糖保留率,筛选出最优树脂进行后续机理探究实验[20]。
1.2.4 菊芋多糖色素的静态吸附动力学 在三角瓶中称量已经滤干的D301-G树脂4 g,倒入实验室制备的菊芋多糖溶液50 mL,293、303、313 K下以170 r/min振荡2 h,分别在第5、10、20、30、50、70、100和130 min时各取样一次,测定并计算脱色率,按公式4计算吸附量[21]。
式(4)
式中:Qt为时间t时树脂的色素吸附量,1/g树脂;A0和A分别为脱色前后溶液在420 nm吸光度;m树脂的质量,g。
1.2.5 菊芋多糖色素吸附等温线的绘制及热力学参数的计算 在三角瓶中称量已经滤干的D301-G树脂2、3、4、5、6、7 g,分别倒入实验室制备的菊芋多糖溶液50 mL,分别在293、303、313 K温度下以170 r/min振荡2 h,定性滤纸过滤,绘制吸附等温线并计算热力学参数。
1.3 数据处理
数据处理采用Excel 2013、Origin 8.0进行绘图和拟合,SPSS 19.0进行显著性分析。
2 结果与分析
2.1 脱色率检测波长的确定
由表2可知,在380、400、420、450和500 nm下所测得的脱色率的标准偏差小于2%,可认为5个波长下所测的脱色率无显著性差异。因此,本实验中以脱色率接近平均脱色率的420 nm波长为代表,测定菊芋多糖溶液脱色前后的吸光度,并计算脱色率。

表2 5种不同波长下菊芋多糖溶液的脱色率
2.2 树脂的筛选
从图1可以看出,六种树脂对菊芋多糖的脱色率相差较大,D301-G大孔树脂脱色率最高达79.63%,S-8大孔树脂最低只有29.02%。不同的树脂,在2 min时脱色率差别显著,可能原因是不同树脂的功能基、树脂的加工工艺不同。D311、D201、D301-G树脂在245 min之后脱色率达到75%以上,明显比其它三种树脂效果好。D301-G树脂在45 min时对色素的吸附已达到了69.34%,与其它树脂相比,吸附速率快,可以短时间对色素进行吸附。而S-8大孔吸附树脂对菊芋多糖色素吸附能力最差,在吸附245 min时才达到了29.02%。这与李焕东[16]的研究结果一致。可能是因为菊芋多糖溶液中的色素主要以阴离子、非极性色素分子为主,所以大孔阴离子树脂对菊芋多糖脱色效果较好。
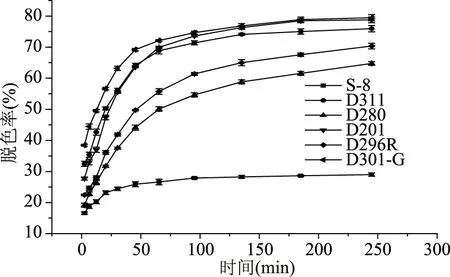
图1 树脂脱色动力学曲线
由图2可见,树脂对菊芋多糖有一定程度的吸附。D301-G树脂对菊芋多糖的保留率最高,为92.28%,其次是D311和D201树脂,对菊芋多糖保留率分别为89.12%、89.60%,三者之间无显著性差异(p>0.05),但都显著高于D296R树脂对菊芋多糖的保留率83.49%(p<0.05)。D280树脂对菊芋多糖的保留率为82.25%,与D296R树脂相比无显著性差异(p>0.05)。而S-8树脂对菊芋多糖的保留率最低,为79.22%,显著低于其他树脂(p<0.05)。

图2 树脂对菊芋多糖保留率的影响(245 min)
不同的树脂对菊芋多糖溶液色素的脱色率和多糖保留率都不相同,这可能与树脂的表面特性、菊芋多糖溶液色素的复杂性以及其它成分的竞争吸附有关[22]。综上考虑,选择对菊芋多糖脱色效果最好、多糖保留率最高的D301-G大孔阴离子树脂。
2.3 D301-G大孔树脂对菊芋多糖色素的静态吸附动力学
2.3.1 吸附动力学曲线 从图3中可以看出,吸附反应开始后,在最初20 min菊芋多糖色素被快速地吸附在D301-G树脂上,此阶段推动力可能主要是由于固液两相中吸附质的浓度差以及吸附剂表面大量空余的吸附位点;20~70 min为慢速吸附阶段,此阶段固液两相中吸附质的浓度差逐渐缩小,吸附剂表面的吸附位点趋于饱和;70~130 min 为吸附平衡阶段,瞬时吸附速率(dQt/dt)逐渐减小到零。
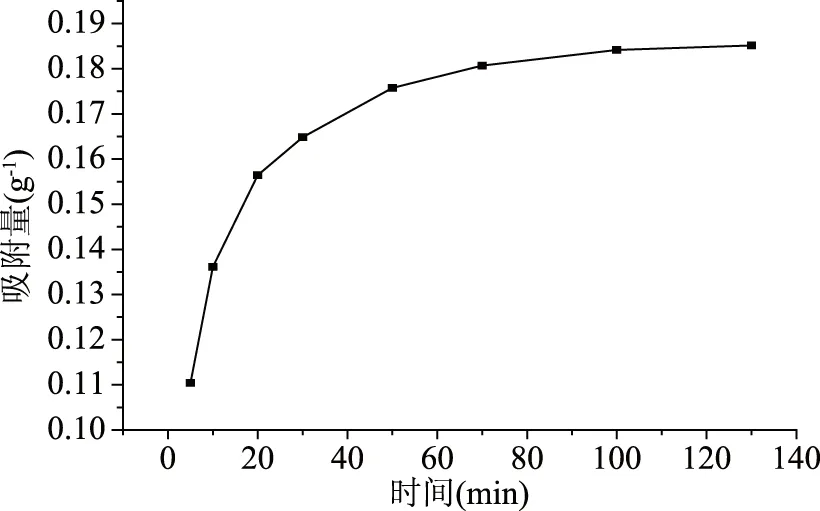
图3 菊芋多糖色素在D301-G树脂上的吸附动力学曲线
2.3.2 吸附动力学特性 吸附速率可体现固-液界面上吸附质的滞留时间,能够控制影响静态吸附的外界因素,保证D301-G大孔树脂对菊芋多糖色素吸附的可重现性。通过对动力学模型进行拟合,可发现吸附剂吸附溶质的变化特征,从而对后续吸附行为具有一定指导和预测作用。常用准一级动力学方程、准二级动力学方程来描述吸附过程。
准一级动力学方程由Lagergren和Svenska提出[23],其方程可表示为:
式(5)
式中:K1为准一级吸附速率常数,min-1;Qt为单位树脂在t时刻的吸附量,g-1;Qe为单位树脂的饱和吸附量,即130 min时的吸附量,g-1。
准二级动力学方程由McKay提出[24],其方程可表示为:
式(6)
式中:K2为准二级吸附速率常数(min-1)。
以时间t横坐标,分别以lg(Qe-Qt)、t/Qt为纵坐标绘制准一级动力学曲线、准二级动力学曲线,得到2条直线,经线性回归得动力学参数如表3所示。

表3 D301-G树脂对菊芋多糖色素的吸附动力学模型的拟合
从表3可以得出,准二级动力学模型的相关系数达到了0.9998,能更好地描述其吸附过程,这表明吸附过程中吸附质的吸附速率与溶液中吸附质含量的二次方成正比,可能通过共用电子或者交换电子完成[25]。
2.3.3 吸附控制机制的分析 通常脱色吸附过程由四个连续的过程组成。色素分子向大孔树脂的扩散,即外扩散;色素分子向大孔树脂表面的液膜中进行扩散,即膜扩散;色素分子在大孔树脂内部孔径中进行扩散,即颗粒内扩散;色素分子到达大孔树脂内部与其内部活性基发生化学反应,最终达到离子交换的目的,其中速度最慢的一步是离子交换过程的速度控制步骤[26-27]。所以认为D301-G树脂吸附色素由液膜扩散,颗粒扩散和化学反应组成。式7~9即分别为液膜扩散、颗粒扩散和化学反应的控制方程[28]:
F=kt
式(7)
3-3(1-F)2/3-2F=kt
式(8)
1-(1-F)1/3=kt
式(9)
式中:F=Qt/Qe,k为扩散系数。
以时间为t横坐标,分别以F、3-3(1-F)2/3-2F、1-(1-F)1/3为纵坐标绘制液膜扩散,颗粒扩散和化学反应动力学曲线,得到3条直线,经线性回归动力学参数如表4所示。

表4 D301-G树脂对菊芋多糖色素粒子扩散模型拟合方程及相关系数
由表4可知,颗粒扩散和化学反应的控制方程线性拟合的决定系数R2>0.94,可以分析得出D301-G大孔树脂吸附色素可能主要受两种模型的共同控制。但是溶液离子与树脂的化学反应速率很快,不能作为吸附速率控制的关键过程[29]。因此树脂颗粒扩散过程是D301-G树脂吸附色素的关键控速步骤,厂家可以通过改变D301-G树脂颗粒孔径的大小改善脱色性能。
2.4 D301-G大孔树脂对菊芋多糖的静态吸附等温线
固液吸附是发生在固液两相界面上的表面效应。当吸附达到表观平衡时,吸附与解吸速率相等。在温度不变条件下,吸附量只和浓度相关,q=f(c),该函数关系称为吸附等温线。本文研究中,ce代表(A/A0),qe代表{(A0-A)/A0}/m,其中A0是菊芋多糖原液的色值,A是某时刻脱色后的色值,m是树脂的用量[30]。利用两个常用的模型,Freundlich模型和Langmuir模型,分析树脂的吸附能力[31]。
Langmuir模型是基于“吸附剂的表面只能发生单分子层吸附”的假设而提出,Freundlich模型基于“非均一吸附的基础,吸附剂表面的活性化学能分布不均匀”而提出[32]。
Langmuir吸附模型:
式(10)
Freundlich吸附模型:
qe=KFce
式(11)
其线性化形式为;
式(12)
式中,qe为单位树脂的平衡吸附量,g-1;qm为最大吸附量,g-1;KL为吸附平衡时的解离常数;ce为吸附质的平衡浓度;KF为平衡吸附系数;n为特征常数,表明吸附剂表面的不均匀性和吸附强度的相对大小。
用线性拟合来描述不同温度条件下不同质量浓度吸附质和吸附剂的吸附平衡关系。以ce为横坐标,ce/qe为纵坐标对Langmuir方程进行线性拟合。同时,以lgce为横坐标,lgqe为纵坐标对Freundlich方程进行线性拟合。不同模型拟合的相关系数列于表5和表6。

表5 Langmuir方程对色素在D301-G树脂上吸附等温线的拟合结果

表6 Freundlich方程对色素在D301-G树脂上吸附等温线的拟合结果
293、303、31 3K条件下D301-G树脂对菊芋多糖溶液色素的吸附等温线见图4。从图4可以看出,提高温度,D301-G大孔树脂对菊芋多糖色素的平衡吸附量呈增加的趋势。等温线为上凸曲线,表明吸附剂在较低溶质浓度的液相中可吸附富集到较高浓度的溶质。

图4 不同温度下D301-G树脂对菊芋多糖色素吸附等温线
由表5、表6可以看出,在所研究的浓度和温度范围内,Freundlich 方程能很好地描述 D301-G树脂对菊芋多糖色素的吸附等温线,R2均大于 0.99。从 Freundlich 模型给出的参数KF、n可知,在293~313 K时,KF随着温度的升高而增大,表明温度升高D301-G树脂对色素的吸附能力和结合能力增大。这可能是由于温度升高使吸附质能够达到能量较高的吸附位点。特征常数n大于1,表明为优惠吸附,吸附比较容易的进行[33]。
2.5 D301-G大孔树脂对菊芋多糖色素的吸附热力学
吸附量为定值时,热力学参数吸附焓变ΔH根据范托夫定律计算[34]:
式(13)
式中:ce1是在绝对温度时,特定吸附量qe1下溶质的平衡浓度,本文考察三种平衡吸附量(qe1=0.1、0.2和0.3),ce1由Freundlich等温方程计算得出;R是气体常数(8.314 J/mol·K);K为常数。
吸附自由能变ΔG通过Gibbs方程计算[35]:
式(14)
式中:X代表平衡溶液中吸附质的摩尔分数,Q为吸附量。若吸附等温线符合Freundlich等温线,当吸附质浓度较低时,得到吸附自由能变与Q无关。
ΔG=-nRT
式(15)
吸附熵变ΔS通过Gibbs-Helmholtz方程计算[36]:
ΔS=(ΔH-ΔG)/T
式(16)
表7为D301-G树脂对菊芋多糖溶液色素的吸附热力学结果。0<|ΔH|<40 kJ·mol-1,表明吸附过程吸热过程,在研究的温度范围内升温是有利于菊芋多糖色素吸附。同时吸附焓随着吸附量的增加逐渐降低,这可能与已吸附分子偶极矩的存在以及树脂表面吸附中心的能量不同有关。一般来说,吸附焓的大小取决于溶质吸附热和溶剂脱附热之间的差值[37]。ΔG<0,表明吸附是可以自发进行,绝对值越大吸附过程的自发趋势也越大。ΔS>0,说明吸附是熵增过程。在树脂吸附色素过程中,色素被吸附到树脂表明时丧失自由度是熵减少的过程,但是色素的吸附会导致树脂上的其它吸附质和水分子解析(水分子脱附是熵增过程),整个吸附过程是总熵变增大的过程。
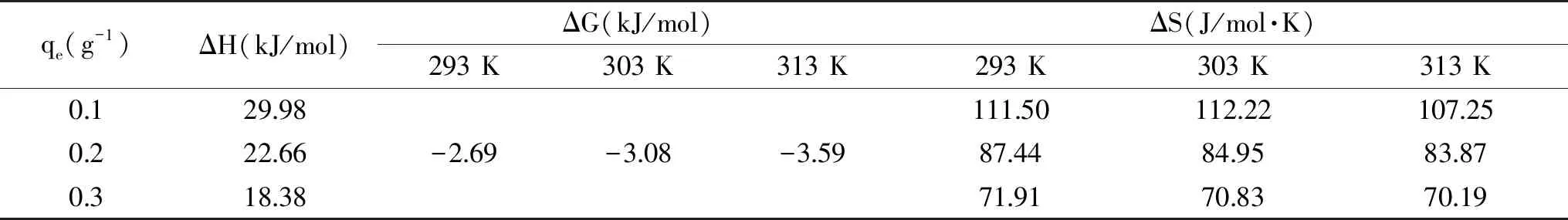
表7 D301-G树脂对菊芋多糖溶液色素的吸附热力学性质
3 结论
D301-G树脂对菊芋多糖溶液脱色效果最好,脱色率为79.63%,多糖的保留率为92.28%。D301-G大孔树脂吸附菊芋多糖时吸附动力学符合准二级动力学方程,而且颗粒扩散是控制吸附速率的主要步骤。另外在293~313 K期间吸附等温线更符合Freundlich模型,吸附过程可能为多分子层。吸附过程焓变为正,且其绝对值小于40 kJ/mol,表明吸附过程为吸热过程;吉布斯自由能为负,说明吸附过程自发进行;熵变为正,说明吸附过程是一个熵增过程。
