《世界卫生组织狂犬病专家磋商会第三版报告》更新与解读
2019-08-24陈瑞丰
陈瑞丰
狂犬病是由狂犬病病毒(rabies virus,RABV)感染引起的急性脑炎或脑膜脑炎的一种动物源性传染病,一旦发病,其病死率几乎100%,全世界每年因狂犬病致死约59 000人。近年来,狂犬病报告死亡数一直位居我国法定报告传染病前列,给人民群众生命健康带来严重威胁,我国也一直是世界卫生组织(World Health Organization,WHO)认定的狂犬病流行高风险国家之一。2017年4月,WHO狂犬病专家磋商会在泰国曼谷召开,2018年4月,WHO公布了《WHO狂犬病专家磋商会第三版报告》[1](以下简称“第三版报告”),同时取代了2013年公布的第二版报告[2]。自2005年《WHO狂犬病专家磋商会第一版报告》[3]公布以来,该报告一直是世界范围内狂犬病免疫、预防和控制方面最权威的指南性文件,对于指导全球范围预防、控制和消除狂犬病具有举足轻重的作用。现就《WHO狂犬病专家磋商会第三版报告》主要更新进行解读,旨在借鉴WHO最新的研究成果和推荐,指导和规范我国的狂犬病免疫预防工作。
1 狂犬病病毒属组成
RABV和一系列相关病毒(能导致以急性进行性脑脊髓炎为特征的狂犬病)均属于单股负链病毒目、弹状病毒科、狂犬病病毒属的RNA病毒。在第二版报告中,提出了14个狂犬病病毒种,其中确定了12个,另2种病毒种已经被发现,但并未明确其宿主动物,确定的12个狂犬病病毒种根据遗传距离和血清学交叉反应特性,分为遗传系谱Ⅰ(9个)和系谱Ⅱ(3个)。第三版报告中提出了18个狂犬病病毒种,其中确定了14个狂犬病病毒种,并增加了遗传系谱Ⅲ,18个狂犬病病毒种分为遗传系谱Ⅰ(12个)、系谱Ⅱ(3个)和系谱Ⅲ(3个)。
国际病毒分类委员会(International Committee on Taxonomy of Viruses,ICTV)是国际公认的病毒分类命名机构。ICTV最新版《主要物种名录》发布于2018年3月[4],其中公布了16种狂犬病病毒种(不包括第三版报告中公布的“Taiwan bat lyssavirus”和“Kotolahti bat lyssavirus”,在WHO列表的标注中,此二者血清学证据显示感染源自肯尼亚,ICTV目前并没有公布此二者的分类与命名。在ICTV公布的16种狂犬病病毒种中,WHO给出的10种为系谱Ⅰ型、3种为系谱Ⅱ型、3种为系谱Ⅲ型)。
关于狂犬病病毒属病毒种的命名和确定,是领域内争议的焦点之一,作者认为,WHO与ICTV公布的差异,源自对狂犬病的持续监测以及新一代测序技术的进步。近年来不断有新的狂犬病病毒种被发现,也说明对狂犬病病毒属的认识越来越深入,相信今后还会有新的狂犬病病毒种被发现。就目前ICTV公布的16种狂犬病病毒种,蝙蝠是其中14种病毒的宿主和传播媒介。虽然伊科马狂犬病毒(Ikoma lyssavirus,IKOV)和莫科拉病毒(Mokola virus,MOKV)分别在非洲灵猫和鼩鼱、家养猫和啮齿动物体内分离出来,但其宿主动物仍未知,根据遗传学距离和血清学交叉反应,有专家认为这两种病毒可能仍来源于蝙蝠,这些个例可能属于溢出性感染[5]。所有的狂犬病病毒属中只有RABV可以在食肉动物中传播,也是导致人狂犬病病例的最主要的病毒种,食肉动物能保持RABV的长期存在[6]。所有狂犬病病毒属的多样性都以蝙蝠为宿主中表现出来,蝙蝠是狂犬病病毒属的主要进化和自然储存宿主[7]。
2 人狂犬病的预防
2.1 狂犬病暴露分级 第三版报告在Ⅱ级暴露中增加了一点:“蝙蝠导致的Ⅱ级暴露按Ⅲ级暴露处置”,在Ⅲ级暴露中明确指出“直接接触蝙蝠属于严重暴露”。从中可以看出,WHO越来越强调蝙蝠在狂犬病暴露中的危险性和重要性[8]。
2.2 暴露类型和犬只特征与发病概率 人狂犬病病例绝大多数(第三版报告的数据是>95%,第二版报告的数据是>99%)是由狂犬咬伤所致。第三版报告指出暴露于RABV的结局取决于几个因素,包括伤口的严重程度、咬伤部位、进入伤口的病毒数量、病毒种别(基因型)以及暴露后预防的及时性,并且第一次提出暴露类型和犬只特征与暴露风险概率(见表1),我国还未有相关报道。
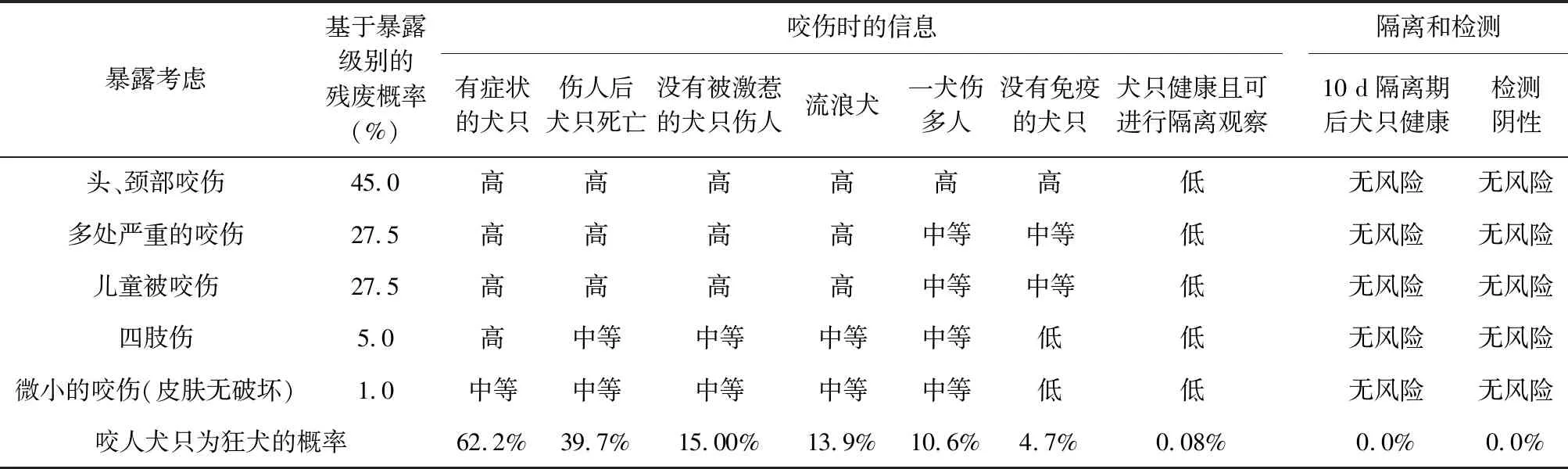
表1 暴露类型和犬只特征与暴露风险概率表
2.3 人用狂犬病疫苗接种方式及接种程序 第三版报告在狂犬病流行地区将狂犬病暴露前预防(pre-exposure prophylaxis,PrEP)纳入儿童常规免疫计划的推荐进行了修改,WHO在研究其效益和相关成本后指出:PrEP作为一种大规模的公共卫生干预措施比预防狂犬病死亡的其他措施昂贵得多,只有在犬咬伤发生率极高的特殊情况下(每年>5 000/10万人),并且该地区人用狂犬病疫苗接种比例很低、暴露后需要使用狂犬病免疫球蛋白(rabies immunoglobulin,RIG)比例较高的情况下,对全人群进行PrEP才不会增加成本,因此不再进行相关推荐。
第三版报告在人用狂犬病疫苗的接种方式上首次推荐皮内注射(intradermal injection,ID),这是以往报告中所没有的,这与此次更新的重点及原则相符,即:关注方案的可行性、疫苗接种程序的简化、成本效益的提高。人用狂犬病疫苗使用方式有肌肉注射(intramuscular injection,IM)和ID两种,目前绝大部分国家和地区都采用IM方式进行免疫接种,在过去的二十年里,多个临床研究已经证实ID在狂犬病暴露后免疫预防(post-exposure prophylaxis,PEP)中的免疫原性和有效性,目前ID接种方式已经在多个亚洲和非洲国家使用。ID途径诱导免疫应答的基础是:皮肤是机体重要的免疫器官,当抗原呈递到真皮层时疫苗功效增强。此外,将抗原用于皮肤层有利于它们暴露于多种抗原呈递细胞,例如巨噬细胞和树突细胞,这些抗原呈递细胞在皮肤中的数量多于在肌肉中的数量[9]。与IM相比,尽管ID使用的抗原量较少,但真皮中抗原呈递细胞可对通过ID的疫苗产生强烈的免疫应答。ID可替代IM为狂犬病疫苗接种提供了一种节约成本和剂量的方案。通过ID进行PEP接种比通过IM至少节约25%的疫苗。随着就诊患者数量的增加,ID方案的成本效益越来越高,使用的疫苗瓶数可以减少85%。另外,第三版报告中明确“即使说明书中没有明确标注,能够IM的狂犬病疫苗也可以安全地用于ID使用”。
接种程序上,WHO进行了较大的变更(图1),WHO在PrEP和PEP疫苗接种方式、接种次数与接种时间上进行了很大的更改和优化,是此版最大的亮点之一。对使用IM和ID途径进行PEP效果评估的研究表明[10-14],与目前WHO推荐的PEP和PrEP程序相比,可以缩短正在使用的PEP和PrEP程序的持续时间和所需剂量[15-17]。另外,近期在泰国、荷兰和比利时进行的单次接种人用狂犬病疫苗的研究显示[18],单次接种疫苗后,99.5%~100%受试者体内的抗体滴度高于0.5 U/mL,并且其所产生的免疫记忆应答可长达1年。尽管这些研究在所包含的年龄组(年龄<50岁)、随访时间和不同的血清学试验时间等方面存在局限性,但证明了单次就诊方案可引起充分的机体免疫应答,也说明我们对人用狂犬病疫苗在激活机体免疫应答方面还知之甚少。
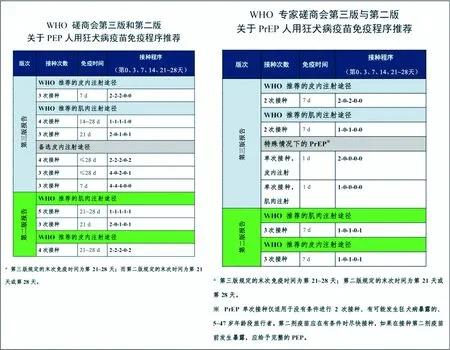
图1 WHO第三版和第二版报告关于PEP和PrEP程序的推荐
2.4 再次暴露后的加强免疫 第三版报告提出:已免疫的任何年龄段的个体,如果有记录证明之前进行过PrEP剂次以上的PEP接种,则可不用RIG。如果再次暴露发生在前次暴露后的3个月内,且暴露者在前次暴露后已进行了完整的PEP,那么再次暴露后只需进行伤口处置,不需要接种狂犬病疫苗和RIG。如果再次暴露发生在前次PEP接种的3个月之后,那么之前已免疫的暴露者需要进行再次的PEP,但不需要注射RIG。再次暴露后的免疫预防程序如下。
两次就诊:IM,1-1-0-0-0;ID,1-1-0-0-0(在第0天和第3天通过IM或ID各接种一剂/次人用狂犬病疫苗)。
单次就诊:ID,4-0-0-0-0(在第0天,四个点位、皮内注射人用狂犬病疫苗各0.1 mL)。
另外,第三版报告指出:在注射第一剂疫苗的7 d内,通常不会产生有效的免疫反应,因此,如果在此期间发生再次暴露,应给予完整的PEP程序,对于Ⅲ级暴露者,还应使用RIG。没有完成完整PEP程序者,但如果已经接种过至少两剂次疫苗,应被认定为具有狂犬病疫苗免疫史者。这种极端状况虽然不常见,但的确时有发生,以往的报告对此没有明确的推荐意见。
2.5 狂犬病免疫球蛋白使用 关于RIG使用的最新推荐,也是此版报告的最大亮点之一。RIG在被动免疫中的作用是:接种狂犬病疫苗后,在机体产生有效的中和抗体之前,在暴露的部位提供特异性的狂犬病病毒中和抗体中和RABV。RABV是高度嗜神经性的RNA病毒,它通过破损皮肤或直接接触黏膜进入机体,在肌肉组织中复制,然后通过运动神经元的终板和轴突到达中枢神经系统。RABV的生物学特性以及狂犬病相对较长的潜伏期为暴露后预防提供了可能性,因此,狂犬病致死率几乎为100%,而狂犬病又是100%可以预防的疾病。预防狂犬病发生的措施包括:①立即对伤口进行彻底地冲洗和清洗;②尽早进行人用狂犬病疫苗接种;③必要时,尽早在伤口及伤口周围注射RIG。
关于RIG的使用,一直是研究和临床的争议焦点之一。新近的研究显示,将伤口周围浸润后剩余的RIG注射至远离伤口的肌肉内,与只进行伤口周围浸润相比,对于预防狂犬病发生没有或仅有少量的额外保护作用,剩余的RIG可供其他患者使用,这种做法在RIG供应不足的情况下特别有用[19-22]。第三版报告推荐马源RIG的最大剂量按40 U/kg计算,人源RIG的最大剂量按20 U/kg计算。如果有许多小的创口,或暴露于蝙蝠,或是咬伤之外的暴露时,推荐将剩余的RIG在尽量靠近暴露部位的周围进行IM;对于没有伤口的黏膜暴露,推荐用RIG进行暴露部位的冲洗;对于可疑狂犬病病毒气溶胶暴露者,推荐RIG IM。已经不再是第二版报告推荐的:马源RIG使用剂量为40 U/kg,人源RIG的使用剂量为按20 U/kg,所有的免疫球蛋白,如果解剖结构上允许(但避免可能的骨筋膜室综合征),应仔细地注射到伤口内及伤口周围。如果有剩余,将其注射到远离疫苗注射点的肌肉部位。
另外,第三版报告还指出:来自狂犬病流行地区的数据显示,即使在没有RIG的情况下,通过立即对伤口进行彻底地冲洗和清洗加尽早接种疫苗并完成PEP,99%以上的患者可以存活。
3 犬狂犬病的预防控制
WHO及其合作伙伴在2015年就已经达成一个战略目标,即到2030年,在全世界范围内消除由犬传播的人狂犬病[23],在第三版报告中用了大量的篇幅来阐述这一战略目标以及实施方案。狂犬病的预防高度依赖于高危人群对该病的认知,提高认知应包括教育、动物咬伤预防部门的参与、犬主人的责任感、暴露后迅速的急救。这些预防措施对控制其他疾病和咬伤(如:棘球蚴病、利什曼病、钩端螺旋体病等)也会产生有益的影响。通过在地方性流行地区进行大规模犬狂犬病疫苗接种证实,使犬只的疫苗覆盖率达到70%即可阻断RABV在犬只间的传播,从而拯救人类生命。
另外,第三版报告继续推荐“10日观察法”,即,暴露于家养的犬、猫和雪貂后,对伤人动物进行严密医学观察,10 d后如果动物仍然健康,则证明伤人动物没有罹患狂犬病的风险。但是第三版报告第一次提出“14日观察法”这一概念,并且明确这一概念适用于家养犬、猫和雪貂以外的其他动物。
4 其他更新及推荐
4.1 免疫缺陷患者 关于免疫缺陷患者的PrEP和PEP改动也比较大,以往的推荐是:一些对艾滋病病毒携带者/艾滋病患者的研究表明,CD4细胞计数非常低的患者RABV的中和抗体反应明显低下或检测不到。当这些患者和其他免疫功能不确切的人群发生的Ⅱ级和Ⅲ级暴露,需要在正确彻底的伤口处理和消毒同时,局部浸润注射人或马的RIG以及全程5个剂量IM人用狂犬病疫苗。如果可行,在疫苗接种2~4周后检测RABV中和抗体以评估是否需要额外剂量的疫苗。第三版报告更新体现在:①重新对免疫缺陷患者进行了划分,并对其免疫效果进行了审视,认为“临床监测和管理良好的免疫缺陷患者,如接受抗逆转录病毒治疗的艾滋病毒感染者不被视为免疫功能低下,并且已证实其对狂犬病和其他疫苗可产生正常的免疫应答”。②其PrEP程序的推荐总体原则与常人相同,仅对于“免疫功能低下的免疫缺陷患者”才推荐PrEP在第0天和第7天的基础上加上第三剂疫苗,即:ID途径2-2-2(0-7-21~28)或IM途径1-1-1(0-7-21~28)。③以往推荐仅能使用IM途径,而新的推荐ID途径也可以使用。
4.2 人狂犬病潜伏期 第三版报告关于人狂犬病病例潜伏期的叙述为:人狂犬病病例的潜伏期从5 d到几年不等,绝大多数人狂犬病病例的潜伏期是2~3个月。2%~3%的人狂犬病病例潜伏期大于1年,有记录的特殊病例为8年[24]。以往的报告叙述为:潜伏期从5 d到几年不等(一般为2~3个月,很少超过1年)。尽管第三版报告提出了1个潜伏期8年的病例(从巴西移民至美国的1个病例),以往曾有文献报导最长潜伏期为6年的1个病例[25](从菲律宾移民至美国的1个病例)。但由于病例数量太少,相关证据链也并不是十分完整,因此笔者建议审慎地看待这个观点,大量的统计数据表明人狂犬病病例的潜伏期一般为1~3个月,越靠近中枢潜伏期越短,超过一年者极罕见。
另外,对于被确诊狂犬病动物暴露者,第三版报告第一次明确,不论暴露时间多久,甚至已经过去几年,也应注射狂犬病疫苗(但是并没有推荐使用RIG)。当出现人狂犬病病例时,应进行回顾性评估,暴露于同一个动物的其他人应给予PEP,即便是暴露数月之后。在以往的推荐中,如果出现类似情况,一直都是按照暴露后或再次暴露程序进行处置,也就是说,如果被确诊狂犬病动物初次暴露且属于Ⅲ级者,无论暴露时间多久,除了狂犬病疫苗,还应使用RIG。第三版报告对此的修订对临床有重要的指导作用。
4.3 人狂犬病病例及人与人之间的传播状况 第三版报告提出:人狂犬病病例的唾液、眼泪、尿液和神经组织中都可以发现RABV,暴露于这些体液和组织在理论上有传播风险。人狂犬病病例的血液中没有发现RABV。RABV通过人与人之间的传播从来没有确诊过,这种极低的风险不应妨碍对人狂犬病病例的护理。有记录的人与人之间传播的病例是由于接受了来自被RABV感染的个体组织和器官移植,以及一个可能由于母婴传播导致的RABU感染病例。尽管缺乏证据,但根据病理学和流行病学,RABV不太可能通过母乳喂养传播。
4.4 人狂犬病病例的暴露方式及特殊考虑 人狂犬病病例主要通过咬伤的方式被传染,其他途径导致的死亡病例极为罕见。动物实验显示,RABV可以通过食用狂犬病动物的肉传播,但是从来没有因食用狂犬病动物的生肉得狂犬病的报道。强烈建议不要食用狂犬病动物的肉,尤其是生肉,如果在处理狂犬病动物肉时发生Ⅱ级或Ⅲ级暴露,应该考虑进行PEP。从狂犬病奶牛的奶中没有发现RABV,也没有因进食狂犬病奶牛的原奶而患狂犬病的报道,虽然不建议饮用狂犬病奶牛的原奶,但是没有证据证实饮用后可以发生狂犬病,因此即使饮用了狂犬病奶牛的原奶,也不推荐进行PEP。经过巴氏消毒的牛奶没有传播RABV的风险。
野生食肉动物和蝙蝠(食肉目和翼手目动物)较其他野生动物传播狂犬病的风险要高,因为它们是RABV的储存宿主动物。但是被其他野生动物,尤其是猴子咬伤通常发生在人们喂食或手持喂食的食物时,或动物处于受威胁、被困住或被捕捉时,应尽量避免类似状况出现,这种情况没必要进行PEP。啮齿动物狂犬病非常罕见,也从没有因啮齿动物咬伤得狂犬病的病例报道。极其罕见的情况下,会出现人狂犬病病例是由于在实验室处理含有高浓度活RABV的材料或在有高密度RABV感染的蝙蝠的洞穴内吸入含有病毒的气溶胶而发生。
以上特殊状况在以往的报告中并未明确涉及,但是在临床上时有出现,这些推荐对于临床工作有非常重要的指导作用。
4.5 其他特殊状况 第三版报告依然非常强调暴露后伤口局部处置的重要性:对于所有咬伤和抓伤的伤口,立即对伤口进行局部治疗是狂犬病暴露后预防中至关重要一步。同时第一次在其系列报告中明确提出“15 min”这一概念,即立即使用肥皂和清水对伤口进行约15 min的冲洗和清洗,然后使用碘伏或其他有杀病毒活性的物质对伤口进行消毒。“15 min”这个概念第一次出现是在WHO 2007版“Rabies vaccines:WHO position paper”[26]中提过,但是在随后的2010版中就没有再提及[27]。
另外,对于疫苗接种程序中变更疫苗品种甚至变更接种途径,第三版报告第一次进行了相关推荐:有证据显示,在不可避免的状况下,变更狂犬病疫苗的品种和(或)接种途径是可以的,而且不需要重新开始PEP程序,但是要按照新的接种途径程序继续完成剩下的PEP。
5 小结
《WHO狂犬病专家磋商会第三版报告》总结和展示了近年来世界范围内在狂犬病免疫、预防、控制和国际间合作等方面的研究结果,在狂犬病病毒学、人类狂犬病防控、人用狂犬病疫苗及狂犬病免疫球蛋白使用、犬狂犬病防控和狂犬病防控国际间合作和国际项目等方面展示了新的证据、提出了新的推荐意见。提出到2030年在全球范围内消除由犬传播的人狂犬病病例的战略目标及其实施方案。这些最新的推荐意见对我国的狂犬病防控工作具有重要的指导作用,也是广大狂犬病暴露预防门诊工作的指南性参考文献。在应用该报告指导临床工作时,需结合国情,为我国狂犬病暴露患者选择最优治疗方案,并积极设计适合我国的狂犬病防控策略和临床研究,为实现我国“2020年在中国达到狂犬病控制标准”[28]的目标提供重要的指导。
