双介入治疗颈部创伤性动脉瘤间异物:动物实验研究
2019-08-23杨秀军李婷婷
文 颖,杨秀军,李婷婷,乐 萱,黄 挺
(上海交通大学附属儿童医院 上海市儿童医院影像科,上海 200062)
伴血管损伤的血管旁、血管间软组织异物临床并不少见[1-3],且危害大,需及时干预。对此外科手术创伤大,异物取出失败风险高;传统介入钳取术虽可取出异物,但在钳取异物过程中无法同时处理血管损伤和出血[1,2,4]。因此,如何联合多种技术综合治疗创伤性动脉瘤间异物[5-7],成为目前的热点问题之一。本研究基于犬颈部创伤性动脉瘤间异物疾病模型,采用直接经血管鞘植入覆膜支架封堵动脉瘤颈口、同时经皮经软组织介入钳取异物的方法进行治疗,探讨双介入方法的可行性及效果,以期为临床一站式微创介入治疗伴血管损伤的软组织异物提供参考。
1 材料与方法
1.1 构建犬颈部创伤性动脉瘤间异物模型 选取2岁健康比格犬5只[由上海交通大学农学院教学实验实习场提供,许可证号:SCXK(沪)2017-0007],雌雄不限。于其右侧颈部构建创伤性颈动脉动脉瘤间异物模型[8],作为研究侧,进行双介入治疗;对其左侧颈部采用直接断针刺入、留置的方法构建颈动脉旁软组织异物模型(即不伴重要血管损伤的软组织异物模型),作为对照侧,采用传统介入技术治疗。5只犬均经颈动脉造影等影像学检查证实造模成功。
1.2 制备可降解覆膜支架 采用JDBM可降解镁合金裸支架(上海交通大学自主研发,图1),以负载肝素钠的电纺纤维生物膜(上海市伤骨科研究所制备)进行裸支架覆膜(图2)[9-10]。而后将覆膜支架存置于-26℃冰箱内存放,使用前进行紫外线消毒,并放置于无菌抗凝管中备用。
1.3 动物模型介入治疗 采用Toshiba Infinix-i INFX8000V单C臂DSA系统引导介入治疗。成功穿刺右侧股动脉后,行选择性双侧颈动脉或主动脉弓造影,评估异物、血管及动脉瘤的位置关系(图3)。
远离动脉瘤造模处下方,于研究侧穿刺置入7F血管鞘(图4),并预先将可降解覆膜支架逆向置入外套管内,将扩张器经支架内腔送入外套管内(图5)。小心推送血管鞘,于右侧颈动脉内越过造模处后,采用尖头离断的7F扩张器顶住、固定支架;于透视下经导管鞘置入6F导管及导丝,定位颈动脉。钳夹取出断针,尽量避开导管、导丝;而后缓慢退出血管鞘外套管并释放支架(勿顶推支架),封堵血管创口和瘤口。随即拔出导管、导丝,并经鞘行颈动脉造影,证实异物和动脉瘤消失、载瘤动脉通畅且无内瘘及对比剂外溢后,拔除颈动脉血管鞘,局部适当加压10 min止血,切忌压迫支架处致其变形;再经股动脉选择性右侧颈动脉造影,进一步观察动脉瘤及血管创口闭合等情况。
在颈动脉导管或/和导丝透视定位和引导下,经皮经软组织取出对照侧异物。经左侧颈动脉造影确认无血管损伤和出血后,拔除导管、导丝和右侧股动脉血管鞘,压迫止血。
术后将实验犬送回动物房复苏、饲养,每日常规给予阿司匹林25 mg抗凝。
1.4 影像学观察与评价 分别于介入治疗术前、术后即刻行双侧颈动脉DSA,并对5只于术后1个月、4只于术后2个月、2只于术后3个月加行CTA或MRA,重点观察术后即刻异物和动脉瘤是否完全消失,载瘤动脉是否通畅,是否存在内瘘和对比剂外溢;术后1、2、3个月有无动脉瘤复发、内瘘,覆膜支架降解的区域、程度以及载瘤动脉狭窄情况。
2 结果
研究侧以直接经鞘法植入支架的技术成功率为100%(5/5),双介入治疗取出异物同时治疗动脉瘤均获成功。异物取出后均发生不同程度动脉瘤出血,DSA表现为异物消失、动脉瘤内对比剂外溢(图6);载瘤动脉内覆膜支架释放封堵瘤口后均有效止血,DSA示动脉瘤及对比剂外溢征象消失,局部颈动脉轻度狭窄,未见内瘘。术后随访期间影像学检查均可见颈动脉局部存在轻度或中度狭窄(图7),未见明显内瘘及动脉瘤复发。
对照侧介入治疗取出软组织内异物的技术成功率亦为100%(5/5),随访期间无颈动脉狭窄等改变。
1只犬由于麻醉过深、时间过长等原因,术后出现深度呼吸抑制,紧急救治后成功复苏。术中、术后未发生动物意外死亡。
3 讨论
临床对于包括颈动脉创伤性动脉瘤间异物在内的复杂软组织异物处置困难,治疗过程主要包括取出异物、封堵血管创口及动脉瘤颈口、止血及血管修复。微创介入治疗方法具有其独特优势,其成功的关键在于:①可靠、精准的异物显像与定位;②了解异物对毗邻结构的影响;③异物邻近重要结构(如血管等)的可视化;④创新性技术,如在介入取出异物的同时有效止血和治疗异物创伤性血管病变。
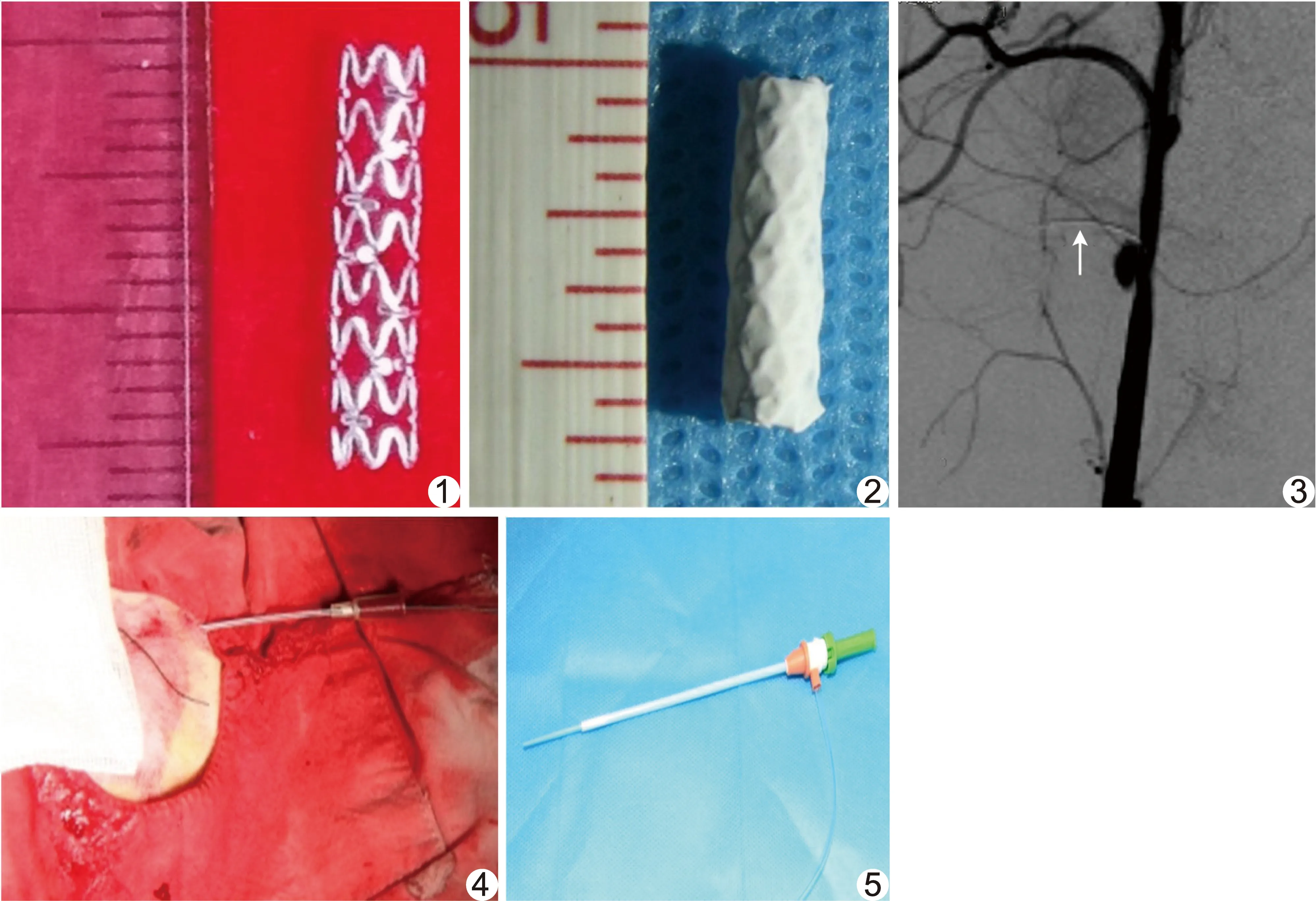
图1JDBM裸支架图2裸支架覆膜后图3双介入治疗前犬颈部创伤性动脉瘤间异物模型右侧颈动脉DSA显示创伤性动脉瘤及其间异物(箭)图4尽量远离动脉瘤处下方经皮穿刺颈动脉,置入7F血管鞘图5将扩张器经支架内腔送入外套管内
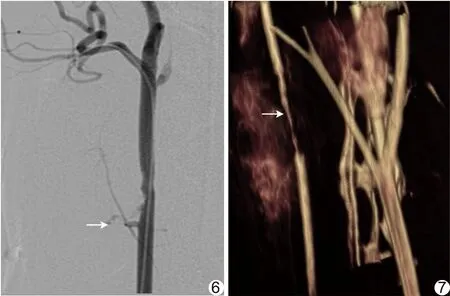
图6 取出犬颈部创伤性动脉瘤间异物后,DSA显示颈动脉局部痉挛,对比剂外溢(箭),动脉瘤显示欠佳 图7 犬颈部创伤性动脉瘤间异物双介入治疗术后1个月,增强MRA示颈动脉局部中度狭窄,内壁欠光整(箭)
研究[2-3,6]发现,基于增强CT动脉期、静脉期源数据进行三维重建分析,尤其是仿真局部解剖成像与评估,能够精准定位异物、直观显示异物与毗邻血管间的距离等位置关系,有助于可靠评估异物摘除风险,指导介入操作。DSA可为其他影像学检查假阴性结果的血管损伤诊断证伪提供有力支持[2,4],但由于X线透视图像缺乏组织层次,尤其是异物处及异物周围神经、血管在透视下不可视,使得介入治疗在取出紧邻大血管或伴血管损伤的软组织异物方面存在一定禁忌。通过血管内介入技术置入导管、导丝,实现对血管的透视标记,即可赋能血管以间接可视性,从而解决介入钳取异物时无法对血管可视化定位的问题[1,4],有效避免异物钳取过程中的血管损伤,使取出既往常规介入治疗视为禁忌的间距2 mm以内血管旁异物成为可能,拓展了异物介入治疗技术的适应证。但是,目前仍无法在微创介入取出异物的同时有效止血和修复损伤血管,导致其成为技术瓶颈。
本研究在成功构建犬颈部创伤性动脉瘤间异物模型[8]基础上,将改良JDBM生物可吸收覆膜支架[11]植入血管,腔内封堵血管创口及动脉瘤颈口,同时经皮经介入钳取软组织异物,初步实现在取出异物的同时修复损伤血管和止血,为破解传统介入技术瓶颈提供了参考。为避免制备支架输送系统时压握处理及释放、球囊膨胀过程中的支架、膜材损伤(镁合金支架易形变)、生物膜分离与脱落,加之受限于研究经费和实验流程优化需要,本研究采用直接经鞘法支架植入技术。操作要点包括:①将覆膜支架逆行置入7F血管鞘的外套管内,其中以外套管7F扩张器逆行反复预扩是关键;②以18G穿刺针成功穿刺后,于导丝引导下将带有支架的7F血管鞘置入血管腔内,并预送至目标位置;③成功置入带有支架的7F血管鞘至目标位置后,换以经尖头离断、钝化处理的7F扩张器顶住、固定支架(注意绝不能顶推支架,否则极易造成支架变形和血管内皮损伤,进而引发血栓形成、血管平滑肌细胞增殖甚至支架内再狭窄[12]),通过缓慢退出血管鞘外套管来实现外套管内支架的释放和血管内植入。本研究结果显示,直接经鞘法颈动脉支架辅助治疗犬颈部创伤性动脉瘤间软组织异物的技术成功率高达100%,且较为有效;但同时也发现相对于传统介入治疗不伴血管损伤的软组织异物,双介入治疗动脉瘤间软组织异物在异物取出后动脉瘤出血发生率达100%,这一方面进一步佐证了伴血管损伤的软组织异物治疗的高风险性,另一方面提示颈静脉片“补丁式”侧-侧吻合移植构建的动脉瘤模型[8]瘤口小、血流量低,易形成瘤栓甚至完全闭塞,尽管对需紧急处置的创伤性动脉瘤间异物研究影响不大,但模型的稳定性欠佳,不利于长期观察。
总之,本实验初步证实了可降解覆膜支架辅助经皮经软组织介入异物钳取技术治疗犬颈部创伤性动脉瘤间异物的可行性及有效性,为临床一站式微创介入治疗颈部创伤性动脉瘤间异物提供了新思路;直接经鞘法植入动脉内覆膜支架颈在动物实验中的成功探索,也为今后临床研究提供了有价值的参考。但直接经鞘法与经输送系统植入覆膜血管内支架不同,对介入操作技术要求较高,损伤目标血管、尤其是造成颈动脉医源性的风险较高,可能增加支架植入术后血管狭窄率,更易导致医源性血管损伤,且拔鞘后不易止血,需长时间压迫,其应用价值有待进一步观察。
