XELOX方案与mFOLFOX6方案的剂量强度对结肠癌术后辅助化疗的效果比较Δ
2019-08-20马妮娜曹邦伟
马妮娜,王 婧,赵 磊,曹邦伟
(首都医科大学附属北京友谊医院肿瘤中心,北京 100050)
虽然靶向治疗和免疫治疗是当今研究的热点,但是化疗仍在结肠癌的治疗中起着举足轻重的作用,XELOX方案(奥沙利铂+卡培他滨)与mFOLFOX6方案(奥沙利铂+亚叶酸钙+5-氟尿嘧啶)是目前临床较为成熟的两种化疗方案,研究结果表明,上述两种方案提高晚期结直肠癌患者总体生存率的效果相当[1],到目前为止两者在结肠癌辅助化疗中的地位仍无法替代。在最初的FOLFOX方案中,5-氟尿嘧啶-亚叶酸钙中心静脉导管相关并发症时有发生,因此,自21世纪初以来,口服卡培他滨代替注射或静脉泵入5-氟尿嘧啶一直是一个活跃的研究领域。在辅助治疗中,几乎所有的研究都将卡培他滨单药治疗与5-氟尿嘧啶-亚叶酸钙方案进行比较,结果显示,两者的应答率、无病生存期(disease free survival,DFS)和总生存期(overall survival,OS)相似[2-3]。因此,是否是不良反应的不同,影响了结肠癌术后两种辅助化疗方案的剂量强度(dose intensity,DI),从而影响到患者的DFS预后,是需要重点探索的问题。本研究回顾性收集了术后使用XELOX方案或mFOLFOX6方案辅助治疗的结肠癌患者的数据,分析两种方案的DI对临床预后的影响。
1 资料与方法
1.1 资料来源
收集2010—2014年首都医科大学附属北京友谊医院行根治性切除术的180例Ⅲ期结肠癌患者的临床资料,按资料中患者的治疗方式分为XELOX组(105例)和mFOLFOX6组(75例)。XELOX组患者中,男性62例,女性43例;年龄18~79岁,中位年龄65岁;美国东部肿瘤协作组(eastern cooperative oncology group,ECOG)评分为0~2分。mFOLFOX6组患者中,男性44例,女性31例;年龄33~78岁,中位年龄66岁;ECOG评分为0~2分。两组患者各项基线资料的均衡性较高,具有可比性,见表1。
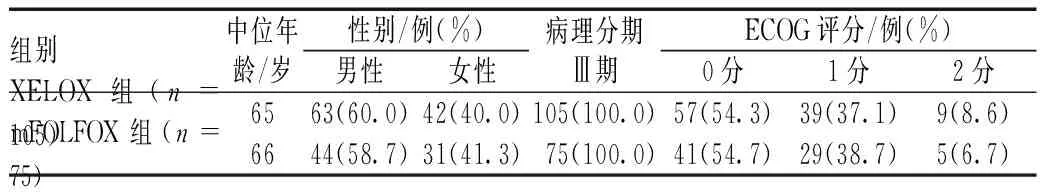
表1 两组患者基线资料比较Tab 1 Comparison of baseline information between two groups
1.2 治疗方法
XELOX组患者采用经典的XELOX方案:奥沙利铂130 mg/m2,静脉滴注,第1日;卡培他滨1 000 mg/m2,口服,1日2次,共14 d,每3周为1个周期,共用药8个周期。mFOLFOX6组患者采用经典的mFOLFOX6方案:奥沙利铂85 mg/m2,静脉滴注,第1日;亚叶酸钙400 mg/m2,静脉滴注,第1日;5-氟尿嘧啶400 mg/m2,静脉滴注,第1日;5-氟尿嘧啶 2 400 mg/m2持续泵入46 h,每2周为1个周期,总用药12个周期。
1.3 结局指标
(1)DI:计算公式为DI=总给药量(mg/m2)/总治疗时间(周)。(2)化疗毒性反应评定:参照美国国立癌症研究所的药物毒性评价标准[4],进行不良事件的判定,包括恶心呕吐、神经毒性、腹泻、中性粒细胞减少症、血小板减少症、手足综合征及周围神经病变。(3)DFS:即从治疗开始到复发的时间或由于疾病进展导致患者死亡的时间,采用美国国立癌症研究所的实体肿瘤疗效评价标准(RECIST 1.1)[5]进行评定。所有患者均需在每个化疗周期前进行相关检查,包括血常规、肝肾功能、电解质、癌胚抗原(CEA)、心电图、B超及胸部X线等。患者术后前2 年应每3~6个月进行1次胸部+全腹部盆腔CT扫描,半年进行1次肠镜检查;然后1年进行1次胸部+全腹部盆腔CT扫描、肠镜检查。若患者临床表现提示肿瘤进展或CEA水平异常升高,则立即复查CT扫描和(或)肠镜检查。
1.4 统计学方法
剂量减少的定义为比标准规定剂量减少>10%。减少的定义和分析有2种不同的方式:在化疗第1周期开始治疗前发生的剂量减少;化疗开始后出现的剂量减少。治疗延迟的定义为当实际治疗周期总时间超过理论治疗周期总时间至少1个周期长度时(XELOX方案:3周;mFOLFOX6方案:2周),确定为治疗延迟。相对剂量强度(relative dose intensity,RDI)的分析采用独立t检验和Fisher精确检验,P<0.05为差异有统计学意义。采用Kaplan-Meir法进行生存数据分析[6]。
2 结果
2.1 两组方案的DI分析
两组方案的DI分析见表2。可见,XELOX组中,奥沙利铂的平均实际DI较理论标准DI降低了25.9%,卡培他滨的平均实际DI较理论标准DI降低了22.0%;相比之下,mFOLFOX6组中,奥沙利铂的实际平均DI较理论标准DI降低了14.6%,5-氟尿嘧啶的实际平均DI较理论标准DI降低了14.1%。t检验分析结果显示,XELOX组中卡培他滨实际用量较其理论标准用量的降低幅度明显大于mFOLFOX6组中氟尿嘧啶实际用量较其理论标准用量的降低幅度,差异有统计学意义(P=0.001 4);XELOX组中奥沙利铂实际用量较其理论标准用量的降低幅度明显大于mFOLFOX6组,差异有统计学意义(P=0.000 1)。mFOLFOX6方案中,亚叶酸钙可促使5-氟尿嘧啶活性代谢产物5-氟尿嘧啶脱氧核苷酸与胸苷酸合成酶共价形成三元复合物,从而加强5-氟尿嘧啶的抗肿瘤作用,但其本身并无抗肿瘤作用,其用量随着5-氟尿嘧啶DI的变化做相应调整,故在此不对其DI进行讨论。
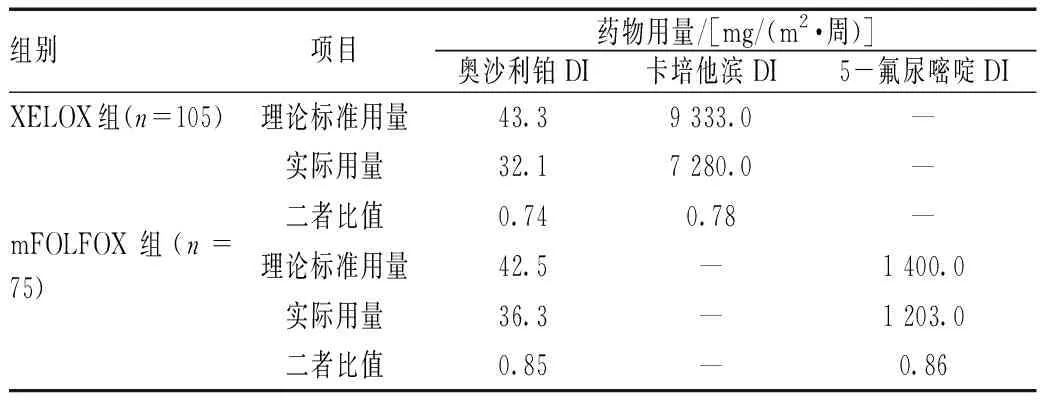
表2 两组方案的DI分析Tab 2 Dose intensity (DI) analysis of the two regimens
注:“—”表示该方案中未用该药
Note:“—” indicates that the drug is not used in the scheme
2.2 两组患者的治疗时间、延误情况及不良事件发生情况比较
所有患者中,完成XELOX方案的中位周期数为8个周期(范围:1~10个周期),完成mFOLFOX6方案的中位周期数为10个周期(范围:1~14期);XELOX组中有21.0%的患者没有完成标准的8个周期化疗,mFOLFOX6组中有29.3%的患者没有完成标准的12个周期化疗;mFOLFOX6组中有37.3%的患者治疗延迟>1个周期,而XELOX组中仅19.0%的患者出现了这种延迟,mFOLFOX6组中治疗延迟>1个周期的患者数为XELOX组的2倍,两者的差异有统计学意义(P=0.039),见表3。mFOLFOX6组中发生腹泻、中性粒细胞减少症、血小板减少症及周围神经病变的患者所占比例明显高于XELOX组,差异均有统计学意义(P<0.05),提示mFOLFOX6方案的化疗相关毒性反应更为常见,见表4。
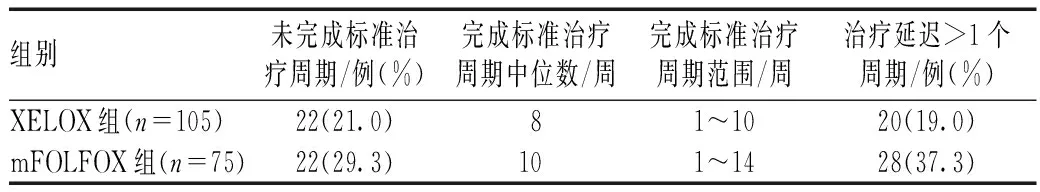
表3 两组患者的治疗时间及延误情况比较Tab 3 Comparison of treatment duration and delays between two groups
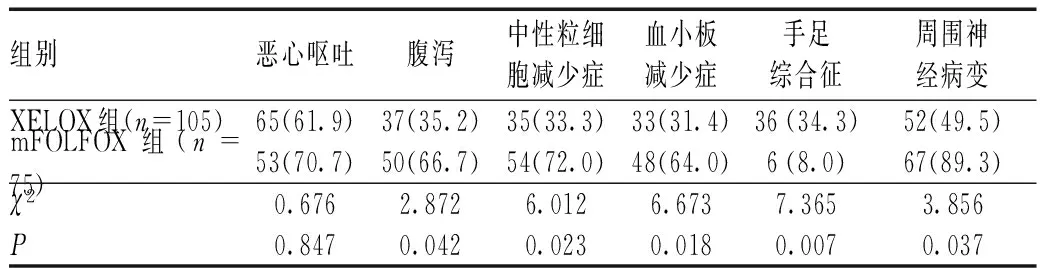
表4 两组患者不良事件发生情况比较[例(%)]Tab 4 Comparison of incidences of adverse drug reactions between two group[cases(%)]
2.3 两组患者的DFS比较
中位随访40个月后,两组患者DFS的差异无统计学意义(P=0.598);两组中均有>80%的患者仍然存活,见图1。
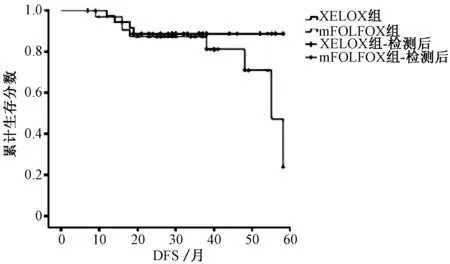
图1 两组患者的DFS曲线Fig 1 DFS curves of the two groups
3 讨论
结直肠癌已成为我国最常见的恶性肿瘤之一[7]。我国恶性肿瘤中,结直肠癌的发病率及死亡率均居第4位,且其发病率呈逐年升高趋势[8]。虽然多数患者可以进行根治性手术切除治疗,但术后5年生存率仍较低。术后辅助化疗是治疗晚期结直肠癌的主要手段,目的在于控制根治性切除术后肿瘤的局部复发、远处转移和生长速度,从而提高患者的生活质量,延长生存时间。关于术后辅助用药,卡培他滨与5-氟尿嘧啶+亚叶酸钙的毒性分布存在一定的差异,但总体而言,XELOX方案的Ⅲ级腹泻、手足综合征的发生率明显更高,而FOLFOX方案的Ⅲ级中性粒细胞减少症、发热性中性粒细胞减少症似乎更为常见[9]。目前缺乏真正的比较FOLFOX与XELOX这两个一线化疗方案的研究,似乎两个方案治疗结直肠癌的疗效和耐受性相似,但上述观点一直存在争议[10]。因为临床数据表明,XELOX方案毒性更大,导致更频繁地减少DI,因此,提出了关于DI对临床结果的影响。
本研究评估了XELOX方案与mFOLFOX6方案用于结肠癌术后辅助化疗的DI和安全性,结果显示,在临床实践中,减少XELOX方案的剂量并不影响临床效果;与mFOLFOX6方案比较,XELOX方案的前期剂量降低幅度更大;mFOLFOX6组中发生腹泻、中性粒细胞减少症、血小板减少症及周围神经病变的患者所占比例明显高于XELOX组,差异均有统计学意义(P<0.05),这些不良事件导致mFOLFOX6组中延迟治疗的患者所在比例高于XELOX组。本研究结果与其他相关文献报道一直,显示应用XELOX方案化疗的患者接受了较低剂量的奥沙利铂和卡培他滨[11-13]。另外,本研究验证了剂量减少是否会影响DFS等临床结果。初步结果显示,与mFOLFOX6相比,XELOX没有生存劣势(见图1)。其他类似研究的结果也显示,使用XELOX患者的OS也有改善的趋势[14-15]。可能的解释是,XELOX方案中奥沙利铂的预期DI高于mFOLFOX6方案,XELOX方案中奥沙利铂的理论剂量为每3周130 mg/m2,而mFOLFOX6方案中为每2周85 mg/m2。虽然在辅助治疗期间两种方案中奥沙利铂的总剂量非常相似,但XELOX方案中每个周期的更大剂量密度可能有助于解释为什么XELOX具有更多的剂量限制毒性,也可能表明XELOX方案在辅助化疗中对残余肿瘤细胞有更多的活性。
总之,在结肠癌的术后辅助化疗中,低DI的XELOX方案不会影响患者的临床预后,反而会更好一些;另外,mFOLFOX6方案的毒性较XELOX方案相对增加,也会影响患者对于辅助化疗的耐受性。当然,上述结果须在大规模的前瞻性研究中证实。
