款冬花配方颗粒的质量标准研究Δ
2019-08-13许洪波蔡兴航毛晶晶杨康许怀礼陕西中医药大学陕西省中药资源产业化协同创新中心陕西咸阳708杨凌科森生物制药有限责任公司西安700西安市中医医院药剂科西安700
许洪波,蔡兴航,毛晶晶,杨康,许怀礼(.陕西中医药大学陕西省中药资源产业化协同创新中心,陕西咸阳 708;.杨凌科森生物制药有限责任公司,西安 700;.西安市中医医院药剂科,西安 700)
款冬花配方颗粒是以款冬花饮片为原料,经现代制药技术提取、浓缩、分离、干燥、制粒、包装而成的颗粒剂,具有润肺下气、止咳化痰之功效,是中医临床常用的药物之一[1]。目前市售不同厂家的款冬花配方颗粒虽有各自的质量标准,但质量良莠不齐,且尚无统一的行业或国家质量标准;此外,现行的企业标准主要从性状、鉴别、检查、浸出物等方面对款冬花配方颗粒的质量进行控制,较少有涉及含量测定的内容[2]。因此,建立款冬花配方颗粒简便可行的定性、定量检测方法显得尤为重要。基于此,本研究采用薄层色谱法(TLC)对款冬花配方颗粒进行定性鉴别,采用高效液相色谱法(HPLC)对该方的特征成分款冬酮进行定量分析,旨在为其质量控制及质量标准的建立提供参考。
1 材料
1.1 仪器
LC-20A型HPLC仪,包括CBM-20A型控制器、LC-20AT型双泵、SPD-20A型紫外检测器、CTO-20A型柱温箱、lab Solutions色谱工作站(日本Shimadzu公司);HT-2109型电磁炉(广东美的生活电器制造有限公司);N-1100型旋转蒸发仪(日本EYELA公司);Vaco 5型冷冻干燥机(德国Zirbus公司);KQ-300DE型数控超声波清洗器(昆山市超声仪器有限公司);CPA2250型电子天平(德国Sartorius公司);PTL型电子天平(福州华志科学仪器有限公司)。
1.2 药品与试剂
款冬花配方颗粒(批号:180401、180402、180403,规格:10 g/袋)、缺款冬花的阴性样品(批号:180407,规格:10 g/袋)均由陕西中医药大学协同创新中心实验室自制;款冬酮对照品(批号:111884-201704,纯度:99.1%)、款冬花对照药材(批号:121449-201704)均由中国食品药品检定研究院提供;硅胶GF254薄层板(青岛海浪硅胶干燥剂有限公司,批号:20160702);甲醇为色谱醇,其余试剂均为分析纯,水为纯净水。
1.3 药材
款冬花饮片(批号:0180303)购自西安药材市场(药材产地为内蒙古),经陕西中医药大学药学院王薇教授鉴定为菊科植物款冬(Tussilago farfaraL.)的干燥花蕾。
2 方法与结果
2.1TLC鉴别
取款冬花配方颗粒1 g,研细,加甲醇10 mL,超声(功率:300 W,频率:40 kHz,下同)处理1.5 h,滤过,蒸干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液。另取款冬花饮片1 g,加乙醇10 mL,超声提取1.5 h,滤过,蒸干,残渣加乙酸乙酯1 mL使溶解,作为饮片样品溶液。取款冬花对照药材1 g,按饮片样品溶液制备方法制成款冬花对照药材溶液。另取款冬酮对照品5 mg,加乙酸乙酯5 mL,制成质量浓度为1 mg/mL的对照品溶液。取缺款冬花的阴性样品1 g,按供试品溶液制备方法制成阴性对照溶液。按2015年版《中国药典》(四部)通则中“TLC法”[3]操作,吸取上述5种溶液各5 μL,分别点于同一硅胶GF254薄层板上,以石油醚(60~90 ℃)-丙酮(10∶1,V/V)为展开剂(温度为21 ℃,湿度为47%),展开,取出,晾干,再以同一展开剂展开,取出,晾干,置于紫外光灯(254 nm)下检视,再喷以硫酸-乙醇溶液,加热至斑点清晰,记录斑点位置。结果,供试品色谱中,在与对照药材相应位置上显相同颜色的斑点,阴性对照无干扰,详见图1。

图1 薄层色谱图Fig 1 TLC chromatograms
2.2 含量测定
2.2.1 色谱条件 色谱柱:Thermo ODS Hypersil C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(85∶15,V/V);流速:1.0 mL/min;检测波长:220 nm;柱温:25℃;进样量:20 μL。
2.2.2 对照品溶液的制备 精密称取款冬酮对照品11.20 mg(实际质量为11.10 mg),加流动相适量,制成质量浓度为27.75 μg/mL的对照品溶液。
2.2.3 供试品溶液的制备 取款冬花配方颗粒1 g,精密称定,置于具塞锥形瓶中,加甲醇10 mL,称定质量,超声处理1.5 h,放冷,再次称定质量,用甲醇补足减失的质量,滤过,取续滤液,即得。
2.2.4 阴性对照溶液的制备 取缺款冬花的阴性样品1 g,按“2.2.3”项下方法制备阴性对照溶液,即得。
2.2.5 系统适用性试验 取上述对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.2.1”项下色谱条件进样测定,记录色谱图,详见图2。结果,在上述色谱条件下,理论板数按款冬酮峰计不低于5 000,分离度>1.5,其他成分对测定无干扰。
2.2.6 线性关系考察 取“2.2.2”项下对照品溶液0.5、1、2、4、8、10 mL,分别置于10 mL量瓶中,加甲醇稀释至刻度,摇匀,得质量浓度分别为1.39、2.78、5.55、11.10、22.20、27.75 μg/mL的系列线性关系标准溶液,取适量,按“2.2.1”项下色谱条件进样测定,记录色谱图。以待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得款冬酮的回归方程为y=43 103.13x+33.58(r=0.999 9)。结果,款冬酮检测质量浓度线性范围为1.39~27.75 μg/mL。
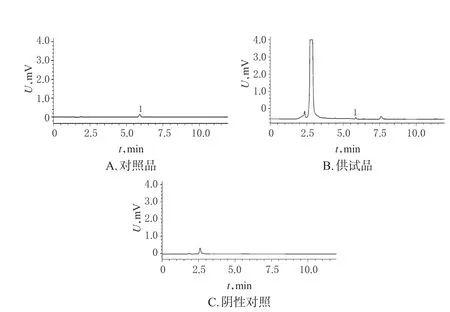
图2 高效液相色谱图Fig 2 HPLC chromatograms
2.2.7 定量限与检测限考察 取“2.2.2”项下对照品溶液适量,倍比稀释,以信噪比10∶1、3∶1分别测定定量限、检测限。结果,款冬酮的定量限为0.153 87 μg/mL,检测限为0.051 42 μg/mL。
2.2.8 精密度试验 取“2.2.2”项下对照品溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,款冬酮峰面积的RSD为0.94%(n=6),表明仪器精密度良好。
2.2.9 稳定性试验 取“2.2.3”项下供试品溶液(批号:180402)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,款冬酮峰面积的RSD为0.86%(n=6),表明供试品溶液于室温下放置24 h内基本稳定。
2.2.10 重复性试验 取配方颗粒样品适量(批号:180402),按“2.2.3”项下方法制备供试品溶液,共6份,再按“2.2.1”项下色谱条件进样测定,记录峰面积并按回归方程计算样品中款冬酮的含量。结果,款冬酮的平均含量为0.003 2%,RSD为1.88%(n=6),表明本方法重复性良好。
2.2.11 加样回收率试验 取已知含量的配方颗粒样品(批号:180402)适量,共6份,精密称定,分别加入一定量的款冬酮对照品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。
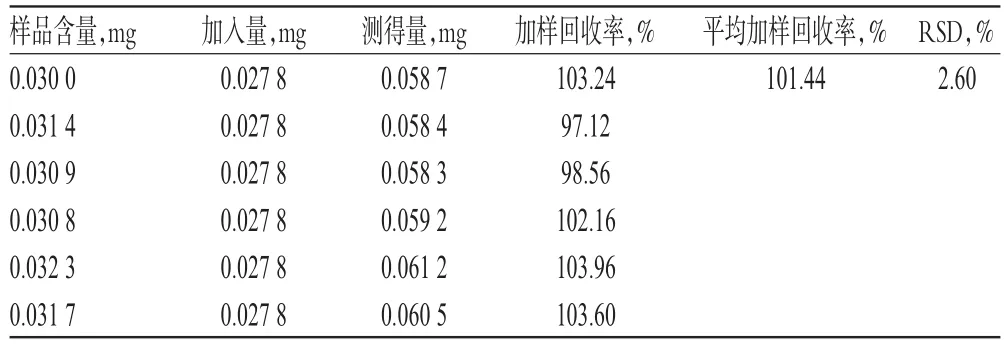
表1 加样回收率试验结果(n=6)Tab 1 Results of recovery tests(n=6)
2.2.12 耐用性试验 精密称取配方颗粒样品(批号:180402)适量,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,考察不同色谱柱(Thermo ODS Hypersil C18、Agilent TC-C18、Hyperil BDS C18)、流速(0.8、1.0、1.2 mL/min)、柱温(20、25、30 ℃)对样品含量测定结果的影响,结果见表2。结果表明,当色谱柱、流速和柱温发生一定程度变化时,本方法能满足试验要求,本方法耐用性良好。
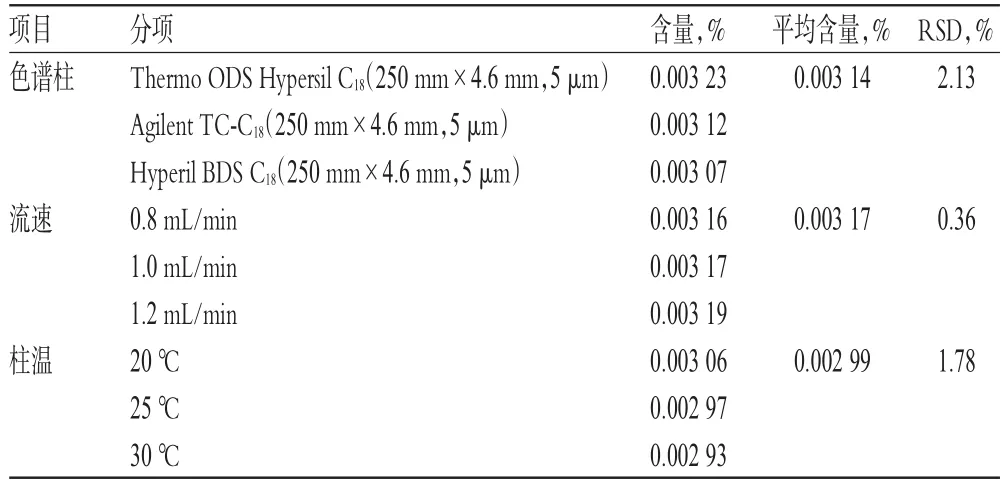
表2 耐用性试验结果Tab 2 Results of durability tests
2.2.13 样品含量测定 取3批配方颗粒样品各适量,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并按回归方程计算样品含量,结果见表3。
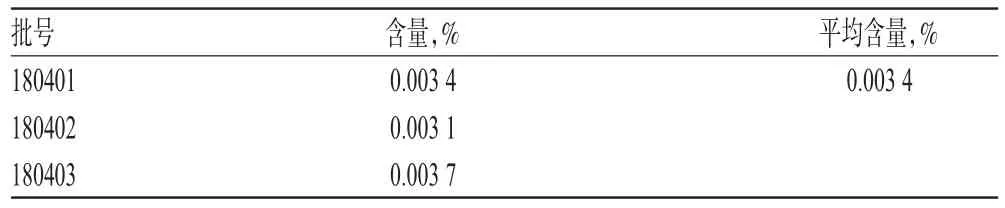
表3 样品含量测定结果(n=3)Tab 3 Results of content determination of samples(n=3)
3 讨论
现代药理学研究表明,款冬花除具有止咳祛痰[4-5]、平喘[6]、抗炎[7-10]、抗氧化[11-13]、抗肿瘤[14-15]、止泻[7]等作
用外,对心血管、血流动力学及血小板活化因子亦具有一定的影响[16]。近年来,配方颗粒等现代中药用药形式的出现,弥补了传统中药汤剂的服用量大、不易携带、不易保存等缺陷[17-18]。款冬花配方颗粒保持了款冬花饮片的性味与功效,可直接用于中医辨证施治,具有不需煎煮、服用方便、吸收迅速、剂量准确、安全清洁、携带方便等优点[19];但目前尚缺乏统一的质量标准。为此,本研究采用TLC法对款冬花配方颗粒进行定性鉴别,采用HPLC法测定了款冬花配方颗粒中款冬酮的含量。
本研究采用2015年版《中国药典》(一部)[20]方法进行TLC,但发现以石油醚-丙酮(6∶1,V/V)为展开剂时极性偏大,主要斑点靠近展开前沿,因此笔者在参考2015年版《中国药典》(一部)[20]TLC法的基础上,将石油醚-丙酮的极性调小(体积比为10∶1),后发现款冬花配方颗粒中主要斑点分离度良好,斑点清晰。
在指标成分选择方面,有文献以芦丁为指标成分[21],但芦丁既不是款冬花含量较高的成分,也不是其专属成分,考虑到款冬酮是款冬花的特征成分,且该成分具有抗炎、升压等药理作用[22]。因此,本研究以款冬酮为款冬花配方颗粒的指标成分进行含量测定。但在研究过程中笔者发现,款冬酮在款冬花配方颗粒中含量较低。其原因可能为:一方面,款冬酮在款冬花药材中含量较低,2015年版《中国药典》(一部)中规定,款冬花药材中款冬酮含量不得少于0.070%[20];另一方面,因款冬酮为亲脂性成分,而款冬花配方颗粒在制备时以水为提取溶剂,因此导致部分款冬酮未被提取出来,以致其在款冬花配方颗粒中含量较低。笔者认为,款冬酮作为款冬花中的特征成分,目前可作为款冬花配方颗粒含量测定的控制项;但同时因其含量较低,故有必要寻找款冬花中其他含量较高的特征成分以替代款冬酮对其进行含量控制。TLC结果显示,在款冬花药材、饮片样品及款冬花配方颗粒TLC图谱中,均出现了一个与款冬酮显相似颜色的清晰斑点(图1B中位于款冬酮上方最为清晰的斑点),该斑点是否为款冬酮的类似物,以及是否可作为款冬花配方颗粒含量测定的指标性成分仍有待后续研究进一步探讨。
综上所述,本研究方法操作简单、准确、重复性好,可用于款冬花配方颗粒的质量控制。
