铁过载在糖尿病发病机制中的研究进展
2019-08-12石彦波
熊 烈 宁 帆 石彦波
糖尿病已是威胁全球人类健康的严重疾病,近几年来更是在全世界范围内呈爆发式增长,中国糖尿病患病率从1980年的0.67%飙升至2013年的10.4%[1]。我国糖尿病患者数量已高达1.5亿人,是世界上糖尿病患者人数最多的国家之一。
近年来的一些研究发现,机体内铁的过多蓄积可以增加2型糖尿病的发生率,同时由铁过载导致的各类损伤也可诱导糖尿病并发症的发生。
一、铁代谢的稳态及失衡
1.铁代谢稳态:铁是人体内含量最多的微量元素,几乎在机体所有组织都有分布,一般成年人体内含铁3~5g。它是合成血红蛋白、肌红蛋白的主要原料之一,其中60%的铁元素在血红蛋白中,10%的铁元素在肌红蛋白中;同时铁还是机体氧化还原反应系统中一些重要生物酶的辅酶,广泛参与氧的运输、氧化还原反应、细胞增殖与分化、基因表达的调控等基本生命过程[2]。因此,铁在机体内发挥着重要的生理功能,铁元素的稳态代谢平衡对于机体有着重要的意义,许多疾病都与铁稳态失衡密切相关。
正常情况下,机体内的铁元素受控于复杂而严密的网络调控体系之中,处于一种动态平衡状态,主要包括吸收、利用、循环、储存、流失等五大环节[3],如图1所示。
2.铁过载:铁过载是一种常见的铁代谢失衡状态,与许多疾病的发生、发展密切关联。铁离子由于存在2价与3价两种形式,在机体内易被氧化或还原,并且这一过程是可逆的。正是由于这种特性,铁对机体代谢至关重要;但也正是因为这种特性,导致了铁具有参与产生氧化自由基的能力,使其具有危害性。在正常机体内,Fe3+与铁蛋白结合并以此参与铁的运输与储存,这可以避免其参与产生氧化自由基;但当机体内铁过载时,大量铁离子被释放,发生Haber-Weiss反应产生大量氧化自由基[4]:
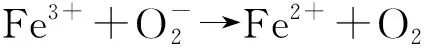

此外,由于铁作为许多生物酶的辅酶,广泛参与人体各种酶促反应,铁过载导致的酶促反应异常也会对人体产生巨大的危害。
通常铁过载存在两种表现形式:(1)由于铁摄入超量,血浆铁超过转铁蛋白结合限度,铁沉积在肝脏、心脏和内分泌组织等处。(2)过量衰老及受损红细胞被巨噬细胞吞噬,红细胞溶解后血红蛋白分解释放铁,一部分储存在巨噬细胞内,过量部分进入血液从而造成铁过载[5]。

图1 机体的铁代谢吸收.十二指肠以1~2mg/d的速率从食物中吸收铁;利用.骨髓红细胞是铁最主要的去处,大约以20~25mg/d的速率将铁用于合成血红蛋白;循环.巨噬细胞以20~25mg/d的速率通过吞噬红细胞分解血红素将铁从衰老受损的红细胞中回收;储存.铁主要以铁蛋白的形式进行储存,以肝脏约1000mg,巨噬细胞约600mg为主;流失.正常情况下,铁主要通过出汗、肠上皮细胞脱落而流失,速率在1~2mg/d
二、铁过载与糖尿病
铁过载是糖尿病的一个风险因素,二者的关联性最早是在遗传性血色素沉着症(1997年)和地中海贫血(1988年)中被发现[6,7]。前者主要由于胃肠道铁吸收能力增强,从而增加了体内铁的含量;后者主要由于需要大量输血维持红细胞数量,过量红细胞衰老后血红蛋白中的铁被释放导致了铁过载。随着病情的发展,上述两种疾病中有相当比例的患者最终发展成为2型糖尿病[8]。后来研究发现,当未患有这两种疾病时,单纯的铁过载,如日常饮食摄入过量铁,依旧与2型糖尿病发生率存在着正相关[9]。
Tuomainen等[10]早在1997年的人群研究中就发现,体内铁储存量的增加与血糖升高存在显著相关性。此后,Ford等[11]在1999年的人群研究中提出了血清铁蛋白的升高与糖尿病风险增加有关的假设。因此,近年来越来越多的研究显示铁代谢稳态失衡是糖尿病的风险因素之一,甚至最新研究认为铁代谢与妊娠期糖尿病密切相关[12,13]。
铁过载导致2型糖尿病的因素有很多,目前主要认为是胰岛β细胞损伤、胰岛素抵抗和肝功能障碍是最主要的因素。
1.铁过载与胰岛β细胞损伤:如图2A所示。在胰岛β细胞中,铁诱导ATP和ROS的合成是葡萄糖刺激胰岛素分泌的必要条件,因此维持铁代谢稳态对于胰岛β细胞分泌胰岛素是至关重要的[14,15]。正是由于ROS对于调节胰岛素合成与分泌的重要性,胰岛细胞抗氧化酶和铁蛋白的表达量均较低,这意味着其更容易受到铁过载带来的氧化损伤[16]。与之相对的是,有研究发现胰岛β细胞能够表达铁代谢中的关键因子——Hepcidin(铁调素),从而缓解铁过载状态,维持铁代谢稳态[17,18]。因此,当胰岛β细胞内铁代谢稳态被破坏时铁过载对其造成的氧化损伤将会更大,Cooksey等[19]在血红蛋白沉着小鼠模型上印证了这样的观点。总之,铁过载会促进胰岛细胞凋亡、胰岛细胞分化障碍以及胰岛素分泌的减少[20]。
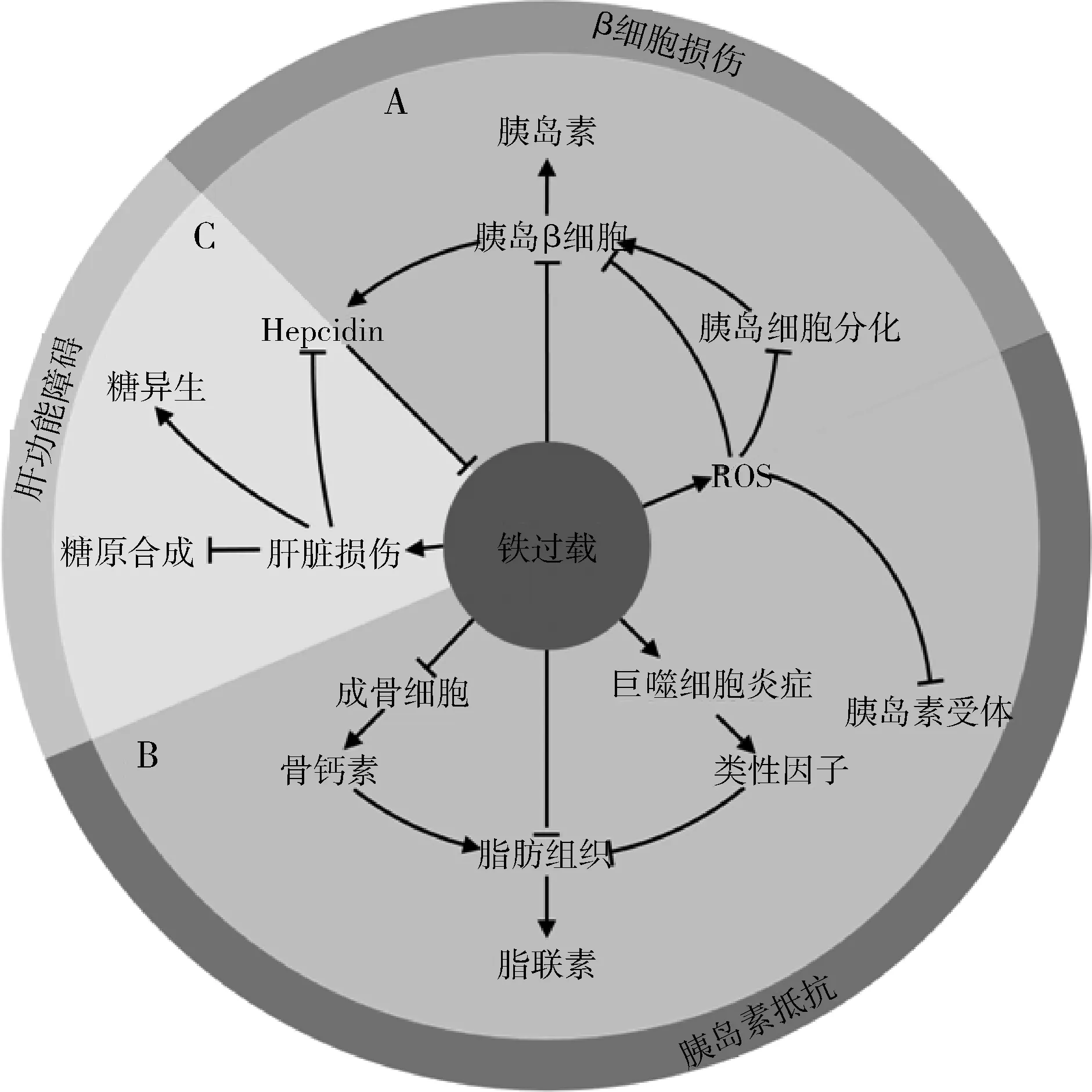
图2 铁过载引起糖尿病机制的示意图
2.铁过载与胰岛素抵抗:如图2B所示。铁过载诱导的胰岛素抵抗主要表现在脂联素的减少以及抑制胰岛素受体两个方面。
脂联素是一种脂肪组织分泌的脂肪因子,增强胰岛素敏感度是其关键作用之一,脂联素表达量的减少往往导致胰岛素抵抗的发生。铁过载主要从3个方面影响脂联素的分泌:(1)脂肪组织内的铁过载可以直接影响其功能,导致脂联素分泌减少,这可能与铁通过FOXO-1介导负调控脂联素有关[21,22]。(2)骨钙素由成骨细胞合成并分泌,可以促进脂肪细胞分泌脂联素,Yang等[23]开展的成骨细胞体外实验证明铁暴露将导致骨钙素表达的减少,Juanolafalgarona等[24]的人群研究也发现铁的累积与骨钙素的降低有关。(3)巨噬细胞在铁的回收与储存中起着关键作用,其铁过载将导致肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、白细胞介素-1β(IL-1β)等炎性因子分泌增加,最终抑制脂联素的表达[24,25]。
胰岛素受体敏感度也是铁过载导致胰岛素抵抗的另一大重要原因。铁过载带来的ROS通过LKB1/AMPK通路抑制胰岛素受体在肝脏、脂肪组织、肌肉等器官中的磷酸化,降低其敏感度[26]。
3.铁过载与肝功能障碍:肝脏在机体铁代谢中的重要作用是毋庸置疑的,它既是Hepcidin合成分泌的主要场所,同时也是机体储存铁的主要器官,因此铁过载对其造成的损伤也较为明显,肝纤维化是导致肝功能障碍的重要原因之一,能够引起慢性肝脏损伤的疾病基本上均伴有不同程度的肝纤维化。在各种损伤因素的交互作用下纤维化程度逐渐加重,最终可引起肝硬化,出现肝衰竭和死亡。然而肝纤维化的机制至今尚未完全阐明。近年来研究表明,各种导致肝纤维化的慢性肝病均与肝脏铁代谢紊乱有关,肝脏过多的铁沉积在肝纤维化发生、发展过程中起重要作用。尤其是铁的负性调节激素hepcidin表达的减少与各种慢性肝纤维化疾病铁代谢紊乱的发生密切相关,如图2C所示。在糖代谢方面,主要表现为铁过载会破坏胰岛素对肝脏糖异生的抑制作用以及抑制肝糖原的合成,导致血糖升高[27,28]。
4.糖尿病与铁过载:铁过载与糖尿病之间的关联,不仅铁过载会增加糖尿病的患病风险,也有研究显示糖尿病会导致铁代谢稳态破坏造成铁过载,从而形成一个恶性循环。这样的恶性循环在血多由糖尿病引发的并发症的发生、发展中起到了促进作用。Batchuluun等[29]进行了一项关于55岁以上糖尿病患者血清铁蛋白的研究,发现该类人群普遍显著高于正常群体。至于糖尿病患者为何会普遍铁过载,有研究认为糖尿病患者实际处于一种慢性炎性状态,炎性因子会影响铁代谢稳态,诱导铁在实质器官中累积,进一步加强铁过载[30]。这也是为何糖尿病患者晚期并发症往往存在着局部或全身性的实质性器官铁过载的状态。
三、展 望
综上所述,铁过载是糖尿病患病风险因素之一,其导致糖尿病发生、发展的机制主要包括:(1)铁过载引起的胰岛细胞氧化损伤,导致胰岛素分泌减少、抑制胰岛细胞分化以及降低β细胞对血糖刺激的敏感度。(2)铁过载通过直接与间接途径降低脂联素的表达,并且ROS带来的损伤降低胰岛素受体对胰岛素的敏感度。(3)铁过载将破坏胰岛素对肝脏糖异生的抑制作用以及抑制肝糖原的合成,使肝糖输出过量。(4)由于糖尿病患者处于一种慢性炎性状态,炎症因子将影响铁代谢稳态,诱导铁在实质器官中的累积,形成恶性循环。
