评价一种新CYP2C9突变型对药物代谢的影响
2019-08-12亢奋恒张博文戴大鹏李传宝蔡剑平
亢奋恒 张博文 戴大鹏 李传宝 蔡剑平
研究报道称细胞色素P2C9(CYP2C9)是人类最重要的药物代谢酶。细胞色素P2C9是P450酶家族中的重要成员,是肝微粒体中一种十分重要的药物代谢酶,催化10%~20%临床常用药物在肝内的代谢[1,2]。大量研究表明,细胞色素P2C9具有众多等位基因,大部分突变体蛋白的活性呈现明显下降,是引起某些药物代谢能力个体差异的重要原因[3,4]。
在1例常年口服低剂量(1.5~2.0mg/d)华法林患者体内发现了一种的新的细胞色素P450 2C9变异型,在1号外显子32位发生了T>C突变,引起Leu11>Pro11的氨基酸改变。为探究其催化能力是否发生明显改变,本研究引入甲苯磺丁脲作为探针药。根据以往研究,作为其重要代谢底物之一的甲苯磺丁脲,在人体内代谢途径单一,几乎均由肝细胞色素P2C9催化代谢,是绝大多数细胞色素P2C9研究者必选的探针药[5,6]。
现有研究表明,中国人群中最常见的细胞色素P2C9缺陷型突变体为细胞色素P2C9*3和*13,其中以*3最为多见,故本研究引入野生型* 1和突变型* 3 作为参照,通过对比3种细胞色素P2C9对底物药甲苯磺丁脲的催化速率,以期指导该等位基因携带者的个体化用药。
材料与方法
1.材料:(1)主要试剂:Trans5α化学感受态细胞(北京全式金生物技术有限公司);DH10 Bac化学感受态细胞(美国 Invitrogen公司);Spodoptera frugiperda昆虫细胞,Sf-900TMⅢSFM昆虫细胞培养基,胎牛血清及Bac-to-Bac Baculovirus Expression System(美国Invitrogen公司),Prime STAR MAX DNA聚合酶、DNA连接试剂盒(日本TaKaRa公司),商业化CYP2C9微粒体及细胞色素b5微粒体(美国BD Gentest公司),兔抗人CYP2C9多克隆抗体(英国AbD serotec公司),小鼠抗人OR单克隆抗体(美国Santa Cruz公司),HRP标记的羊抗兔及羊抗鼠二抗(北京中杉金桥公司),蛋白定量及ECL显色kit(美国Pierce公司),甲苯磺丁脲(美国Sigma公司),4-Hydroxytolbutamide(加拿大Toronto Research Chemicals公司),NADPH生成系统(北京汇智泰康医药技术有限公司),HPLC级溶剂(美国Fisher Scientific公司),其余常规试剂均为优级纯或分析纯。(2)主要仪器:冷冻离心机、高速冷冻离心机(日本Kubota公司),PCR扩增仪(美国ABI公司)、细胞超声破碎仪(美国 Sonic公司),电泳仪及水平电泳槽(美国Bio-Rad公司)、Tanon 5200化学发光成像系统(上海天能科技有限公司),Agilent 1200高效液相色谱仪(美国Agilent公司),所用常规耗材均购自美国Axygen公司。
2.CYP2C9基因定点诱变和ORF区扩增引物设计:根据NCBI公布的CYP2C9全基因组序列(NM 000771.3),利用Primer 5.0软件设计开放阅读框(ORF)区扩增引物、突变位点相应的上下游寡核苷酸引物(分别命名为-2F和-1R)以及测序引物(表1),引物由北京天一辉远公司合成。
3.pFastBac-dual-OR-2C9双表达载体的构建:将美国Origen公司购买的细胞色素P450氧化还原酶(CYPOR)的ORF区扩增,扩增产物切胶回收,回收之后进行XhoⅠ/KpnⅠ双酶切,再将产物与同样双酶切的空载体 pFastBac-dual连接,即获得可接收 CYP2C9 扩增产物的中间载体pFastBac-dual-OR。利用重叠延伸PCR技术,以细胞色素P2C9*1质粒为模板,获得细胞色素P2C9*3、细胞色素P2C9(32T>C)的cDNA全长[7,8]。将细胞色素P2C9的cDNA区扩增产物切胶回收后进行EcoRΙ/SalΙ双酶切,与同样酶切的中间载体pFastbac-dual-OR(含CYPOR的结构基因)连接,连接产物转化Trans5α化学感受态细胞后用PCR法筛选阳性克隆,挑取阳性克隆隔夜摇菌,提取质粒后送北京天一辉远公司进行序列测定,以确认所获载体中定点诱变位点碱基与设计完全一致。

表1 构建CYP2C9重组质粒载体的引物
下划线处序列为限制性内切酶切割位点,下划线处碱基为突变位点;CYP2C9(32T>C)突变位点为1号外显子第32位,CYP2C9*3突变位点为7号外显子第1075位
4.杆粒载体Bacmid-OR-CYP2C9s的制备及PCR验证:阳性重组质粒转化DH10bac感受态细胞以后,筛选阳性克隆,挑取阳性克隆隔夜摇菌,利用杆状病毒穿梭载体bacmid抽提试剂盒提取重组杆粒DNA,并进行PCR验证,验证所用引物如下(表2)。

表2 对重组杆粒载体进行PCR验证的正向和反向引物
5.杆状病毒的获得和增殖:参照Bac-to-Bac Baculovirus Expression System试剂盒使用说明,包装Bacmid-OR-CYP2C9昆虫病毒,所获病毒侵染伪黏虫卵巢细胞,观察细胞在不同生长阶段的特征(表3),在转染后期阶段收集P1代病毒,利用获得的P1代病毒继续扩增产生P2代病毒。

表3 病毒侵染后的伪黏虫卵巢细胞不同生长阶段显微镜下特征
6.高表达细胞色素P2C9昆虫微粒体的获得:将P2代病毒上清继续培养,72h后离心收集细胞,洗涤后重悬于5ml重悬液(0.25mol/L蔗糖,1mmol/L EDTA,0.5mmol/L PMSF)中,利用超声破碎仪进行破碎,破碎产物经12000g 离心后去除细胞碎片,将得到的上清经100000g超速离心,再将得到的沉淀物(微粒体)重悬于微粒体储存液中,冻存于-80℃冰箱。
7.使用免疫印迹法对重组细胞色素P2C9突变型蛋白进行鉴定:用BCA法测定微粒体蛋白浓度,取5μg进行SDS-聚丙烯酰胺凝胶电泳,电泳结束后样品转移至PVDF膜,用封闭液封闭,封闭后进行一抗孵育(一抗选择兔抗人CYP2C9抗体和鼠抗人CYPOR抗体),4℃条件下孵育过夜,次日将PVDF膜取出洗涤后进行二抗孵育(二抗选择山羊抗兔IgG和山羊抗鼠IgG),滴加曝光液后用化学发光图像分析系统进行检测。
8.LCMS/MS检测细胞色素P2C9对甲苯磺丁脲的代谢:(1)催化体系:由重组细胞色素P2C9蛋白、细胞色素b5、NADPH辅酶、Tris-HCl以及甲苯磺丁脲组成200μl反应体系。(2)催化过程:37℃孵育1h后,加入氯磺丙脲和HCl,置于涡旋震荡器震荡 2min,加入冰乙酸乙酯继续涡旋震荡2min,离心后转移有机层,用氮吹仪吹干,加入100μl流动相复溶并取20μl于Agilent 1200高效液相色谱仪检测。(3)色谱检测条件:色谱柱为ZORBAX EclipseXDB-C18柱(4.6mm×150.0mm,5μm,美国Agilent公司),流动相为0.05%TFA∶乙腈=70∶30,流速为0.4ml/min,柱温40℃,上样体积为2μl,内标为氯磺丙脲。(4)最大反应速度Vm及米氏常数Km值的计算:根据标准曲线,将代谢产物4-Hydroxytolbutamide定量后,利用Prism软件(version 5,美国GraphPad公司)计算Vm、Km值以及清除率(Vm/Km)。
结 果
1.对新细胞色素P2C9突变体重组质粒进行测序验证:以CYP2C9-EF和CYP2C9-SR为引物,将提取的pFastBac-dual-OR-2C9重组质粒送北京天一辉远公司测序,测序结果用Oligo7软件进行序列分析,箭头所指处显示,碱基T→C诱变成功(图1)。
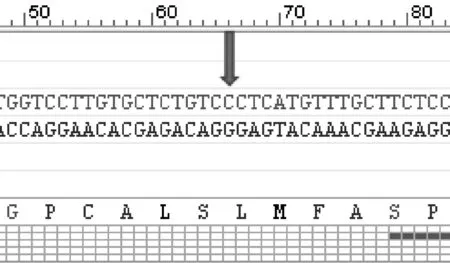
图1 细胞色素P2C9新突变型重组质粒测序结果
2.利用琼脂糖凝胶电泳技术对重组质粒载体进行鉴定:将提取的pFastBac-dual-OR-2C9重组质粒进行PCR扩增,产物经琼脂糖凝胶电泳,大小约1500bp(图2)。
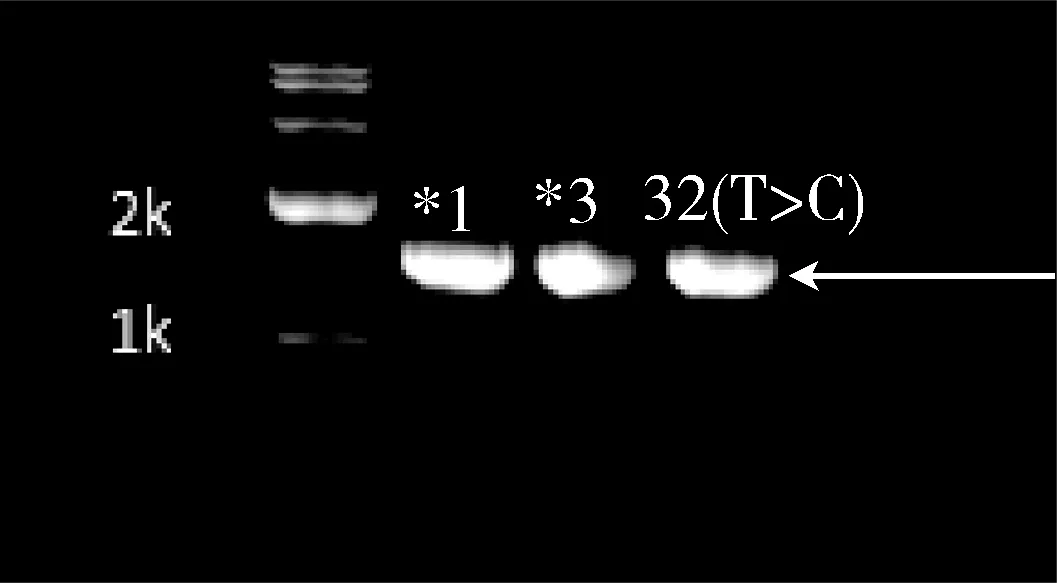
图2 重组细胞色素P2C9质粒载体PCR产物琼脂糖凝胶电泳结果
3.使用免疫印迹法对重组细胞色素P2C9突变型蛋白进行定性检测:免疫印迹结果显示,在同一张PVDF膜55000与78000左右出现以下两个条带(图3),与目标蛋白相对分子质量接近,箭头以上条带为细胞色素P2C9(相对分子质量约为53000~55000),箭头以下条带为细胞色素P450氧化还原酶(相对分子质量约为78000)。
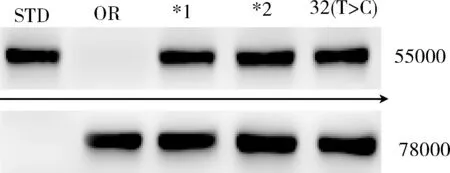
图3 免疫印迹法检测重组细胞色素P2C9微粒体蛋白STD.购自美国BD Gentest公司的CYPC29标准品;OR.只表达细胞色素P450氧化还原酶的阴性对照
4.使用免疫印迹法对重组细胞色素P2C9突变型蛋白进行定量检测:将美国BD Gentest公司购买的细胞色素P2C9*1微粒体标准品梯度稀释为2.4、1.2、0.6和0.3pmol/μl 4种不同浓度(图4),利用Image J软件进行灰度分析后,经对比定量计算,重组微粒体细胞色素P2C9*1、重组细胞色素P2C9*3、重组细胞色素P2C9(32T>C)浓度分别为:2.256、2.103、2.434pmol/μl。

图4 免疫印迹法对重组细胞色素P2C9进行定量检测S1~S4分别为2.4、1.2、0.6、0.3pmol/μl 4种不同浓度的CYP2C9标准品
5.细胞色素P2C9(32T>C)对甲苯磺丁脲的催化活性:体外代谢检测结果表明,细胞色素P2C9(32T>C)对于甲苯磺丁脲的清除率为野生型*1的12.40%,差异有统计学意义(表4)。细胞色素P2C9(32T>C)对甲苯磺丁脲的清除率明显低于野生型,接近典型突变型*3(图5)。

表4 细胞色素P2C9催化甲苯磺丁脲代谢的酶动力学参数
与CYP2C9*1比较,*P<0.05
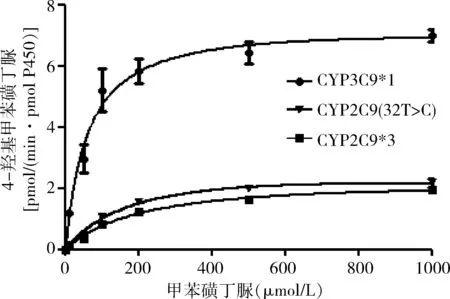
图5 细胞色素P2C9催化甲苯磺丁脲的酶促动力学曲线图
讨 论
作为人体肝脏中一种非常重要的药物代谢酶,细胞色素P2C9不仅含量丰富(约占细胞色素P450总量的20%),而且可以催化众多不同类型药物的代谢[9~12]。从中选择哪些药物作为研究的底物药,是首先要考虑的问题。虽然该突变型是从1例华法林慢代谢型患者身上发现的,但由于人体对华法林的代谢受多种因素影响,除了细胞色素P2C9以外,VKORC1的基因多态性也具有重要影响[13,14]。本研究仅对携带者CYP2C9基因编码区的9个外显子进行测序,并不知道VKORC1等基因的变异情况。因此,单独研究细胞色素P2C9对华法林的代谢功能,对于患者个体化用药的指导意义并不是很大。相比之下,甲苯磺丁脲在人体内代谢途径单一,80%以上在肝内被细胞色素P2C9羟化代谢,是体外研究细胞色素P2C9活性的绝佳底物药[15]。
与其他细胞色素P450家族比较,细胞色素P2C9的等位基因在人群中存在高度的遗传多态性,目前已被统计命名的有60种,其中最常见的突变型是*2和*3,它们和野生型细胞色素P2C9*1是目前研究最多的3种型别[16~19]。中国人群中最常见的突变类型是*3与*13,其中以*3最为多见,故本项研究选择了我国人群中最多见的细胞色素P2C9基因型*1和*3作为参照,通过对比对细胞色素P2C9(32T>C)新突变型的催化功能作出评价。
Western blot法检测结果表明,细胞色素P2C9(32T>C)的蛋白表达量与野生型比较,差异无统计学意义,说明该变异基因并未影响蛋白质的正常表达。体外药物代谢检测结果显示,细胞色素P2C9*3的清除率为9.09%,与以往研究结果相似,说明在同等条件下测得的细胞色素P2C9(32T>C)的催化活性具有一定的可信度。细胞色素P2C9(32T>C)对于探针药物甲苯磺丁脲的体外清除率为细胞色素P2C9野生型的12.40%,略高于细胞色素P2C9*3(表4)。酶促反应曲线显示细胞色素P2C9(32T>C)对甲苯磺丁脲的催化能力接近于典型突变型细胞色素P2C9*3,酶学活性明显下降,提示携带该基因型的患者服用经由细胞色素P2C9代谢的药物时,体内药物代谢速率可能会发生不同程度的降低,用药时忽视这一点可能会造成药物在体内蓄积,引发不良反应甚至毒性反应(图5)。
以往研究表明,细胞色素P2C9的催化作用具有底物依赖性,即对不同底物呈现出不同程度的活性改变,提示细胞色素P2C9(32T>C)在催化其他种类药物代谢时可能会表现出不同的活性。本项研究选用细胞色素P2C9的特异性探针药甲苯磺丁脲作为检测活性的底物药,虽然对临床用药具有重要的指导作用,但仍然有必要开展大量体内及体外实验进一步全面研究该突变型的催化功能。
