脑血管支架置入术后再狭窄的危险因素分析▲
2019-07-22梅育嘉罗杰峰许红玉
梅育嘉 罗杰峰* 许红玉
(1 广西医科大学第二附属医院神经内科,南宁市 530007;2 广西壮族自治区民族医院神经内科,南宁市 530001)
近年来,脑血管疾病的发生率及致残率居高不下,而支架置入是其首选的治疗方法之一[1-2]。支架内再狭窄(ISR)是支架置入术后的一个严重并发症,其发生与相应脑动脉供血区域的脑卒中显著相关[3]。研究发现,颅内外支架置入术后随访期的ISR概率约为30%[4],ISR的评估、预防及控制仍是一个难题。本研究通过分析脑血管支架置入术后ISR的危险因素,以期指导评估ISR的风险并加以控制,降低再狭窄发生率。现将结果报告如下。
1 资料与方法
1.1 一般资料 选择2013年5月至2017年9月在广西医科大学第一附属医院神经内科经数字减影血管造影(digital substraction angiography,DSA)、CT血管造影(CT angiography,CTA)确诊的脑动脉狭窄患者86例为观察对象,其中17例患者同时行双侧脑血管支架置入术治疗,按2例单独病例进行计算,故实际统计为103例,其中男82例,女21例;年龄34~88(63.0±11.2)岁。出院后1~60个月再住院复查DSA、CTA,其中2次住院者49例,3次住院者5例,以ISR为终点事件,分为对照组69例和再狭窄组34例,发生再狭窄的中位时间为24个月。
1.2 纳入及排除标准 纳入标准:(1)支架置入术选择、围术期及术后抗血小板方案均符合《中国缺血性脑血管病血管内介入诊疗指南(2015)》;(2)术后血管残余狭窄<30%;(3)支架内、两端或支架体内+两端管腔内径狭窄≥50%。排除标准:(1)术后血管残余狭窄≥30%;(2)支架严重变形、断裂所致的狭窄。
1.3 资料采集 按照纳入、排除标准,搜集数据并记录基本资料,如年龄、性别、并发症、手术相关信息、支架类型以及血液生化指标、全脑DSA、CTA等资料。血管狭窄率参照WASID计算法,多次住院患者的血液生化指标取平均值。

2 结 果
2.1 单因素分析 两组平均血小板体积(MPV)、嗜烟酒、基底动脉比较,P<0.1,可能与再狭窄相关。两组年龄、性别、并发症、同型半胱氨酸水平(Hcy)、血小板(PLT)等指标比较,差异无统计学意义(P>0.05)。见表1。

表1 两组单因素分析结果
续表1

项 目再狭窄组(n=34)对照组(n=69)t/χ2值P值 颈内动脉[n(%)]14(41.2)28(40.6)0.0060.954 颈总动脉[n(%)]4(11.8)4(5.8)0.1050.287 开口与否[n(%)]27(79.4)52(75.4)0.0450.648 支架长度(mm)25.6±11.324.1±10.40.6290.531 支架内径(mm)6.2±2.55.9±2.40.6930.490 支架重叠[n(%)]4(11.8)12(17.4)0.0730.458 支架扩张方式[n(%)] 球扩支架6(17.6)12(17.4)0.0040.999 自膨支架25(73.5)51(73.9) 球扩支架+自膨支架3(8.8)6(8.7)
2.2.2 COX比例风险回归模型 经计数资料双变量相关性检验提示,MPV与PLT相关系数=-0.393且P<0.001,PLT与Pct相关性P<0.001,MPV与Fbs相关性P=0.002,之间显著相关。为减少共线性干扰,保留主要参数MPV,删除共线性参数PLT、Pct、Fbs。采用向前LR法,0阶迭代数据作为单因素分析数据,与再狭窄显著相关的因素有MPV(P=0.022)、基底动脉(P=0.008)、嗜烟酒(P=0.095);向前LR法COX回归分析,2次迭代后建模,保留显著相关参数MPV、基底动脉。见表2。

表2 影响椎动脉起始段支架置入术后再狭窄的多因素分析
向后LR法COX回归分析,19次迭代后建模,保留较显著相关参数基底动脉、MPV、性别、年龄。见表3。

表3 影响椎动脉起始段支架置入术后再狭窄的多因素分析
按参数设置男性=1,女性=0;基底动脉=1,非基底动脉=0。基底动脉部位支架相对风险HR大于1,是再狭窄危险因素。见图1。性别HR<1,女性再狭窄风险较男性大。MPV的HR<1,所以MPV值增大是保护性因素,也可以说MPV减小是再狭窄的危险因素。年龄的HR>1,所以高龄是再狭窄的危险因素。向前法模型χ2=11.491,P=0.003;向后法模型χ2=15.913,P=0.003。向前法模型较向后法模型拟合数据更好。
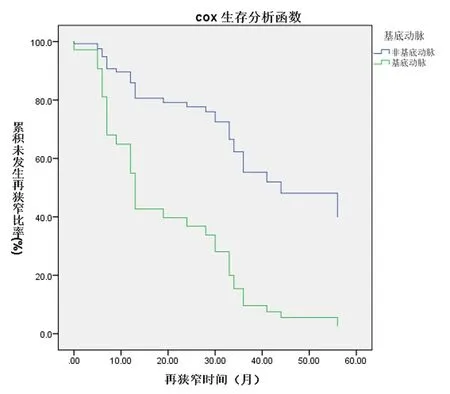
图1 基底动脉再狭窄发生情况
3 讨 论
支架置入术后再狭窄是脑血管病血管内治疗的一个重大难题。ISR早期与血管弹性回缩、血管壁夹层动脉瘤有关,亚急性期与血栓形成有关,晚期则与血管平滑肌细胞的增殖、迁移有关。新生内膜形成、平滑肌细胞增殖是ISR的主要病理机制。支架术后几天至几周内,由于血管机械性扩张,粥样斑块与正常血管交界处断裂,内皮下成分暴露,植入部位血小板黏附、聚集、血栓形成及血管炎性反应,几周后平滑肌细胞发生表型转化,转化为肌纤维母细胞,肌纤维母细胞不断增殖,合成并分泌细胞外基质,沉积于血管壁上,最终导致了再狭窄的发生[5]。所以血小板在ISR发生发展过程中发挥了重要作用。血小板从骨髓释放至周围循环后,MPV就不再改变,是与血小板数量及活性相关的稳定指标。一方面MPV的增大反映了血小板黏附、聚集与释放并形成血栓能力的提高,是血小板活化增强和“动脉内血栓前状态”的重要标志[6];另一方面,血小板是从骨髓成熟的巨核细胞胞浆脱落下来的小块胞质,由于巨核细胞胞质总量稳定,所以血小板在体积和数量上存在负相关,即MPV增大的同时PLT减小。血栓形成时消耗了大量血小板,导致巨核细胞应激性释放相对胞质更多的大体积血小板。早期虽然MPV增大、胞质增多有助于活性增高和血栓形成,但是血小板活性只有7~14 d,ISR过程却以月计算,后期随着消耗持续,巨核细胞产生的血小板胞质浓度相应减少,血小板在活性及数量上都下降。本研究中MPV为多次随诊住院的平均值,MPV增大反映血小板长期耗竭功能减退的趋势,对应ISR的慢性过程存在着保护作用。
ISR的原因主要分为患者因素、病变血管因素、支架因素和操作因素。患者因素方面,高龄是ISR的危险因素。研究发现年龄每增高10岁,所有血管及血管受损处发生ISR的相对危险增加14%~19%[7]。由于支架置入后受到血管弹性回缩力的影响,术后较原内径会不同程度变窄,所以支架良好的回弹率是减少再狭窄的重要指标。年龄增高是动脉硬化、血管舒张弹性受损的重要因素,主要机制为年龄相关血管的中膜、内膜自然增厚及粥样斑块形成所致的病理性增厚。另外高龄还是内皮细胞调控血管舒缩能力下降的重要因素。随着年龄增长,内皮细胞分泌血管舒张因子NO减少,同时超阴氧离子增多加速了NO的灭活,另外与年龄相关的环氧合酶缩血管因子增多,也造成了血管弹性功能紊乱[8]。所以导致动脉硬化和血管舒张功能障碍的高龄,是ISR的危险因素。
本研究中,性别作为ISR的影响因素,HR<1,提示男性较女性ISR风险低。类似的,Rosamond等[9]研究发现,首次卒中发病的女性患者5年复发率比男性高。虽然很多研究发现ISR与性别相关,但相对风险仍存在争议。有研究认为由于男性较女性的血管病危险因素更多,因而男性的ISR风险比女性更高[10]。所以只有在平衡了生活习惯、并发症等危险因素的干扰后,才能较为准确地判断性别对ISR的影响。还有研究发现,女性较男性更容易出现阿司匹林和氯吡格雷抵抗现象,这可能与男性患者CYP2C19等位基因功能缺失,导致肝细胞内细胞色素P450酶系功能强于女性,肝细胞内氯吡格雷转化活性产物增加,导致氯吡格雷抵抗现象少于女性[11-13]。所以基因上的差别,可能是导致女性抗血小板药物反应低下而更容易发生ISR的原因。
病变血管因素也是ISR的重要原因。本研究发现基底动脉部位的ISR发生率显著增高。目前血管因素中比较公认的是,小血管病变、开口处病变、血管转角增大迂曲是ISR的危险因素。基底动脉ISR增高的机制考虑有:(1)管径相对较小,与椎动脉成角,加上基底动脉延长、迂曲变异,造成了双椎动脉汇合处血液剪切力对血管内膜的损伤;(2)基底动脉位于颅内段,相对颅外段动脉的中外膜壁薄、支撑力弱,在支架扩张过程中易引发血管内膜损伤;(3)基底动脉支架置入术的操作相对困难,其路径相对较长,变异较多,容易造成支架系统释放前在体内停留时间过长,从而发生急性、亚急性血栓事件。因此,在基底动脉引入支架前应充分准备,尽量减少支架系统在体内停留时间,防止支架释放前血栓形成[14]。本研究中1例基底动脉手术患者出现支架内急性血栓闭塞也是发生在术后复苏当天。
综上所述,女性、高龄、支架部位(基底动脉)是ISR的危险因素。长期MPV增大所反映的慢性血小板耗竭是ISR的保护性因素。建议存在以上危险因素的患者,应遵循支架操作流程,做好充分准备,加强抗血小板药物的使用,减少操作时间。
