羟氯喹联合外用糖皮质激素治疗儿童泛发型环状肉芽肿一例并文献复习
2019-07-18付希安刘永霞张福仁
张 皓 付希安 刘永霞 刘 红 张福仁
环状肉芽肿(granuloma annulare, GA)是一种以环状丘疹性损害为特征的慢性皮肤病,主要发生于真皮或皮下组织。1895年由Fox首次报道,1902年由Crocker正式命名[1]。大多数泛发型环状肉芽肿(generalized granuloma annulare,GGA)患者的发病年龄在31~70岁,其余病例发生在10岁以内[2],较为少见。回顾近几年文献发现关于儿童GGA的报道较少,现报道羟氯喹联合外用糖皮质激素治疗儿童GGA一例,并进行文献复习。
1 临床资料
患儿,男,8岁。全身泛发性环状皮疹2个月。2个月前无明显诱因患儿四肢出现绿豆大环状丘疹,边缘隆起,无自觉症状。后逐渐泛发至全身,四肢较为显著,无自觉症状。皮损未见坏死、结痂,无鳞屑附着(图1)。触之较硬,无压痛。患儿既往体健,家族成员中无类似病史。
体格检查:系统检查无明显异常。皮肤科检查:躯干、四肢可见绿豆大红色环状丘疹。
实验室及辅助检查:血常规及生化常规检查未见明显异常,血糖正常。左上肢皮损组织病理示:表皮轻度增生,真皮内见上皮样肉芽肿,中央胶原纤维变性、坏死,肉芽肿周围组织细胞、淋巴细胞浸润,胶原纤维增生,胶原间散在单一核细胞浸润(图2)。
诊断:泛发型环状肉芽肿。治疗:口服硫酸羟氯喹片0.1 g每日一次,外用复方丙酸氯倍他索软膏。1个月后复诊,皮损大部分消退,四肢皮损颜色变淡(图3)。治疗有效,继续使用该治疗方案,患者仍在随访患者中。
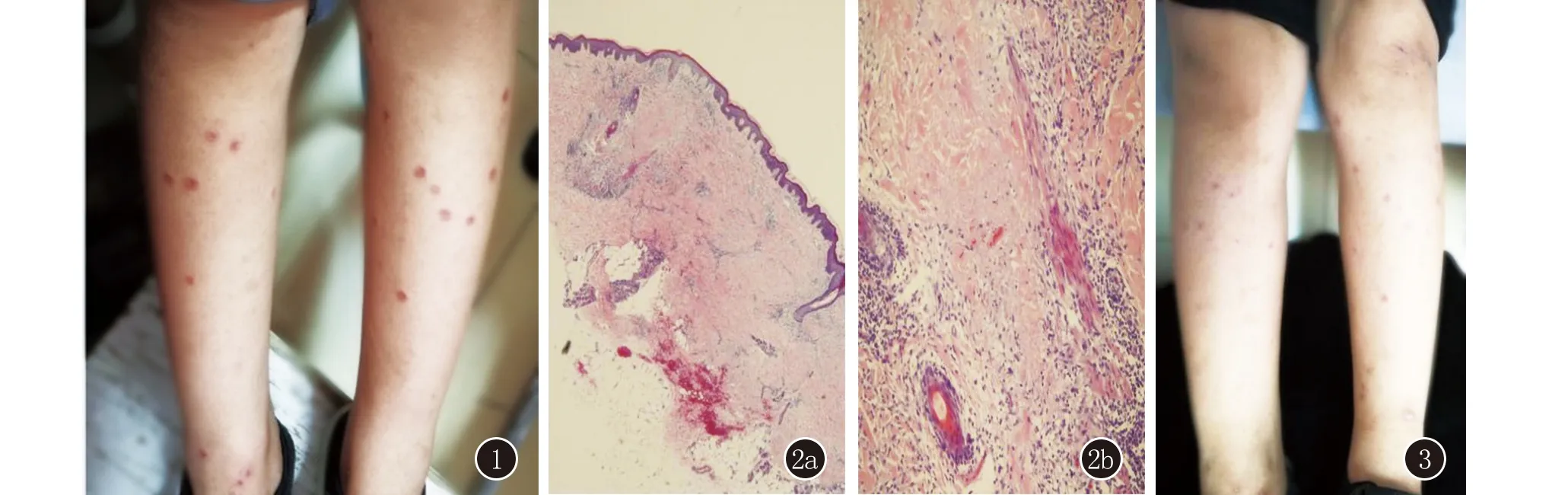
图1治疗前患儿下肢皮损图2表皮轻度增生,真皮内见上皮样肉芽肿,中央胶原纤维变性、坏死,肉芽肿周围组织细胞、淋巴细胞浸润,胶原纤维增生,胶原间散在单一核细胞浸润(HE,2a:×100;2b:×400)图3治疗后患儿下肢皮损
2 讨论
GA是发生于真皮或皮下组织以环状丘疹或结节损害为特征的慢性皮肤病。任何年龄均可发病,女性患者多于男性。根据皮损的数量、分布、大小、形状等临床上将GA分为六种亚型:局限型、泛发型、穿通型、皮下型、丘疹型和线状GA。其他还包括较少见的毛囊脓疱性皮疹和斑片状皮疹。其中局限型是最常见的类型,女性好发。大多数GGA患者发病年龄较晚,发生在儿童的GGA较少见[2]。
关于GA的病因和发病机制尚不完全清楚,目前大多数学者认为GA可能是一种细胞介导的迟发性超敏反应,Val[3]报道了一例同时患有萎缩性硬化苔藓和GA的患者,免疫组化显示T细胞标志物(CD3、CD4和CD8)主要以CD4+淋巴细胞在血管周围浸润,导致巨噬细胞持续存在。且活化的巨噬细胞有助于释放溶酶体酶和细胞因子,从而导致GA特征性局部胶原变性(渐进性坏死)和黏液沉积形成。除此之外,GA的病因可能还与以下因素相关:(1)紫外线照射:Uenotsuchi[4]报道了一例5岁的日本GA患儿,皮损只发生在有紫外线照射的部位,且数量经日晒后增加;随着紫外线照射量的增加和减少,皮损会呈现增加和减少的改变。(2)HIV病毒感染:HIV病毒感染患者的肉芽肿称为HIV相关性肉芽肿(HAGA),可发生在HIV患者的各个时期,HAGA的发病机制尚不清楚,推测可能是由对未知抗原的迟发型超敏反应引起[5]。(3)免疫球蛋白介导的血管炎:1977年,Dahl等[6]在20例GA患者中6例的血管壁上发现了免疫球蛋白M(IgM),20例患者中10例的血管壁发现存在C3。(4)其他:还有学者认为GA可能与遗传、虫咬、糖尿病、肿瘤、甲状腺炎等疾病有关。
GA的诊断依靠临床表现结合组织病理检查。GGA定义为患者的皮损至少应该发生于躯干和上肢或者下肢,或者上下肢同时受累。绝大多数GGA皮疹为排列成环状的丘疹,但也可见斑丘疹和结节。皮疹颜色可为红色、褐色或黄色。数目由几十个到数百个不等。皮疹可无自觉症状或感觉瘙痒[7]。GA皮损组织病理最主要的特征是栅栏状肉芽肿。肉芽肿的中央为变性的胶原纤维,周围常有放射状排列的淋巴细胞、组织细胞和成纤维细胞。病灶中弹性纤维消失,肉芽肿周围可见吞噬了弹性纤维的巨噬细胞[2]。GA需要与类脂质渐进性坏死、类风湿结节、光化性肉芽肿等疾病相鉴别。类脂质渐进性坏死的皮损常对称分布于下肢,女性较多见。典型皮损呈圆形或卵圆形,境界清楚,经常有轻度隆起的边缘[2]。类风湿结节好发于经常受摩擦的部位,结节通常呈肤色,可单发或多发,常位于皮下深层。实验室检查RF(+),X线常见骨囊肿改变,GA常无此改变。
GA的治疗目前尚无一线药物,主要包括局部治疗和系统性治疗。局部治疗包括冷冻治疗、手术切除、放射治疗、激光治疗和电凝治疗。系统性治疗包括抗疟药、甲状腺素、碘化钾和氨苯砜等药物[8]。局部和病灶内注射糖皮质激素被认为是GA的一线治疗方法,1975年,52例GA患者分别被注射5 mg/mL曲安奈德或生理盐水,注射曲安奈德组中68%的患者皮损被清除,而注射生理盐水组中只有44%的患者皮损被清除[9]。由于长期注射可引起皮肤萎缩,所以局部使用糖皮质激素较病灶内注射较为安全。许多学者都探讨了光疗法在治疗GA中的作用。补骨脂素加紫外光光疗(PUVA)被认为对GGA患者有效,有文献报道5例患者在开始治疗的1个月内(每周2~3次治疗后)好转[10]。但长期照射可能会增加皮肤恶性肿瘤的发病几率,补骨脂可引起胃肠道反应,儿童应慎用。1959年氯喹首次被报道用于GA,1987年羟氯喹首次被报道对GA患者有效[11]。虽然抗疟药在治疗GA中已经被提出,但关于临床应用报道却很少。在一6例GA患儿的治疗案例中,对2例患儿使用羟氯喹,4~6周内2例患儿症状均得到缓解[12]。国内报道了一例10岁播散性环状肉芽肿患儿[13],仅外用糠酸莫米松乳膏、氟轻松二甲基亚砜,4周后复诊皮损部分消退,偶有轻微痒感。关于羟氯喹治疗GA的机制有文献称GA可能是一种Th1介导的延迟超敏反应,Th1淋巴细胞通过活化的肥大细胞表达TNF-α和金属蛋白酶2和9从而引起基质降解[14]。羟氯喹会对眼睛、中枢神经系统、肝脏、肾脏等器官产生副作用,其中最严重的副作用是会导致不可逆的视网膜病变。这些副作用多由过量服用导致的,因此安全、有效的治疗方法需要建立在正确的计量上[15]。即使是使用低剂量羟氯喹治疗的儿童服药后也应密切监督,特别是眼睛和血液系统,以及对肝功能、血尿素水平和肌酐水平的检测[12]。本例报道的GGA患儿服用硫酸羟氯喹片0.1 g每日1次,外用复方丙酸氯倍他索软膏治疗1个月后复诊,皮损颜色明显变淡。复查血常规、肝功能、血肌酐水平均在正常范围内。
GA的病程是一个变化的过程,大多数病例在几个月或几年内能自发缓解,也有许多病例有复发的可能。与成年人相比,儿童GA的预后较好[9],有报道50%患儿可在2年内自行吸收,也有40%患儿可在原部位或远端复发,但仍可消退。
总之,本文报道了1例儿童GGA,经口服羟氯喹及外用糖皮质激素治疗后有效。GA的发病机制尚不完全清楚。发生在儿童的GGA较少,治疗时要更加重视。应根据患儿皮损的具体状况确定合适的治疗方案。羟氯喹在用于治疗GGA上较为安全,但应注意定期检查患儿眼睛、肝肾功等指标,并长期随访。
