两种入路治疗SandersⅡ、Ⅲ型跟骨骨折的疗效观察
2019-07-15蒋志刚韩雪昆杨文贵
蒋志刚,韩雪昆,方 玮,杨文贵,徐 俊
跟骨骨折是跗骨骨折中最常见的骨折(约占60%),约占人体所有骨折的2%[1],其中关节内骨折约占跟骨骨折的75%。跟骨承担着人体负重和行走的重要功能。解剖结构复杂,骨折形态差异大,关节内的跟骨骨折需要解剖复位来获取更好的临床效果[2-3]。外侧扩大“L”型入路经临床多年检验,暴露充分、疗效确切,但由于对软组织创伤较大,伤口并发症较高[4];而近年来跗骨窦入路因创伤小而得到推广。笔者回顾性分析使用该两种手术入路的患者的治疗效果。
临床资料
1 一般资料
2012年3月—2017年2月于笔者科室行手术治疗的72例跟骨SandersⅡ、Ⅲ型骨折患者。其中跗骨窦入路组共34例,男性21例,女性13例;左足18例,右足16例;年龄74~26岁,平均43.4岁。外侧扩大“L”型入路组38例,男性30例,女性8例;左足17例,右足21例;年龄72~27岁,平均43.1岁。所有患者中道路交通伤11例(其中4例有患肢切口处轻度皮肤损伤),高处坠落伤61例(其中有3例合并腰椎椎体压缩性骨折),均为闭合型骨折。所有患者经全程门诊随访并于笔者医院拆除内固定。入院后常规对患侧跟骨摄侧位、轴位X线片,螺旋CT扫描加3D重建,甘露醇、呋塞米脱水消肿,患足冰敷。入组患者均为单侧闭合新鲜骨折;病理性、陈旧性、开放性骨折予以排除,不纳入本研究。患者一般情况见表1,其中两组受伤至手术时间差别大是因为外侧入路组须等待皮肤条件允许时才能手术,而跗骨窦入路则不需要。

表1 两组患者一般资料比较
2 手术方法
两组患者选择全身麻醉或连续硬膜外麻醉,取健侧卧位,患肢屈髋、屈膝;患肢大腿近端均安装气囊止血带,压力约450mmHg。
跗骨窦入路组:取侧卧位,以外踝尖下方约1cm处为起点,向第4跖骨基底部作一约5cm长横形切口,逐层分离,游离并保护腓肠神经,牵开腓骨长短肌肌腱,清除跗骨窦区脂肪。对于SandersⅡ型骨折,先使用克氏针或骨膜剥离器撬拨内侧骨块以恢复后关节面的平整,然后将1枚克氏针从跟骨结节处打入,向后下方牵引以恢复跟骨高度,横向挤压跟骨以恢复宽度,经C臂机透视确认后使用解剖锁定钢板固定,必要时打入空心螺钉保持轴向稳定;对于Ⅲ型骨折,优先复位载距突骨折块及关节面中间的骨折块,克氏针临时固定,将其简化为SandersⅡ型骨折,然后按前述SandersⅡ型骨折处理。术后所有患者切口内放置引流管1根,接负压吸引。
外侧扩大“L”型入路:取侧卧位,外侧“L”型切口(转角处保持圆润弧形)必须将皮瓣全层锐性掀起(不要逐层分离),将3根直径2.0mm的克氏针分别打入骰骨、外踝和距骨,将皮瓣挡在手术区外,充分暴露距下关节和骨折端,掀起突出的外侧壁,在跟骨结节打入直径3.0mm的克氏针,向后向远端牵引,然后进行内、外翻恢复跟骨高度;用骨膜剥离子插入关节间隙,暴露跟骨后关节面,撬拨恢复Böhler角和Gissane角,通过挤压恢复跟骨宽度,克氏针临时固定,经C臂机透视侧位及轴位满意后,使用解剖锁定钢板及螺钉固定,保证有螺钉固定对侧载距突,关闭切口,常规放置引流,接负压吸引。
3 术后处理
围手术期禁烟,应用支具固定患足于功能性背伸位,术后6h起使用低分子肝素钙抗凝,24h内常规使用抗生素。术后24~48h(引流量少于50mL时)拔除引流管。术后第1天即鼓励患者进行足趾及踝泵锻炼,以减少深静脉血栓(DVT)的发生及距下关节的僵硬,1周后行足底踩皮球锻炼。具体负重时间以X线片示骨折愈合为准。
4 观察指标
比较组内X线上测量的手术前后跟骨的宽度、高度及Böhler角与Gissane角的变化;比较组间的术前等待时间、切口长度、手术时间、术后引流量、骨折愈合时间的差异;疼痛评价:术后3d内,每日早、中、晚各1次,利用VAS评分评估疼痛程度,取平均值;疗效评价:随访时,使用美国骨科足踝外科协会(American Orthopaedic Foot and Ankle Society,AOFAS)踝-后足评分系统评估术后功能情况,满分为100分,其中90~100分为优,80~89分为良,70~79分为可,<70分为差[5]。
5 统计学分析
结 果
72例患者术后均获12~18个月(平均14.3个月)门诊随访。术后无切口感染发生,外侧扩大“L”型入路组2例切口有较多渗液,经换药后好转;跗骨窦入路组1例出现腓肠神经牵拉症状,未经特殊处理3个月后症状缓解。患者术后8~12周(平均9.5周)获骨折临床愈合。
各组内术后3d复查跟骨X线片上的重要复位指标较术前均明显改善,见表2、3。两组患者在术前等待时间、切口长度、手术时间、术后引流量、术后VAS评分等方面的差异具有统计学意义(P<0.05),证明跗骨窦入路组较外侧扩大入路组有优势;而在AOFAS 评分方面差异无统计学意义(P>0.05)。见表4。典型病例见图1~2。
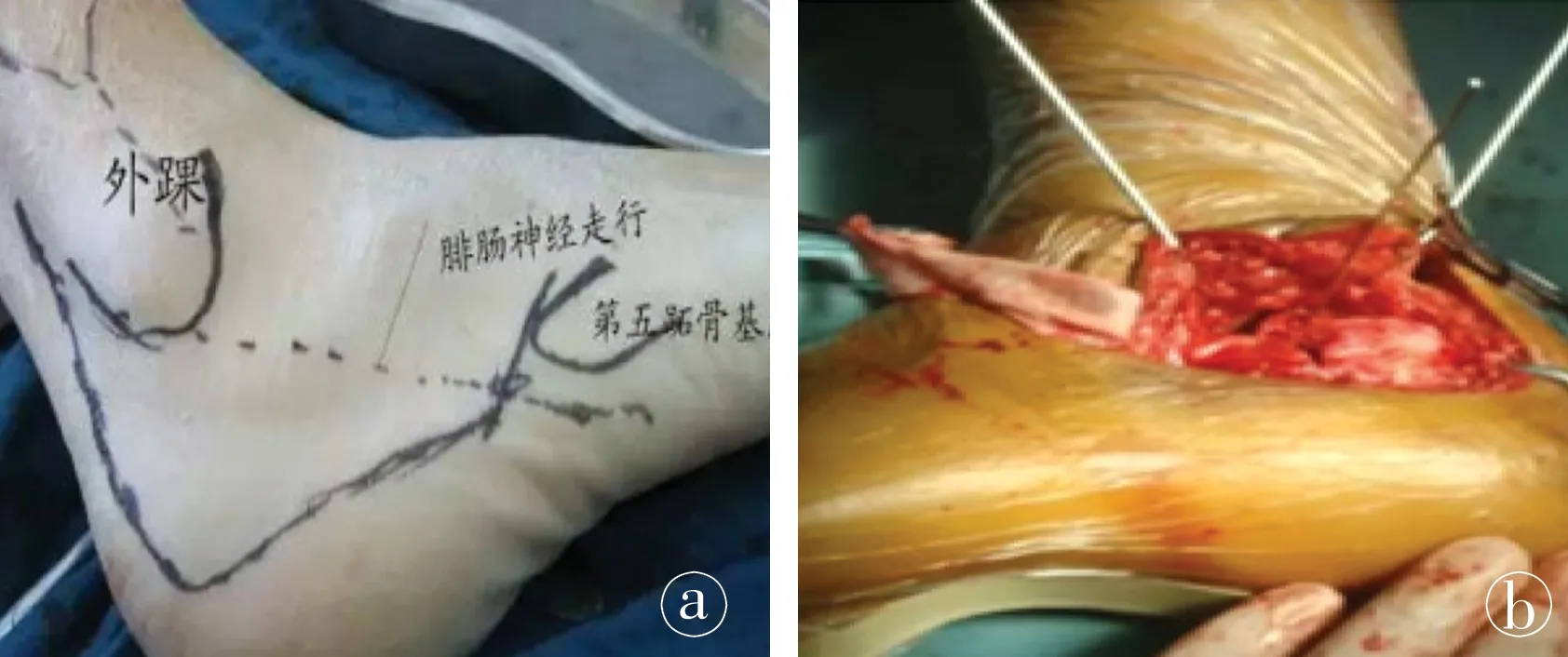
图1 患者男性,32岁,高处坠落致SandersⅢ型跟骨骨折。a.外侧扩大“L”形入路示意图; b.手术情况

表2 跗骨窦组术前、术后3d复位指标比较

表3 外侧扩大“L”型入路组术前、术后3d复位指标比较
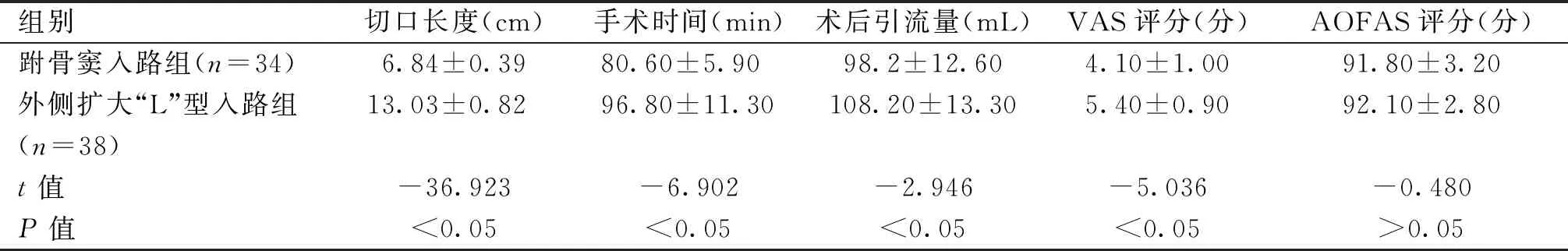
表4 两组在术中、术后相关指标及临床评价的比较

图2 患者男性,45岁,高处坠落伤,SandersⅢ型跟骨骨折,行跗骨窦入路手术治疗。a.跗骨窦入路示意图;b.使用克氏针辅助跟骨骨折复位;c.跗骨窦入路钢板置入后切口情况;d.术后第2天拟拔出引流管前切口情况;e.术前跟骨侧位X线片,见跟骨骨折,跟骨高度变矮,Böhler角明显减小;f.术后跟骨侧位X线片,跟骨高度得到纠正,Böhler角明显改善
讨 论
解剖复位、坚强固定及早期功能锻炼是关节内骨折通用的治疗原则,对于跟骨骨折亦不例外。对于骨折移位2mm以上合并距下关节不匹配、Böhler角减小、消失或成反角的跟骨骨折采取手术治疗已成共识[6]。Rammelt等[7]甚至认为大于1mm的后关节面台阶都是不可接受的,而对切口的选择上一直有争议。基于Benirschke和Kramer的研究[8]以及Knight等[9]的报道,跟骨骨折复位时要兼顾到跟骨的三度(长度、宽度、高度)、二角(Böhler角和Gissane角)等方面,力求恢复关节面的平整及正常解剖关系,恢复后足的负重轴线,固定方法要稳定可靠,尽可能地减少创伤及疼痛,允许早期锻炼。所以手术入路的选择也需基于以上原则。当跟骨关节面不能准确复位、跟骨宽度不能有效恢复时,将会导致距下关节炎等严重后果[10]。
外侧扩大“L”型入路适用于90%以上累及后关节面的跟骨骨折[11],对伴有跟骨关节面骨折的患者尤为适用[12];其并发症主要是软组织剥离多,创伤相对大。刘新成等[13]Meta分析指出跟骨骨折术后切口边缘坏死率为2.6%,伤口感染率为8.6%。但此入路早已被广泛接受,操作者技术熟练,而且随着跟骨手术中电刀的弃用及对软组织保护的理念深入人心,近年来皮缘坏死、创口感染的发生率呈逐步下降趋势,目前仍是治疗跟骨关节内骨折的“金标准”。
对于外侧扩大“L”型入路,手术的最佳时间是伤后2周[14]。但此时骨折部位已明显吸收,周围软组织粘连,给骨折的复位造成了阻碍;而附骨窦入路可以将手术日提前到伤后1周左右,完美地解决了这个问题。跗骨窦入路直接跨越了皮瓣坏死这一难题,可直接进入关节面复位,在置入钢板时对软组织的损伤也很小;而外侧扩大“L”型入路易损伤下方跟骨外侧动脉,致皮瓣缺血、坏死[15]。跗骨窦区域腓动脉终末穿支与周围血管形成广泛的交通支、血管网,可相互代偿,易形成侧支循环,故跗骨窦切口对皮瓣血供影响小,有利于血供的重新建立。余斌[16]和李云鹏等[17]的研究表明跗骨窦切口治疗跟骨骨折术后皮肤坏死率明显降低。
比较两组患者手术前后的数据,两种术式术后跟骨X线片上的重要复位指标较术前均明显改善,在AOFAS 评分上两组差异无统计学意义,证明两种术式都是治疗跟骨骨折有效的手段;纵观两组间围术期的相关指标,结果显示跗骨窦入路组在术前等待时间、切口长度、手术时间、术后引流量、术后VAS 评分方面均优于外侧扩大“L”型入路组。究其原因,跗骨窦入路省略了皮瓣大面积分离及暴露时间,所以手术时间得以缩短、术后引流量少;切口小,软组织干扰小,故术后疼痛较轻,更利于患者早期功能锻炼。
本研究存在以下不足:(1)为回顾性研究且样本量较小;(2)手术医师非固定医师,操作水平不一,会造成偏倚,对统计造成了一定影响;(3)术后引流量的统计只计算了显性出血量,未计算隐形失血量。
通过本研究笔者发现跗骨窦入路简便易行,手术功能与常规手术方式结果相当,Basile等[18]的研究也证明两种入路的效果都是确切且相似的 ;而在术前等待时间、切口长度、手术时间、术后引流量、VAS评分方面有优势。因此对于Sanders II、Ⅲ骨折,该术式可替代外侧扩大“L”型入路;但术式的选择很大程度上仍依赖于术者对术式的熟悉程度,外侧扩大“L”型入路亦不失为有效的治疗跟骨骨折的方法。对于Sanders IV骨折,仍然推荐外侧扩大“L”型入路治疗[19-20]。
