水通道蛋白3介导过氧化氢转运对宫颈癌HeLa细胞增殖、迁移的作用研究*
2019-07-06袁芳史永华
袁芳,史永华
(1.新疆医科大学基础医学院,新疆 乌鲁木齐 830011;2.新疆医科大学基础医学院病理教研室,新疆 乌鲁木齐 830011)
宫颈癌是女性生殖系统常见的恶性肿瘤之一[1]。宫颈癌患者一个重要的临床病理特点是常合并长期慢性宫颈炎并伴随组织水肿。水肿是病变组织水代谢紊乱的外在表现,而其内在原因可能与水通道蛋白(Aquaporins,AQPs)功能异常关系密切。AQPs 是一组跨细胞质膜由渗透压驱动选择性转运水分子的小而完整的糖蛋白,广泛存在于活细胞内,主要参与各种涉及水代谢与转运的生理病理过程[2]。研究表明,AQPs 广泛参与恶性肿瘤的生长、转移等过程[3-4]。
在慢性炎症向癌症的转化过程中,缺氧、持续性炎症等应激性微环境引起组织水肿,活性氧(reactive oxygen species,ROS)尤其过氧化氢H2O2不断产生。新近研究报道,AQPs 的某些亚型不仅能够跨膜转运水分子,还可以转运H2O2[5]。目前有关应激性微环境中H2O2的异常与AQPs 在恶性肿瘤特别是宫颈癌发生、进展中的作用文献报道极少,其具体的分子机制更是鲜有报道。本研究初步探讨AQP3 和肿瘤微环境中H2O2的关系及其对宫颈癌HeLa 细胞增殖、迁移的影响,现报道如下。
1 材料与方法
1.1 细胞与试剂
HeLa 细胞(本实验室保存),pLVshRNA-EGFP (2A)Puro-shRNA 干扰双标RNAi 慢病毒载体(VL3103,北京Inovogen 公司),慢病毒包装系统(12260,12259,美国Addgene 公司),质粒抽提试剂盒(D6915,美国Omega Bio-Tek 公司),AQP3 一抗(ab125219,英国Abcam 公司),ROS 检测试剂盒(含绿色荧光探针DCFH-DA 和高纯度H2O2,E004,南京建成生物工程所),cDNA 逆转录试剂盒(K1622,美国Fermentas 公司)。
1.2 细胞培养
宫颈癌HeLa(人子宫颈腺癌细胞,HPV18 阳性)培养于DMEM 培养基,添加10%胎牛血清(fetal bovine serum,FBS)、青/链霉素(10 万u/L),于37℃、5%二氧化碳CO2培养箱培养。
1.3 AQP3 shRNA 稳定转染HeLa 细胞系的构建
1.3.1 构建pLVshRNA-EGFP(2A)Puro-shRNA-AQP3 重组质粒根据GenBank 中AQP3基因mRNA 序列(NM_004925),设计3 对siRNA 片段:AQP3-homo-464 (正向5'-GGGCUGUAUUAUGAUGCAATT-3',反向5'-U UGCAUCAUAAUACAGCCCTT-3')、AQP3-homo-198 (正向5'-CCCUCAUCCUGGUGAUGUUTT-3',反向5'-A ACAUCACCAGGAUGAGGGTT-3')、AQP3-homo-612(正向5'-CCCUUAUCGUGUGUGUGCUTT-3',反向5'-AGCACACACACGAUAAGGGTT-3')。用LipofectamineTM2000 分别转染3 组siRNA 到293T 细胞中,培养24 h后做实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction,qRT-PCR)检测筛选干扰效应明显的干扰片段。选择pLV shRNA-EGFP(2A)PuroshRNA 双标干扰载体,设计2 对shRNA:shRNA-464(正向5'-GATCCGGGCTGTATTATGATGCAATCAAGA GTTGCATCATAATACAGCCCTTTTTTG-3',反向5'-AA TTCAAAAAAGGGCTGTATTATGATGCAACTCTTGATTG CATCATAATACAGCCCG-3')和shRNA-612(正向5'-G ATCCCCCTTATCGTGTGTGTGCTTCAAGAGAGCACAC ACACGATAAGGGTTTTTTG-3',反向5'-AATTCAAAA AACCCTTATCGTGTGTGTGCTCTCTTGAAGCACACAC ACGATAAGGGG-3'),退火片段与酶切后的载体进行连接并转化JM109 感受态细胞,挑单克隆摇菌及PCR鉴定菌液,选取阳性菌液测序并经BLAST 比对证实。
1.3.2 慢病毒包装及生物学滴度测定接种293T 细胞于6 cm 培养皿中,1×105个/ml。用脂质体转染法将慢病毒包装质粒和目的质粒转染到293T 细胞中。收集转染48 h 培养上清液,离心、过滤,进行滴度测定,测定结果滴度较高,可以进行转染。病毒置入-80℃冰箱冷冻保存。
1.3.3 慢病毒感染细胞及嘌呤霉素筛选稳转细胞系接种HeLa 细胞于6 孔板,5×105个/孔,按复感染指数(multiplicity of infection,MOI)=10 加入慢病毒。400 ng/ml 嘌呤霉素筛选稳转细胞株,Western blotting检测。
1.4 H2O2 诱导前后宫颈癌HeLa 细胞内ROS 水平检测
取对数生长期的宫颈癌细胞,胰酶消化,以5×105个/ml 接种于6 孔板,2 ml/孔,37℃、5% CO2培养箱中培养细胞至汇合70.0%~80.0%,100 μmol/L H2O2的完全培养基作用6 h,更换10 μmol/L DCFH-DA 37℃孵育30 min,消化、收集细胞,激光共聚焦检测细胞内代表ROS(主要为H2O2)水平的绿色荧光强度。
1.5 细胞增殖实验
CCK-8 法检测实验组(HeLa-AQP3-464 shRNA)和对照组[HeLa、HeLa(-)]宫颈癌HeLa 细胞增殖情况。选择对数期细胞,胰酶消化并计数,应用96 孔板,2 000 个/孔、培养液200 μl/孔,每组设5 个复孔,24 h 后每孔分别加入0、5、10、20 及50 μmol/L H2O2,继续培养24 h 后加入CCK-8 10 μl/孔,加入无血清培养基90 μl/孔,37℃孵育2.5 h,用酶标仪测定450 nm 处吸光度(A)值。
1.6 细胞损伤愈合实验
不同组细胞分别以1×106个/孔接种在6 孔板中,24 h 后细胞培养至单层汇合状态时用含1% FBS的DMEM 培养液进行细胞同步化24 h。用10 μl 无菌移液头尖端于培养板垂直方向轻轻划过细胞层,形成宽度为300~500 μm的无细胞划痕区。PBS洗3次,加入含10% FBS 的完全培养基、H2O210 μmol/L 继续培养,分别于0和24 h倒置显微镜下照相,设3个重复。
1.7 Western blotting 检测
细胞接种于6 孔板24 h 后,100 ng/ml 表皮生长因子(EGF)刺 激10 min 后 用200 μmol/L H2O2作用实验组和对照组细胞各20 min,收集细胞沉淀,加入细胞裂解液,10 000 r/min 离心10 min,取上清液30 μl,加入4×loading buffer 10 μl,95℃加热10 min使蛋白质变性,12 000 r/min 离心1 min,取上清液。利用BCA 试剂盒测定样品蛋白含量。取测定样品,每孔上样量为20 μg,8% SDS-PAGE 电泳分离:浓缩胶电泳80 V 30 min,分离电泳120 V 70 min,然后电压80 V 下转至PVDF 膜。封闭液封闭1 h,加蛋白激酶B(PKB)、磷酸化蛋白激酶B(p-PKB)一抗,4℃过夜,PBST 洗3 次,10 min/次;加二抗,室温孵育1 h,PBST 洗3 次,10 min/次。用ECL 底物完成化学发光检测,显影、定影后采用扫描仪扫描,数据传输到Gel Proanalyzer 软件中完成灰度分析定量。
1.8 统计学方法
数据分析采用SPSS 18.0 统计软件,计量资料以均数±标准差(±s)表示,比较行Student'st检验或单因素方差分析(Dunnett's 多重比较检验),P<0.05 为差异有统计学意义。
2 结果
2.1 成功构建并鉴定重组质粒pLV shRNA-EGFP(2A)Puro-shRNA-AQP3 稳定转染HeLa 细胞系
设计的3 对干扰片段经qRT-PCR 检测筛选出AQP3 mRNA 表达相对较低的片段464 和612(见图1A);选 择pLVshRNA-EGFP(2A)Puro-shRNA 双标干扰载体,设计AQP3-464-shRNA 和AQP3-612-shRNA,连接转化后,细菌的阳性克隆经扩大培养,抽提质粒,酶切鉴定,证实构建的干扰质粒AQP3-464-shRNA 和AQP3-612-shRNA 正确(见图1B),并经测序比对证实。选择干扰质粒AQP3-464-shRNA 病毒液稳定转染HeLa 细胞,经Western blotting 分析验证,HeLa、HeLa(-)、HeLa-AQP3-464 shRNA 细胞中AQP3/GAPDH 的相对表达分别为(1.00±0.02)、(1.04±0.04)和(0.63±0.08),重组质粒稳定转染HeLa 细胞后在蛋白水平抑制AQP3 的表达(见图2A、B)。
2.2 AQP3 shRNA 抑制HeLa 细胞中H2O2 的跨膜转运
激光共聚焦结果显示,与HeLa、HeLa(-)比较,HeLa-AQP3-464-shRNA 细胞内代表ROS(主要为H2O2)水平的绿色荧光变弱,AQP3 shRNA 抑制H2O2的跨膜转运。见图3。

图1 重组质粒pLV shRNA-EGFP(2A)Puro-shRNA-AQP3 的构建
2.3 AQP3 shRNA 介导肿瘤微环境中H2O2 转运抑制宫颈癌HeLa 细胞的增殖
结果表明,低浓度H2O2(10 μmol/L)促进HeLa细胞增殖,AQP3 shRNA 抑制肿瘤微环境中H2O2转运从而抑制HeLa 细胞增殖,20 μmol/L 以上高浓度H2O2则显示出细胞毒性,诱导细胞凋亡。见图4A。
细胞平板克隆实验显示,低浓度H2O2(5 或10 μmol/L)分别加入不同组细胞培养10 d,至出现肉眼可见的克隆时终止培养。与HeLa、HeLa(-)比较,HeLa-AQP3-464-shRNA 组细胞克隆形成减少(见图4B),该实验进一步证实CCK-8 结果。
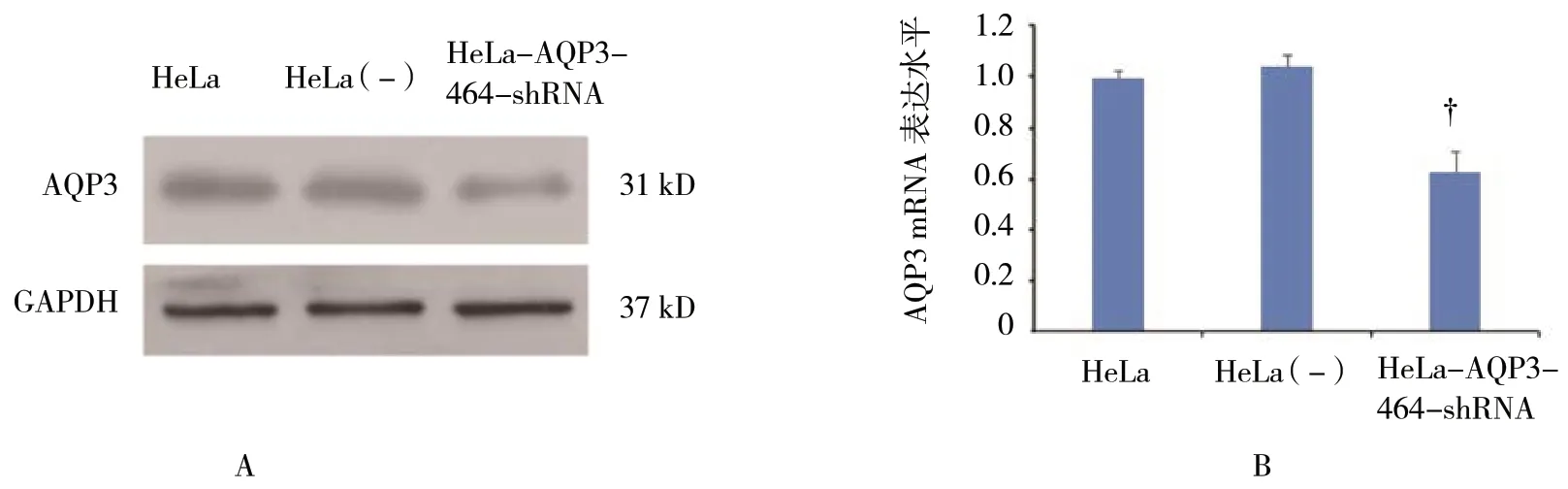
图2 重组质粒pLV shRNA-EGFP(2A)Puro-shRNA-AQP3 的鉴定

图3 H2O2 处理后不同组别HeLa 细胞内的H2O2 变化 (激光共聚焦×200)
2.4 AQP3 shRNA 介导肿瘤微环境中H2O2 转运抑制宫颈癌HeLa 细胞迁移
10 μmol/L H2O2作用于HeLa、HeLa(-)、HeLa-AQP3-464-shRNA 细胞24 h 后,其平均愈合速度分别为(296.91±88.86)、(309.02±11.25)和(223.46±12.94)μm。HeLa-AQP3-464-shRNA 与HeLa、HeLa(-)比较,差异有统计学意义(F=86.300,P=0.000)。见图5、6。
2.5 AQP3 shRNA 介导肿瘤微环境中H2O2 转运抑制下游信号PKB 的激活
在H2O2分别为0 和200 μmol 时,HeLa 组p-PKB的相对表达为(0.20±0.087)、(0.58±0.041),HeLa(-)组p-PKB的相对表达为(0.390±0.055)、(0.430±0.068),HeLa-AQP3-shRNA 组p-PKB 的相对表达为(0.480±0.067)、(0.790±0.043)。在200 μmol H2O2作用后各组内的p-PKB 变化均差异有统计学意义(P<0.05),但HeLa-AQP3-shRNA组与HeLa组比较,p-PKB 变化幅度小(F=634.900,P=0.000)。见图7、8。
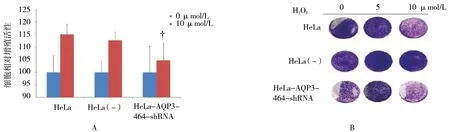
图4 AQP3-shRNA 介导H2O2 转运抑制宫颈癌HeLa 细胞的增殖

图5 10 μmol/L H2O2 处理后不同组别HeLa 细胞的迁移
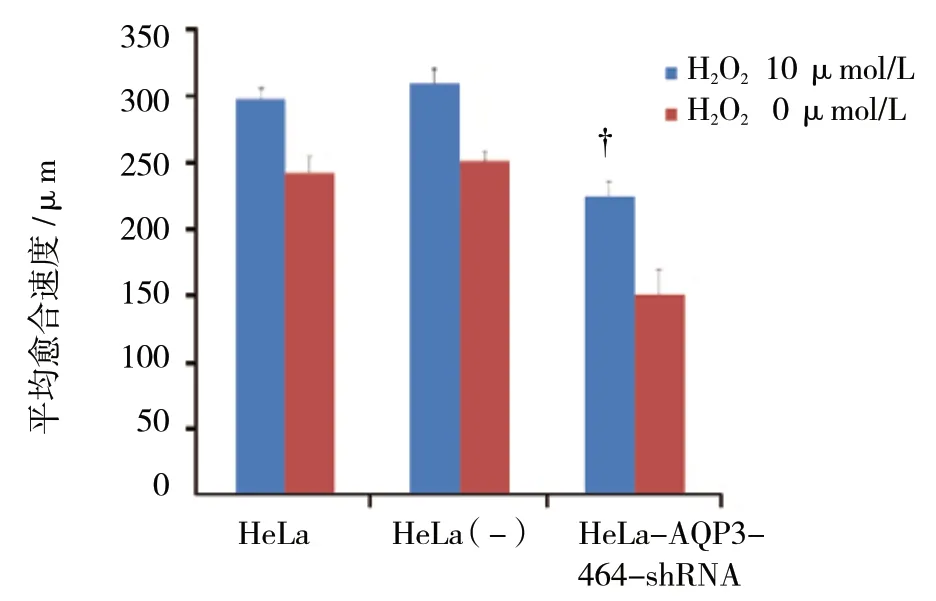
图6 10 μmol/L H2O2 处理后不同组别HeLa 细胞的 平均愈合速度 (±s)
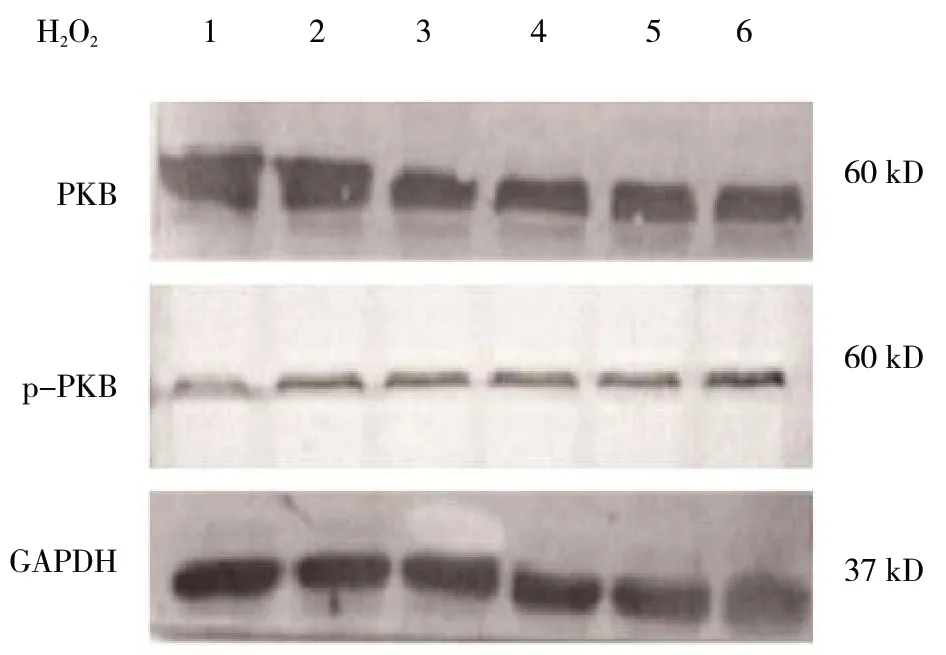
图7 AQP3 介导H2O2 转运抑制PKB 的激活

图8 AQP3 介导H2O2 转运抑制PKB 激活的 灰度扫描量化结果 (±s)
3 讨论
本研究成功构建慢病毒介导的AQP3 shRNA 稳转HeLa 细胞株,并经测序比对证实,重组质粒稳定转染HeLa 细胞后在蛋白水平抑制AQP3 的表达。还发现,抑制HeLa 细胞中AQP3 的表达可减少细胞内ROS(主要为H2O2)水平,提示AQP3 可跨膜转运H2O2。笔者进一步研究AQP3 跨膜转运H2O2对HeLa 细胞相关表型如增殖、迁移的作用。CCK-8 和细胞平板克隆实验结果表明,低浓度的H2O2可促进HeLa 细胞的增殖,抑制AQP3 的表达则抑制HeLa 细胞增殖;损伤愈合实验结果也提示,低浓度的H2O2可促进HeLa 细胞的迁移,抑制AQP3 的表达则抑制HeLa 细胞迁移。以上实验结果提示,AQP3 介导肿瘤微环境中H2O2转运促进宫颈癌HeLa 细胞的迁移、增殖,抑制AQP3 的表达则减弱肿瘤微环境中H2O2跨膜转运入细胞内,从而抑制宫颈癌HeLa 细胞的迁移、增殖。目前认为H2O2不再是细胞代谢过程中的有毒副产品,而是信号转导过程中重要的第二信使,主要通过氧化关键含硫基蛋白的敏感位点、调控相关信号从而参与多种生理病理过程[6-7],而癌细胞中持续上调的H2O2依赖信号调控凋亡、增殖、血管生成、转移、能量代谢等与癌症发生、进展相关的诸多重要过程[8-9]。文献报道,AQP3、AQP8介导H2O2跨膜转运加速鼠T 细胞的迁移,促进肿瘤细胞的能量合成代谢和细胞增殖[10-11],抑制AQP8 表达则可抑制H2O2跨膜转运及下游靶蛋白的酪氨酸磷酸化[12]。但高浓度H2O2也可诱导细胞周期停滞或细胞凋亡[6]。本研究结果与上述文献报道相符。由于H2O2的这种双重效应,肿瘤细胞上调抗氧化系统如超氧化物歧化酶等以降低细胞内H2O2浓度,形成适当的H2O2浓度梯度从而选择性、局灶性启动H2O2信号事件[13]。临床上宫颈癌常合并长期慢性宫颈炎并伴随组织水肿。笔者推测,在慢性宫颈炎向宫颈癌的转化过程中,缺氧、持续性炎症等局部微环境引起组织水肿,水肿的长期存在加重缺氧,ROS 尤其H2O2不断产生,局部微环境代谢异常,触发AQPs 将H2O2不断转运入细胞内,进一步加重缺氧,导致局部组织修复信号过多,诱使局部细胞过度增殖,甚至癌变。
文献报道,PKB 信号通路参与多种恶性肿瘤包括宫颈癌的发生、进展[14-15]。本研究Western blotting 实验结果表明,EGF 刺激10 min 后用200 μmol/L H2O2作用于HeLa 细胞20 min,激发PKB 磷酸化,抑制AQP3 的表达则减弱PKB 磷酸化。本研究结果提示AQP3 能跨膜转运肿瘤微环境中的H2O2,激发细胞内依赖第二信使H2O2的下游信号PKB,从而促进HeLa 细胞的增殖、迁移。有文献报道[5],AQP3 介导H2O2吸收激活人结肠癌HT29 细胞内信号PKB,与笔者的结果相似。
综上所述,AQP3 介导宫颈癌HeLa 细胞中H2O2跨膜转运,激发细胞内依赖第二信使H2O2的下游信号PKB,促进宫颈癌HeLa 细胞的增殖、迁移。本研究结果尚需在更多的肿瘤细胞系和癌组织中得到证实。
